

Oestrogel

Consulta con un médico sobre la receta médica de Oestrogel

Cómo usar Oestrogel
Hoja de instrucciones del paquete: información para el paciente
Oestrogel, 0,75 mg/dosis, gel transdérmico
Estradiol
Es importante leer detenidamente el contenido de esta hoja de instrucciones antes de usar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- Si tiene alguna duda, debe consultar a su médico o farmacéutico.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente presenta algún efecto adverso, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice de la hoja de instrucciones
- 1. Qué es Oestrogel y para qué se utiliza
- 2. Información importante antes de usar Oestrogel
- 3. Cómo usar Oestrogel
- 4. Posibles efectos adversos
- 5. Cómo conservar Oestrogel
- 6. Contenido del paquete y otra información
1. Qué es Oestrogel y para qué se utiliza
Oestrogel es un medicamento utilizado en la terapia hormonal sustitutiva (THS). El medicamento contiene el hormona femenino estradiol. Después de aplicar el gel en la piel, el hormona se absorbe y pasa al torrente sanguíneo.
Oestrogel se utiliza en mujeres posmenopáusicas, es decir, que han pasado al menos 6 meses desde su última menstruación natural.
Oestrogel se utiliza en las siguientes situaciones:
Alivio de los síntomas posmenopáusicos
Durante la menopausia, la cantidad de estrógenos producidos por el organismo de la mujer disminuye. Esto puede causar síntomas como sensación de calor en la cara, cuello y pecho („olas de calor”). Oestrogel alivia estos síntomas posmenopáusicos. Oestrogel solo se prescribe cuando los síntomas afectan significativamente la vida diaria de la paciente.
Prevención de la osteoporosis
Después de la menopausia, algunas mujeres pueden desarrollar osteoporosis. Debe discutir todas las opciones de tratamiento con su médico.
Si la paciente tiene un mayor riesgo de fracturas debido a la osteoporosis y otros medicamentos no son adecuados, se puede utilizar Oestrogel para prevenir la osteoporosis posmenopáusica.
2. Información importante antes de usar Oestrogel
Historia médica y controles regulares
El uso de la THS conlleva un riesgo que debe ser considerado al tomar la decisión de iniciar o continuar el tratamiento.
La experiencia con el uso de la terapia en mujeres con menopausia prematura (causada por la falla ovárica o cirugía) es limitada. En el caso de mujeres con menopausia prematura, el riesgo de la THS puede ser diferente. Debe consultar a su médico.
Antes de iniciar (o reanudar) la THS, el médico realizará una historia médica de la paciente y su familia. El médico puede realizar un examen físico, incluyendo un examen de los senos y (o) órganos internos, si es necesario.
Después de iniciar el uso de Oestrogel, debe asistir regularmente a controles (al menos una vez al año). Durante estas visitas, debe discutir con su médico los beneficios y riesgos de continuar usando Oestrogel.
Según las recomendaciones de su médico o enfermera, debe someterse a exámenes de senos regulares.
Cuándo no usar Oestrogel:
Si alguna de las siguientes condiciones se aplica a la paciente. En caso de duda sobre alguna de las siguientes condiciones, antes de usar Oestrogel, debe consultar a su médico.
- si la paciente actualmente padece o ha padecido de cáncer de mamao si se sospecha;
- si la paciente padece cáncer maligno sensible a los estrógenos, como el cáncer del endometrio, o si se sospecha;
- si hay sangrado vaginal de causa desconocida;
- si la paciente tiene hiperplasia endometrial no tratada(crecimiento excesivo del revestimiento del útero);
- si la paciente ha tenido o tiene trombosis venosa(coágulos de sangre en las venas), como la trombosis venosa profunda o la embolia pulmonar;
- si la paciente tiene trastornos de coagulación(como la deficiencia de proteína C, proteína S o antitrombina);
- si la paciente ha tenido o tiene enfermedad arterial causada por coágulos, como el infarto de miocardio, el accidente cerebrovascular o la angina de pecho;
- si la paciente actualmente padece o ha padecido de enfermedad hepática, y los resultados de las pruebas hepáticas no han regresado a la normalidad;
- si la paciente tiene porfiria, una enfermedad rara de la sangre que se transmite de generación en generación;
- si la paciente es alérgica(hipersensible) al principio activo o a alguno de los demás componentes de este medicamento (enumerados en el punto 6). Si alguno de los síntomas anteriores aparece por primera vez mientras usa Oestrogel, debe dejar de usarlo y consultar a su médico de inmediato.
Cuándo tener precaución al usar Oestrogel
Debe informar a su médico si la paciente actualmente padece o ha padecido de alguno de los siguientes estados, ya que pueden empeorar o reaparecer durante el tratamiento con Oestrogel.
Debe asistir a controles más frecuentes si alguna de las siguientes situaciones se aplica a la paciente:
o miomas uterinos;
o endometriosis (crecimiento del revestimiento del útero fuera del útero) o historial de hiperplasia endometrial (crecimiento excesivo del revestimiento del útero);
o mayor riesgo de trombosis venosa [véase „Trombosis venosa (trombosis)”];
o mayor riesgo de cáncer sensible a los estrógenos (por ejemplo, si la madre, hermana o abuela de la paciente ha tenido cáncer de mama);
o hipertensión arterial;
o enfermedades hepáticas, como los tumores hepáticos benignos;
o diabetes;
o cálculos biliares;
o migraña o dolores de cabeza severos;
o enfermedad del sistema inmunológico que afecta muchos órganos del cuerpo (lupus eritematoso sistémico, LES);
o epilepsia;
o asma;
o enfermedad que afecta el oído y la audición (otosclerosis);
o niveles muy altos de grasas en la sangre (triglicéridos);
o retención de líquidos en el cuerpo debido a enfermedades cardíacas o renales;
o edema angioneurótico hereditario o adquirido.
Debe dejar de usar Oestrogel y consultar a su médico de inmediato si se presenta alguno de los siguientes estados durante el uso de la THS:
- cualquiera de las enfermedades enumeradas en el punto „Cuándo no usar Oestrogel”,
- ictericia (color amarillo de la piel y los ojos). Puede ser un signo de enfermedad hepática;
- hinchazón de la cara, lengua y (o) garganta y (o) dificultad para tragar o erupción cutánea con dificultad para respirar, que sugieren edema angioneurótico;
- aumento significativo de la presión arterial (síntomas pueden ser dolor de cabeza, fatiga, mareo);
- dolores de cabeza tipo migraña que aparecen por primera vez;
- embarazo;
- signos de coágulo, como:
- hinchazón y enrojecimiento doloroso de las piernas;
- dolor súbito en el pecho;
- dificultad para respirar;
Más información en el punto „Trombosis venosa (trombosis)”.
Nota: Oestrogel no es un método anticonceptivo. Si han pasado menos de 12 meses desde la última menstruación o si la paciente tiene menos de 50 años, pueden ser necesarias medidas anticonceptivas adicionales para evitar el embarazo. Debe consultar a su médico.
THS y cáncer
Hiperplasia endometrial (crecimiento excesivo del revestimiento del útero) y cáncer del endometrio
El uso de la THS solo con estrógenos aumenta el riesgo de hiperplasia endometrial y cáncer del endometrio.
El uso adicional de progestágeno durante al menos 12 días en cada ciclo de 28 días protege a la paciente de este mayor riesgo. El médico recetará progestágeno por separado si la paciente tiene útero conservado. Si el útero ha sido extirpado (histerectomía), debe discutir con su médico si el uso de este medicamento sin progestágeno es seguro.
En mujeres con útero conservado que no usan THS, se diagnostica cáncer del endometrio en aproximadamente 5 de cada 1.000 mujeres entre 50 y 65 años.
En mujeres con útero conservado que usan THS solo con estrógenos, se diagnostica cáncer del endometrio en 10-60 de cada 1.000 mujeres (es decir, de 5 a 55 casos adicionales), dependiendo de la dosis y la duración del tratamiento.
Oestrogel contiene una dosis mayor de estrógenos que otras THS que solo contienen estrógenos. El riesgo de cáncer del endometrio durante el uso de Oestrogel en combinación con progestágeno no es conocido.
Sangrado irregular
Durante los primeros 3 a 6 meses de tratamiento con Oestrogel, pueden ocurrir sangrados irregulares o leves (manchado). Sin embargo, si el sangrado irregular:
- dura más de 6 meses,
- comienza después de usar Oestrogel durante más de 6 meses,
- persiste después de dejar de usar Oestrogel, debe consultar a su médico de inmediato.
Sangrado de causa desconocida
Durante el uso de Oestrogel con progestágeno (es decir, progestina) una vez al mes, ocurrirá un sangrado (llamado sangrado de retirada). Sin embargo, si ocurre un sangrado de causa desconocida o manchado fuera del sangrado de retirada, que:
- dura más de los primeros 6 meses,
- aparece cuando la paciente ha estado usando Oestrogel durante más de 6 meses,
- persiste después de dejar de usar Oestrogel, debe consultar a su médico de inmediato.
THS y cáncer de mama
Los datos confirman que el uso de la THS, ya sea en forma de estrógeno y progestágeno o solo estrógeno, aumenta el riesgo de cáncer de mama. El riesgo adicional depende de la duración del uso de la THS. Este riesgo adicional se manifiesta después de 3 años de uso de la THS. Después de dejar de usar la THS, el riesgo adicional disminuirá con el tiempo, pero puede persistir durante 10 años o más si la THS duró más de 5 años.
Comparación
En mujeres de 50 a 54 años que no usan THS, se diagnostica cáncer de mama en aproximadamente 13-17 de cada 1.000 mujeres en un período de 5 años.
En mujeres de 50 años que comienzan una THS de 5 años con estrógeno, el número de casos será de 16-17 por 1.000 pacientes (es decir, 0-3 casos adicionales).
En mujeres de 50 años que comienzan una THS de 5 años con estrógeno y progestágeno, el número de casos será de 21 por 1.000 pacientes (es decir, 4-8 casos adicionales).
En mujeres de 50 a 59 años que no usan THS, se diagnostica cáncer de mama en aproximadamente 27 de cada 1.000 mujeres en un período de 10 años.
En mujeres de 50 años que comienzan una THS de 10 años con estrógeno, el número de casos será de 34 por 1.000 pacientes (es decir, 7 casos adicionales).
En mujeres de 50 años que comienzan una THS de 10 años con estrógeno y progestágeno, el número de casos será de 48 por 1.000 pacientes (es decir, 21 casos adicionales).
- Debe examinar regularmente los senos. Debe consultar a su médico si aparecen cambios como:
- depresiones en la piel,
- cambios en el pezón,
- cualquier bulto visible o palpable. Además, se recomienda participar en programas de detección de cáncer de mama. Es importante informar al personal que realiza la mammografía sobre el uso de la THS, ya que el medicamento puede causar un aumento en la densidad radiológica de los senos, lo que puede afectar el resultado de la mammografía. En áreas de mayor densidad, la mammografía puede no detectar todos los bultos.
Cáncer de ovario
El cáncer de ovario es raro, mucho más raro que el cáncer de mama. El uso de la THS que solo contiene estrógenos o la combinación de estrógenos y progestágenos se asocia con un ligero aumento del riesgo de cáncer de ovario.
El riesgo de cáncer de ovario depende de la edad. Por ejemplo, en mujeres de 50-54 años que no usan THS, se diagnostica cáncer de ovario en 2 de cada 2.000 mujeres en un período de 5 años. En mujeres que han usado THS durante 5 años, se diagnostica cáncer de ovario en aproximadamente 3 de cada 2.000 usuarias (es decir, aproximadamente 1 caso adicional).
Efecto de la THS en el corazón y la circulación
Trombosis venosa (trombosis)
El riesgo de trombosis venosaes aproximadamente 1,3 a 3 veces mayor en mujeres que usan THS, especialmente durante el primer año de tratamiento, que en mujeres que no la usan.
Los coágulos de sangre pueden ser graves y, si llegan a los pulmones, pueden causar dolor en el pecho, dificultad para respirar, pérdida de conocimiento e incluso la muerte.
La probabilidad de formación de coágulos en las venas aumenta con la edad y depende de la presencia de factores como:
- la paciente no puede caminar durante un período prolongado debido a una cirugía mayor, lesión o enfermedad (véase también el punto 3 „Si es necesaria una operación”),
- la paciente es obesa (IMC >30 kg/m2),
- la paciente tiene problemas de coagulación que requieren tratamiento a largo plazo con medicamentos para prevenir coágulos de sangre,
- algún familiar cercano ha tenido un coágulo en una pierna, pulmón u otro órgano,
- la paciente tiene lupus eritematoso sistémico (LES),
- la paciente tiene cáncer. Los síntomas que indican la presencia de coágulos de sangre, véase el punto „Dejar de usar Oestrogel y consultar a su médico de inmediato”.
Oestrogel y dejar de usar el medicamento y consultar a su médico de inmediato
En mujeres de 50 a 59 años que no usan THS, es probable que ocurra una trombosis venosa en 4-7 de cada 1.000 mujeres en un período de 5 años.
En mujeres de 50 a 59 años que han usado THS combinada con estrógeno y progestágeno durante más de 5 años, es probable que ocurra una trombosis venosa en 9-12 de cada 1.000 mujeres (es decir, 5 casos adicionales).
En mujeres de 50 a 59 años con útero extirpado que han usado THS solo con estrógeno durante 5 años, es probable que ocurra una trombosis venosa en 5-8 de cada 1.000 mujeres (es decir, 1 caso adicional).
Enfermedad cardíaca (infarto de miocardio/ataque cardíaco)
No hay evidencia científica que respalde que la THS pueda prevenir los infartos de miocardio.
Las mujeres mayores de 60 años que usan THS combinada con estrógeno y progestágeno tienen un ligero aumento del riesgo de enfermedad cardíaca en comparación con las mujeres que no usan THS.
En mujeres con útero extirpado que usan solo THS con estrógeno, no hay un aumento del riesgo de enfermedad cardíaca.
Accidente cerebrovascular
El riesgo de accidente cerebrovascular es aproximadamente 1,5 veces mayor en personas que usan THS que en personas que no la usan. El número de casos adicionales de accidente cerebrovascular debido al uso de la THS aumenta con la edad.
En mujeres de 50 a 59 años que no usan THS, es probable que ocurra un accidente cerebrovascular isquémico en 8 de cada 1.000 mujeres en un período de 5 años.
En mujeres de 50 a 59 años que usan THS, es probable que ocurra un accidente cerebrovascular isquémico en 11 de cada 1.000 mujeres en un período de 5 años (es decir, 3 casos adicionales).
Niños
El estradiol en forma de gel puede ser transferido accidentalmente de la piel de la paciente a otras personas.
No debe permitir que otras personas, especialmente niños, entren en contacto con el área de la piel de la paciente donde se ha aplicado el gel, y debe cubrir el área con ropa si es necesario.
Si un niño entra en contacto con el área de la piel donde se ha aplicado el estradiol, debe lavar la piel del niño con agua y jabón lo antes posible. Debido a la transferencia de estradiol, los niños pequeños pueden mostrar signos de pubertad prematura (por ejemplo, crecimiento de los senos). En la mayoría de los casos, estos signos desaparecen cuando el niño ya no está expuesto al estradiol en forma de gel.
Si se observan signos de pubertad en un niño que puede haber estado expuesto accidentalmente al estradiol en forma de gel (por ejemplo, crecimiento de los senos u otros cambios sexuales), debe consultar a su médico.
Otras condiciones
- El uso de Oestrogel puede causar retención de líquidos en el cuerpo. Por lo tanto, en caso de enfermedad cardíaca o renal, la paciente debe ser monitoreada cuidadosamente mientras usa Oestrogel.
- La THS no previene la pérdida de memoria. Hay algunas pruebas de que el inicio de la THS después de los 65 años puede aumentar el riesgo de pérdida de memoria. Debe consultar a su médico.
Uso de Oestrogel con otros medicamentos
Ciertos medicamentos pueden afectar el efecto de Oestrogel. Esto puede causar sangrados irregulares. Se aplica a los siguientes medicamentos:
- otros medicamentos para la piel (por ejemplo, medicamentos contra el cáncer);
- medicamentos para tratar la epilepsia(como fenobarbital, fenitoína y carbamazepina);
- medicamentos para tratar la tuberculosis(como rifampicina, rifabutina);
- medicamentos para tratar el VIH(como nevirapina, efavirenz, ritonavir y nelfinavir);
- productos herbales que contienen hierba de San Juan(Hypericum perforatum). La THS puede afectar el efecto de otros medicamentos:
- el medicamento para la epilepsia lamotrigina, ya que puede aumentar la frecuencia de los ataques;
- los medicamentos para tratar la hepatitis C (como el esquema de tratamiento combinado con ombitasvir/paritaprevir/ritonavir con dasabuvir o sin dasabuvir, y el esquema de tratamiento combinado con glecaprevir/pibrentasvir), ya que pueden causar un aumento en los resultados de las pruebas de función hepática [aumento de la actividad de la enzima hepática alanina aminotransferasa (ALT)] en mujeres que usan productos anticonceptivos hormonales combinados que contienen etinilestradiol. Oestrogel contiene estradiol en lugar de etinilestradiol. No se sabe si el uso de Oestrogel con estos esquemas de tratamiento para la hepatitis C puede causar un aumento en la actividad de la ALT.
Debe informar a su médico o farmacéutico sobre todos los medicamentos que está tomando actualmente o recientemente, incluyendo los medicamentos sin receta, los medicamentos herbales y otros productos naturales o cosméticos para la piel que contengan alcohol, agentes limpiadores o detergentes. Su médico le aconsejará.
Análisis de laboratorio
Si es necesario realizar un análisis de sangre, debe informar al personal del laboratorio sobre el uso de Oestrogel, ya que puede afectar los resultados de algunos análisis.
Embarazo y lactancia
Oestrogel está indicado solo para mujeres posmenopáusicas.
Si la paciente queda embarazada, debe dejar de usar Oestrogel y consultar a su médico.
Oestrogel contiene etanol
Este medicamento contiene 500 mg de alcohol (etanol) en cada dosis de 1,25 g, lo que equivale a 400 mg/g (40% p/p). Puede causar ardor en la piel dañada. El medicamento es inflamable hasta que se seca.
3. Cómo usar Oestrogel
Este medicamento debe usarse siempre según las indicaciones de su médico o farmacéutico. En caso de duda, debe consultar a su médico o farmacéutico.
Su médico recetará la dosis más baja posible para tratar los síntomas durante el menor tiempo posible. Si siente que el efecto del medicamento es demasiado fuerte o demasiado débil, debe informar a su médico.
Oestrogel es un gel que contiene el hormona femenino estradiol. Después de aplicar el gel en la piel, se seca en 5 minutos y el hormona se absorbe rápidamente en el torrente sanguíneo.
Debe aplicar una capa delgada de gel en todo el brazo, desde la muñeca hasta el hombro y (o) en la parte interna del muslo. Debe extender el gel sobre la mayor superficie de piel posible.
No use el gel en los senos ni en las membranas mucosas, especialmente no use en la membrana mucosa de la vagina o el cuello uterino.
Antes de usar un nuevo frasco de gel, debe llenar el dosificador presionando y descartar la primera dosis.
Un presionado del dosificador proporciona 1,25 g de gel (1 dosis), que equivale a 0,75 mg de estradiol.
Dónde aplicar Oestrogel
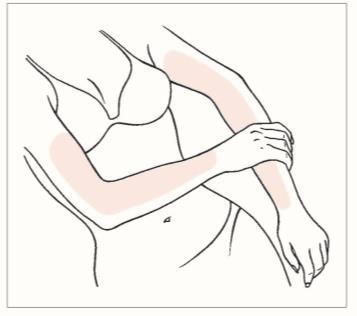

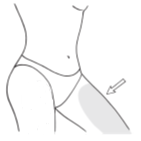
- La dosis más baja comúnmente utilizada es UNA dosis (1,25 g de gel); debe aplicarla en un brazo, desde la muñeca hasta el hombro y (o) en la parte interna del muslo. Cada frasco contiene 80 g de gel y proporciona al menos 60 dosis de 1,25 g.
Debe aplicar una dosis de Oestrogel al día, durante 21 días (3 semanas) y luego hacer una pausa de 7 días (1 semana) (véase „Aplicación del gel Oestrogel” a continuación).
Aplicación del gel Oestrogel:
- la paciente debe aplicar el gel ella misma,
- debe aplicar el gel por la mañana o por la noche, preferiblemente después de bañarse, a la misma hora cada día.
- durante una hora después de aplicar el gel, debe evitar el contacto con la piel de otras personas adultas y niños. Debe extender el gel sobre la mayor superficie de piel posible en el brazo, desde la muñeca hasta el hombro y (o) en la parte interna del muslo, en la piel sana y no dañada. Si después de 5 minutos de aplicar el gel, la piel sigue siendo pegajosa, es probable que el gel no se haya extendido lo suficiente. La próxima vez, debe extender el gel sobre una superficie más grande de la piel de los brazos y hombros y (o) la parte interna del muslo. Después de aplicar el gel en la piel, siempre debe lavar sus manos con agua y jabón. No debe permitir que otras personas toquen el área de la piel donde se ha aplicado el gel hasta que se seque y, si es necesario, cubrir con ropa.
- Pacientes con útero conservado:Su médico recetará la dosis más baja efectiva que se necesite. Debe aplicar una dosis de Oestrogel al día, durante 21 días (3 semanas) y luego hacer una pausa de 7 días (1 semana). El uso prolongado de estrógenos sin progestágeno (por ejemplo, progestina) aumenta el riesgo de cáncer del endometrio en mujeres con útero conservado. Por lo tanto, los estrógenos deben usarse con progestágeno durante al menos 12 a 14 días al mes. Es probable que su médico recete progestina. La progestina debe tomarse durante al menos 12 a 14 días en el ciclo menstrual. En la 4ª semana, cuando no se usa estrógeno, no se usa progestágeno. Puede ocurrir un sangrado de retirada („menstruación”).
- Pacientes con útero extirpado:En el caso de una enfermedad en la que las células del revestimiento del útero se encuentran también en otros lugares fuera del útero (endometriosis), no se debe combinar el tratamiento con estrógenos con progestágenos si la paciente ha tenido una histerectomía. Si la paciente usa Oestrogel para tratar los síntomas posmenopáusicos y siente que el efecto de Oestrogel es demasiado fuerte o demasiado débil, debe consultar a su médico.
Duración del tratamiento
Su médico le informará durante cuánto tiempo debe usar Oestrogel. Es importante seguir esta recomendación. No debe dejar de usar el medicamento sin consultar antes a su médico.
Uso de una dosis mayor de la recomendada de Oestrogel
Los síntomas desagradables en los senos (tensión en los senos), sangrado o nerviosismo pueden ser signos de sobredosis, que generalmente desaparecen después de reducir la cantidad de gel utilizado.
En estos casos, debe reducir la dosis de Oestrogel con el consentimiento de su médico.
Si usa una dosis mayor de la recomendada de Oestrogel, debe consultar a su médico o farmacéutico de inmediato.
Olvido de una dosis de Oestrogel
No debe usar una dosis doble al día siguiente para compensar la dosis olvidada. Si faltan menos de 12 horas para la próxima dosis, debe tomar la dosis a la hora habitual. Si faltan más de 12 horas para la próxima dosis, debe tomar la dosis olvidada de inmediato y tomar la próxima dosis a la hora habitual.
Si es necesaria una operación
Antes de la operación, debe informar al cirujano sobre el uso de Oestrogel. Puede ser necesario dejar de usar Oestrogel 4 a 6 semanas antes de la operación para reducir el riesgo de trombosis [véase el punto 2 „Trombosis venosa (trombosis)”]. Debe consultar a su médico sobre cuándo puede volver a usar Oestrogel.
Si tiene alguna duda adicional sobre el uso de este medicamento, debe consultar a su médico o farmacéutico.
4. Posibles efectos adversos
Como todos los medicamentos, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Las siguientes enfermedades se informan con más frecuencia en mujeres que usan la THS que en mujeres que no la usan:
o cáncer de mama,
o crecimiento anormal o cáncer del endometrio (hiperplasia o cáncer del endometrio),
o cáncer de ovario,
o coágulos de sangre en las piernas o los pulmones (enfermedad tromboembólica venosa),
o enfermedades cardíacas,
o accidente cerebrovascular,
o riesgo de demencia, si se inicia la THS después de los 65 años.
Más información sobre estos efectos adversos se encuentra en el punto 2.
Frecuentes: pueden ocurrir en hasta 1 de cada 10 personas:dolores menstruales, sangrados menstruales abundantes, sangrado leve (manchado), problemas menstruales, secreción vaginal, sangrado vaginal inesperado, hiperplasia endometrial (crecimiento anormal del revestimiento del útero), dolores y calambres abdominales, hinchazón abdominal, náuseas o vómitos, dolor de cabeza, calambres musculares, dolor en las extremidades, nerviosismo y depresión.
Poco frecuentes: pueden ocurrir en hasta 1 de cada 100 personas:tumor benigno de mama, pólipos uterinos, crecimiento de los miomas uterinos, crecimiento de las células del revestimiento del útero en lugares anormales, lo que causa dolor (endometriosis), dolor en los senos (mastodinia), empeoramiento de los tumores que dependen de los estrógenos, migraña, mareo, somnolencia, dolores en las articulaciones (artralgia), trombosis venosa superficial o profunda, dolor y hinchazón de las venas (tromboflebitis), hinchazón de las manos, pies y tobillos (edema periférico), picazón, retención de sodio en el cuerpo, sensación de hinchazón, erupción cutánea, prurito, manchas marrones en la piel (melasma), resultados anormales de las pruebas hepáticas, tumores hepáticos, cálculos biliares.
Raros: pueden ocurrir en hasta 1 de cada 1.000 personas:intolerancia a las lentes de contacto, reacciones alérgicas graves (que pueden ser mortales), resultados anormales de las pruebas hepáticas, ictericia (color amarillo de la piel y los ojos) que indica trastornos hepáticos, intolerancia a la glucosa (especialmente en pacientes con diabetes), dolores óseos, empeoramiento de la epilepsia (convulsiones), cambios en el deseo sexual, manchas en la piel, acné, hipertensión arterial.
- tumores benignos y malignos que dependen de los estrógenos, como el cáncer del endometrio;
- infarto de miocardio y accidente cerebrovascular;
- enfermedades de la vesícula biliar;
- diversas enfermedades de la piel, como la purpura (pequeñas manchas de sangre bajo la piel);
- signos de demencia;
- la trombosis venosa y la embolia pulmonar ocurren con más frecuencia en personas que usan la THS que en personas que no la usan. Más información en el punto 2 „Cuándo no usar Oestrogel” y „THS y trombosis”.
- el riesgo de cáncer de mama es ligeramente mayor en mujeres que usan la THS y aumenta con la duración del uso de la THS. Se estima que el cáncer de mama ocurre en aproximadamente 32 de cada 1.000 mujeres de 50 a 64 años que no usan la THS. Se estima que en 1.000 mujeres que usan la THS durante 5 años o recientemente, ocurren 2 a 6 casos adicionales de cáncer de mama. En el caso de uso de la THS durante 10 años, este aumento puede ser de 5 a 19 casos adicionales por 1.000 usuarias. El número de casos adicionales de cáncer de mama no depende de la edad en la que se inicia el uso de la THS (siempre que se inicie entre los 45 y los 65 años). Más información en el punto 2 „Cuándo no usar Oestrogel” y „THS y cáncer de mama”.
- en mujeres con útero conservado que usan la THS que solo contiene estrógenos, el riesgo de cáncer del endometrio aumenta con la duración del uso de la THS. Se estima que en 1.000 mujeres de 50 a 65 años que no usan la THS, se diagnostica cáncer del endometrio en aproximadamente 5 mujeres. Dependiendo de la duración y la dosis, se estima que en 1.000 mujeres que usan solo estrógeno, se diagnostica cáncer del endometrio en 10-60 casos adicionales. En el caso de uso combinado de progestágeno, se puede evitar en gran medida este mayor riesgo. Se han informado los siguientes efectos adversos en el uso de otras THS:
- enfermedades de la vesícula biliar,
- diversas enfermedades de la piel:
- manchas marrones en la piel, especialmente en la cara o el cuello, llamadas „melasma”;
- erupciones cutáneas dolorosas y rojas (eritema nodoso);
- erupción cutánea con manchas rojas y anulares (eritema multiforme).
Informar de los efectos adversos
Si ocurren efectos adversos, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Los efectos adversos se pueden informar directamente al Departamento de Farmacovigilancia del Ministerio de Sanidad, Consumo y Bienestar Social, o al centro de farmacovigilancia de su comunidad autónoma.
La colaboración de los pacientes en la notificación de efectos adversos es importante para obtener más información sobre la seguridad de los medicamentos.
5. Cómo conservar Oestrogel
Debe conservar este medicamento en un lugar donde no pueda ser visto o alcanzado por los niños.
Este medicamento no requiere condiciones especiales de conservación.
No debe usar este medicamento después de la fecha de caducidad que se indica en el paquete después de „CADUCIDAD”. La fecha de caducidad es el último día del mes indicado. El código „LOTE” es el número de lote.
No debe tirar los medicamentos por el desagüe ni a los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se necesitan. Este comportamiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Oestrogel?
- El principio activo de Oestrogel es estradiol (Estradiolum).
- Los demás componentes son: etanol 96% (véase el punto 2 Oestrogel contiene etanol), carboxipolimetilcelulosa, trietanolamina y agua purificada.
Cómo se presenta Oestrogel y qué contiene el paquete?
Oestrogel está disponible en paquetes que contienen 1, 2 o 3 recipientes multidosis. Cada paquete de 80 g consiste en un recipiente con un dispositivo dosificador. Un presionado del dosificador proporciona 1,25 g de gel que contiene 0,75 mg de estradiol. Cada recipiente contiene 80 g de gel y proporciona al menos 60 dosis de 1,25 g.
No todas las tallas de paquete pueden estar disponibles en el mercado.
Titular de la autorización de comercialización
Besins Healthcare SA
Calle Washington 80
1050 Ixelles – Bélgica
Fabricante
Besins Manufacturing Belgium
Calle Groot-Bijgaardenstraat, 128 – B-1620 Drogenbos – Bélgica
o
Laboratoires Besins International
Calle Périer, 13
Montrouge 92120
Francia
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo bajo los siguientes nombres:
Bélgica – Estradiol Besins 0,75 mg/dosis gel transdérmico
Bulgaria - Естрогел 0,75 mg/доза трансдермален гел
República Checa - Estradiol Besins 0,75 mg/dávka transdermální gel
Croacia - Estradiol Besins 0,75 mg po potisku transdermalni gel
Estonia - Estradiol Besins 0,75mg/annus transdermaalne geel
Lituania – Estradiol Besins 0,75 mg / dozėje transderminis gelis
Luxemburgo – Estradiol Besins 0,75 mg/ dose transdermal gel
Letonia - Estradiol Besins 0,75 mg/devā transdermālais gels
Países Bajos - Oestrogel 0,75 mg/dosis transdermale gel
Noruega - Estrogel 0,75 mg/dose transdermalgel
Polonia – Oestrogel, 0,75 mg/dosis, gel transdérmico
Rumania - Estradiol Besins 0,75 mg/doză gel transdermic
Eslovaquia - Estradiol Besins 0,75 mg/dávka transdermálny gél
Eslovenia - Estradiol Besins 0,75 mg/potisk transdermalni gel
Suecia - Estrogel 0,75 mg/dos transdermal gel
Hungría - Estradiol Besins 0,75 mg/adag transzdermális gél
Fecha de la última revisión del prospecto: 12/2023
- País de registro
- Principio activo
- Requiere recetaNo
- ImportadorBesins Manufacturing Belgium Laboratoires Besins International
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a OestrogelForma farmacéutica: Gel, 0.5 mgPrincipio activo: EstradiolFabricante: Orion CorporationRequiere recetaForma farmacéutica: Gel, 1 mgPrincipio activo: EstradiolFabricante: Orion CorporationRequiere recetaForma farmacéutica: Gel, 1 mg/gPrincipio activo: EstradiolRequiere receta
Alternativas a Oestrogel en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Oestrogel en España
Alternativa a Oestrogel en Ucrania
Médicos online para Oestrogel
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Oestrogel – sujeta a valoración médica y normativa local.










