

Octaplex

Consulta con un médico sobre la receta médica de Octaplex

Cómo usar Octaplex
HOJA DE INSTRUCCIONES DEL PAQUETE: INFORMACIÓN PARA EL USUARIO
Octaplex, 500 UI, polvo y disolvente para la preparación de una solución para infusión
Complejo de protrombina humana
Octaplex, 1000 UI, polvo y disolvente para la preparación de una solución para infusión
Complejo de protrombina humana
Es importante leer atentamente el contenido de la hoja de instrucciones antes de usar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a un médico, farmacéutico o enfermera.
- Este medicamento ha sido recetado específicamente para una persona. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es Octaplex y para qué se utiliza
- 2. Información importante antes de usar Octaplex
- 3. Cómo usar Octaplex
- 4. Posibles efectos adversos
- 5. Cómo conservar Octaplex
- 6. Contenido del paquete y otra información
1. QUÉ ES OCTAPLEX Y PARA QUÉ SE UTILIZA
Octaplex pertenece a un grupo de medicamentos llamados factores de coagulación. Contiene factores de coagulación humanos dependientes de la vitamina K II, VII, IX y X.
Octaplex se utiliza para tratar y prevenir hemorragias:
- causadas por el tratamiento con antagonistas de la vitamina K (como la warfarina). Estos medicamentos bloquean la acción de la vitamina K y causan una deficiencia de factores de coagulación dependientes de la vitamina K. Octaplex se utiliza cuando se requiere una corrección rápida de la deficiencia;
- en pacientes nacidos con deficiencia de factores de coagulación II y X dependientes de la vitamina K. Se administra cuando no está disponible un producto purificado de ese factor de coagulación.
2. INFORMACIÓN IMPORTANTE ANTES DE USAR OCTAPLEX
Cuándo no usar Octaplex:
- si el paciente es alérgico a alguno de los componentes de este medicamento (enumerados en el punto 6),
- si el paciente tiene alergia a la heparina o ha experimentado una disminución del recuento de plaquetas después de la heparina en el pasado.
- si el paciente tiene deficiencia de IgA con anticuerpos contra IgA.
Advertencias y precauciones
- Debe consultar a un especialista con experiencia en el tratamiento de trastornos de la coagulación mientras recibe Octaplex.
- En pacientes con deficiencia adquirida de factores de coagulación dependientes de la vitamina K (por ejemplo, causada por el tratamiento con antagonistas de la vitamina K), Octaplex debe usarse solo cuando sea necesario una corrección rápida del nivel de complejo de protrombina, como en el caso de hemorragias graves o procedimientos quirúrgicos de emergencia. En otros casos, la reducción de la dosis de antagonistas de la vitamina K y / o la administración de vitamina K suele ser suficiente.
- Los pacientes tratados con antagonistas de la vitamina K (como la warfarina) pueden tener un mayor riesgo de formación de coágulos. En este caso, el tratamiento con Octaplex puede aumentar el riesgo.
- En la deficiencia congénita de un factor de coagulación dependiente de la vitamina K, debe usarse un producto específico de ese factor de coagulación si está disponible.
- En caso de reacción alérgica o anafiláctica, la infusión debe detenerse inmediatamente y se debe administrar el tratamiento adecuado.
- Existe un riesgo de trombosis o síndrome de coagulación intravascular diseminada (una enfermedad grave que implica la formación de coágulos en todo el cuerpo) en pacientes que reciben Octaplex (especialmente cuando se administra de forma regular). Los pacientes que reciben complejo de protrombina humana deben ser monitoreados de cerca para detectar signos y síntomas de síndrome de coagulación intravascular diseminada y trombosis. Esto es especialmente importante en pacientes con enfermedad cardíaca isquémica en su historia, enfermedad hepática, pacientes que están a punto de someterse a una operación y cuando Octaplex se administra a niños pequeños.
- No hay datos disponibles sobre el uso de Octaplex en caso de hemorragia posparto asociada con deficiencia de vitamina K en recién nacidos.
Seguridad viral
- En el caso de productos medicinales derivados de la sangre o el plasma humano, se aplican métodos adecuados para prevenir la transmisión de infecciones a los pacientes. Estos incluyen una selección estricta de donantes de sangre y plasma para eliminar a los portadores infectados, y la prueba de donaciones y pools de plasma para detectar marcadores virales específicos. Los fabricantes de estos productos también incorporan métodos adecuados en el proceso de fabricación para inactivar o eliminar los virus. A pesar de esto, en el caso de la administración de productos derivados de la sangre o el plasma humano, no se puede excluir completamente la posibilidad de transmisión de un agente infeccioso. Esto se aplica también a infecciones causadas por un virus desconocido o nuevo, o otros tipos de infecciones. Los métodos aplicados se consideran efectivos contra virus envueltos como el virus de la inmunodeficiencia humana (VIH), el virus de la hepatitis B (VHB) y el virus de la hepatitis C (VHC). Los métodos aplicados pueden tener una eficacia limitada contra virus no envueltos como el virus de la hepatitis A (VHA) o el parvovirus B19. El parvovirus B19 puede ser peligroso para las mujeres embarazadas (infección fetal) y para los pacientes con deficiencias del sistema inmunitario o que padecen una cierta forma de anemia (por ejemplo, anemia falciforme o anemia hemolítica). Se recomienda registrar el nombre y el número de lote del producto en cada administración de Octaplex para poder vincularlo con el lote utilizado.
- Se recomiendan las vacunas adecuadas (contra la hepatitis viral A y B) en caso de administración regular o repetida de productos de complejo de protrombina derivados del plasma humano.
Niños y adolescentes
No hay datos disponibles sobre el uso de Octaplex en niños y adolescentes.
Octaplex y otros medicamentos
No debe mezclarse Octaplex con otros productos medicinales.
Octaplex neutraliza el efecto del tratamiento con antagonistas de la vitamina K, pero no se conocen interacciones con otros
productos medicinales .
Octaplex puede afectar los resultados de las pruebas de coagulación que dependen de la heparina.
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando actualmente o que planea tomar.
Embarazo y lactancia
Octaplex debe usarse durante el embarazo y la lactancia solo si es estrictamente necesario. Antes de usar el producto, debe consultar a un médico o farmacéutico.
Conducción de vehículos y uso de máquinas
No se conoce el efecto de Octaplex en la capacidad para conducir vehículos o operar máquinas.
Información importante sobre algunos componentes de Octaplex
- La heparina puede causar reacciones alérgicas y una disminución del recuento de plaquetas. Los pacientes con reacciones alérgicas conocidas a la heparina deben evitar el uso de medicamentos que contengan heparina.
- El medicamento contiene 75-125 mg (frasco de 500 UI) o 150-250 mg (frasco de 1000 UI) de sodio (principal componente de la sal común) en cada frasco. Esto corresponde al 3,8-6,3% o 7,5-12,5% de la dosis diaria máxima recomendada de sodio en la dieta para adultos.
3. CÓMO USAR OCTAPLEX
El tratamiento con Octaplex debe iniciarse bajo la supervisión de un médico especialista en el tratamiento de trastornos de la coagulación.
- Primero, el polvo debe disolverse en agua para inyección.
- Luego, la solución debe administrarse por vía intravenosa.
La dosis de Octaplex y la duración del tratamiento dependen de:
- la gravedad de la enfermedad;
- el lugar de la hemorragia, su gravedad y
- el estado general del paciente.
Uso de una dosis mayor que la recomendada de Octaplex
En caso de sobredosis, aumenta el riesgo de
- desarrollo de complicaciones trombóticas (como infarto de miocardio y trombosis en las venas o los pulmones),
- coagulación intravascular diseminada (una enfermedad grave que implica la formación de coágulos en todo el cuerpo).
4. POSIBLES EFECTOS ADVERSOS
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Frecuentes (pueden ocurrir en hasta 1 de cada 10 personas)
Coágulos en los vasos sanguíneos.
Poco frecuentes (pueden ocurrir en hasta 1 de cada 100 personas)
Ansiedad, aumento de la presión arterial, síntomas que recuerdan al asma, tos con sangre, sangrado nasal, ardor en el lugar de la inyección, coágulos en el dispositivo.
Raros (pueden ocurrir en hasta 1 de cada 1000 personas)
Pueden ocurrir reacciones alérgicas. Raramente se observa un aumento temporal de los resultados de las pruebas hepáticas (transaminasas).
En pacientes tratados con Octaplex para la terapia de reemplazo, pueden desarrollarse anticuerpos neutralizantes (inhibidores) contra alguno de los factores de coagulación contenidos. En caso de que aparezcan estos inhibidores, el tratamiento de reemplazo no será muy efectivo.
Muy raros (pueden ocurrir en hasta 1 de cada 10 000 personas)
Se han observado casos de aumento de la temperatura corporal (fiebre).
Existe un riesgo de formación de coágulos después de la administración de este medicamento.
Frecuencia no conocida (la frecuencia no puede determinarse a partir de los datos disponibles)
Reacciones alérgicas graves y shock, hipersensibilidad, temblor, insuficiencia cardíaca, taquicardia, trastornos de la circulación, hipotensión, insuficiencia respiratoria, trastornos de la respiración, náuseas, urticaria, erupciones, escalofríos.
La heparina contenida en el producto puede causar una disminución repentina del recuento de plaquetas. Esta es una reacción alérgica llamada "trombocitopenia inducida por heparina tipo II". En casos raros, esta disminución del recuento de plaquetas puede ocurrir 6-14 días después del inicio del tratamiento en pacientes sin hipersensibilidad previa a la heparina. En pacientes con hipersensibilidad conocida a la heparina, este cambio puede ocurrir dentro de unas horas después del inicio del tratamiento.
Debe interrumpirse inmediatamente el tratamiento con Octaplex en pacientes que experimenten esta reacción alérgica. A estos pacientes no se les debe administrar en el futuro productos medicinales que contengan heparina.
Información sobre la seguridad viral, véase el punto 2.
Notificación de efectos adversos
Si ocurren algún efecto adverso, incluidos cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad,
Al. Jerozolimskie 181C, 02-222 Varsovia,
tel.: + 48 22 49 21 301, fax: + 48 22 49 21 309
correo electrónico: [email protected].
La notificación de efectos adversos permite recopilar más información sobre la seguridad del medicamento.
5. CÓMO CONSERVAR OCTAPLEX
El medicamento debe conservarse en un lugar fuera del alcance de los niños.
No debe usarse este medicamento después de la fecha de caducidad indicada en el paquete. La fecha de caducidad es el último día del mes indicado.
No debe conservarse a una temperatura superior a 25°C. No debe congelarse. Debe conservarse en el paquete original para protegerlo de la luz.
El polvo debe disolverse solo inmediatamente antes de la inyección. Se ha demostrado la estabilidad de la solución durante un período de hasta 8 horas a 25°C. Sin embargo, para evitar la contaminación, la solución debe usarse de inmediato y solo una vez.
6. CONTENIDO DEL PAQUETE Y OTRA INFORMACIÓN
Qué contiene Octaplex en el frasco y después de la reconstitución en 20 ml (500 UI) / 40 ml (1000 UI)
de disolvente
Los principios activos son:
| Nombre del principio activo | Octaplex Contenido en frasco 500 UI | Octaplex Contenido en frasco 1000 UI | Octaplex Contenido en 1 ml de solución reconstituida |
| Proteína total: | 260–820 mg | 520–1640 mg |
|
| Principios activos | |||
| Factor de coagulación humano II | 280–760 UI | 560–1520 UI |
|
| Factor de coagulación humano VII | 180–480 UI | 360–960 UI |
|
| Factor de coagulación humano IX | 500 UI | 1000 UI | 25 UI/ml |
| Factor de coagulación humano X | 360–600 UI | 720–1200 UI |
|
| Principios activos adicionales | |||
| Proteína C | 260–620 UI | 520–1240 UI |
|
| Proteína S | 240–640 UI | 480–1280 UI |
|
La actividad específica del producto es ≥ 0,6 UI/mg, expresada como actividad del factor IX.
Los demás componentes son:
heparina, citrato de trisodio dihidratado, agua para inyección.
Cómo se presenta Octaplex y qué contiene el paquete
Octaplex se presenta en forma de polvo y disolvente para la preparación de una solución para infusión. Es un polvo higroscópico, blanco o ligeramente coloreado, o una masa quebradiza en un frasco de vidrio.
El disolvente es agua para inyección suministrada en un frasco de vidrio. La solución reconstituida es clara o ligeramente opalescente y puede estar coloreada.
Octaplex se vende en una caja individual que contiene:
- 1 frasco con polvo para la preparación de una solución para infusión
- 1 frasco con disolvente, agua para inyección
- 1 conjunto de transferencia Nextaro.
Titular de la autorización de comercialización y fabricante
Octapharma (IP) SPRL
Allée de la Recherche 65
1070 Anderlecht
Bélgica
Para obtener información más detallada, debe ponerse en contacto con el representante local del titular de la autorización de comercialización:
Octapharma Poland Sp. z o.o.
ul. Domaniewska 39a
02-135 Varsovia
tel. (22) 415-51-42
Fabricantes:
Octapharma Pharmazeutika Produktionsges.m.b.H.
Oberlaaer Str. 235
1100 Viena
Austria
Octapharma Lingolsheim S.A.S.
72 Rue du Maréchal Foch
67380 Lingolsheim
Francia
Este medicamento está autorizado para su comercialización en los estados miembros del Espacio Económico Europeo bajo los siguientes nombres:
Nombres del medicamento en otros países:
Austria, Bélgica, Bulgaria, Croacia, Chipre, Dinamarca, Estonia, Finlandia, Francia, Alemania, Hungría,
Islandia, Irlanda, Letonia, Lituania, Luxemburgo, Malta, Países Bajos, Noruega, Polonia, Portugal,
Eslovenia, Eslovaquia, España, Reino Unido: Octaplex
República Checa, Suecia: Ocplex
Italia, Rumania: Pronativ
Fecha de la última revisión de la hoja de instrucciones: 06.07.2024 -------------------------------------------------------------------------------------------------------------------------
INFORMACIÓN PARA EL PERSONAL MÉDICO
La información general sobre el uso de Octaplex se presenta en el punto 3.
La siguiente información es solo para el personal médico o los trabajadores de la salud:
Instrucciones para el tratamiento
Debe leer todas las instrucciones y seguir las mismas!
Debe garantizarse la esterilidad durante las siguientes operaciones!
El producto se disuelve rápidamente a temperatura ambiente.
La solución reconstituida debe ser transparente o ligeramente opalescente.
No debe usarse si la solución es turbia o contiene partículas sólidas.
Antes de la administración, debe evaluar visualmente si la solución contiene partículas sólidas o ha cambiado de color.
Después de la reconstitución, la solución debe usarse de inmediato.
Debe eliminarse cualquier resto del producto no utilizado o material utilizado de acuerdo con las regulaciones locales.
Dosificación
Hemorragias y profilaxis de hemorragias en el tratamiento con antagonistas de la vitamina K:
La dosis depende del INR antes del tratamiento y del peso corporal. En la tabla se indican las dosis aproximadas (en UI/kg de peso corporal de producto reconstituido).
| INR antes del tratamiento |
|
| > 6 |
| Dosis de producto (UI de factor IX) / kg de peso corporal | 25 | 35 | 50 |
La dosis se determina en función de un peso corporal máximo de 100 kg. Por lo tanto, en el caso de pacientes con un peso corporal superior a 100 kg, la dosis máxima única (UI de factor IX) no debe exceder los 2500 UI para un INR de 2 a <4, 3500 UI para un INR de 4 a 6 y 5000 UI para un INR > 6.
- La dosis se calcula en función de los datos experimentales, y la recuperación y la duración del efecto pueden variar, por lo que es obligatorio el monitoreo del INR durante el tratamiento.
Hemorragias y profilaxis de hemorragias durante los procedimientos quirúrgicos en la deficiencia congénita de factores de coagulación II y X dependientes de la vitamina K, cuando no esté disponible el producto específico de ese factor de coagulación:
La dosis necesaria se calcula en función de los datos experimentales, de modo que aproximadamente 1 UI de factor II o X por kg de peso corporal aumenta la actividad del factor II o X en el suero en 0,02 y 0,017 UI/ml, respectivamente.
Instrucciones para la reconstitución:
- 1. Si es necesario, llevar el disolvente (agua para inyección) y el polvo en frascos cerrados a temperatura ambiente. Esta temperatura debe mantenerse durante la reconstitución. Si se utiliza un baño de agua para calentar, debe tener cuidado de evitar el contacto del agua con los tapones de goma o las tapas de los frascos. La temperatura del baño de agua no debe exceder los 37°C.
- 2. Retirar las tapas de "flip-off" de los frascos con el polvo y el disolvente, y desinfectar adecuadamente los tapones de goma.
- 3. Retirar la tapa del paquete exterior del conjunto Nextaro. Colocar el frasco con el disolvente sobre una superficie plana y sostenerlo firmemente. Sin retirar el paquete exterior, colocar la parte azul del Nextaro sobre el frasco con el disolvente y presionar firmemente hasta que se bloquee (fig. 1). No girar durante la conexión. Sostener el frasco con el disolvente y retirar cuidadosamente el paquete exterior del conjunto Nextaro, teniendo cuidado de dejar el conjunto Nextaro firmemente unido al frasco con el disolvente (fig. 2)
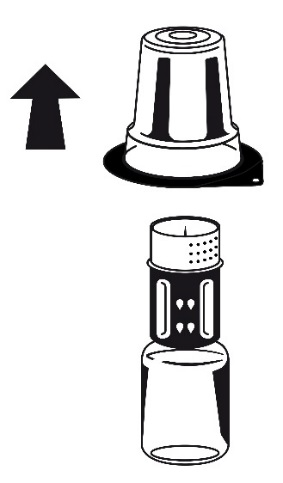
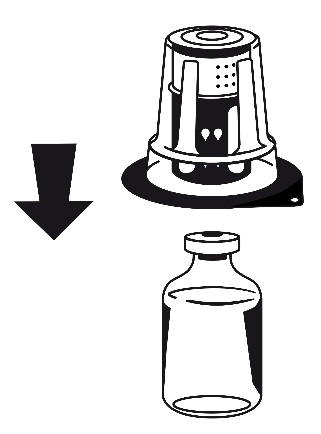
Fig. 2
Fig. 1
- 4. Colocar el frasco con el polvo sobre una superficie plana y sostenerlo firmemente. Tomar el frasco con el disolvente con el conjunto Nextaro conectado y girarlo hacia abajo. Colocar la parte transparente blanca del conector Nextaro sobre el frasco con el polvo y presionar firmemente hasta que se bloquee (fig. 3). No girar durante la conexión. El disolvente fluye automáticamente hacia el frasco con el polvo.
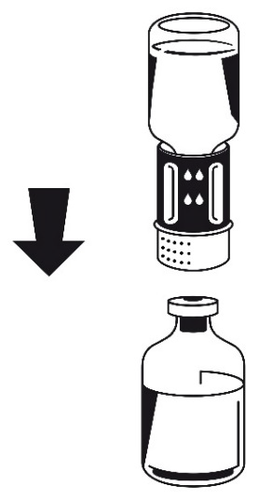
Fig. 3
- 5. Con ambos frascos aún conectados, girar suavemente el frasco con el polvo hasta que el producto esté disuelto. Octaplex se disuelve rápidamente a temperatura ambiente, dando una solución transparente o ligeramente azulada. Desenroscar el Nextaro en dos partes (fig. 4).
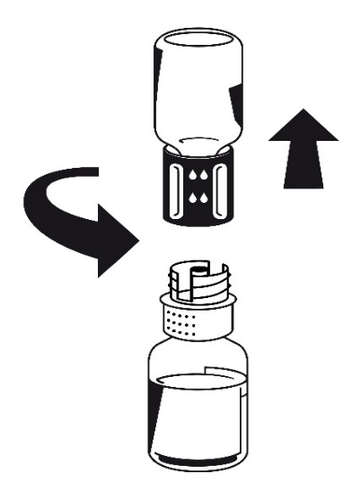
Desechar el frasco vacío con el disolvente con
la parte azul del Nextaro.
Fig. 4
Si el polvo no se disuelve completamente o se forma una sustancia sólida, no debe usarse el producto.
Instrucciones para la infusión:
Como medida de precaución, debe evaluarse el pulso del paciente antes y durante la infusión del factor IX. Si
aparece un aumento significativo del pulso, debe reducirse la velocidad de infusión o interrumpirse la administración.
- 1. Conectar una jeringa de 20 ml (en el caso de un frasco de 500 UI) o 40 ml (en el caso de un frasco de 1000 UI) al conector luer lock en la parte blanca del Nextaro. Girar el frasco hacia abajo y aspirar la solución a la jeringa. Después de transferir la solución, sostener firmemente el émbolo de la jeringa (sostener hacia abajo) y retirar la jeringa del Nextaro. Desechar el Nextaro y el frasco vacío.
- 2. Desinfectar adecuadamente el lugar de la inyección.
- 3. Inyectar la solución por vía intravenosa a una velocidad de 0,12 ml/kg/min (~3 UI/kg/min), hasta un máximo de 8 ml/min (~210 UI/min), en condiciones estériles.
No debe entrar sangre en la jeringa debido al riesgo de formación de coágulos de fibrina.
El conjunto Nextaro está diseñado solo para un uso único.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorOctapharma Pharmazeutika Produktionsgesellschaft mbH (OPG)
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a OctaplexForma farmacéutica: Polvo, 1000 UIPrincipio activo: Coagulation factor IX, II, VII and X in combinationRequiere recetaForma farmacéutica: Polvo, 250 UIPrincipio activo: Coagulation factor IX, II, VII and X in combinationRequiere recetaForma farmacéutica: Polvo, 500 UIPrincipio activo: Coagulation factor IX, II, VII and X in combinationRequiere receta
Alternativas a Octaplex en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Octaplex en España
Alternativa a Octaplex en Ucrania
Médicos online para Octaplex
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Octaplex – sujeta a valoración médica y normativa local.














