
Multimel N7-1000e

Consulta con un médico sobre la receta médica de Multimel N7-1000e

Cómo usar Multimel N7-1000e
Hoja de instrucciones del paquete: información para el usuario
Multimel N7-1000 E, emulsión para infusión
Debe leer el contenido de la hoja de instrucciones antes de usar el medicamento, ya que contiene información
importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- Si tiene alguna duda adicional, debe consultar a su médico o enfermera.
- Si el paciente experimenta algún efecto adverso, incluidos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico o enfermera. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es Multimel N7-1000 E y para qué se utiliza
- 2. Información importante antes de administrar Multimel N7-1000 E
- 3. Cómo administrar Multimel N7-1000 E
- 4. Posibles efectos adversos
- 5. Cómo conservar Multimel N7-1000 E
- 6. Contenido del paquete y otra información
1. Qué es Multimel N7-1000 E y para qué se utiliza
Multimel N7-1000 E es una emulsión para infusión. Se presenta en una bolsa de tres cámaras.
La primera cámara contiene una solución de glucosa con calcio, la segunda cámara contiene una emulsión grasosa, y
la tercera cámara contiene una solución de aminoácidos con electrolitos.
Grupo farmacoterapéutico: líquidos para nutrición parenteral/mezclas.
Multimel N7-1000 E se administra para la nutrición parenteral de adultos y niños mayores de 2 años,
cuando la nutrición oral no es adecuada.
Multimel N7-1000 E debe administrarse únicamente bajo supervisión médica.
2. Información importante antes de administrar Multimel N7-1000 E
Cuándo no debe administrarse Multimel N7-1000 E:
- en el caso de prematuros, lactantes y niños menores de 2 años;
- si el paciente es alérgico a los huevos, la soja, las proteínas de cacahuate, el maíz/productos que contienen maíz (véase también el punto "Advertencias y precauciones" a continuación) o cualquier otro componente de Multimel N7-1000 E;
- si la administración de algunos aminoácidos provoca una reacción anormal en el paciente;
- si el paciente tiene una concentración de grasas en la sangre muy alta (hiperlipidemia);
- -si el paciente tiene hiperglucemia severa (concentración de azúcar en la sangre demasiado alta);
- si el paciente tiene una concentración anormalmente alta de algún electrolito (sodio, potasio, magnesio, calcio y/o fosforo) en la sangre.
En cada caso, el médico tomará la decisión de administrar el medicamento en función de factores como la edad,
el peso del paciente y su estado clínico, teniendo en cuenta los resultados de las pruebas realizadas.
Advertencias y precauciones
Antes de comenzar a recibir Multimel N7-1000 E, debe discutirlo con su médico o enfermera.
La administración demasiado rápida de soluciones para la nutrición parenteral total puede ser mortal.
Si se producen síntomas o signos de reacción alérgica, como fiebre, escalofríos, erupción cutánea o dificultad para respirar, sudoración excesiva, náuseas y dolor de cabeza,
la infusión debe interrumpirse de inmediato. El medicamento contiene aceite de soja y fosfatidas de huevo de gallina. Las proteínas de la soja y el huevo pueden provocar reacciones de hipersensibilidad. Se han observado reacciones alérgicas cruzadas entre las proteínas de la soja y los cacahuetes.
Multimel N7-1000 E contiene glucosa derivada del maíz, que puede provocar reacciones de hipersensibilidad si el paciente es alérgico al maíz o a productos que contienen maíz (véase el punto "Cuándo no debe administrarse Multimel N7-1000 E" anterior).
La dificultad para respirar también puede ser un síntoma de la formación de pequeñas partículas que bloquean los vasos sanguíneos en los pulmones (precipitados en los vasos pulmonares). Debe informar a su médico o enfermera si experimenta dificultad para respirar. Ellos decidirán el curso de acción.
El antibiótico ceftriaksona no debe mezclarse ni administrarse al mismo tiempo que cualquier solución que contenga calcio y se administre por goteo en una vena (incluyendo Multimel N7-1000 E).
Estos medicamentos no deben administrarse al mismo tiempo, incluso a través de diferentes líneas de infusión o diferentes sitios de inyección.
Sin embargo, Multimel N7-1000 E y ceftriaksona pueden administrarse uno después del otro, siempre que las líneas de infusión se cambien o se hayan lavado cuidadosamente con solución salina fisiológica entre las infusiones, para evitar la formación de un precipitado (formación de partículas de sales de ceftriaksona-calcio).
El médico controlará y monitoreará la concentración de triglicéridos (un tipo de grasa que se encuentra en la sangre).
Algunos medicamentos y enfermedades pueden aumentar el riesgo de infección o sepsis (presencia de bacterias en la sangre). El riesgo de infección o sepsis es particularmente alto después de la inserción de un catéter (catéter venoso) en la vena del paciente. El médico vigilará atentamente al paciente para detectar cualquier síntoma de infección. Los pacientes que requieren nutrición parenteral (administración de nutrientes a través de un tubo en una vena) pueden estar más expuestos a la infección debido a su estado clínico. El uso de técnicas asépticas (libres de gérmenes) durante la inserción y el mantenimiento del catéter, así como durante la preparación del medicamento para la nutrición, puede reducir el riesgo de infección.
Debe informar a su médico:
- sobre enfermedades renales graves. También debe informar a su médico si el paciente está sometido a diálisis (riñón artificial) u otros métodos de limpieza de la sangre;
- sobre enfermedad hepática grave;
- sobre trastornos de la coagulación de la sangre;
- sobre disfunción suprarrenal (insuficiencia suprarrenal). Las glándulas suprarrenales son glándulas con forma de triángulo que se encuentran en la parte superior de los riñones;
- sobre insuficiencia cardíaca;
- sobre enfermedad pulmonar;
- sobre retención de líquidos en el cuerpo (sobrehidratación);
- sobre falta de líquidos en el cuerpo (deshidratación);
- sobre diabetes no tratada;
- sobre infarto de miocardio o shock causado por la insuficiencia cardíaca repentina;
- sobre acidosis metabólica grave (pH de la sangre demasiado ácido);
- sobre sepsis generalizada;
- sobre coma.
Si el paciente es un niño, el médico controlará cuidadosamente el estado de los líquidos y los parámetros sanguíneos.
Se han notificado casos de síndrome de sobrecarga de grasas durante el uso de Multimel y medicamentos similares. La capacidad reducida o limitada del cuerpo para eliminar las grasas contenidas en Multimel N7-1000 E puede provocar un "síndrome de sobrecarga de grasas" (véase el punto 4 - "Posibles efectos adversos").
No debe agregar componentes adicionales a la bolsa sin verificar antes su compatibilidad. Esto podría provocar la formación de partículas o alterar la estabilidad de la emulsión grasosa. Esto puede provocar la obstrucción de los vasos sanguíneos.
Si la concentración de glucosa en la sangre aumenta demasiado, el médico debe ajustar la velocidad de administración de Multimel N7-1000 E o administrar insulina al paciente.
En casos de desnutrición grave que requieren la administración de nutrientes por vía intravenosa, se recomienda comenzar la nutrición parenteral de manera lenta y con precaución.
Antes de iniciar la infusión, debe corregir los trastornos del equilibrio hidroelectrolítico y los trastornos metabólicos del paciente. El médico controlará el estado del paciente durante la terapia y puede cambiar la dosis o, si lo considera necesario, recomendar componentes nutricionales adicionales, como vitaminas, electrolitos y oligoelementos.
Durante la administración del medicamento, el médico realizará pruebas clínicas y de laboratorio para evaluar la eficacia y controlar la seguridad de la administración del medicamento. Si el paciente recibe el medicamento durante varias semanas, se realizarán pruebas de sangre de manera regular. Estas pruebas son particularmente necesarias en caso de ciertas enfermedades, como la insuficiencia hepática, la insuficiencia renal, la enfermedad en la que los aminoácidos no pueden ser procesados correctamente por el cuerpo, la enfermedad en la que la sangre tiene un pH demasiado ácido, la enfermedad en la que la concentración de grasas y colesterol es mayor que la normal, la diabetes, la anemia o los trastornos de la coagulación de la sangre.
Si durante la infusión se produce dolor, ardor, rigidez, hinchazón o decoloración de la piel en el sitio de infusión o fugas de la infusión, debe informar a su médico o enfermera. La administración se interrumpirá de inmediato y se reanudará en una vena diferente.
Niños
Si el paciente es un niño, debe tener especial cuidado para administrar la dosis correcta.
Puede ser necesario un suministro adicional de vitaminas y oligoelementos, dependiendo de la dosis y la duración de la administración. Debido a la mayor sensibilidad de los niños al riesgo de infección, también se deben tomar medidas de precaución adicionales.
Multimel N7-1000 E y otros medicamentos
Debe informar a su médico o enfermera sobre todos los medicamentos que el paciente esté tomando actualmente o haya tomado recientemente, así como sobre cualquier medicamento que el paciente planea tomar.
No debe administrarse Multimel N7-1000 E al mismo tiempo que la sangre a través del mismo conjunto de infusión.
Multimel N7-1000 E contiene calcio. No debe administrarse con el antibiótico ceftriaksona o a través del mismo tubo, ya que pueden formarse partículas. Si se utiliza el mismo conjunto de administración de estos medicamentos al paciente, debe administrarse uno después del otro, y el conjunto debe lavarse cuidadosamente.
El aceite de oliva y el aceite de soja presentes en Multimel N7-1000 E contienen vitamina K. Por lo general, esto no afecta la acción de los medicamentos anticoagulantes, como la warfarina. Sin embargo, si el paciente está tomando medicamentos anticoagulantes, debe informar a su médico.
Las grasas contenidas en esta emulsión pueden alterar los resultados de algunas pruebas de laboratorio, siempre que las muestras de sangre se hayan tomado antes de que se eliminen las grasas (las grasas suelen eliminarse después de aproximadamente 5-6 horas después de dejar de administrarlas).
Multimel N7-1000 E con electrolitos contiene potasio. Debe tener especial cuidado en caso de pacientes que estén tomando diuréticos, inhibidores de la enzima convertidora de angiotensina (ECA), antagonistas del receptor de angiotensina II (medicamentos utilizados para la hipertensión) o medicamentos inmunosupresores.
Este tipo de medicamentos puede provocar un aumento de la concentración de potasio en la sangre.
Embarazo y lactancia
Si la paciente está embarazada o en período de lactancia, o si cree que puede estar embarazada o planea tener un hijo, debe consultar a su médico antes de tomar este medicamento.
3. Cómo administrar Multimel N7-1000 E
Multimel N7-1000 E solo se puede administrar a adultos y niños mayores de 2 años.
Es una emulsión para infusión que se administra a través de un tubo de plástico en una vena grande en el pecho del paciente.
El tratamiento puede continuar durante el tiempo que sea necesario, dependiendo del estado clínico del paciente.
Multimel N7-1000 E está destinado solo para un uso único.
Dosis - Adultos
La dosis se determina según las necesidades individuales y el estado clínico del paciente.
La dosis máxima diaria es de 33 ml/kg de peso corporal. Por ejemplo: para un paciente de 70 kg,
la dosis máxima diaria no debe exceder los 2310 ml de emulsión para infusión (33 ml de emulsión para infusión multiplicado por 70 kg).
Dosis - Niños mayores de 2 años
La dosis del medicamento para un niño y el período de administración se determinan según la edad, el peso corporal, el crecimiento, el estado clínico, el volumen diario de líquidos y las necesidades de energía y azúcar.
Administración de una dosis mayor de la recomendada de Multimel N7-1000 E
Si se administra al paciente una dosis demasiado grande del medicamento o una infusión demasiado rápida, los aminoácidos contenidos pueden provocar un aumento de la acidez de la sangre y un aumento del volumen de líquido en el sistema circulatorio. La glucosa contenida en el medicamento puede aumentar la concentración de glucosa en la sangre y en la orina, y las grasas contenidas en la emulsión pueden aumentar la concentración de triglicéridos en la sangre. La administración de una cantidad excesiva de Multimel N7-1000 E puede provocar náuseas, vómitos, escalofríos, dolor en el pecho, dolor de cabeza, latido cardíaco irregular o acelerado y trastornos electrolíticos. En tal caso, debe interrumpirse de inmediato la infusión.
En algunos casos graves, para ayudar a los riñones del paciente a eliminar el exceso de medicamento, el médico puede recurrir a un tratamiento de diálisis de manera periódica.
Para evitar tales situaciones, el médico controlará regularmente el estado del paciente y verificará los parámetros sanguíneos.
En caso de duda sobre el uso del medicamento, debe consultar a su médico.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede provocar efectos adversos, aunque no todos los pacientes los experimentarán.
Si se producen cambios en el estado de ánimo durante el tratamiento o después de su finalización, debe informar a su médico o enfermera de inmediato.
Las pruebas realizadas por el médico durante el tratamiento tienen como objetivo minimizar el riesgo de efectos adversos.
Si se producen signos o síntomas de reacción alérgica, como fiebre, escalofríos, erupción cutánea o dificultad para respirar, sudoración excesiva, náuseas y dolor de cabeza, debe interrumpirse de inmediato la infusión.
Se han notificado los siguientes efectos adversos durante el uso de Multimel:
- reacciones alérgicas
Frecuencia: desconocida(no puede determinarse a partir de los datos disponibles)
- broncoespasmo, respiración silbante y (o) tos (broncoespasmo, como parte de una reacción alérgica)
- temblor
- diarrea, náuseas, vómitos
- enrojecimiento cutáneo anormal (rubor), sudoración excesiva
- dolor en las extremidades, calambres musculares
- fuga de la infusión en los tejidos circundantes (extravasación), que puede causar hinchazón/edema en el sitio de infusión, dolor, irritación y inflamación de la vena, enrojecimiento/calor, pérdida local de tejido, necrosis del tejido o ampollas
- fiebre, escalofríos, inflamación
- una capacidad reducida o limitada para eliminar las grasas contenidas en Multimel N7-1000 E puede provocar un "síndrome de sobrecarga de grasas". Puede ser el resultado de una sobredosis, pero también puede ocurrir al comienzo de la infusión, incluso cuando se administra el medicamento según las instrucciones. Se asocia con un empeoramiento repentino del estado clínico del paciente. Se caracteriza por una alta concentración de grasas en la sangre, fiebre, esteatosis hepática (alta concentración de grasas en el hígado) y (o) hepatomegalia. También puede ocurrir anemia (disminución del número de glóbulos rojos, que puede causar palidez, debilidad o falta de aliento), disminución del número de glóbulos blancos y plaquetas, trastornos de la coagulación de la sangre y (o) coma. Este síndrome suele desaparecer después de interrumpir la infusión de la emulsión grasosa.
Se han notificado los siguientes efectos adversos para medicamentos similares:
Frecuencia desconocida (no puede determinarse a partir de los datos disponibles)
- formación de pequeñas partículas, que puede provocar la obstrucción de los vasos sanguíneos en los pulmones (precipitados en los vasos pulmonares), lo que puede causar embolia pulmonar y dificultad para respirar (insuficiencia respiratoria)
- disminución del número de plaquetas (disminución del número de glóbulos que participan en la coagulación de la sangre, lo que puede causar hemorragias, como la hemorragia nasal)
- dificultad para eliminar la bilis (colestasis), hepatomegalia, ictericia (decoloración amarilla de la piel o la parte blanca de los ojos debido a trastornos hepáticos o sanguíneos)
- hipersensibilidad
- aumento de la actividad de las enzimas hepáticas, aumento de la concentración de grasas en la sangre (aumento de la concentración de triglicéridos en la sangre), aumento de la concentración de bilirrubina en la sangre
- aumento de la concentración de azoto en la sangre (azotemia)
Se han notificado casos de disminución del número de glóbulos blancos y plaquetas en niños.
Notificación de efectos adversos
Si se producen efectos adversos, incluidos los efectos adversos no mencionados en la hoja de instrucciones, debe informar a su médico o enfermera. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Efectos Adversos de Productos Farmacéuticos de la Agencia de Registro de Productos Farmacéuticos, Dispositivos Médicos y Productos Biocidas:
Al. Jerozolimskie 181 C
PL 02-222 Varsovia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Página web: https://smz.ezdrowie.gov.pl
Los efectos adversos también pueden notificarse al titular del producto.
La notificación de efectos adversos permitirá recopilar más información sobre la seguridad del medicamento.
5. Cómo conservar Multimel N7-1000 E
El medicamento debe conservarse en un lugar donde no pueda ser visto ni alcanzado por los niños.
No debe usar este medicamento después de la fecha de caducidad indicada en el envase y el paquete exterior. La fecha de caducidad es el último día del mes indicado.
No congelar.
Conservar en envase protector.
Conservar en caja de cartón exterior para proteger del sol.
No debe tirar los medicamentos por el desagüe ni por los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Multimel N7-1000 E?
Los principios activos presentes en cada bolsa de emulsión preparada:
Principios activos 1000 ml 1500 ml 2000 ml 2500 ml
Aceite de oliva purificado y
aceite de soja purificado*
100,00 g
L-alanina
8,28 g
12,42 g
16,56 g
20,70 g
L-arginina
4,60 g
6,90 g
9,20 g
11,50 g
Glicina
4,12 g
6,18 g
8,24 g
10,30 g
L-histidina
1,92 g
2,88 g
3,84 g
4,80 g
L-isoleucina
2,40 g
3,60 g
4,80 g
6,00 g
L-leucina
2,92 g
4,38 g
5,84 g
7,30 g
L-lisina
2,32 g
3,48 g
4,64 g
5,80 g
40,00 g
60,00 g
80,00 g
(lo que equivale a clorhidrato de lisina)
(2,90 g)
(4,35 g)
(5,80 g)
(7,25 g)
L-metionina
1,60 g
2,40 g
3,20 g
4,00 g
L-fenilalanina
2,24 g
3,36 g
4,48 g
5,60 g
L-prolina
2,72 g
4,08 g
5,44 g
6,80 g
L-serina
2,00 g
3,00 g
4,00 g
5,00 g
L-treonina
1,68 g
2,52 g
3,36 g
4,20 g
L-triptófano
0,72 g
1,08 g
1,44 g
1,80 g
L-tirosina
0,16 g
0,24 g
0,32 g
0,40 g
L-valina
2,32 g
3,48 g
4,64 g
5,80 g
Octanoato de sodio trihidratado
2,45 g
3,67 g
4,90 g
6,12 g
Glicerofosfato de sodio pentahidratado
2,14 g
3,22 g
4,29 g
5,36 g
Cloruro de potasio
1,79 g
2,68 g
3,58 g
4,47 g
Cloruro de magnesio hexahidratado
0,45 g
0,67 g
0,90 g
1,12 g
Glucosa
(lo que equivale a glucosa monohidratada)
400,00 g
(440,00 g)
Cloruro de calcio dihidratado
0,30 g
0,44 g
0,59 g
0,74 g
Valor energético total (kcal)
1200
1800
2400
3000
Valor energético no proteico (kcal)
1040
1560
2080
2600
160,00 g
(176,00 g)
240,00 g
(264,00 g)
320,00 g
(352,00 g)
Los demás componentes son fosfatidas de huevo de gallina purificadas, glicerol, oleato de sodio, hidróxido de sodio, ácido acético glacial, ácido clorhídrico, agua para inyección.
Cómo se presenta Multimel N7-1000 E y qué contiene el paquete?
Multimel N7-1000 E es una emulsión para infusión que se presenta en una bolsa de tres cámaras. La bolsa es una bolsa de plástico de varias capas. La capa interior (en contacto con el contenido de la bolsa) está hecha de polímeros (mezcla de copolímeros de poliolefinas) y es compatible con el contenido de la bolsa (soluciones de aminoácidos, soluciones de glucosa y emulsiones grasosas) y los aditivos permitidos, y permite la creación de soldaduras rompibles. Los polímeros utilizados para hacer la capa de recubrimiento se fabrican con EVA (acetato de polietilenvinilo) y copolímero de poliéster.
Antes de mezclar el contenido de las tres cámaras de la bolsa, la primera cámara contiene un líquido homogéneo de apariencia lechosa (emulsión grasosa), mientras que las dos cámaras restantes (que contienen la solución de aminoácidos con electrolitos y la solución de glucosa con calcio) contienen soluciones incoloras o ligeramente amarillentas,
prácticamente sin partículas visibles. Después de mezclar, Multimel N7-1000 E es una emulsión para infusión de apariencia homogénea y blanca lechosa.
La bolsa se coloca en un paquete protector que protege del oxígeno, que contiene una bolsa que absorbe el oxígeno.
Tamaños de los paquetes
Bolsa de 1000 ml: 6 bolsas en una caja de cartón
Bolsa de 1500 ml: 4 bolsas en una caja de cartón
Bolsa de 2000 ml: 4 bolsas en una caja de cartón
Bolsa de 2500 ml: 2 bolsas en una caja de cartón
No todos los tamaños de paquetes pueden estar en circulación.
Titular del producto:
Para obtener información sobre Multimel N7-1000 E, debe ponerse en contacto con el representante del titular del producto:
Baxter Polska Sp. z o.o.
ul. Kruczkowskiego 8
00-380 Varsovia
Fabricante:
Baxter S.A.
Boulevard René Branquart 80
7860 Lessines
Bélgica
Fecha de la última actualización de la hoja de instrucciones: 06.03.2020
--------------------------------------------------------------------------------------------------------------
Información destinada solo al personal médico especializado:
Multimel N7-1000 E, emulsión para infusión
1. COMPOSICIÓN CUANTITATIVA
Después de mezclar el contenido de las tres cámaras, la mezcla tiene la forma de una emulsión homogénea de apariencia lechosa.
La emulsión preparada después de la mezcla contiene los siguientes componentes en bolsas de diferentes tamaños:
** Incluyendo fosfatos contenidos en la emulsión grasosa
2. DOSIS Y MODO DE ADMINISTRACIÓN
La dosis se determina según el gasto energético, el estado clínico del paciente, el peso corporal y la capacidad para metabolizar los componentes del producto Multimel N7-1000 E, así como según los componentes energéticos o proteicos adicionales administrados por vía oral/enteral; por lo tanto, debe elegirse el tamaño de la bolsa adecuadamente.
La administración puede continuar durante el tiempo que sea necesario según el estado clínico del paciente.
| Por bolsa | 1000 ml | 1500 ml | 2000 ml | 2500 ml |
| Azúcar (g) | 6,6 | 9,9 | 13,2 | 16,5 |
| Aminoácidos (g) | 40 | 60 | 80 | 100 |
| Glucosa (g) | 160 | 240 | 320 | 400 |
| Grasas (g) | 40 | 60 | 80 | 100 |
| Valor energético total (kcal) | 1200 | 1800 | 2400 | 3000 |
| Valor energético no proteico (kcal) | 1040 | 1560 | 2080 | 2600 |
| Valor energético de la glucosa (kcal) | 640 | 960 | 1280 | 1600 |
| Valor energético de las grasas (kcal) | 400 | 600 | 800 | 1000 |
| Valor energético no proteico/contenido de nitrógeno (kcal/gN) | 158 | 158 | 158 | 158 |
| Sodio (mmol) | 32 | 48 | 64 | 80 |
| Potasio (mmol) | 24 | 36 | 48 | 60 |
| Magnesio (mmol) | 2,2 | 3,3 | 4,4 | 5,5 |
| Calcio (mmol) | 2 | 3 | 4 | 5 |
| Fosfatos (mmol)** | 10 | 15 | 20 | 25 |
| Octanoato (mmol) | 57 | 86 | 114 | 143 |
| Cloruro (mmol) | 48 | 72 | 96 | 120 |
| pH | 6 | 6 | 6 | 6 |
| Osmolalidad (mOsm/l) | 1450 | 1450 | 1450 | 1450 |
No debe exceder la dosis máxima diaria en adultos ni en niños y adolescentes. Debido a la composición fija de la bolsa de varias cámaras,
es posible que no se puedan satisfacer todas las necesidades nutricionales del paciente. Puede ocurrir una situación clínica en la que el paciente requiera una cantidad diferente de nutrientes de la disponible en la composición fija de la bolsa.
Como regla general, no debe exceder la dosis de 3 g de aminoácidos/kg de peso corporal por día y (o) 17 g de glucosa/kg de peso corporal por día y (o) 3 g de grasas/kg de peso corporal por día y (o) 100 ml de líquido/kg de peso corporal por día, excepto en casos especiales.
Multimel está destinado solo para un uso único.
El tiempo de infusión recomendado para la nutrición parenteral es de 12 a 24 horas.
Dosis y velocidad de infusión - Adultos
La necesidad media de nitrógeno es de 0,16 a 0,35 g/kg de peso corporal por día (aproximadamente 1 a 2 g de aminoácidos/kg de peso corporal por día).
La necesidad energética varía según el estado de nutrición del paciente y el nivel de catabolismo. En promedio, es de 20 a 40 kcal/kg de peso corporal por día.
Dosis máxima diaria:
Para Multimel N7-1000 E:La dosis máxima diaria depende del valor energético de los componentes del producto. La dosis máxima diaria es de 33 ml/kg de peso corporal (lo que equivale a 1,32 g de aminoácidos, 5,28 g de glucosa, 1,32 g de grasas, 1,06 mmol de sodio y 0,79 mmol de potasio/kg de peso corporal), es decir, 2310 ml de emulsión para infusión para un paciente de 70 kg.
Velocidad máxima de infusión
Como regla general, no debe exceder la velocidad de infusión de 0,10 g de aminoácidos/kg de peso corporal por hora y (o) 0,25 g de glucosa/kg de peso corporal por hora y (o) 0,15 g de grasas/kg de peso corporal por hora, excepto en casos especiales.
Para Multimel N7-1000 E:Como regla general, no debe exceder la velocidad de infusión de 1,5 ml/kg de peso corporal por hora, es decir, 0,06 g de aminoácidos, 0,24 g de glucosa y 0,06 g de grasas/kg de peso corporal por hora.
Dosis y velocidad de infusión - Niños mayores de 2 años y adolescentes
No se han realizado estudios en niños y adolescentes.
La dosis se determina según la cantidad de líquidos administrados y la necesidad diaria de nitrógeno.
La administración debe corregirse teniendo en cuenta el estado de hidratación del niño.
La necesidad diaria de líquidos, nitrógeno y energía disminuye constantemente con la edad.
Las directrices para la velocidad máxima de infusión por hora y el volumen diario para niños y adolescentes son:
Multimel N7-1000 E:
Dosis máxima diaria:
| Componente | 2 a 11 años | 12 a 18 años | ||
| Dosis máxima diaria recomendadaa | Dosis máxima diaria de MULTIMEL N7-1000 Eb | Dosis máxima diaria recomendadaa | Dosis máxima diaria de MULTIMEL N7-1000 Ec | |
| Líquidos (ml/kg de peso corporal/día) |
| 45 |
| 36 |
| Aminoácidos (g/kg de peso corporal/día) |
| 1,8 |
| 1,4 |
| Glucosa (g/kg de peso corporal/día) | 1,4 – 8,6 | 7,2 | 0,7 – 5,8 | 5,8 |
| Grasas (g/kg de peso corporal/día) | 0,5 – 3 | 1,8 | 0,5 – 2 (hasta 3) | 1,4 |
| Valor energético total (kcal/kg de peso corporal/día) | 30-75 | 54,0 | 20-55 | 43,2 |
| Sodio (mmol/kg de peso corporal/día) | 1-3 | 1,4 | 1-3 | 1,2 |
| Potasio (mmol/kg de peso corporal/día) | 1-3 | 1,1 | 1-3 | 0,9 |
Velocidad máxima por hora
| Componente | 2 a 11 años | 12 a 18 años | ||
| Velocidad máxima por hora recomendadaa | Velocidad máxima por hora de MULTIMEL N7-1000 Eb | Velocidad máxima por hora recomendadaa | Velocidad máxima por hora de MULTIMEL N7-1000 Eb | |
| Líquidos (ml/kg de peso corporal/hora) | No aplica | 2,2 | No aplica | 1,5 |
| Aminoácidos (g/kg de peso corporal/hora) | 0,20 | 0,09 |
|
|
| Glucosa (g/kg de peso corporal/hora) | 0,36 | 0,35 | 0,24 | 0,24 |
| Grasas (g/kg de peso corporal/hora) | 0,13 | 0,09 | 0,13 | 0,06 |
Vía de administración
Multimel N7-1000 E debe administrarse por vía intravenosa a través de una vena central.
La velocidad de infusión debe adaptarse a la dosis administrada, las características de la mezcla final,
el volumen total previsto para administrar en 24 horas y el tiempo de infusión.
3. PRECAUCIONES Y ADVERTENCIAS ESPECIALES
4. INFORMACIÓN PRÁCTICA SOBRE LA PREPARACIÓN PARA
LA ADMINISTRACIÓN DEL PRODUCTO MÉDICO Y ELIMINACIÓN DE SUS
RESIDUOS
Multimel N7-1000 E debe utilizarse solo si:
- el saco no está dañado
- las soldaduras no están dañadas
- las soluciones de aminoácidos y glucosa son transparentes, incoloras o ligeramente amarillas, y prácticamente no contienen partículas visibles
- la emulsión grasosa es un líquido homogéneo con apariencia lechosa.
Antes de usar, debe llevarse el producto Multimel N7-1000 E a temperatura ambiente.
Administrar solo después de romper las soldaduras que dividen las 3 cámaras del saco y mezclar el contenido
de las 3 cámaras, como se muestra a continuación.
Debe asegurarse de que la emulsión preparada para infusión no muestre signos de separación de fases.
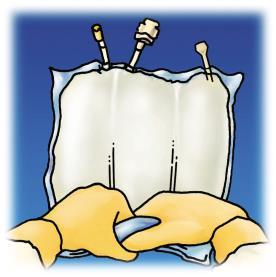
1. 2. 3.



Romper el paquete protector
desde arriba.
Retirar la parte delantera
del paquete protector para
exponer el saco
Multimel N7-1000 E. Desechar
el paquete protector y el paquete
de absorción de oxígeno.
Colocar el saco en una superficie
plana, horizontal y limpia con el
asidero hacia sí.
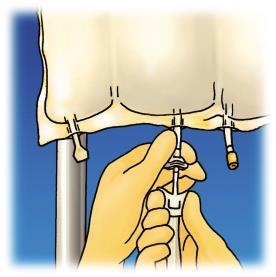
4. 5. 6.
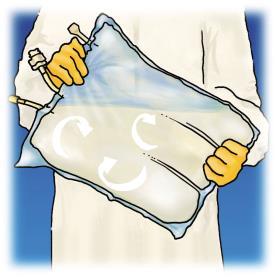
Levantar el saco sosteniendo el
asidero para eliminar el líquido de
la parte superior del saco.
Enrollar firmemente el saco con
ambas manos, comenzando desde
la parte superior del saco, hasta
que se rompan las soldaduras (aproximadamente la mitad de su longitud).
Mezclar el contenido del saco,
girándolo al menos 3 veces. Debe
asegurarse de que la mezcla sea homogénea y que no se produzca separación de fases.
Colgar el saco. Retirar la cubierta
plástica del sitio de inserción
del conjunto de infusión.
Insertar firmemente la punta del
conjunto de infusión.
Después de abrir el saco, su contenido debe usarse de inmediato. No se debe almacenar el saco abierto para una infusión posterior.
No se deben conectar sacos parcialmente utilizados.
No se deben conectar sacos en serie para evitar la formación de embolias gaseosas causadas por el aire residual contenido en el primer saco.
Solo para uso único. Todos los residuos del producto no utilizado o sus desechos, así como todo el conjunto de infusión, deben destruirse.
No se deben almacenar sacos parcialmente utilizados y se deben desechar todos los componentes del conjunto después de su uso.
Componentes adicionales
No se deben agregar otros productos o sustancias medicinales a ninguna de las cámaras del saco o a la emulsión preparada sin verificar antes su compatibilidad y estabilidad
de la mezcla resultante (en particular, la estabilidad de la emulsión grasosa). El producto Multimel N7-1000 E puede utilizarse sin agregar componentes adicionales o, si es necesario, después de agregar electrolitos, oligoelementos o vitaminas.
La capacidad del saco es suficiente para permitir la adición de componentes adicionales, como vitaminas, electrolitos y oligoelementos. Todos los componentes adicionales (incluyendo vitaminas) pueden agregarse a la emulsión preparada (después de romper las soldaduras y mezclar el contenido de las 3 cámaras).
Las vitaminas también pueden agregarse a la cámara con la solución de glucosa antes de preparar la emulsión (antes de romper las soldaduras y mezclar las soluciones y la emulsión).
En caso de agregar componentes adicionales al producto, antes de la administración por vía periférica, debe medirse la osmolalidad final de la mezcla.
Al producto Multimel N7-1000 E se pueden agregar:
- electrolitos: debe tenerse en cuenta la cantidad de electrolitos ya presentes en el saco; se ha demostrado la estabilidad de la mezcla que contiene hasta 150 mmol de sodio, 150 mmol de potasio, 5,6 mmol de magnesio, 5 mmol de calcio por litro de mezcla de tres componentes;
- fosfatos orgánicos: se ha demostrado la estabilidad de la mezcla que contiene hasta 15 mmol de fosfatos adicionados por saco.
Oligoelementos y vitaminas: se ha demostrado la estabilidad después de agregar productos de vitaminas y oligoelementos disponibles en el mercado (que contienen como máximo 1 mg de hierro). La compatibilidad con otros componentes adicionales está disponible a petición.
Los componentes adicionales deben agregarse por personal calificado en condiciones asépticas.
Los componentes adicionales se agregan a través del sitio de inyección utilizando una aguja:
- preparar el sitio de inyección;
- insertar la aguja en el sitio de inyección e inyectar;
- mezclar el contenido del saco con los componentes adicionados.
Interacciones con otros medicamentos
No se han realizado estudios de interacción con el producto Multimel.
Multimel N7-1000 E contiene vitamina K, naturalmente presente en las emulsiones grasas. La cantidad de vitamina K en las dosis recomendadas del producto Multimel N7-1000 E no debe tener efecto sobre la acción de los derivados de la cumarina.
No se debe mezclar o administrar ceftriaksona simultáneamente con soluciones intravenosas que contengan calcio, incluyendo el producto Multimel N7-1000 E, a través de la misma línea de infusión, debido al riesgo de precipitación de sales de calcio de ceftriaksona.
La ceftriaksona y las soluciones que contienen calcio pueden administrarse secuencialmente una después de la otra, si se utilizan líneas de infusión en diferentes sitios o si las líneas de infusión se cambian o se lavan cuidadosamente entre las infusiones con una solución salina fisiológica, para evitar la formación de precipitados.
Debido a la presencia de potasio en el producto Multimel N7-1000 E, debe tenerse cuidado al administrarlo a pacientes que están recibiendo diuréticos que ahorran potasio (como amilorida, espironolactona, triamtereno), inhibidores de la conversión de angiotensina (ACE), antagonistas del receptor de angiotensina II o medicamentos inmunosupresores: tacrolimus y ciclosporina, debido al riesgo de hiperpotasemia.
Las grasas presentes en esta emulsión pueden interferir con los resultados de algunos análisis de laboratorio (por ejemplo, determinación de bilirrubina, dehidrogenasa láctica, saturación de oxígeno, hemoglobina de los glóbulos rojos), siempre y cuando las muestras de sangre se hayan tomado antes de que se produzca la eliminación de las grasas (las grasas suelen eliminarse después de aproximadamente 5-6 horas después de suspender su administración).
Incompatibilidades farmacéuticas
No se debe administrar esta emulsión para infusión simultáneamente con sangre a través del mismo conjunto de infusión.
Multimel N7-1000 E contiene iones de calcio, que representan un riesgo adicional de coagulación y formación de depósitos en sangre anticoagulada/conservada con citrato o componentes de la sangre.
La causa de la incompatibilidad puede ser, por ejemplo, una acidez excesiva (pH bajo) o una cantidad inadecuada de cationes divalentes (Ca y Mg), lo que puede afectar desfavorablemente la estabilidad de la emulsión grasosa.
Al igual que con cualquier mezcla para nutrición parenteral, debe tenerse en cuenta el contenido de calcio y fosfato. El exceso de calcio o fosfato, especialmente en forma de sales minerales, puede llevar a la formación de depósitos de fosfato de calcio.
Debe verificarse la compatibilidad del producto con las soluciones que se administran simultáneamente a través del mismo conjunto de infusión, catéter o cánula.
No se debe mezclar o administrar ceftriaksona simultáneamente con soluciones intravenosas que contengan calcio, incluyendo el producto Multimel N7-1000 E, a través de la misma línea de infusión (por ejemplo, un conector en forma de Y), debido al riesgo de precipitación de sales de calcio de ceftriaksona (ver sección Interacciones).
5. PERÍODO DE VALIDEZ
2 años, si el paquete protector no está dañado.
Se recomienda que el producto se utilice inmediatamente después de abrir las soldaduras que dividen el contenido de las 3 cámaras. Sin embargo, se ha demostrado que la emulsión preparada mantiene su estabilidad durante 7 días a una temperatura de 2 °C a 8 °C y luego durante 48 horas adicionales a una temperatura no superior a 25 °C.
Después de agregar componentes adicionales (electrolitos, oligoelementos, vitaminas) a la emulsión preparada Multimel N7-1000 E (ver sección anterior), la emulsión mantiene su estabilidad química y física durante 7 días a una temperatura de 2 °C a 8 °C y luego durante 48 horas adicionales a una temperatura inferior a 25 °C. Desde el punto de vista microbiológico, cualquier mezcla preparada que contenga componentes adicionales debe utilizarse de inmediato. De lo contrario, el usuario es responsable del tiempo y las condiciones de almacenamiento de la mezcla hasta su uso. Sin embargo, las mezclas preparadas de esta manera no deben almacenarse durante más de 24 horas a una temperatura de 2-8 °C, a menos que la adición de componentes adicionales se realice en condiciones asépticas controladas y validadas.
- País de registro
- Principio activo
- Requiere recetaNo
- Fabricante
- ImportadorBaxter S.A.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a Multimel N7-1000eForma farmacéutica: Solución, -Principio activo: combinationsNo requiere recetaForma farmacéutica: Solución, -Principio activo: combinationsNo requiere recetaForma farmacéutica: Solución, -Principio activo: combinationsNo requiere receta
Alternativas a Multimel N7-1000e en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Multimel N7-1000e en España
Alternativa a Multimel N7-1000e en Ucrania
Médicos online para Multimel N7-1000e
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Multimel N7-1000e – sujeta a valoración médica y normativa local.














