
Fluarix
Consulta con un médico sobre la receta médica de Fluarix

Cómo usar Fluarix
Hoja de instrucciones del paquete: información para el usuario
Fluarix, suspensión para inyección en jeringa precargada
Vacuna triple contra la gripe (virión escindido, inactivada)
El contenido de esta hoja de instrucciones se ha redactado con el supuesto de que será leído por la persona que recibe
la vacuna. Sin embargo, como esta vacuna puede ser administrada a adultos y niños, es posible que los padres o tutores
del niño lean el contenido de la hoja de instrucciones.
Es importante leer atentamente el contenido de la hoja de instrucciones antes de administrar la vacuna, ya que contiene
información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a un médico, farmacéutico o enfermera.
- Esta vacuna ha sido prescrita específicamente para una persona. No debe ser transferida a otros.
- Si el paciente experimenta algún efecto adverso, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones,
debe informar a su médico, farmacéutico o enfermera. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es la vacuna Fluarix y para qué se utiliza
- 2. Información importante antes de administrar la vacuna Fluarix
- 3. Cómo administrar la vacuna Fluarix
- 4. Posibles efectos adversos
- 5. Cómo almacenar la vacuna Fluarix
- 6. Contenido del paquete y otra información
1. Qué es la vacuna Fluarix y para qué se utiliza
Fluarix es una vacuna destinada a personas adultas y niños a partir de los 6 meses de edad para prevenir la gripe.
La gripe es una enfermedad de las vías respiratorias superiores e inferiores causada por el virus de la gripe. Los síntomas más comunes
de la gripe son fiebre alta, dolor de garganta, tos, dolores generales y malestar, dolor de cabeza, debilidad y
fatiga. Las complicaciones de la gripe pueden ocurrir especialmente en personas muy jóvenes, ancianas y aquellas con
sistema inmunológico debilitado.
Cómo funciona la vacuna Fluarix?
- La vacuna Fluarix contiene virus inactivados que no pueden causar gripe.
- La vacuna Fluarix estimula el sistema inmunológico de la persona vacunada para producir anticuerpos contra los virus específicos
contra los que se ha diseñado la vacuna. Esto ayudará a prevenir la enfermedad. - La vacuna se ha diseñado contra los virus de la gripe según las recomendaciones oficiales.
- Al igual que con todas las vacunas, Fluarix puede no proteger completamente a todas las personas vacunadas.
2. Información importante antes de administrar la vacuna Fluarix
Cuándo no administrar la vacuna Fluarix:
- Si el paciente es alérgico a los principios activos o a alguno de los demás componentes de esta vacuna (enumerados en el punto 6) o a alguno de los componentes que pueden estar presentes en cantidades muy pequeñas, como la albúmina de huevo (ovalbumina, proteína del huevo), hidrocortisona, sulfato de gentamicina, formaldehído y desoxicolato de sodio.
Precauciones y advertencias:
Antes de administrar la vacuna Fluarix, debe discutir con su médico, farmacéutico o enfermera:
- si el paciente tiene una infección aguda con fiebre alta. La vacunación debe retrasarse hasta que el paciente se sienta mejor. Una infección leve, como un resfriado, no es una contraindicación para la vacunación, pero debe discutir con su médico, farmacéutico o enfermera antes de la vacunación.
- si el paciente tiene problemas de coagulación o tendencia a formar moretones.
Después o incluso antes de la administración de cada vacuna en forma de inyección, puede ocurrir una pérdida de conocimiento
(especialmente en adolescentes). Por lo tanto, debe informar a su médico, farmacéutico o enfermera si el paciente ha experimentado una pérdida de conocimiento durante la administración de una inyección.
Si el paciente tiene un sistema inmunológico debilitado, por ejemplo, debido a una infección por el virus de la inmunodeficiencia humana (VIH) o al consumo de medicamentos que afectan el sistema inmunológico, la vacuna Fluarix puede no ser completamente efectiva.
Debe informar a su médico, farmacéutico o enfermera si alguna de las afirmaciones anteriores se aplica a la persona a quien se le administrará la vacuna Fluarix o si el paciente no está seguro de si alguna de las afirmaciones anteriores se aplica a él.
La vacuna Fluarix y otros medicamentos
Debe informar a su médico, farmacéutico o enfermera sobre todos los medicamentos que esté tomando actualmente o
recientemente, así como sobre los medicamentos que planea tomar. Debe informar sobre todas las vacunas que ha recibido recientemente.
Si Fluarix se administra al mismo tiempo que otras vacunas, cada vacuna debe administrarse en un lugar diferente del cuerpo.
Embarazo, lactancia y fertilidad
Si la paciente está embarazada o en período de lactancia, o si cree que puede estar embarazada o planea tener un hijo,
debe consultar a su médico o farmacéutico antes de recibir esta vacuna.
Conducción de vehículos y uso de máquinas
Algunos de los efectos mencionados a continuación en el punto 4 "Posibles efectos adversos" (por ejemplo, fatiga o mareo)
pueden tener un efecto temporal en la capacidad para conducir vehículos y operar máquinas. No debe conducir vehículos o operar máquinas si no se siente bien.
Fluarix contiene sodio
Esta vacuna contiene menos de 1 mmol de sodio (23 mg) por dosis, es decir, el medicamento se considera "libre de sodio".
Fluarix contiene potasio
Esta vacuna contiene potasio, menos de 1 mmol (39 mg) por dosis, es decir, el medicamento se considera "libre de potasio".
Fluarix contiene polisorbato 80
Esta vacuna contiene no más de 0,415 mg de polisorbato 80 por dosis. Los polisorbatos pueden causar reacciones alérgicas. Debe consultar a su médico si es alérgico a esta sustancia.
3. Cómo administrar la vacuna Fluarix
La vacuna Fluarix se administra en forma de una sola inyección intramuscular, en una dosis de 0,5 ml.
Administración en niños
Los niños menores de 9 años que no han sido vacunados previamente contra la gripe deben recibir una segunda dosis al menos 1 mes después de la primera dosis. Debe asegurarse de que el niño reciba todas las dosis de la vacuna para obtener una mejor protección contra la gripe.
En caso de dudas adicionales sobre la administración de esta vacuna, debe consultar a su médico, farmacéutico o enfermera.
4. Posibles efectos adversos
Como cualquier medicamento, esta vacuna puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Para obtener más información sobre los posibles efectos adversos de la vacuna Fluarix, debe consultar a su médico, farmacéutico o enfermera.
Los efectos adversos informados durante el uso general de la vacuna Fluarix incluyen:
Efectos adversos graves
Debe informar inmediatamente a su médico si experimenta alguno de los siguientes efectos adversos graves; puede ser necesaria atención médica de emergencia.
Raro:puede ocurrir en menos de 1 de cada 1.000 dosis de la vacuna
- Reacciones alérgicas graves (anafilácticas). Pueden reconocerse por:
- erupción cutánea con picazón en las manos y los pies
- edema de los ojos y la cara
- dificultad para respirar o tragar
- caída repentina de la presión arterial y pérdida de conocimiento. Estas reacciones suelen ocurrir dentro de los 15 minutos después de la vacunación. Sin embargo, si ocurre alguno de estos síntomas, debe buscar atención médica de inmediato.
Otros efectos adversos
Debe informar a su médico, farmacéutico o enfermera si experimenta alguno de los siguientes efectos adversos.
Raro:puede ocurrir en menos de 1 de cada 1.000 dosis de la vacuna
- Inflamación de los nervios (neuritis), inflamación del cerebro y la médula espinal (encefalomielitis), inflamación nerviosa transitoria que causa dolor, debilidad y parálisis conocida como síndrome de Guillain-Barré
- Reacciones cutáneas que pueden extenderse por todo el cuerpo, incluyendo picazón (urticaria) y enrojecimiento de la piel (eritema), erupción cutánea
- Hinchazón temporal de los ganglios linfáticos en el cuello, las axilas o la ingle (linfadenopatía transitoria)
- Síntomas similares a los de la gripe, malestar general. Debe informar a su médico, farmacéutico o enfermera si experimenta alguno de los efectos adversos anteriores.
En los estudios clínicos con la vacuna Fluarix, se han observado los siguientes efectos adversos:
Efectos adversos que ocurrieron en niños de 6 meses a menos de 6 años
Muy frecuentes:pueden ocurrir en más de 1 de cada 10 dosis de la vacuna
- pérdida de apetito
- irritabilidad
- somnolencia
- dolor en el lugar de la inyección
- enrojecimiento en el lugar de la inyección
- hinchazón en el lugar de la inyección
Frecuentes:pueden ocurrir en menos de 1 de cada 10 dosis de la vacuna
- vómitos
- diarrea
- dolor abdominal
- fiebre
Efectos adversos que ocurrieron en niños de 6 a menos de 18 años
Muy frecuentes:pueden ocurrir en más de 1 de cada 10 dosis de la vacuna
- dolor de cabeza
- dolor muscular
- fatiga
- dolor en el lugar de la inyección
- enrojecimiento en el lugar de la inyección
- hinchazón en el lugar de la inyección
Frecuentes:pueden ocurrir en menos de 1 de cada 10 dosis de la vacuna
- náuseas
- vómitos
- diarrea
- dolor abdominal
- dolor articular
- escalofríos
- fiebre
Efectos adversos que ocurrieron en adultos de 18 años o más
Muy frecuentes:pueden ocurrir en más de 1 de cada 10 dosis de la vacuna
- dolor en el lugar de la inyección
- fatiga
- dolor de cabeza
- dolor muscular
Frecuentes:pueden ocurrir en menos de 1 de cada 10 dosis de la vacuna
- enrojecimiento, hinchazón o bulto duro en el lugar de la inyección
- escalofríos
- sudoración
- dolor articular
- náuseas
- vómitos
- diarrea
- dolor abdominal
Raro:puede ocurrir en menos de 1 de cada 100 dosis de la vacuna
- fiebre
- mareo
Notificación de efectos adversos
Si ocurren efectos adversos, incluyendo cualquier efecto adverso no mencionado en la hoja de instrucciones, debe informar a su médico o farmacéutico. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad, Consumo y Bienestar Social, calle Alcalá, 56, 28071 Madrid, teléfono: +34 91 596 24 00, fax: +34 91 596 24 01, sitio web: www.aemps.gob.es
Al notificar los efectos adversos, se puede recopilar más información sobre la seguridad del medicamento.
Los efectos adversos también pueden notificarse al titular de la autorización de comercialización.
5. Cómo almacenar la vacuna Fluarix
- La vacuna debe almacenarse en un lugar fuera del alcance de los niños.
- No debe utilizarse después de la fecha de caducidad indicada en el etiquetado y el paquete de cartón después de: EXP. La fecha de caducidad es el último día del mes indicado.
- El código "Lot" se refiere al número de lote del producto.
- Debe almacenarse en el refrigerador (2°C - 8°C).
- No debe congelarse.
- Debe almacenarse en el paquete original para protegerlo de la luz.
- No debe desechar los medicamentos por el desagüe o en los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Fluarix?
El principio activo es el virus de la gripe escindido e inactivado procedente de las siguientes cepas*:
A/Victoria/4897/2022 (H1N1)pdm09 - cepa similar (A/Victoria/4897/2022, IVR-238)
15 microgramos de HA**
A/Croacia/10136RV/2023 (H3N2) - cepa similar (A/Croacia/10136RV/2023, X-425A)
15 microgramos de HA**
B/Austria/1359417/2021 - cepa similar (B/Austria/1359417/2021, BVR-26)
15 microgramos de HA**
en una dosis de 0,5 ml
* cultivado en huevos de gallina embrionados procedentes de granjas sanas
** hemaglutinina
Esta vacuna se ajusta a las recomendaciones de la Organización Mundial de la Salud (OMS) (para el hemisferio norte) y la Unión Europea para la temporada 2025/2026.
Los demás componentes de la vacuna son: cloruro de sodio, fosfato disódico dodecahidratado, dihidrogenofosfato de potasio, cloruro de potasio, cloruro de magnesio hexahidratado, α-tocoferil hidrogenosuccinato, polisorbato 80, octoxinol 10 y agua para inyección.
Cómo se presenta la vacuna Fluarix y qué contiene el paquete?
- Fluarix es una suspensión para inyección en jeringa precargada.
- Fluarix es un líquido incoloro y ligeramente opalescente.
- Fluarix está disponible en forma de jeringa precargada de una dosis, con agujas incluidas en el paquete o sin agujas, en paquetes de 1 y 10 unidades.
- No todas las tallas de paquete deben estar en circulación.
Titular de la autorización de comercialización y fabricante
Titular de la autorización de comercialización: Fabricante:
GlaxoSmithKline Biologicals S.A.
GlaxoSmithKline Biologicals
Rue de l’Institut 89
Filia SmithKline Beecham Pharma GmbH&Co. KG
1330 Rixensart
Zirkusstrasse 40
Bélgica
01069 Dresde
Alemania
Este medicamento está autorizado para su comercialización en los estados miembros del Espacio Económico Europeo bajo los siguientes nombres:
| Estado miembro | Nombre |
| Austria | Fluarix Trivalente |
| Bélgica, Luxemburgo | Alpharix |
| Finlandia, Francia, España, Holanda, Noruega, Polonia, Portugal, Suecia, Italia | Fluarix |
| Grecia, Alemania | Influsplit |
Fecha de la última revisión de la hoja de instrucciones: julio de 2025
Otras fuentes de información
La información detallada sobre este medicamento está disponible en el sitio web del Ministerio de Sanidad, Consumo y Bienestar Social.
---------------------------------------------------------------------------------------------------------------------------
Información destinada exclusivamente al personal médico cualificado:
Antes de la administración de la vacuna, debe inspeccionarla para detectar cualquier cuerpo extraño y/o cambios físicos.
Debe agitar antes de usar para obtener un líquido incoloro y ligeramente opalescente. Si se observan cambios, no debe administrar la vacuna.
Debe administrar todo el contenido de la jeringa precargada.
Instrucciones para la jeringa precargada
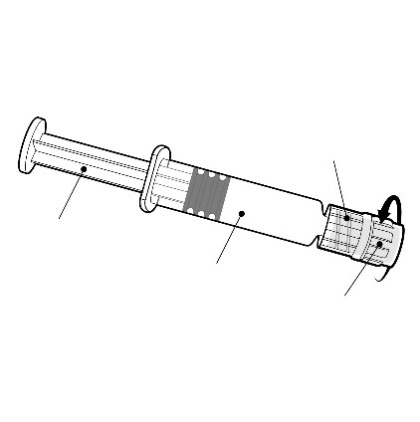
Debe sostener la jeringa precargada por
el cuerpo, no por el émbolo.
Adaptador de tipo Luer Lock
Debe girar la punta de la jeringa precargada
en el sentido contrario a las agujas del reloj.
Émbolo
Cuerpo
Punta
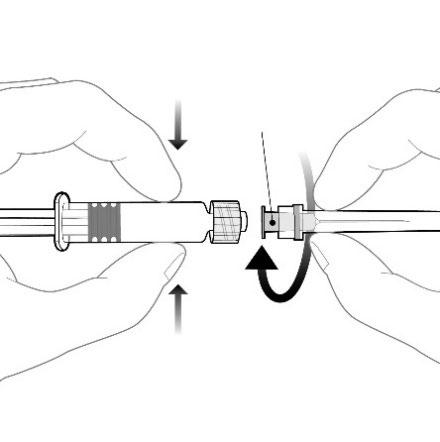
Debe fijar la aguja a la jeringa precargada
mediante la conexión de la punta de la aguja al adaptador Luer Lock (ang. Luer
Lock Adaptor, LLA) y girarla un cuarto de vuelta en el sentido de las agujas del reloj, hasta que se sienta el bloqueo de la aguja.
No debe retirar el émbolo del cuerpo de la jeringa precargada. Si esto sucede, no debe administrar la vacuna.
Punta de la aguja
Eliminación
Los restos de producto medicinal no utilizado o sus desechos deben eliminarse de acuerdo con las regulaciones locales.
- País de registro
- Principio activo
- Requiere recetaSí
- ImportadorGlaxoSmithKline Biologicals Filia SmithKline BeechamPharma GmbH & Co. KG
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a FluarixForma farmacéutica: Suspensión, 60 mcg HA/cepa, 1 dosis (0.7 ml)Principio activo: influenza, inactivated, split virus or surface antigenRequiere recetaForma farmacéutica: Suspensión, 60 mcg HA/cepa, 1 dosis (0.5 ml)Principio activo: influenza, inactivated, split virus or surface antigenRequiere recetaForma farmacéutica: Suspensión, 1 dosis (0.5 ml)Principio activo: influenza, inactivated, split virus or surface antigenRequiere receta
Alternativas a Fluarix en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Fluarix en España
Alternativa a Fluarix en Ucrania
Médicos online para Fluarix
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Fluarix – sujeta a valoración médica y normativa local.














