
Biotrakson
Consulta con un médico sobre la receta médica de Biotrakson

Cómo usar Biotrakson
Hoja de instrucciones para el paciente
Biotrakson, 1 g polvo para preparar solución para inyección o infusión
Biotrakson, 2 g, polvo para preparar solución para inyección o infusión
Ceftriaxona
Es importante leer atentamente el contenido de esta hoja de instrucciones antes de tomar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- Si tiene alguna duda, debe consultar a su médico, farmacéutico o enfermera.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Véase el punto 4.
Índice de la hoja de instrucciones
- 1. Qué es Biotrakson y para qué se utiliza
- 2. Información importante antes de tomar Biotrakson
- 3. Cómo tomar Biotrakson
- 4. Posibles efectos adversos
- 5. Cómo conservar Biotrakson
- 6. Contenido del envase y otra información
1. Qué es Biotrakson y para qué se utiliza
Biotrakson es un antibiótico utilizado en adultos y niños (incluidos recién nacidos). Su acción consiste en matar las bacterias que causan infecciones. Pertenece a un grupo de medicamentos llamados cefalosporinas.
Biotrakson se utiliza para tratar infecciones:
- del cerebro (meningitis),
- de los pulmones,
- del oído medio,
- del abdomen y la pared abdominal (peritonitis),
- del tracto urinario y los riñones,
- de los huesos y las articulaciones,
- de la piel y los tejidos blandos,
- de la sangre,
- del corazón.
Este medicamento se puede utilizar:
- para tratar ciertas infecciones de transmisión sexual (gonorrea y sífilis),
- para tratar a pacientes con un bajo recuento de glóbulos blancos (neutropenia) que tienen fiebre causada por una infección bacteriana,
- para tratar infecciones del tracto respiratorio en adultos con bronquitis crónica,
- para tratar la enfermedad de Lyme (enfermedad transmitida por garrapatas) en adultos y niños, incluidos recién nacidos a partir del día 15 de vida,
- para prevenir infecciones durante las operaciones.
2. Información importante antes de tomar Biotrakson
Cuándo no tomar Biotrakson:
- si el paciente es alérgico a la ceftriaxona;
- si el paciente ha tenido una reacción alérgica grave o repentina a la penicilina o antibióticos similares (como cefalosporinas, carbapenémicos, monobactámicos); los síntomas de esta reacción pueden incluir hinchazón repentina de la garganta o la cara, que puede dificultar la respiración o la deglución, hinchazón repentina de las manos, los pies y los tobillos, dolor en el pecho y erupción cutánea grave que aparece rápidamente;
- si el paciente es alérgico a la lidocaína y va a recibir Biotrakson por inyección intramuscular.
No se debe administrar Biotrakson a niños pequeños si:
- el niño es prematuro,
- el niño es un recién nacido (de hasta 28 días) y tiene ciertos trastornos sanguíneos o ictericia (amarillamiento de la piel y/o la esclera del ojo), o va a recibir un medicamento que contiene calcio por vía intravenosa.
Precauciones y advertencias
Antes de comenzar a tomar Biotrakson, debe discutirlo con su médico, farmacéutico o enfermera si:
- el paciente ha recibido o va a recibir pronto productos que contienen calcio,
- el paciente ha tenido diarrea después de tomar un antibiótico,
- el paciente ha tenido problemas intestinales, especialmente colitis (inflamación del intestino grueso),
- el paciente tiene problemas de hígado o riñón (véase el punto 4),
- el paciente tiene cálculos biliares o cálculos renales,
- el paciente tiene otras enfermedades, como anemia hemolítica (disminución del recuento de glóbulos rojos, que causa palidez y debilidad o dificultad para respirar),
- el paciente sigue una dieta baja en sodio,
- el paciente ha tenido o tiene algunos de los siguientes síntomas: erupción cutánea, enrojecimiento de la piel, ampollas en la boca, los ojos o la boca, descamación de la piel, fiebre alta, síntomas similares a los de la gripe, aumento de la actividad enzimática hepática en los resultados de las pruebas de sangre y aumento del recuento de un tipo de glóbulos blancos (eosinofilia) y ganglios linfáticos inflamados (síntomas de reacciones cutáneas graves, véase también el punto 4 "Posibles efectos adversos").
En caso de que sea necesario realizar un análisis de sangre o orina
Si el paciente recibe Biotrakson durante un período prolongado, es posible que se necesiten análisis de sangre regulares.
Biotrakson puede afectar los resultados de la determinación de la cantidad de azúcar en la orina y de una prueba de sangre llamada prueba de Coombs. Si el paciente se somete a pruebas:
- debe informar a la persona que tome la muestra de que está tomando Biotrakson.
Si el paciente tiene diabetes o necesita controlar su nivel de glucosa en sangre, no debe utilizar algunos de los tests que pueden dar resultados incorrectos de la cantidad de glucosa en sangre mientras toma ceftriaxona. Si el paciente controla su nivel de glucosa en sangre, debe consultar las instrucciones del test y hablar con su médico, farmacéutico o enfermera.
Niños
Antes de administrar Biotrakson a un niño, debe discutirlo con su médico, farmacéutico o enfermera si:
- el niño ha recibido o va a recibir pronto un producto que contiene calcio por vía intravenosa.
Biotrakson y otros medicamentos
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando actualmente o recientemente, y sobre los medicamentos que planea tomar.
En particular, debe informar a su médico o farmacéutico si está tomando alguno de los siguientes medicamentos:
- un antibiótico que pertenece a la clase de los aminoglucósidos,
- un antibiótico llamado clorafenicol, utilizado para tratar infecciones, especialmente infecciones oculares.
Embarazo, lactancia y fertilidad
Si la paciente está embarazada o en período de lactancia, o si cree que podría estar embarazada o planea quedarse embarazada, debe consultar a su médico antes de tomar este medicamento.
Su médico evaluará los beneficios del tratamiento con Biotrakson para la madre y los riesgos para el feto.
Conducción de vehículos y uso de máquinas
Biotrakson puede causar mareos. Si el paciente se siente mareado, no debe conducir vehículos ni operar máquinas. Debe informar a su médico si experimenta estos síntomas.
Biotrakson contiene sodio
El medicamento contiene 83 mg de sodio (3,6 mmol) (principal componente de la sal común) en 1 g. Esto equivale al 4,15% de la ingesta diaria máxima recomendada de sodio en la dieta para adultos.
Preparación del medicamento para administración - véase el punto: "Información destinada exclusivamente al personal médico especializado" al final de la hoja de instrucciones. Al calcular el contenido total de sodio en la solución diluida preparada del medicamento, debe tener en cuenta el sodio procedente del diluyente. Para obtener información precisa sobre el contenido de sodio en la solución utilizada para diluir el medicamento, debe consultar la hoja de instrucciones del paciente del diluyente utilizado.
3. Cómo tomar Biotrakson
Este medicamento siempre debe administrarse según las indicaciones de su médico. En caso de duda, debe consultar a su médico.
Biotrakson se administra generalmente por un médico o enfermera. Puede administrarse por infusión intravenosa (goteo) o por inyección directa en una vena o en un músculo. Biotrakson se prepara por un médico, farmacéutico o enfermera y no se mezcla ni se administra al mismo tiempo que soluciones que contengan calcio.
Dosis habitual
Su médico decidirá qué dosis de Biotrakson es adecuada para usted. La dosis depende de la gravedad y el tipo de infección; de si está tomando otros antibióticos; de su edad y peso; de la función de su hígado y riñones. El número de días o semanas durante los cuales recibirá Biotrakson depende del tipo de infección.
Adultos, personas de edad avanzada y niños de 12 años o más y con un peso de al menos 50 kg:
- 1 a 2 g una vez al día, según la gravedad y el tipo de infección. En caso de infección grave, su médico puede administrar una dosis mayor (hasta 4 g una vez al día). Si la dosis diaria es mayor que 2 g, el medicamento se puede administrar en una sola dosis o en dos dosis separadas.
Recién nacidos, lactantes y niños de 15 días a 12 años con un peso inferior a 50 kg:
- 50 a 80 mg de Biotrakson por kilogramo de peso del niño una vez al día, según la gravedad y el tipo de infección. En caso de infección grave, su médico puede administrar una dosis mayor, hasta 100 mg por kilogramo de peso del niño, con un máximo de 4 g una vez al día. Si la dosis diaria es mayor que 2 g, el medicamento se puede administrar en una sola dosis al día o en dos dosis separadas.
- Los niños con un peso de 50 kg o más deben recibir la dosis habitual para adultos.
Recién nacidos de 0 a 14 días
- 20 a 50 mg de Biotrakson por kilogramo de peso del niño una vez al día, según la gravedad y el tipo de infección.
- La dosis diaria máxima no debe ser mayor que 50 mg por kilogramo de peso del niño.
Pacientes con trastornos de la función hepática o renal
El paciente puede recibir una dosis diferente a la habitual. Su médico determinará qué dosis de Biotrakson es adecuada para usted y controlará su estado de cerca, dependiendo de la gravedad de la enfermedad hepática o renal.
Administración de una dosis mayor que la recomendada de Biotrakson
En caso de que se administre accidentalmente una dosis mayor que la prescrita por su médico, debe ponerse en contacto de inmediato con su médico o con el hospital más cercano.
Olvido de la administración de Biotrakson
Si el paciente olvida una inyección, debe recibirla lo antes posible. Sin embargo, si se acerca la hora de la siguiente inyección, no debe tomar la inyección olvidada. No debe tomar una dosis doble (dos inyecciones al mismo tiempo) para compensar la inyección olvidada.
Interrupción del tratamiento con Biotrakson
No debe interrumpir el tratamiento con Biotrakson a menos que su médico lo indique. En caso de duda adicional sobre el uso de este medicamento, debe consultar a su médico o enfermera.
4. Posibles efectos adversos
Como cualquier medicamento, Biotrakson puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Los siguientes efectos adversos pueden ocurrir durante el tratamiento con este medicamento:
Reacciones alérgicas graves (frecuencia desconocida - no puede determinarse a partir de los datos disponibles)
En caso de una reacción alérgica grave, debe informar de inmediato a su médico.
Los síntomas pueden incluir:
- hinchazón repentina de la cara, la garganta, los labios o la boca; puede dificultar la respiración o la deglución;
- hinchazón repentina de las manos, los pies y los tobillos;
- dolor en el pecho asociado con una reacción alérgica, que puede ser un síntoma de un ataque al corazón causado por alergia (síndrome de Kounis).
Reacciones cutáneas graves (frecuencia desconocida - no puede determinarse a partir de los datos disponibles)
En caso de una reacción cutánea grave, debe informar de inmediato a su médico.
Los síntomas de esta reacción pueden incluir:
- erupción cutánea grave que se desarrolla rápidamente, con ampollas o descamación de la piel y posible formación de ampollas en la boca;
- cualquiera de los siguientes síntomas: erupción cutánea que se extiende, fiebre alta, aumento de la actividad enzimática hepática en los resultados de las pruebas de sangre, anormalidades en los resultados de las pruebas de sangre (eosinofilia), ganglios linfáticos inflamados y afectación de otros órganos (reacción a medicamentos con eosinofilia y síntomas sistémicos, también conocida como síndrome DRESS o síndrome de hipersensibilidad a medicamentos);
- reacción de Jarisch-Herxheimer que causa fiebre, escalofríos, dolor de cabeza, dolor muscular y erupción cutánea, generalmente autolimitada; esta reacción ocurre poco después del inicio del tratamiento con Biotrakson para infecciones causadas por espiroquetas, como la enfermedad de Lyme.
Otros posibles efectos adversos
Muy frecuentes (hasta 1 de cada 10 pacientes)
- anomalías en los glóbulos blancos (como disminución del recuento de leucocitos y aumento del recuento de eosinófilos) y plaquetas (disminución del recuento de plaquetas),
- heces sueltas o diarrea,
- cambios en los resultados de las pruebas de sangre que evalúan la función hepática,
- erupción cutánea.
Frecuentes (hasta 1 de cada 100 pacientes)
- infecciones por hongos (como candidiasis),
- disminución del recuento de glóbulos blancos (granulocitopenia),
- disminución del recuento de glóbulos rojos (anemia),
- problemas de coagulación de la sangre; los síntomas de este efecto pueden incluir moretones fáciles y dolor o hinchazón en las articulaciones,
- dolor de cabeza,
- mareos,
- náuseas y/o vómitos,
- picazón (prurito),
- dolor o ardor a lo largo de la vena en la que se administró Biotrakson; dolor en el lugar de la inyección del medicamento,
- fiebre alta,
- resultado anormal de la prueba de función renal (aumento de la creatinina en sangre).
Poco frecuentes (hasta 1 de cada 1.000 pacientes)
- colitis (inflamación del intestino grueso); los síntomas pueden incluir diarrea, generalmente con sangre y moco, dolor abdominal y fiebre,
- dificultad para respirar (broncoespasmo),
- erupción cutánea con ampollas (urticaria) que puede afectar una gran parte del cuerpo, picazón y hinchazón,
- sangre o azúcar en la orina,
- hinchazón (retención de líquidos en el cuerpo),
- escalofríos. El tratamiento con ceftriaxona, especialmente en pacientes de edad avanzada con trastornos renales o neurológicos graves, puede causar raramente una disminución del nivel de conciencia, movimientos anormales, agitación y convulsiones.
Frecuencia desconocida (frecuencia no puede determinarse a partir de los datos disponibles)
- infección secundaria que no responde a los antibióticos recetados previamente,
- un tipo de anemia en el que se destruyen los glóbulos rojos (anemia hemolítica),
- disminución grave del recuento de glóbulos blancos (agranulocitosis),
- convulsiones,
- mareos intensos (sensación de girar),
- pancreatitis; los síntomas pueden incluir dolor abdominal intenso que irradia hacia la espalda,
- inflamación de la mucosa que reviste la boca,
- inflamación de la lengua; los síntomas pueden incluir hinchazón, enrojecimiento y dolor de la lengua,
- problemas con la vesícula biliar y/o el hígado, que pueden causar dolor, náuseas, vómitos, ictericia, picazón, orina de color muy oscuro y heces de color arcilla,
- un trastorno neurológico que puede ocurrir en recién nacidos con ictericia grave (ictericia nuclear del cerebro),
- problemas renales causados por la precipitación de sales de calcio de ceftriaxona; pueden manifestarse como dolor al orinar o producción de una pequeña cantidad de orina,
Los síntomas pueden incluir:
- resultado falso positivo de la prueba de Coombs (prueba que detecta ciertos trastornos sanguíneos),
- resultado falso positivo de la prueba de galactosemia (trastorno en el que se acumula azúcar en el cuerpo),
- Biotrakson puede afectar los resultados de algunas pruebas que miden la glucosa en sangre - debe consultar con su médico.
Notificación de efectos adversos
Si se producen efectos adversos, incluidos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad.
5. Cómo conservar Biotrakson
El medicamento debe conservarse en un lugar donde no pueda ser visto ni alcanzado por los niños.
Conservar a una temperatura de hasta 25°C. Proteger de la luz.
Según las normas de buena práctica, se recomienda preparar las soluciones justo antes de la administración.
La solución preparada se puede conservar durante 24 horas en el refrigerador, es decir, a una temperatura entre 2°C y 8°C.
No se deben conservar las soluciones para infusión intravenosa preparadas con cloruro de sodio y glucosa al mismo tiempo, debido a la incompatibilidad física de los componentes a bajas temperaturas.
No debe tomar este medicamento después de la fecha de caducidad indicada en el envase.
La fecha de caducidad indicada en el envase después de la abreviatura "EXP" es la fecha de caducidad, y después de la abreviatura "Lot" es el número de lote.
No debe tirar los medicamentos por el desagüe ni por los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del envase y otra información
Qué contiene Biotrakson?
- El principio activo del medicamento es ceftriaxona. Cada vial contiene 1 g o 2 g de ceftriaxona en forma de ceftriaxona sódica.
- El medicamento no contiene excipientes.
Cómo es Biotrakson y qué contiene el envase?
El medicamento tiene la forma de un polvo cristalino blanco o amarillento.
Biotrakson, 1 g: vial de vidrio de 26 ml, cerrado con un tapón de goma y protegido con una tapa de aluminio o una tapa de aluminio con caperuza, en una caja de cartón.
Biotrakson, 2 g: vial de vidrio incoloro de 26 ml, cerrado con un tapón de goma bromobutilica y protegido con una tapa de aluminio o una tapa de aluminio con caperuza, en una caja de cartón.
La caja de cartón contiene 1 o 10 viales.
No todas las tallas de envase deben estar en circulación.
Titular de la autorización de comercialización y fabricante
Titular de la autorización de comercialización
Zakłady Farmaceutyczne POLPHARMA S.A.
ul. Pelplińska 19, 83-200 Starogard Gdański
tel. + 48 22 364 61 01
Fabricante
Zakłady Farmaceutyczne POLPHARMA S.A.
División de producción en Duchnice
ul. Ożarowska 28/30, 05-850 Ożarów Mazowiecki
Fecha de la última actualización de la hoja de instrucciones:mayo de 2024
INFORMACIÓN DESTINADA EXCLUSIVAMENTE AL PERSONAL MÉDICO ESPECIALIZADO
Método de punción del vial
| Zakłady Farmaceutyczne POLPHARMA S.A. | |
| ul. Pelplińska 19, 83-200 Starogard Gdański |
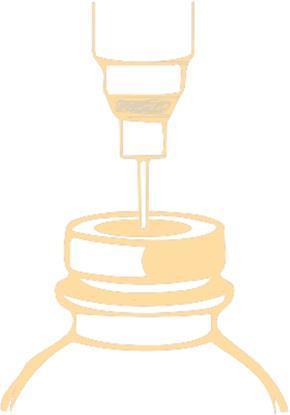
Para puncionar el tapón, debe utilizar una aguja con un diámetro no mayor que 0,8 mm (21 G en la escala Gauge [G]).
La aguja debe introducirse en el campo central designado con un ángulo de 90°.
Método de administración
Biotrakson se puede administrar por infusión intravenosa durante al menos 30 minutos (método de administración recomendado) o por inyección intravenosa lenta durante 5 minutos o por inyección intramuscular profunda.
En la inyección intravenosa intermitente, el medicamento debe administrarse durante 5 minutos, preferiblemente en una vena grande. En niños y lactantes, las dosis intravenosas de 50 mg/kg o más deben administrarse en forma de infusión. En recién nacidos, las dosis intravenosas deben administrarse durante un período más largo de 60 minutos para reducir el riesgo de encefalopatía por bilirrubina.
Las inyecciones intramusculares deben realizarse a una profundidad adecuada en un músculo relativamente grande; no debe inyectarse más de 1 g en un solo lugar. La administración intramuscular debe considerarse cuando la administración intravenosa no sea posible o no sea adecuada para el paciente.
Las dosis mayores que 2 g deben administrarse por vía intravenosa.
Para reconstituir Biotrakson o para diluir ulteriormente la solución preparada para administración intravenosa, no debe utilizar diluyentes que contengan calcio (por ejemplo, solución de Ringer o solución de Hartmann) debido al riesgo de precipitación. La sal de calcio de ceftriaxona también puede precipitar al mezclar ceftriaxona con una solución que contiene calcio en el mismo conjunto de administración intravenosa. Por lo tanto, no debe mezclar ni administrar ceftriaxona al mismo tiempo que soluciones que contengan calcio.
El volumen de eyección de Biotrakson de 1 g es de 0,68 ml, tanto en agua para inyección como en solución al 1% de lidocaína.
Después de agregar 10 ml de agua para inyección, la concentración final de la solución resultante es de 93,63 mg/ml. Después de agregar 3,5 ml de solución al 1% de lidocaína, la concentración final de la solución resultante es de 239,23 mg/ml.
El volumen de eyección de Biotrakson de 2 g es de 1,36 ml en agua para inyección.
Para evitar la precipitación de un sedimento en pacientes mayores de 28 días, ceftriaxona y soluciones que contengan calcio se pueden administrar secuencialmente uno después de otro, siempre que las líneas de infusión estén insertadas en lugares diferentes o se hayan intercambiado, o se hayan lavado cuidadosamente con solución fisiológica de cloruro de sodio entre las infusiones. Si es necesario administrar soluciones de nutrición parenteral total (TPN) que contengan calcio a pacientes, el personal médico especializado puede considerar el uso de métodos de tratamiento antibacteriano alternativos que no conlleven este riesgo de precipitación. Si se considera necesario el uso de ceftriaxona en pacientes que requieren nutrición parenteral total, ceftriaxona y soluciones de TPN se pueden administrar al mismo tiempo, pero a través de líneas de infusión diferentes insertadas en lugares diferentes. Otra opción es interrumpir la administración de TPN durante la infusión de ceftriaxona y lavar la línea de infusión entre las administraciones de las soluciones.
Preparación de soluciones para inyección e infusión
| Contenido de antibiótico en el vial | Volumen del diluyente | ||
| Inyección intramuscular | Inyección intravenosa | Infusión intravenosa | |
| 1 g | 3,5 ml | 10 ml | 40-50 ml |
| 2 g | 7,0 ml | 20 ml | 40-50 ml |
Antes de la administración, debe comprobar que la solución es transparente y no contiene partículas no disueltas.
Inyección intramuscular
El medicamento debe administrarse profundamente en el músculo después de disolverlo en la cantidad adecuada de agua para inyección o solución al 1% de lidocaína.
No debe mezclar el medicamento en la misma jeringa con otros medicamentos, excepto con una solución al 1% de lidocaína.
No debe administrar por vía intravenosa la solución del medicamento con lidocaína.
Las dosis mayores que 1 g deben dividirse y inyectarse en más de un lugar.
Las dosis mayores que 2 g deben administrarse por vía intravenosa.
Inyección intravenosa (5 minutos)
El contenido del vial se disuelve en agua para inyección en un volumen que depende de la dosis, como se muestra en la tabla anterior. No debe administrar por vía intravenosa la solución del medicamento con lidocaína.
Infusión intravenosa (al menos 30 minutos)
Para preparar soluciones para infusión intravenosa con una concentración de ceftriaxona de 10 mg/ml a 40 mg/ml, el polvo se disuelve en agua para inyección. La solución resultante se diluye entonces con uno de los siguientes diluyentes:
solución al 0,9% de cloruro de sodio;
solución al 5% de glucosa;
solución al 10% de glucosa;
solución al 6% de dextrano en solución al 5% de glucosa;
solución al 0,45% de cloruro de sodio en solución al 2,5% de glucosa.
No debe administrar por vía intravenosa la solución del medicamento con lidocaína.
La solución de Biotrakson puede ser incolora o ligeramente amarillenta; la intensidad de la coloración depende del tipo de diluyente y de la concentración de ceftriaxona.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorZakłady Farmaceutyczne POLPHARMA S.A. Zakłady Farmaceutyczne POLPHARMA S.A. Oddział Produkcyjny w Duchnicach
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a BiotraksonForma farmacéutica: Polvo, 1 gPrincipio activo: CeftriaxonaFabricante: Zakłady Farmaceutyczne POLPHARMA S.A. Zakłady Farmaceutyczne POLPHARMA S.A. Oddział Produkcyjny w DuchnicachRequiere recetaForma farmacéutica: Polvo, 1 gPrincipio activo: CeftriaxonaFabricante: ACS Dobfar S.p.A ACS Dobfar S.p.A.Requiere recetaForma farmacéutica: Polvo, 2 gPrincipio activo: CeftriaxonaFabricante: ACS Dobfar S.p.A ACS Dobfar S.p.A.Requiere receta
Alternativas a Biotrakson en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Biotrakson en España
Alternativa a Biotrakson en Ucrania
Médicos online para Biotrakson
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Biotrakson – sujeta a valoración médica y normativa local.















