How to use FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show translationContents of the leaflet
Introducción
PROSPECTO: INFORMACIÓN PARA EL USUARIO
FibCLOT 1,5g
Polvo y disolvente para solución inyectable y para perfusión
fibrinógeno humano
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es FibCLOT y para qué se utiliza
- Qué necesita saber antes de empezar a usar FibCLOT
- Cómo usar FibCLOT
- Posibles efectos adversos
- Conservación de FibCLOT
- Contenido del envase e información adicional
1. Qué es FibCLOT y para qué se utiliza
Qué es FibCLOT
Es un medicamento que pertenece al grupo de los antihemorrágicos. El principio activo es el fibrinógeno humano, una proteína presente de forma natural en el organismo. La función de esta proteína es asegurar que la sangre se coagule con normalidad y evitar que el sangrado dure demasiado tiempo.
Para qué se utiliza FibCLOT
Se utiliza en todos los grupos de edad para compensar la carencia de fibrinógeno humano y, de este modo, tratar el sangrado (hemorragias) en los pacientes con deficiencia de fibrinógeno congénita.
La deficiencia de fibrinógeno congénita es una enfermedad hereditaria caracterizada por una cantidad inferior a la normal o la ausencia de una proteína llamada fibrinógeno. Esta carencia puede provocar sangrados prolongados.
2. Qué necesita saber antes de empezar a usar FibCLOT
No use FibCLOT
Si es alérgico al principio activo (fibrinógeno humano) o a alguno de los demás componentes de este medicamento (incluidos en la sección 6. «Contenido del envase e información adicional»).
Informe a su médico si es alérgico a algún medicamento.
Advertencias y precauciones:
Consulte a su médico, farmacéutico o enfermero antes de empezar a usar FibCLOT.
Trazabilidad
Con el objetivo de mejorar la trazabilidad de los medicamentos biológicos, el nombre y el número de lote del medicamento administrado deben estar claramente registrados.
Riesgo de coágulos sanguíneos
Con dosis elevadas o administraciones repetidas, este medicamento puede aumentar el riesgo de coágulos en los vasos sanguíneos.
Por tanto, su médico debe sopesar los beneficios de este medicamento frente al riesgo de coágulos sanguíneos, especialmente:
- Si ha tenido un ataque al corazón (antecedentes de cardiopatía coronaria o infarto de miocardio).
- Si tiene una enfermedad hepática.
- Si acaba de someterse a una intervención quirúrgica.
- Si va a someterse pronto a una intervención quirúrgica.
- En recién nacidos (neonatos).
- Si tiene más probabilidades de lo normal de sufrir coágulos sanguíneos.
Su médico puede solicitarle pruebas adicionales para vigilar dicho riesgo.
Riesgo de alergias
Su médico le informará de las señales de advertencia de una reacción alérgica o de una reacción alérgica grave (reacción anafiláctica) (ver sección 4. «Posibles efectos adversos»). Si aparece alguno de estos efectos, debe interrumpirse inmediatamente la administración de este medicamento.
Seguridad vírica
Este medicamento se elabora a partir de plasma humano (la parte líquida de la sangre).
Cuando se elaboran medicamentos de sangre o plasma humanos, se adoptan ciertas medidas para impedir el contagio de infecciones a los pacientes. Algunas de estas medidas son:
- cuidadosa selección de los donantes de sangre y plasma, para garantizar que se descartan aquellos con riesgo de ser portadores de infecciones,
- comprobación de cada donación y mezclas de plasma para detectar signos de infecciones víricas,
- inclusión de etapas en el procesamiento de la sangre o el plasma que pueden inactivar o eliminar los virus.
A pesar de estas medidas, cuando se administran medicamentos derivados de la sangre o el plasma humanos, no puede descartarse por completo la posibilidad de contagio de una infección. Esto también se aplica a los virus desconocidos o emergentes y otros tipos de infecciones.
Las medidas adoptadas se consideran eficaces para los virus encapsulados, como el virus de la inmunodeficiencia humana (VIH o virus del SIDA), el virus de la hepatitis B y el virus de la hepatitis C y para el virus no encapsulado de la hepatitis A.
Las medidas adoptadas pueden tener un valor limitado frente a los virus no encapsulados como el parvovirus B19. La infección por parvovirus B19 puede ser grave en las mujeres embarazadas (infección del feto) y en las personas con el sistema inmunitario debilitado o con algunos tipos de anemia (por ejemplo, enfermedad de células falciformes o anemia hemolítica).
Si recibe de forma periódica/repetida productos derivados del plasma humano, su médico puede recomendarle que considere vacunarse contra la hepatitis A y B.
Riesgo inmunitario
En caso de terapia sustitutiva con factores de la coagulación en el contexto de otras deficiencias congénitas, se han observado reacciones inmunitarias, pero no se dispone de datos sobre el fibrinógeno.
Niños y adolescentes
Las advertencias y precauciones anteriormente indicadas son válidas para los niños y adolescentes.
Uso de FibCLOT con otros medicamentos
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento, incluso los adquiridos sin receta.
No se han observado interacciones entre este tratamiento y otros medicamentos hasta la fecha. No obstante, no debe mezclarse con otros productos y/o medicamentos.
Embarazo y lactancia
- Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico antes de utilizar este medicamento. Este medicamento solo debe utilizarse durante el embarazo y la lactancia por recomendación del médico.
- Consulte a su médico si descubre que está embarazada durante el tratamiento, ya que es el único que puede determinar si necesita seguir con él.
Conducción y uso de máquinas
La influencia de este medicamento sobre la capacidad para conducir y utilizar máquinas es nula.
FibCLOT contiene sodio.
Este medicamento contiene hasta 3 mmol (o 69 mg) de sodio (el principal componente de la sal de cocina o de mesa) por vial. Esta cantidad es equivalente al 3,45 % de la ingesta máxima diaria recomendada de sodio para un adulto.
Si está siguiendo una dieta baja en sal, deberá tenerlo en cuenta.
3. Cómo usar FibCLOT
El tratamiento debe iniciarse bajo la supervisión de un médico con experiencia en el tratamiento de la deficiencia de fibrinógeno congénita.
Dosis
Su médico será el que determine la dosis y la frecuencia apropiadas, que dependerán de los siguientes factores:
- su peso corporal,
- la gravedad de su trastorno,
- la localización y alcance del sangrado, o la naturaleza de su intervención quirúrgica,
- su estado de salud.
Su médico le recomendará que se realice análisis de sangre durante el tratamiento para comprobar la cantidad de fibrinógeno que tiene en el organismo.
Dependiendo del resultado de los análisis, su médico puede decidir adaptar la dosis y la frecuencia de las inyecciones.
Frecuencia de la administración
Su médico determinará con qué frecuencia deben administrarse las inyecciones.
Además, adaptará el número de inyecciones dependiendo de la intensidad del sangrado y la eficacia del tratamiento.
En la sección reservada a los profesionales sanitarios al final de este prospecto se incluye información sobre la frecuencia y la duración del tratamiento en diversas situaciones.
Forma de administración:
Este medicamento debe inyectarse en una vena. Es obligatorio el uso de un equipo de perfusión con filtro de 15 µm, como el suministrado con el envase.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
Si usa más FibCLOT del que debe
Para evitar el riesgo de sobredosis, el médico le realizará análisis de sangre periódicos para comprobar la cantidad de fibrinógeno que tiene en el organismo.
En caso de sobredosis, no puede descartarse el riesgo de formación anormal de coágulos en la sangre.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Los efectos adversos más graves son:
- Reacciones alérgicas:al igual que con cualquier producto proteínico intravenoso, pueden producirse reacciones alérgicas. En algunos casos, estas reacciones han empeorado hasta convertirse en una reacción alérgica grave, a veces con un descenso pronunciado de la presión arterial (choque anafiláctico).
Las señales de advertencia de las reacciones alérgicas son:
- sensación de ardor y hormigueo en el lugar de inyección,
- hormigueo,
- enrojecimiento, picazón y erupción,
- urticaria,
- inflamación cutánea,
- palidez,
- hinchazón de la cara o la garganta,
- tos,
- sibilancia (similar a la de tipo asmático),
- opresión en el pecho,
- frecuencia cardiaca rápida,
- presión arterial baja,
- cansancio extremo (letargia),
- inquietud,
- escalofrío,
- sensación de enfermedad (náuseas), vómitos,
Si se produce alguno de estos efectos, póngase en contacto inmediatamente conun médico, que suspenderá el tratamiento de este medicamento y/oiniciará el tratamiento oportuno dependiendo del tipo y la intensidad de la reacción. |
- Coágulos sanguíneos: pueden formarse coágulos sanguíneos en el torrente circulatorio. Estos pueden producir:
- un ataque al corazón, cuyas señales de advertencia son dolor repentino en el pecho o respiración difícil;
- un ictus, cuyas señales de advertencia son aparición repentina de debilidad muscular, pérdida de las sensaciones y/o el equilibrio, disminución del estado de alerta o dificultad para hablar;
- una enfermedad grave llamada embolia pulmonar (coágulo sanguíneo que obstruye una arteria de los pulmones), cuyas señales de advertencia son dolor en el pecho, dificultad para respirar o tos con sangre;
- un coágulo en una vena (trombosis venosa), cuyas señales de advertencia son enrojecimiento, sensación de calor, dolor, dolor a la palpación o hinchazón en una o las dos piernas.
Si se produce alguno de estos efectos, póngase en contacto inmediatamente conun médico, que suspenderá el tratamiento con este medicamento y/oiniciará el tratamiento oportuno dependiendo del tipo y la intensidad de la reacción. |
Los siguientes efectos adversos son frecuentes(pueden afectar en hasta 1 de cada 10 perfusiones):
- cefalea.
Los siguientes efectos adversos son poco frecuentes(pueden afectar en hasta de 1 de cada 100 perfusiones):
- reacción alérgica (como shock anafiláctico, palidez, vómitos, tos, presión arterial baja, escalofrío, habón urticarial [urticaria]; ver también la sección «Reacciones alérgicas»),
- mareo,
- vomitos (asociados con cefalea)
- pitido en los oídos,
- trastornos de la circulación sanguínea (trombosis venosa profunda, flebotrombosis superficial),
- dificultad para respirar (asma),
- erupción cutánea, enrojecimiento de la piel, irritación de la piel, sudores nocturnos,
- sensación de calor.
Niños y adolescentes
La frecuencia, el tipo y la gravedad de los efectos adversos son similares en los pacientes pediátricos (desde el nacimiento hasta los 17 años incluidos) y adultos, salvo en lo que respecta a las reacciones de tipo alérgicas o anafilácticas, que se produjeron con más frecuencia en la población pediátrica.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de FibCLOT
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y la caja. La fecha de caducidad es el último día del mes que se indica.
No conservar a temperatura superior a 25 °C. No congelar.
Conservar el vial en el embalaje exterior para protegerlo de la luz y la humedad.
El producto debe utilizarse inmediatamente después de la reconstitución. No conservar el producto reconstituido.
No utilice este medicamento si la solución reconstituida está turbia o contiene sedimento.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de FibCLOT
El principio activo es fibrinógeno humano (1,5 g por vial). Tras la reconstitución con 100 mL de agua para preparaciones inyectables, FibCLOT contiene 15 mg/mL de fibrinógeno humano.
Los demás componentes son hidrocloruro de arginina, isoleucina, hidrocloruro de lisina, glicina, citrato de sodio dihidratado y disolvente (agua para preparaciones inyectables).
Aspecto del producto y contenido del envase
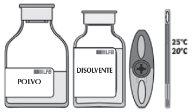
Este medicamento se presenta en forma de polvo acompañado de disolvente para solución para preparaciones inyectables en viales de vidrio, un equipo de transferencia y un equipo de perfusión con un filtro de 15 µm.
La solución reconstituida debe ser prácticamente incolora, ligeramente opalescente (debe tener un brillo perlado).
Titular de la autorización de comercialización:
Laboratoire français du Fractionnement et des Biotechnologies
Tour W – 102 Boieldieu 19ème Étage, 92800 Puteaux, FRANCIA
Tel.: +33(0) 1 69 82 70 10
Fax: +33(0) 1 69 82 19 03
Responsable de la fabricación:
LFB BIOMEDICAMENTS
59 rue de Trévise, 59000 Lille, FRANCIA
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
LFB BIOTERAPIAS HISPANIA
C/ Diego de León 47
28006 Madrid
(España)
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo con los siguientes nombres:
Alemania, Austria, España, Grecia, Reino Unido: FibCLOT
Dinamarca, Finlandia, Hungría, Luxemburgo, Noruega, Países Bajos, Suecia: FibclotBélgica: Fibclot 1,5 g, poudre et solvant pour solution injectable/pour perfusion
Italia: Fibriclotte
Fecha de la última revisión de este prospecto: 06/2024
---------------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario:
El tratamiento debe iniciarse bajo la supervisión de un médico con experiencia en el tratamiento de los trastornos de la coagulación.
Posología
La dosis y la duración de la terapia sustitutiva dependen de la gravedad del trastorno, la localización y la magnitud de la hemorragia, así como del estado clínico del paciente.
Debe determinarse la concentración de fibrinógeno (funcional) con el fin de calcular la dosis individual; además, la cantidad y la frecuencia de la administración deben calcularse para cada paciente concreto mediante la determinación periódica de la concentración de fibrinógeno en plasma y la supervisión continua del estado clínico del paciente y de las demás terapias sustitutivas empleadas.
La concentración normal de fibrinógeno en plasma oscila entre 1,5 y 4,5 g/L. En la hipo o afibrinogenemia congénita, la concentración crítica de fibrinógeno en plasma por debajo de la cual pueden producirse hemorragias es aproximadamente de entre 0,5 y 1,0 g/L.
En el caso de una intervención quirúrgica mayor, es esencial supervisar la terapia de sustitución mediante ensayos de coagulación.
Tratamiento de las hemorragias y profilaxis perioperatoria en pacientes con hipo o afibrinogenemia congénita y tendencia al sangrado conocida.
Para el tratamiento de los episodios hemorrágicos no quirúrgicos, se recomienda aumentar la concentración de fibrinógeno a 1 g/L y mantener dicha concentración hasta que la hemostasia esté controlada, y por encima de 0,5 g/L hasta que la cicatrización haya finalizado.
Para evitar el sangrado excesivo durante los procedimientos quirúrgicos, se recomienda un tratamiento profiláctico para aumentar la concentración de fibrinógeno a 1 g/L y mantener dicha concentración hasta que la hemostasia esté controlada, y por encima de 0,5 g/L hasta que la cicatrización haya finalizado.
En el caso de un procedimiento quirúrgico o el tratamiento de una hemorragia no quirúrgica, la dosis debe calcularse del siguiente modo:
Dosis (g) = [concentración deseada (g/L) - concentración basal (g/L)] x 1/recuperación (g/L) (g/kg) x peso corporal (kg),
El «ratio 1/recuperación» está definido por la recuperación* del paciente (ver sección 5.2 de la ficha técnica), o si la recuperación es desconocida:
- 0,053 (g/kg)/(g/L) para niños y adolescentes <40 kg de peso corporal
- 0,043 (g/kg)/(g/L) para adultos y adolescentes ?40 kg de peso corporal.
- Ejemplo para la recuperación del paciente y el cálculo de la dosis
Para un paciente de 60 kg con una concentración basal de fibrinógeno indetectable y un aumento de fibrinógeno a 1,20 g/L 1 hora después de la perfusión de 0,060 g por kg de FibCLOT:
- Cálculo de la recuperación del paciente:
1,20 (g/L) / 0,060 (g/kg) = 20,0 (g/L)/(g/kg)
- Cálculo de la dosis para un aumento a 1,0 g/L:
1,0 g/L x 1 / 20,0 (g/L)/(g/kg) [o 0,050 (g/kg)/(g/L)]x 60 kg = 3 g
En caso de producirse una situación de urgencia en la que se desconozca la concentración basal de fibrinógeno, la dosis inicial recomendada es de 0,05 g por kg de peso corporal administrada por vía intravenosa en adultos y adolescentes ?40 kg de peso corporal, y de 0,06 g/kg de peso corporal en los pacientes pediátricos < 40 kg de peso corporal.
La posología posterior (dosis y frecuencia de las inyecciones) debe adaptarse en función del estado clínico y los resultados analíticos del paciente.
La semivida biológica del fibrinógeno es de entre 3 y 4 días. Por tanto, si no existe consumo, no suele ser necesario el tratamiento repetido con fibrinógeno humano. Teniendo en cuenta la acumulación que se produce con la administración repetida con fines profilácticos, la dosis y la frecuencia deben determinarse en función de los objetivos terapéuticos del médico para cada paciente concreto.
Población pediátrica
La recuperación y la semivida en niños y adolescentes ?40 kg de peso corporal es inferior a la de los adultos y adolescentes ?40 kg de peso corporal (ver sección 5.2 de la ficha técnica). Por consiguiente, deben usarse recuperaciones adaptadas para calcular la dosis de FibCLOT en los grupos de peso corporal respectivos cuando no se conozca la recuperación individual del paciente. Cabe suponer que un peso corporal de < 40 kg cubre el rango de edad desde el nacimiento hasta los 12 años de edad aproximadamente. La posología (dosis y frecuencia de las inyecciones) debe adaptarse según la respuesta clínica individual del paciente.
Reconstitución:
Siga las directrices vigentes para procedimientos asépticos.
| En caso necesario, caliente los dos viales (polvo y disolvente) hasta que alcancen la temperatura ambiente. |
| Retire la cápsula protectora del vial de disolvente y la del vial de polvo. Desinfecte la superficie de ambos tapones. |
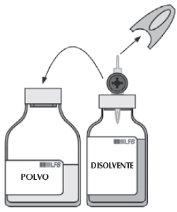
| Retire la funda protectora translúcida del equipo de transferencia y, con un movimiento giratorio, introduzca completamente el punzón que queda a la vista en el centro del tapón del vial de disolvente. |
| Retire la segunda funda protectora gris del otro extremo del equipo de transferencia. Gire el vial de disolvente e introduzca rápidamente el extremo libre del punzón en el centro del tapón del vial de polvo para permitir que el disolvente llegue hasta el polvo. Asegúrese de que el punzón permanece sumergido en todo momento en el disolvente, para evitar que el vacío desaparezca antes de tiempo. |
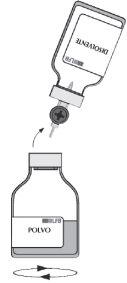
| Durante la transferencia, realice un movimiento giratorio horizontal para que el chorro de disolvente se reparta por toda la superficie del polvo y la pared del vial. Asegúrese de que se transfiere todo el disolvente. El vacío se elimina automáticamente al final del procedimiento de transferencia mediante el aire estéril que atraviesa el respiradero del equipo de transferencia. |
| Retire el vial vacío (disolvente) con el equipo de transferencia. Para evitar que se forme espuma, agite suavemente durante unos minutos, con un movimiento rotatorio, hasta que el polvo esté completamente disuelto. |
Antes de administrar el producto reconstituido, debe examinarse visualmente para comprobar que no contenga partículas. La solución reconstituida debe ser prácticamente incolora y ligeramente opalescente. No utilice las soluciones turbias o con sedimentos.
Administración:
FibCLOT debe administrarse únicamente por vía intravenosa, como dosis única, inmediatamente después de la reconstitución y a una velocidad que no supere los 4 mL/min.
Es obligatorio el uso de un equipo de perfusión con filtro de 15 µm, como el suministrado con el envase.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
Este medicamento no debe mezclarse con otros y deberá administrarse con un catéter de inyección/perfusión diferente.
-


- Country of registration
- Dosage formINJECTABLE, 1.5 g
- ATC codeB02BB01
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSIONDosage form: INJECTABLE, 1 gActive substance: fibrinogen, humanManufacturer: Octapharma S.A.Prescription requiredDosage form: INJECTABLE, 1 g (20 mg/mL)Active substance: fibrinogen, humanManufacturer: Csl Behring GmbhPrescription requiredDosage form: INJECTABLE, 1,000 IUActive substance: coagulation factor VIIIManufacturer: Takeda Manufacturing Austria AgPrescription required
Online doctors for FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION
Discuss questions about FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Get FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION Prescription Online
Fill in a 2-min form
Tell us your symptoms, history, and what medicine you're requesting.
Pick a doctor or let us assign
Choose a specialist or we'll match you with the next available doctor.
Doctor reviews your case
Usually within 30 minutes. They may ask follow-up questions via chat.
Collect from any pharmacy
Electronic prescription sent to your email — valid across Spain.
Frequently Asked Questions
FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION requires a prescription in Spain. You can check with a doctor online whether this medicine may be appropriate for your situation.
The active ingredient in FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION is fibrinogen, human. This information helps identify medicines with the same composition but different brand names.
FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION is manufactured by Laboratoire Francais Du Fractionnement Et Des Biotechnologies. Pharmacy brands and packaging may differ depending on the distributor.
Doctors such as Family doctors, Psychiatrists, Dermatologists, Cardiologists, Endocrinologists, Gastroenterologists, Pulmonologists, Nephrologists, Rheumatologists, Hematologists, Infectious disease physicians, Allergists, Geriatricians, Paediatricians, Oncologists may assess whether FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION is appropriate, depending on your situation and local regulations. You can book an online consultation to discuss your symptoms and possible next steps.
Spain has a well-developed healthcare infrastructure across major cities such as Madrid, Barcelona, Valencia, and Seville. Pharmacies are widely available and operate under strict regulations, ensuring access to prescribed medications.
You can buy FIBCLOT 1.5 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION in Madrid, Barcelona, Seville, or Valencia at any local pharmacy with a valid prescription.
To obtain a prescription, you can use Oladoctor:
Other medicines with the same active substance (fibrinogen, human) include FIBRYGA 1 g POWDER AND SOLVENT FOR INJECTABLE SOLUTION AND FOR INFUSION, RIASTAP 1 g POWDER FOR INJECTABLE SOLUTION OR INFUSION, ADVATE 1,000 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION. These may have different brand names or formulations but contain the same therapeutic ingredient. Always consult a doctor before switching or starting a new medicine.