How to use BYOOVIZ 10 mg/ml INJECTABLE SOLUTION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show translationContents of the leaflet
Introducción
Prospecto: información para el paciente adulto
Byooviz 10 mg/ml solución inyectable
ranibizumab
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
ADULTOS
Lea todo el prospecto detenidamente antes de que le administren este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico.
- Si experimenta efectos adversos, consulte a su médico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Byooviz y para qué se utiliza
- Qué necesita saber antes de que le administren Byooviz
- Cómo se administra Byooviz
- Posibles efectos adversos
- Conservación de Byooviz
- Contenido del envase e información adicional
1. Qué es Byooviz y para qué se utiliza
Qué es Byooviz
Byooviz es una solución que se inyecta en el ojo. Byooviz pertenece a un grupo de medicamentos denominados agentes antineovascularización. Contiene el principio activo denominado ranibizumab.
Para qué se utiliza Byooviz
Byooviz se utiliza en adultos para tratar varias enfermedades oculares que causan alteración de la visión.
Estas enfermedades son el resultado de una lesión en la retina (capa sensible a la luz en la parte posterior del ojo) provocada por:
- El crecimiento de vasos sanguíneos anómalos, que pierden líquido. Esto se observa en enfermedades como la degeneración macular asociada a la edad (DMAE) y la retinopatía diabética proliferativa (RDP, una enfermedad provocada por la diabetes). También puede ir asociado con la neovascularización coroidea (NVC) debida a miopía patológica (MP), estrías angioides, coriorretinopatía serosa central o NVC inflamatoria.
- Edema macular (hinchazón del centro de la retina). La causa de esta hinchazón puede ser la diabetes (una enfermedad conocida como edema macular diabético [EMD]) o un bloqueo de las venas retinianas de la retina (una enfermedad conocida como oclusión de la vena de la retina [OVR]).
Cómo actúa Byooviz
Byooviz reconoce y se une de forma específica a una proteína denominada factor de crecimiento endotelial vascular A (VEGF-A) humano presente en los ojos. En exceso, el VEGF-A causa el crecimiento de vasos sanguíneos anómalos e hinchazón en el ojo que puede ocasionar una alteración de la visión en enfermedades como DMAE, EMD, RDP, OVR, MP y NVC. Mediante la unión al VEGF-A, Byooviz puede impedir que actúe y prevenir dicho crecimiento e hinchazón anómalos.
En estas enfermedades, Byooviz puede ayudar a estabilizar y, en muchos casos, mejorar su visión.
2. Qué necesita saber antes de que le administren Byooviz
No le deben administrar Byooviz
- Si es alérgico al ranibizumab o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si tiene una infección en el ojo o alrededor del mismo.
- Si tiene dolor o enrojecimiento (inflamación intraocular grave) en el ojo.
Advertencias y precauciones
Consulte a su médico antes de que le administren Byooviz.
- Byooviz se administra mediante una inyección en el ojo. Ocasionalmente, tras el tratamiento con Byooviz puede aparecer una infección en la parte interna del ojo, dolor o enrojecimiento (inflamación), desprendimiento o desgarro de una de las capas situadas en la parte posterior del ojo (desprendimiento o desgarro de la retina y desprendimiento o desgarro del epitelio pigmentario de la retina), o enturbiamiento del cristalino (catarata). Es importante identificar y tratar tal infección o desprendimiento de retina lo antes posible. Informe inmediatamente a su médico si nota signos como dolor en el ojo o aumento de las molestias en el ojo, si empeora el enrojecimiento en el ojo, visión borrosa o disminución de la visión, un aumento del número de pequeñas manchas en la visión o aumento de la sensibilidad a la luz.
- En algunos pacientes, justo después de la inyección la presión en el ojo puede aumentar durante un corto periodo de tiempo. Es posible que usted no se dé cuenta de ello, por lo que puede que su médico le realice un seguimiento de la presión ocular después de cada inyección.
- Informe a su médico si ha tenido enfermedades en los ojos o ha recibido algún tratamiento en los ojos anteriormente, o si ha sufrido un accidente cerebrovascular o ha tenido signos pasajeros de accidente cerebrovascular (debilidad o parálisis de una extremidad o cara, dificultad en el habla o en la comprensión). Esta información se tendrá en consideración para evaluar si Byooviz es el tratamiento apropiado para usted.
Para consultar información más detallada sobre los efectos adversos que podrían ocurrir durante el tratamiento con Byooviz, ver sección 4 (“Posibles efectos adversos”).
Niños y adolescentes (menores de 18 años)
No se ha establecido el uso de Byooviz en niños y adolescentes y, por lo tanto, no está recomendado.
Otros medicamentos y Byooviz
Informe a su médico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Embarazo y lactancia
- Las mujeres que pudieran quedarse embarazadas deben utilizar un método anticonceptivo eficaz durante el tratamiento y durante al menos los tres meses posteriores a la última inyección de Byooviz.
- No hay experiencia en el uso de Byooviz en mujeres embarazadas. Byooviz no se debe usar durante el embarazo salvo que el beneficio potencial supere el riesgo potencial para el feto. Si está embarazada, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico antes del tratamiento con Byooviz.
- Pequeñas cantidades de ranibizumab pueden pasar a la leche materna, por lo que no se recomienda el uso de Byooviz durante la lactancia. Consulte a su médico o farmacéutico antes del tratamiento con Byooviz.
Conducción y uso de máquinas
Después del tratamiento con Byooviz usted puede experimentar visión borrosa temporalmente. Si esto le ocurre, no conduzca ni use máquinas hasta que este síntoma desaparezca.
3. Cómo se administra Byooviz
Byooviz se administra por el oftalmólogo en forma de inyección única en el ojo bajo anestesia local. La dosis habitual de una inyección es 0,05 ml (que contiene 0,5 mg de principio activo). El intervalo entre dos dosis aplicadas en el mismo ojo debe ser como mínimo de cuatro semanas. Todas las inyecciones serán administradas por un oftalmólogo.
Para prevenir una infección, antes de la inyección su médico le lavará el ojo cuidadosamente. Su médico también le administrará un anestésico local para reducir o prevenir cualquier dolor que pudiera sentir con la inyección.
El tratamiento se inicia con una inyección de Byooviz cada mes. Su médico controlará la enfermedad de su ojo y dependiendo de cómo responda al tratamiento, decidirá si necesita o no recibir más tratamiento y cuándo necesita ser tratado.
Al final del prospecto en el apartado “Cómo preparar y administrar Byooviz” se dan instrucciones detalladas de uso.
Pacientes de edad avanzada (65 años y mayores)
Byooviz puede utilizarse en personas de 65 años de edad o más, y no es necesario un ajuste de la dosis.
Antes de interrumpir el tratamiento con Byooviz
Si usted se está planteando interrumpir el tratamiento con Byooviz, acuda a la siguiente consulta y coméntelo antes con su médico. Su médico le aconsejará y decidirá durante cuánto tiempo debe ser tratado con Byooviz.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Los efectos adversos asociados con la administración de Byooviz se deben o al propio medicamento o al procedimiento de inyección y la mayoría afectan al ojo.
A continuación se describen los efectos adversos más graves:
Efectos adversos graves frecuentes(pueden afectar hasta 1 de cada 10 pacientes): desprendimiento o desgarro de la capa en la parte posterior del ojo (desprendimiento o desgarro de la retina), que da como resultado destellos de luz con partículas flotantes que progresan a una pérdida de visión transitoria o a un enturbiamiento del cristalino (catarata).
Efectos adversos graves poco frecuentes(pueden afectar hasta 1 de cada 100 pacientes): ceguera, infección del globo ocular (endoftalmitis) con inflamación de la parte interna del ojo.
Los síntomas que podría experimentar son dolor o aumento de las molestias en el ojo, empeoramiento del enrojecimiento en el ojo, visión borrosa o disminución de la visión, un aumento del número de pequeñas manchas en la visión o aumento de la sensibilidad a la luz. Informe a su médico inmediatamente si presenta alguno de estos efectos adversos.
A continuación se describen los efectos adversos comunicados más frecuentemente:
Efectos adversos muy frecuentes(pueden afectar a más de 1 de cada 10 pacientes)
Los efectos adversos oculares incluyen: inflamación del ojo, sangrado en la parte posterior del ojo (hemorragia en la retina), alteraciones visuales, dolor en el ojo, pequeñas partículas o manchas en la visión (partículas flotantes), sangre en el ojo, irritación del ojo, sensación de tener algo dentro del ojo, aumento de la producción de lágrima, inflamación o infección en el borde de los párpados, ojo seco, enrojecimiento o picor en el ojo y aumento de la presión en el ojo.
Los efectos adversos no oculares incluyen: dolor de garganta, congestión nasal, goteo nasal, dolor de cabeza y dolor en las articulaciones.
A continuación se describen otros efectos adversos que pueden ocurrir tras el tratamiento con Byooviz:
Efectos adversos frecuentes
Los efectos adversos oculares incluyen: disminución de la nitidez de la visión, hinchazón de una sección del ojo (úvea, córnea), inflamación de la córnea (parte delantera del ojo), pequeñas marcas en la superficie del ojo, visión borrosa, sangrado en el lugar de inyección, sangrado en el ojo, secreción del ojo con picor, enrojecimiento e hinchazón (conjuntivitis), sensibilidad a la luz, molestias en el ojo, hinchazón del párpado, dolor en el párpado.
Los efectos adversos no oculares incluyen: infección de las vías urinarias, recuento de glóbulos rojos bajo (con síntomas tales como cansancio, dificultad al respirar, mareo, palidez), ansiedad, tos, náuseas, reacciones alérgicas tales como erupción, urticaria, picor y enrojecimiento de la piel.
Efectos adversos poco frecuentes
Los efectos adversos oculares incluyen: inflamación y sangrado en la parte anterior del ojo, acúmulo de pus en el ojo, cambios en la parte central de la superficie ocular, dolor o irritación en el lugar de inyección, sensación anormal en el ojo, irritación del párpado.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Byooviz
- Mantener este medicamento fuera de la vista y del alcance de los niños.
- No utilice este medicamento después de la fecha de caducidad que aparece en la caja después de CAD y en la etiqueta del vial después de EXP. La fecha de caducidad es el último día del mes que se indica.
- Conservar en nevera (entre 2 ºC y 8 ºC). No congelar.
- Antes de usar, el vial sin abrir se puede conservar a temperaturas que no excedan los 30 ºC durante un máximo de 2 meses.
- Conservar el vial en el embalaje exterior para protegerlo de la luz.
- No utilice ningún envase que esté dañado.
6. Contenido del envase e información adicional
Composición de Byooviz
- El principio activo es ranibizumab. Cada ml contiene 10 mg de ranibizumab. Cada vial contiene 2,3 mg de ranibizumab en 0,23 ml de solución. Esto aporta una cantidad adecuada para proporcionar una dosis única de 0,05 ml, que contiene 0,5 mg de ranibizumab.
- Los demás componentes son a,a-trehalosa dihidrato; hidrocloruro de histidina monohidrato; histidina; polisorbato 20; agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Byooviz es una solución inyectable contenida en un vial (0,23 ml). La solución es transparente, de incolora a amarillo pálido y acuosa.
Se dispone de dos tipos de envase diferentes:
Envase solo con vial
Envase que contiene un vial de vidrio con ranibizumab, con tapón de goma de clorobutilo. El vial es para un solo uso.
Envase con un vial + aguja con filtro + aguja para inyección
Envase que contiene un vial de vidrio con ranibizumab, con tapón de goma de clorobutilo, una aguja roma con filtro (18G x 1½″, 1,2 mm x 40 mm, 5 micrómetros) para extraer el contenido del vial y una aguja para inyección (30G x ½″, 0,3 mm x 13 mm). Todos los componentes son para un solo uso.
Puede que solamente estén comercializados algunos tipos de envases.
Titular de la autorización de comercialización y responsable de la fabricación
Samsung Bioepis NL B.V.
Olof Palmestraat 10
2616 LR Delft
Países Bajos
Fecha de la última revisión de este prospecto: Julio 2025
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu
ESTA INFORMACIÓN ESTÁ DESTINADA ÚNICAMENTE A PROFESIONALES DEL SECTOR SANITARIO:
Ver también la sección 3 “Cómo se administra Byooviz”.
Cómo preparar y administrar Byooviz en adultos
Vial para un solo uso. Únicamente para vía intravítrea.
Byooviz debe ser administrado por un oftalmólogo que tenga experiencia en la administración de inyecciones intravítreas.
En la DMAE exudativa, en la NVC, en la RDP y en la alteración visual debida a EMD o a edema macular secundario a OVR la dosis recomendada de Byooviz es 0,5 mg administrada en forma de inyección intravítrea única. Esto corresponde a un volumen de inyección de 0,05 ml. El intervalo entre dos dosis inyectadas en el mismo ojo debe ser como mínimo de cuatro semanas.
El tratamiento se inicia con una inyección al mes hasta alcanzar la agudeza visual máxima y/o no haya signos de actividad de la enfermedad, es decir ningún cambio en la agudeza visual ni en otros signos y síntomas de la enfermedad bajo tratamiento continuado. En pacientes con DMAE exudativa, EMD, RDP y OVR inicialmente pueden ser necesarias tres o más inyecciones consecutivas administradas mensualmente.
A partir de ese momento, los intervalos de monitorización y tratamiento se deben determinar según criterio médico y en base a la actividad de la enfermedad, valorada mediante la agudeza visual y/o parámetros anatómicos.
Se debe interrumpir el tratamiento con Byooviz si, bajo criterio del médico, los parámetros visuales y anatómicos indican que el paciente no se está beneficiando del tratamiento continuado.
La monitorización para determinar la actividad de la enfermedad puede incluir examen clínico, control funcional o técnicas de imagen (p. ej., tomografía de coherencia óptica o angiografía con fluoresceína).
Si se está tratando a los pacientes de acuerdo a un régimen de tratar y extender, una vez se ha alcanzado la agudeza visual máxima y/o no hay signos de actividad de la enfermedad, los intervalos de tratamiento se pueden espaciar de forma gradual hasta que vuelvan a aparecer signos de actividad de la enfermedad o alteración visual. En el caso de la DMAE exudativa el intervalo de tratamiento no debe espaciarse en más de dos semanas cada vez y en el caso del EMD se puede espaciar hasta un mes cada vez. Para la RDP y la OVR, los intervalos de tratamiento también pueden espaciarse de forma gradual; sin embargo, los datos que hay no son suficientes para determinar la duración de estos intervalos. Si vuelve a aparecer actividad de la enfermedad, se debe acortar el intervalo de tratamiento de manera consecuente.
El tratamiento de la alteración visual debida a NVC se debe determinar para cada paciente de forma individualizada en base a la actividad de la enfermedad. Algunos pacientes pueden necesitar solo una inyección durante los primeros 12 meses; otros pueden necesitar tratamiento con mayor frecuencia, incluyendo una inyección mensual. En el caso de la NVC secundaria a miopía patológica (MP), muchos pacientes pueden necesitar solo una o dos inyecciones durante el primer año.
Ranibizumab y fotocoagulación con láser en EMD y edema macular secundario a oclusión de la rama venosa retiniana (ORVR)
Existe alguna experiencia con ranibizumab administrado concomitantemente con fotocoagulación con láser. Cuando se administren en el mismo día, ranibizumab debe ser administrado como mínimo 30 minutos después de la fotocoagulación con láser. Ranibizumab puede administrarse en pacientes que han recibido fotocoagulación con láser previamente.
Ranibizumab y terapia fotodinámica con verteporfina en la NVC secundaria a MP
No hay experiencia en la administración concomitante de ranibizumab y verteporfina.
Antes de la administración de Byooviz se debe comprobar visualmente la ausencia de partículas y decoloración.
El procedimiento de inyección debe llevarse a cabo bajo condiciones asépticas, que incluyen el lavado quirúrgico de las manos, el uso de guantes estériles, un campo estéril, un blefarostato estéril para los párpados (o equivalente) y la disponibilidad de una paracentesis estéril (en caso necesario). Antes de realizar el procedimiento de inyección intravítrea, se debe evaluar detalladamente la historia clínica del paciente en cuanto a reacciones de hipersensibilidad. Antes de la inyección se debe administrar una anestesia adecuada y un microbicida tópico de amplio espectro para desinfectar la piel de la zona periocular, párpado y superficie ocular, de acuerdo con la práctica local.
Envase solo con vial
El vial es para un solo uso. Tras la inyección se debe desechar cualquier sobrante de producto no utilizado. No debe utilizarse ningún vial que muestre signos de deterioro o manipulación. La esterilidad solo se puede garantizar si el sellado del envase se mantiene intacto.
Para la preparación y la inyección intravítrea se necesitan los siguientes productos sanitarios (para un solo uso):
- una aguja con filtro de 5 µm (18G)
- una aguja para inyección (30G x ½″)
- una jeringa estéril de 1 ml (que incluya una marca en 0,05 ml)
Estos productos sanitarios no se incluyen en el envase de Byooviz.
Envase con vial + aguja con filtro + aguja para inyección
Todos los componentes son estériles y para un solo uso. No se debe utilizar ningún componente cuyo envase muestre signos de deterioro o manipulación. La esterilidad solo se puede garantizar si el sellado del envase de los componentes se mantiene intacto. La reutilización puede dar lugar a una infección u otra enfermedad/lesión.
Para la preparación y la inyección intravítrea se necesitan los siguientes productos sanitarios (para un solo uso):
- una aguja con filtro de 5 µm (18G x 1½″, 1,2 mm x 40 mm, suministrada)
- una aguja para inyección (30G x ½″, 0,3 mm x 13 mm, suministrada)
- una jeringa estéril de 1 ml (que incluya una marca en 0,05 ml, no incluida en el envase de Byooviz)
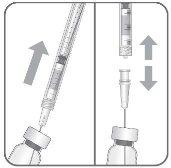
Para la preparación de Byooviz para administración intravítrea en pacientes adultos, siga las siguientes instrucciones:
|
|
|
|
|
Nota: Sujetar la aguja para inyección por el cono mientras se retira la cápsula de cierre.
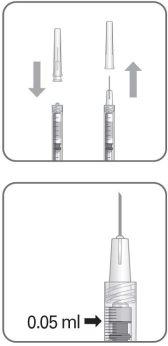
Nota: No secar la aguja para inyección. No tirar del émbolo hacia atrás. |
La aguja para inyección se debe introducir 3,5-4,0 mm por detrás del limbo en la cavidad vítrea, evitando el meridiano horizontal y en dirección al centro del globo. Seguidamente debe liberarse el volumen de inyección de 0,05 ml; las inyecciones siguientes deben aplicarse cada vez en un punto escleral distinto.
Tras la inyección, no tapar la aguja con la cápsula de cierre ni separarla de la jeringa. Eliminar la jeringa usada junto con la aguja en un contenedor para objetos punzantes o eliminar de acuerdo con la normativa local.
- Country of registration
- Dosage formINJECTABLE, 10 mg/mL
- ATC codeS01LA04
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to BYOOVIZ 10 mg/ml INJECTABLE SOLUTIONDosage form: INJECTABLE, 10 mg/mLActive substance: ranibizumabManufacturer: Novartis Europharm LimitedPrescription requiredDosage form: INJECTABLE, 10 mg/mLActive substance: ranibizumabManufacturer: Novartis Europharm LimitedPrescription requiredDosage form: INJECTABLE, 10 mg/mlActive substance: ranibizumabManufacturer: Midas Pharma GmbhPrescription required
Online doctors for BYOOVIZ 10 mg/ml INJECTABLE SOLUTION
Discuss questions about BYOOVIZ 10 mg/ml INJECTABLE SOLUTION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Get BYOOVIZ 10 mg/ml INJECTABLE SOLUTION Prescription Online
Fill in a 2-min form
Tell us your symptoms, history, and what medicine you're requesting.
Pick a doctor or let us assign
Choose a specialist or we'll match you with the next available doctor.
Doctor reviews your case
Usually within 30 minutes. They may ask follow-up questions via chat.
Collect from any pharmacy
Electronic prescription sent to your email — valid across Spain.
Frequently Asked Questions
BYOOVIZ 10 mg/ml INJECTABLE SOLUTION requires a prescription in Spain. You can check with a doctor online whether this medicine may be appropriate for your situation.
The active ingredient in BYOOVIZ 10 mg/ml INJECTABLE SOLUTION is ranibizumab. This information helps identify medicines with the same composition but different brand names.
BYOOVIZ 10 mg/ml INJECTABLE SOLUTION is manufactured by Samsung Bioepis Nl B.V.. Pharmacy brands and packaging may differ depending on the distributor.
Doctors such as Family doctors, Psychiatrists, Dermatologists, Cardiologists, Endocrinologists, Gastroenterologists, Pulmonologists, Nephrologists, Rheumatologists, Hematologists, Infectious disease physicians, Allergists, Geriatricians, Paediatricians, Oncologists may assess whether BYOOVIZ 10 mg/ml INJECTABLE SOLUTION is appropriate, depending on your situation and local regulations. You can book an online consultation to discuss your symptoms and possible next steps.
Spain has a well-developed healthcare infrastructure across major cities such as Madrid, Barcelona, Valencia, and Seville. Pharmacies are widely available and operate under strict regulations, ensuring access to prescribed medications.
You can buy BYOOVIZ 10 mg/ml INJECTABLE SOLUTION in Madrid, Barcelona, Seville, or Valencia at any local pharmacy with a valid prescription.
To obtain a prescription, you can use Oladoctor:
Other medicines with the same active substance (ranibizumab) include LUCENTIS 10 mg/ml Injectable Solution in Pre-filled Syringe, LUCENTIS 10 mg/ml INJECTABLE SOLUTION, RANIVISIO 10 mg/ml INJECTABLE SOLUTION IN PRE-FILLED SYRINGE. These may have different brand names or formulations but contain the same therapeutic ingredient. Always consult a doctor before switching or starting a new medicine.