
FANHDI 50 IU FVIII/60 IU FVW per ml POWDER AND SOLVENT FOR INJECTABLE SOLUTION

How to use FANHDI 50 IU FVIII/60 IU FVW per ml POWDER AND SOLVENT FOR INJECTABLE SOLUTION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
Introduction
Package Leaflet: Information for the User
Fanhdi 25 UI FVIII/30 UI FVW per ml, powder and solvent for solution for injection
Fanhdi 50 UI FVIII/60 UI FVW per ml, powder and solvent for solution for injection
Fanhdi 100 UI FVIII/120 UI FVW per ml, powder and solvent for solution for injection
human coagulation factor VIII and von Willebrand factor complex
Read all of this leaflet carefully before you start using this medicine because it contains important information for you.
- Keep this leaflet. You may need to read it again.
- If you have any further questions, ask your doctor or pharmacist.
- This medicine has been prescribed for you only. Do not pass it on to others. It may harm them, even if their signs of illness are the same as yours.
- If you get any side effects, talk to your doctor, pharmacist or nurse. This includes any possible side effects not listed in this leaflet. See section 4.
Contents of the pack
- What is Fanhdi and what is it used for
- What you need to know before you use Fanhdi
- How to use Fanhdi
- Possible side effects
- Storage of Fanhdi
- Contents of the pack and other information
1. What is Fanhdi and what is it used for
Fanhdi belongs to a group of medicines called antihemorrhagics: blood coagulation factors: von Willebrand factor and factor VIII coagulation in combination.
This medicine is used for:
Hemophilia A
Fanhdi is indicated for the treatment and prophylaxis (prevention) of bleeding in patients with hemophilia A (congenital deficiency of factor VIII). These patients do not have enough functional factor VIII. Fanhdi serves to increase the amount of factor VIII in the blood, allowing it to clot.
This product may be useful in the management of acquired factor VIII deficiency.
von Willebrand disease
Fanhdi is indicated for the treatment of bleeding and surgical bleeding treatment and prophylaxis in patients with von Willebrand disease (VWD) when treatment with desmopressin (DDAVP) alone is not effective or is contraindicated.
Patients may suffer from different types of VWD. All types of VWD are innate diseases where bleeding can last longer than expected. This may be due to a lack of VWF in the blood or because VWF does not work as it should.
2. What you need to know before you use Fanhdi
Do not use Fanhdi
If you are allergic to the human coagulation factor VIII and von Willebrand factor complex or to any of the other components of this medicine (listed in section 6).
If you have any doubts about the above, consult your doctor.
Warnings and precautions
Consult your doctor, pharmacist, or nurse before starting to use Fanhdi.
- There is a remote possibility that you may experience an anaphylactic reaction (severe allergic reaction). If you observe skin rashes or generalized urticaria, feel chest tightness, dizziness, vertigo, or nausea, or if you feel dizzy while standing, you may be suffering from an anaphylactic reaction to Fanhdi. If this occurs, immediately discontinue administration of the product and seek medical attention.
- It is possible that your doctor may want to perform some tests to ensure that the dose you receive from Fanhdi is sufficient to achieve and maintain adequate levels of factor VIII.
The formation of inhibitors (antibodies) is a known complication that can occur during treatment with all medicines composed of factor VIII. These inhibitors, especially in large quantities, prevent the treatment from working properly, so you and your child will be carefully monitored for the development of such inhibitors. If your bleeding or your child's bleeding is not being controlled with Fanhdi, consult your doctor immediately.
- If you have previously developed factor VIII inhibitors and have changed from one factor VIII product to another, you may develop inhibitors again.
- In the case of von Willebrand disease treatment, there is a risk of thrombotic events, particularly in patients with clinical risk factors. Therefore, your doctor should perform some tests to detect early signs of thrombosis and initiate treatment against vascular thromboembolism according to current recommendations.
- Patient with von Willebrand disease, especially those patients with type 3, may develop neutralizing antibodies (inhibitors) to von Willebrand factor. Von Willebrand factor inhibitors are antibodies present in the blood that block the von Willebrand factor you are using. If the expected levels of von Willebrand factor activity in plasma are not achieved, or if bleeding is not controlled with the appropriate dose, your doctor should perform tests to determine the presence of von Willebrand factor inhibitor. This makes von Willebrand factor less effective in controlling bleeding.
- If you are going to need a central venous access device (CVAD) for the administration of Fanhdi, your doctor should consider the risk of complications related to CVAD, including local infections, presence of bacteria in the blood (bacteremia), and the formation of a blood clot in the blood vessel (thrombosis) where the catheter is inserted.
- When medicines are manufactured from human blood or plasma, a number of measures must be taken to prevent the possible transmission of infections to patients. These measures include careful selection of blood and plasma donors to ensure the exclusion of donors at risk of infection, analysis of each donation and plasma pools for possible viruses or infections, and inclusion of a series of stages in the processing of blood or plasma that can inactivate or eliminate viruses.
Despite these measures, when medicines prepared from human blood or plasma are administered, the possibility of transmission of infections cannot be completely excluded. This applies to unknown or emerging viruses and other types of infections.
The measures taken are considered effective for enveloped viruses such as human immunodeficiency virus (HIV), hepatitis B virus, and hepatitis C virus, and for the non-enveloped hepatitis A virus. The measures taken may have limited value for non-enveloped viruses such as parvovirus B19.
Parvovirus B19 infection can be severe for a pregnant woman (fetal infection) and for individuals whose immune system is depressed or who have some type of anemia (e.g., with sickle cell anemia or hemolytic anemia).
Your doctor may recommend that you consider vaccination against hepatitis A and B if you regularly receive human plasma-derived factor VIII concentrates.
Each time you are administered a dose of Fanhdi, it is recommended to record the name and batch number of the medicine to keep a record of the batches used.
See also section 4.
Children and adolescents
The warnings and precautions indicated apply to both adults and children.
Using Fanhdi with other medicines
Tell your doctor or pharmacist if you are taking, have recently taken, or might take any other medicines.
No interactions have been observed between the human coagulation factor VIII and von Willebrand factor complex and other medicines.
Pregnancy and breastfeeding
Consult your doctor or pharmacist before using any medicine.
During pregnancy and breastfeeding, the FVIII/FVW complex may only be used if it is clearly indicated.
Driving and using machines
There is no indication that Fanhdi may affect the ability to drive vehicles or use machines.
Sodium content
The residual sodium content in Fanhdi, derived from the manufacturing process, does not exceed 23 mg per vial in the 250, 500, and 1000 UI presentations, and 34.5 mg per vial in the 1500 UI presentation. This is equivalent to 1.15% and 1.72%, respectively, of the maximum daily sodium intake recommended for an adult. However, depending on the patient's weight and dosage, the patient may receive more than one vial.
3. How to use Fanhdi
The product must be administered intravenously. The administration rate should not exceed 10 ml/min.
Follow exactly the administration instructions indicated by your doctor or the healthcare staff at the hemophilia center. If you have any doubts, consult your doctor or pharmacist.
The amount of Fanhdi you should use depends on many factors, such as your weight, clinical condition, and the location and importance of the bleeding. Your doctor will calculate the dose of Fanhdi and how often and at what intervals it should be administered to achieve the necessary level of factor VIII or von Willebrand factor in your blood.
Your doctor will indicate the duration of your treatment with Fanhdi.
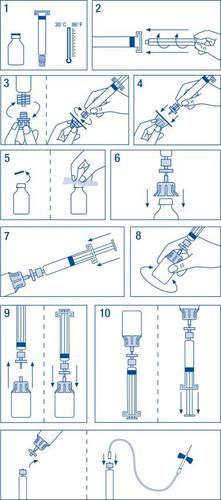
Preparation of the solution:
Make sure you work in the most suitable conditions at all stages of the process to avoid contaminating the product.
- Bring the vial and syringe of solvent to room temperature without exceeding 30 °C.
- Attach the plunger to the syringe of solvent.
- Remove the seal from the filter. Separate the cap from the cone of the syringe of solvent and attach it to the filter.
- Remove the seal from the vial adapter and attach it to the filter-syringe assembly.
- Remove the seal from the vial, disinfecting the cap with one of the alcohol swabs.
- Insert the spike of the adapter into the vial.
- Transfer all the solvent from the syringe to the vial.
- Gently rotate the vial, trying not to produce foam, until the powder is completely dissolved. Do not shake. As with all parenteral products, do not use if the dissolution is incomplete or if particles are present.
- Separate the filter-syringe assembly from the rest to facilitate subsequent aspiration of the solution and immediately reattach the filter-syringe assembly to the vial.
- Invert the vial and aspirate the contents into the syringe.
Administration
Prepare the patient's injection site, separate the syringe from the rest, and inject the product using the supplied butterfly needle at a rate of 3 ml/min intravenously. The administration rate should not exceed 10 ml/min to avoid vasomotor reactions.
It is recommended to use the injection equipment supplied with the medicine. In the case of using medical perfusion equipment, check the compatibility of the system with the preloaded syringe. An adapter may be required to ensure adequate administration of the product.
Administration equipment should not be reused. In no case should the unused fraction be reused, nor should it be stored in the refrigerator.
If you use more Fanhdi than you should
No cases of overdose with human coagulation factor VIII and von Willebrand factor complex have been reported. However, if you have used Fanhdi more than you should, consult your doctor or pharmacist immediately.
In case of overdose or accidental administration, consult the Toxicology Information Service. Telephone 91 562 04 20.
If you forget to use Fanhdi
- Proceed immediately with the next administration and continue at regular intervals following your doctor's instructions.
- Do not administer a double dose to make up for forgotten doses.
4. Possible side effects
Like all medicines, this medicine can cause side effects, although not everybody gets them.
In rare cases, you may notice some of these side effects after administration of Fanhdi:
- Itching, local reactions at the injection site (e.g., burning sensation or tingling and transient redness)
- Allergic reactions (e.g., chest tightness/general feeling of discomfort, difficulty breathing, dizziness, nausea, and slight drop in blood pressure that may cause dizziness while standing)
- Unusual taste in the mouth
- Fever
- Tachycardia
- Restlessness
- Headache
- Drowsiness
- Vomiting
- Chills
It cannot be completely excluded that you may experience an anaphylactic shock. If you notice any of the following symptoms during administration:
- Chest tightness/general feeling of discomfort
- Dizziness
- Mild hypotension (slight decrease in blood pressure with dizziness while standing)
- Nausea
it may be an early sign of hypersensitivity and anaphylactic reaction. If an allergic or anaphylactic reaction occurs, administration should be discontinued and your doctor consulted immediately.
Hemophilia A
In children who have not previously received treatment with factor VIII medicines, inhibitory antibodies (see section 2) may frequently occur (more than 1 in 10 patients); however, in patients who have received previous treatment with factor VIII (more than 150 days of treatment), the risk is infrequent (less than 1 in 100 patients). If this happens, the medicines you or your child are taking may stop working properly, and you or your child may suffer from persistent bleeding. In this case, contact your doctor immediately.
von Willebrand disease
When a von Willebrand factor product containing factor VIII is used to treat von Willebrand disease, continued treatment may cause an excessive increase in factor VIII in the blood. This may increase the risk of altered blood flow (thrombosis).
If you are a patient with known clinical or laboratory risk factors, you should be monitored for early signs of thrombosis. Your doctor should establish prevention (prophylaxis) of thrombotic episodes according to current recommendations.
Especially if you are a patient with type 3 von Willebrand disease, you may rarely develop neutralizing antibodies (inhibitors) to von Willebrand factor. If such inhibitors appear, von Willebrand factor is less effective in controlling bleeding. In case your bleeding continues, the presence of these inhibitors should be analyzed in your blood. These antibodies may appear associated with anaphylactic reactions. Therefore, in patients who experience anaphylactic reactions, the presence of inhibitors should be evaluated. In such cases, consult your doctor immediately.
For information on viral safety, see section 2.
Reporting of side effects
If you experience any side effects, talk to your doctor, pharmacist, or nurse. This includes any possible side effects not listed in this leaflet. You can also report side effects directly through the Spanish Medicines Vigilance System for Human Use: www.notificaRAM.es
By reporting side effects, you can help provide more information on the safety of this medicine.
5. Storage of Fanhdi
Keep this medicine out of the sight and reach of children.
Do not store above 30 °C. Do not freeze.
Do not use this medicine after the expiry date stated on the carton after "EXP".
Do not use this medicine if you notice that the solution is turbid or contains sediment. The solution is usually clear or slightly opalescent.
Once reconstituted, the solution should be discarded if particles are observed inside or if any discoloration is noted.
After reconstitution, the product is chemically and physically stable for 12 hours at 25 °C. From a microbiological point of view, the product should be used immediately. If not used immediately, the storage time and conditions before use are the responsibility of the user and will normally not exceed 24 hours at 2 °C - 8 °C, unless reconstitution has been performed under controlled and validated aseptic conditions.
Any unused product and waste material should be disposed of in accordance with local requirements.
Medicines should not be disposed of via wastewater or household waste. Ask your pharmacist how to dispose of medicines no longer required. This will help protect the environment.
6. Additional Information
Composition of Fanhdi
- The active ingredient is the complex of human coagulation factor VIII and human von Willebrand factor. Once reconstituted, Fanhdi contains 25 IU FVIII/30 IU FVW per ml, 50 IU FVIII/60 IU FVW per ml, or 100 IU FVIII/120 IU FVW per ml. See below "Presentations of Fanhdi".
- The other components are albumin, histidine, and arginine.
Appearance of the Product and Package Contents
Vial containing white or pale yellow powder and syringe with water for injectable preparations (solvent).
Box contents: 1 vial of lyophilized product, 1 pre-filled syringe of solvent, and accessories (vial adapter, filter, 2 alcohol swabs, and butterfly needle).
Presentations of Fanhdi
Fanhdi 25 IU FVIII/30 IU FVW per ml
It is presented as a powder for injectable solution containing 250 IU of human coagulation factor VIII and 300 IU of human von Willebrand factor per vial, which is reconstituted with 10 ml of water for injections.
Fanhdi 50 IU FVIII/60 IU FVW per ml
It is presented as a powder for injectable solution containing 500 IU of human coagulation factor VIII and 600 IU of human von Willebrand factor per vial, which is reconstituted with 10 ml of water for injections.
Fanhdi 100 IU FVIII/120 IU FVW per ml
It is presented as a powder for injectable solution containing 1000 IU of human coagulation factor VIII and 1200 IU of human von Willebrand factor per vial, which is reconstituted with 10 ml of water for injections.
Or
It is presented as a powder for injectable solution containing 1500 IU of human coagulation factor VIII and 1800 IU of human von Willebrand factor per vial, which is reconstituted with 15 ml of water for injections.
Marketing Authorization Holder and Manufacturer
Instituto Grifols, S.A.
Can Guasc, 2 - Parets del Vallès
08150 Barcelona – SPAIN
Date of the Last Revision of this Prospectus:
December 2020.
Detailed and updated information on this medicinal product is available on the website of the Spanish Agency for Medicines and Health Products (AEMPS) http://www.aemps.gob.es//
……………………………………………………………………………………………………………
This information is intended only for healthcare professionals:
Dosage
Hemophilia A
The dosage and duration of treatment depend on the severity of the factor VIII deficiency, the location and degree of bleeding, and the patient's clinical condition.
The number of units of factor VIII administered is expressed in International Units (IU), in relation to the World Health Organization (WHO) standard for factor VIII concentrates. The plasma activity of factor VIII is expressed as a percentage (in relation to normal human plasma) or in International Units (in relation to an international standard for factor VIII in plasma).
One International Unit (IU) of factor VIII activity is equivalent to the amount of factor VIII in one ml of normal human plasma.
On-demand treatment
The calculation of the required dose of factor VIII is based on the empirical observation that 1 International Unit (IU) of factor VIII per kg of body weight increases the plasma activity of factor VIII by 2.1 ± 0.4% of normal activity. The required dose is determined using the following formula:
Units required = body weight (kg) x desired increase in factor VIII (%) (IU/dl) x 0.5
The dose and frequency of administration should be calculated according to the patient's clinical response.
In the case of bleeding episodes as detailed below, the factor VIII activity should not be lower than the established plasma activity level (in % of normal plasma or IU/dl) during the corresponding period. The following table can be used as a dosage guide for bleeding episodes and surgery:
Severity of bleeding/ Type of surgery | Required factor VIII level (%)(IU/dl) | Dosing frequency (hours)/Duration of therapy (days) |
Bleeding | ||
Minor hemarthrosis and muscle or oral bleeding | 20 - 40 | Repeat every 12 - 24 hours. At least 1 day, until the bleeding episode manifested by pain stops or until healing. |
Moderate hemarthrosis and muscle bleeding or hematoma | 30 - 60 | Repeat administration every 12 - 24 hours for 3 - 4 days or more until pain and acute disability disappear. |
Life-threatening bleeding | 60 - 100 | Repeat administration every 8 - 24 hours until the risk disappears. |
Surgery | ||
Minor surgery including dental extractions Major surgery | 30 - 60 80 - 100 (pre- and postoperative) | Every 24 hours, at least 1 day until healing. Repeat administration every 8 - 24 hours until adequate wound healing, and continue therapy for at least 7 days to maintain a factor VIII activity level of 30% to 60% (IU/dl). |
Prophylaxis
In long-term prophylaxis to prevent bleeding in patients with severe hemophilia A, doses of 20 to 40 IU of FVIII/kg of body weight should be administered at intervals of 2 to 3 days. In some cases, especially in young patients, it may be necessary to shorten the administration intervals or use higher doses.
Von Willebrand Disease (VWD)
Generally, 1 IU of VWF:RCo/kg increases the circulating level of VWF:RCo by approximately 2%. Levels of VWF:RCo > 0.6 IU/ml (60%) and FVIII:C > 0.4 IU/ml (40%) should be achieved.
Normally, 40 - 80 IU/kg of von Willebrand factor (VWF:RCo) and 20 - 40 IU/kg of FVIII:C are recommended to achieve hemostasis.
An initial dose of 80 IU/kg of von Willebrand factor may be required, especially in patients with type 3 von Willebrand disease, where maintaining adequate levels may require higher doses than in other types of von Willebrand disease.
An appropriate dose should be readministered every 12 - 24 hours. The dose and duration of treatment depend on the patient's clinical condition, the type and severity of bleeding, and the levels of VWF:RCo and FVIII:C.
In the use of a von Willebrand factor preparation that contains factor VIII, the treating physician should consider that continued treatment may cause excessive increase in FVIII:C. After 24 - 48 hours of treatment, and to avoid excessive increase in FVIII:C, reduction of the dose and/or prolongation of the administration interval, or the use of products with von Willebrand factor that contain a low level of factor VIII, should be considered.
Pediatric Population
The safety and efficacy of Fanhdi have not been established in children under 6 years of age for the authorized indications.
The dosage in children 6 years of age or older is not considered different from that of adults, as it is associated with body weight and adjusted to the clinical outcome of the conditions indicated above.
- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to FANHDI 50 IU FVIII/60 IU FVW per ml POWDER AND SOLVENT FOR INJECTABLE SOLUTIONDosage form: INJECTABLE, 100 IU FVIII/ 120 IU FVW per mlActive substance: von Willebrand factor and coagulation factor VIII in combinationManufacturer: Instituto Grifols S.A.Prescription requiredDosage form: INJECTABLE, 25 IU FVIII/ 30 IU FVW per mlActive substance: von Willebrand factor and coagulation factor VIII in combinationManufacturer: Instituto Grifols S.A.Prescription requiredDosage form: INJECTABLE, 500 IU Factor VIIIActive substance: von Willebrand factor and coagulation factor VIII in combinationManufacturer: Csl Behring S.A.Prescription required
Online doctors for FANHDI 50 IU FVIII/60 IU FVW per ml POWDER AND SOLVENT FOR INJECTABLE SOLUTION
Discuss questions about FANHDI 50 IU FVIII/60 IU FVW per ml POWDER AND SOLVENT FOR INJECTABLE SOLUTION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions















