
АФСТИЛА 3000 МЕ ПОРОШОК И РАСТВОРИТЕЛЬ ДЛЯ ПРИГОТОВЛЕНИЯ ИНЪЕКЦИОННОГО РАСТВОРА


Инструкция по применению АФСТИЛА 3000 МЕ ПОРОШОК И РАСТВОРИТЕЛЬ ДЛЯ ПРИГОТОВЛЕНИЯ ИНЪЕКЦИОННОГО РАСТВОРА
Введение
Прошу: информация для пользователя
АФСТИЛА 250 МЕ, порошок и растворитель для инъекционного раствора
АФСТИЛА 500 МЕ, порошок и растворитель для инъекционного раствора
АФСТИЛА 1 000 МЕ, порошок и растворитель для инъекционного раствора
АФСТИЛА 1 500 МЕ, порошок и растворитель для инъекционного раствора
АФСТИЛА 2 000 МЕ, порошок и растворитель для инъекционного раствора
АФСТИЛА 2 500 МЕ, порошок и растворитель для инъекционного раствора
АФСТИЛА 3 000 МЕ, порошок и растворитель для инъекционного раствора
лономкотовг альфа (рекомбинантный фактор свертывания VIII с единственной цепью)
Прочитайте внимательно весь листок инструкции перед тем, как вы или ваш ребенок начнете использовать это лекарство, поскольку в нем содержится важная информация для вас.
- Сохраните этот листок инструкции, поскольку вам может понадобиться прочитать его снова.
- Если у вас есть какие-либо вопросы, проконсультируйтесь с вашим врачом, фармацевтом или медсестрой.
- Это лекарство было назначено только вам или вашему ребенку и не должно быть передано другим людям, даже если у них такие же симптомы, как у вас, поскольку оно может нанести им вред.
- Если вы испытываете побочные эффекты, проконсультируйтесь с вашим врачом, фармацевтом или медсестрой, даже если это возможные побочные эффекты, которые не указаны в этом листке инструкции. См. раздел 4.
Содержание листка инструкции:
- Что такое АФСТИЛА и для чего оно используется
- Что вам нужно знать перед тем, как вы или ваш ребенок начнете использовать АФСТИЛА
- Как использовать АФСТИЛА
- Возможные побочные эффекты
- Хранение АФСТИЛА
- Содержание упаковки и дополнительная информация
1. Что такое АФСТИЛА и для чего оно используется
АФСТИЛА - это препарат с фактором свертывания VIII человека, который производится с помощью технологии рекомбинантной ДНК. Активным веществом АФСТИЛА является лономкотовг альфа.
АФСТИЛА используется для лечения и профилактики геморрагических эпизодов у пациентов с гемофилией А (врожденным дефицитом фактора VIII). Фактор VIII - это белок, необходимый для свертывания крови. У пациентов с гемофилией А отсутствует этот фактор, поэтому их кровь не свертывается так быстро, как должна, и существует повышенный риск кровотечения. АФСТИЛА действует, заменяя отсутствующий фактор VIII у пациентов с гемофилией А, что позволяет их крови свертываться нормально.
АФСТИЛА можно использовать во всех возрастных группах.
2. Что вам нужно знать перед тем, как начать использовать АФСТИЛА
Не используйте АФСТИЛА
- Если пациент имел потенциально смертельную аллергическую реакцию на АФСТИЛА или любой из его компонентов (перечисленных в разделе 6).
- Если пациент аллергичен к белкам хомяка.
Предостережения и меры предосторожности
Отслеживаемость
Важно вести учет номера партии АФСТИЛА.
Следовательно, каждый раз, когда вы используете новый пакет АФСТИЛА, записывайте дату и номер партии (который указан на коробке после "Партия") и сохраняйте эту информацию в безопасном месте.
Проконсультируйтесь с вашим врачом, фармацевтом или медсестрой перед началом использования АФСТИЛА.
- Могут возникнуть аллергические реакции (гиперчувствительность). Препарат содержит остатки белков хомяка (см. также "Не используйте АФСТИЛА"). Если出现 симптомы аллергии, немедленно прекратите лечение и свяжитесь с вашим врачом.Ваш врач должен проинформировать вас о первых признаках аллергических реакций. Это включает в себя крапивницу, общую сыпь, давление на грудь, затруднение дыхания, падение артериального давления и анафилаксию (тяжелую аллергическую реакцию, вызывающую тяжелые трудности с дыханием и головокружение).
- Формирование ингибиторов(антител) - это известная осложнение, которое может возникнуть во время лечения всеми препаратами, содержащими фактор VIII. Эти ингибиторы, особенно в больших количествах, препятствуют правильному функционированию лечения. Вы или ваш ребенок будете тщательно наблюдаться на предмет развития ингибиторов. Если у вас или вашего ребенка не контролируется кровотечение с помощью АФСТИЛА, немедленно проконсультируйтесь с вашим врачом.
- Если вам сказали, что у вас или вашего ребенка есть сердечно-сосудистое заболевание или риск его развития, сообщите об этом вашему врачу или фармацевту.
- Если используется устройство для центрального венозного доступа (ЦВД) для введения АФСТИЛА, ваш врач должен рассмотреть и обсудить с вами риск осложнений, таких как местные инфекции, бактериемия и образование тромбов в кровеносных сосудах в месте введения.
Другие лекарства и АФСТИЛА
Сообщите вашему врачу или фармацевту, если вы используете, недавно использовали или можете использовать любое другое лекарство.
Беременность и лактация
- Если вы беременны или кормите грудью, считаете, что можете быть беременной или планируете стать беременной, проконсультируйтесь с вашим врачом или фармацевтом перед использованием этого лекарства.
- Во время беременности и лактации АФСТИЛА следует использовать только в случае явной необходимости.
Вождение и использование машин
АФСТИЛА не влияет на вашу способность управлять транспортными средствами или работать с машинами.
АФСТИЛА содержит натрий
Это лекарство содержит 35 мг натрия (основного компонента поваренной соли) в каждом флаконе. Это эквивалентно 1,8% от максимально допустимой суточной нормы потребления натрия для взрослого.
3. Как использовать АФСТИЛА
Ваше лечение должно быть под наблюдением врача с опытом лечения нарушений свертывания крови.
Следуйте точно инструкциям по введению этого лекарства, указанным вашим врачом. В случае сомнений проконсультируйтесь с вашим врачом снова.
Доза
Количество АФСТИЛА, которое вам или вашему ребенку необходимо, и продолжительность лечения зависят:
- от тяжести вашего заболевания
- от места и интенсивности кровотечения
- от вашего клинического состояния и реакции на лечение
- от вашего веса
Следуйте инструкциям, указанным вашим врачом.
Переработка и введение
Общие инструкции
- Порошок должен быть смешан с растворителем (жидкостью) и извлечен из флакона в асептических условиях.
- АФСТИЛА не должен быть смешан с другими лекарствами или растворителями, кроме тех, которые указаны в разделе 6.
- Раствор должен быть прозрачным или слегка опалесцирующим, желтым или бесцветным, т.е. он может блестеть при освещении, но не должен содержать видимых частиц. После фильтрации или извлечения раствора (см. ниже) его необходимо проверить снова перед использованием. Не используйте раствор, если он显но мутный или содержит хлопья или частицы.
- Утилизация неиспользованного продукта и всех остальных материалов должна быть проведена в соответствии с местными правилами и указаниями вашего врача.
Переработка и введение
Не открывая ни один из флаконов, убедитесь, что порошок АФСТИЛА и жидкость находятся при комнатной температуре или температуре тела. Это можно сделать, оставив флаконы при комнатной температуре примерно на час или держа их в руках несколько минут. Не подвергайте флаконы прямому нагреву. Флаконы не должны быть нагреты выше температуры тела (37 °C).
Аккуратно удалите защитные колпачки с флаконов и затем очистите открытую часть резиновых пробок ватной палочкой, смоченной в спирте. Дайте флаконам высохнуть, прежде чем открыть упаковку Mix2Vial (которая содержит перистальтический насос с фильтром), и затем следуйте инструкциям, указанным ниже.
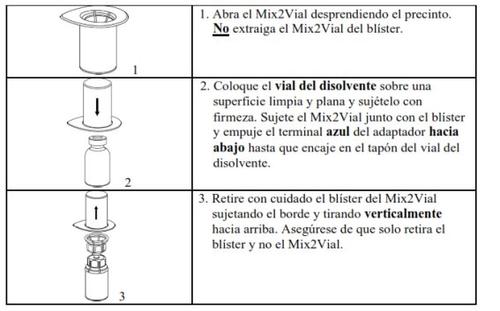

Используйте набор для венепункции, поставляемый с продуктом, и вставьте иглу в вену. Дайте крови течь до конца трубки. Подключите шприц к резьбовому концу набора для венепункции. Медленно вводите реконституированный раствор (с скоростью, которая вам удобна, до максимальных 10 мл/мин) в венув соответствии с инструкциями, которые дал вам ваш врач. Постарайтесь, чтобы кровь не попала в шприц, содержащий препарат.
Проверьте, испытываете ли вы побочные эффекты сразу после введения. Если вы испытываете любой побочный эффект, который может быть связан с введением АФСТИЛА, введение должно быть прекращено (см. также раздел 2).
Использование у детей и подростков
АФСТИЛА может быть использован у детей и подростков всех возрастов. В случае с детьми младше 12 лет может потребоваться более высокая доза или более частое введение. У детей старше 12 лет можно использовать такую же дозу, как и у взрослых.
Если вы использовали больше АФСТИЛА, чем положено
Если было введено больше АФСТИЛА, чем положено, сообщите об этом вашему врачу.
Если вы пропустили использование АФСТИЛА
Не вводите двойную дозу, чтобы компенсировать пропущенную дозу. Введите следующую дозу немедленно и следуйте инструкциям вашего врача.
Если вы прекратили лечение АФСТИЛА
Если вы прекратите использование АФСТИЛА, вы можете перестать быть защищенным от кровотечения или можете не остановить кровотечение, если у вас есть текущее кровотечение. Не прекращайте использование АФСТИЛА без предварительной консультации с вашим врачом.
Если у вас есть какие-либо другие вопросы о использовании этого лекарства, проконсультируйтесь с вашим врачом, фармацевтом или медсестрой.
4. Возможные побочные эффекты
Как и все лекарства, АФСТИЛА может вызывать побочные эффекты, хотя не все люди испытывают их.
Немедленно прекратите использование лекарства и свяжитесь с вашим врачом:
- если вы заметили симптомы аллергических реакций
- Могут возникнуть аллергические реакции, которые включают следующие симптомы: крапивница, общая сыпь, давление на грудь, затруднение дыхания, низкое кровяное давление и анафилаксия (тяжелая аллергическая реакция, вызывающая тяжелые трудности с дыханием или головокружение). Если это происходит, немедленно прекратите лечение и свяжитесь с вашим врачом.
- если вы заметили, что лекарство перестало действовать правильно(кровотечение не останавливается) Для детей, которые не были ранее лечены препаратами фактора VIII, могут часто образовываться ингибиторы (антитела) (см. раздел 2); однако у пациентов, которые получали предыдущее лечение фактором VIII (более 150 дней лечения), риск является редким (менее 1 из 100 пациентов). Если у вас или вашего ребенка образовался ингибитор из-за лекарства, вы можете испытывать постоянное кровотечение. Если это происходит, немедленно свяжитесь с вашим врачом.
Частые побочные эффекты (могут возникнуть у до 1 из 10 человек)
- Онемение или покалывание (парестезия).
- Сыпь на коже.
- Лихорадка.
Редкие побочные эффекты (могут возникнуть у до 1 из 100 человек)
- Зуд.
- Покраснение кожи.
- Боль в месте введения.
- Озноб.
- Чувство жара.
Побочные эффекты у детей и подростков
Не было обнаружено никаких специфических возрастных различий в побочных реакциях между детьми, подростками и взрослыми.
Сообщение о побочных эффектах
Если вы испытываете любой побочный эффект, проконсультируйтесь с вашим врачом, фармацевтом или медсестрой, даже если это возможные побочные эффекты, которые не указаны в этом листке инструкции. Вы также можете сообщить о них напрямую через национальную систему уведомления, указанную в Приложении V. Сообщая о побочных эффектах, вы можете внести свой вклад в предоставление более полной информации о безопасности этого лекарства.
5. Хранение АФСТИЛА
- Храните это лекарство в недоступном для детей месте.
- Не используйте это лекарство после даты истечения срока годности, указанной на этикетке и коробке.
- Храните в холодильнике (при температуре между 2 °C и 8 °C).
- До реконституирования порошка АФСТИЛА его можно хранить при комнатной температуре (ниже 25 °C) в течение единого периода, не превышающего 3 месяцев, в пределах срока годности, указанного на коробке и флаконе. Запишите дату, с которой вы начали хранить АФСТИЛА при комнатной температуре, на коробке лекарства.
- Как только лекарство было удалено из холодильника, его нельзя снова помещать в холодильник.
- Не замораживайте.
- Храните флакон в коробке, чтобы защитить его от света.
- Как только препарат был реконституирован, его следует использовать предпочтительно немедленно.
- Если реконституированный продукт не вводится немедленно, сроки и условия хранения до его использования являются ответственностью пользователя.
6. Содержание упаковки и дополнительная информация
Состав АФСТИЛА
Активное вещество:
250 МЕ на флакон; после восстановления 2,5 мл воды для инъекционных препаратов, раствор содержит 100 МЕ/мл лоноктокога альфа.
500 МЕ на флакон; после восстановления 2,5 мл воды для инъекционных препаратов, раствор содержит 200 МЕ/мл лоноктокога альфа.
1000 МЕ на флакон; после восстановления 2,5 мл воды для инъекционных препаратов, раствор содержит 400 МЕ/мл лоноктокога альфа.
1500 МЕ на флакон; после восстановления 5 мл воды для инъекционных препаратов, раствор содержит 300 МЕ/мл лоноктокога альфа.
2000 МЕ на флакон; после восстановления 5 мл воды для инъекционных препаратов, раствор содержит 400 МЕ/мл лоноктокога альфа.
2500 МЕ на флакон; после восстановления 5 мл воды для инъекционных препаратов, раствор содержит 500 МЕ/мл лоноктокога альфа.
3000 МЕ на флакон; после восстановления 5 мл воды для инъекционных препаратов, раствор содержит 600 МЕ/мл лоноктокога альфа.
Другие компоненты:
Л-истидин, полисорбат 80, дигидрат хлорида кальция, хлорид натрия (см. последний раздел раздела 2), сахароза.
Растворитель: вода для инъекционных препаратов.
Внешний вид АФСТИЛА и содержание упаковки
АФСТИЛА представлен в виде белого или слегка желтоватого порошка или рыхлой массы и прозрачного бесцветного растворителя для инъекционного раствора.
Восстановленный раствор должен быть прозрачным или слегка опалесцирующим, желтоватым или бесцветным, т.е. может блестеть при освещении, но не должен содержать видимых частиц.
Презентации
Упаковка с 250, 500 или 1000 МЕ, содержащая:
1 флакон с порошком
1 флакон с 2,5 мл воды для инъекционных препаратов
1 переливатель с фильтром 20/20
Внутренняя коробка, содержащая:
1 одноразовая инъекционная система объемом 5 мл
1 набор для венепункции
2 ватных шарика, пропитанных спиртом
1 нестерильный повязочный материал
Упаковка с 1500, 2000, 2500 или 3000 МЕ, содержащая:
1 флакон с порошком
1 флакон с 5 мл воды для инъекционных препаратов
1 переливатель с фильтром 20/20
Внутренняя коробка, содержащая:
1 одноразовая инъекционная система объемом 10 мл
1 набор для венепункции
2 ватных шарика, пропитанных спиртом
1 нестерильный повязочный материал
Могут быть доступны только некоторые размеры упаковки.
Первичная упаковка
250 МЕ | Стеклянный флакон с резиновой пробкой, оранжевым пластиковым диском и алюминиевой крышкой с зелеными полосами |
500 МЕ | Стеклянный флакон с резиновой пробкой, синим пластиковым диском и алюминиевой крышкой с зелеными полосами |
1000 МЕ | Стеклянный флакон с резиновой пробкой, зеленым пластиковым диском и алюминиевой крышкой с зелеными полосами |
1500 МЕ | Стеклянный флакон с резиновой пробкой, бирюзовым пластиковым диском и алюминиевой крышкой с зелеными полосами |
2000 МЕ | Стеклянный флакон с резиновой пробкой, фиолетовым пластиковым диском и алюминиевой крышкой с зелеными полосами |
2500 МЕ | Стеклянный флакон с резиновой пробкой, светло-серым пластиковым диском и алюминиевой крышкой с зелеными полосами |
3000 МЕ | Стеклянный флакон с резиновой пробкой, желтым пластиковым диском и алюминиевой крышкой с зелеными полосами |
Владелец разрешения на маркетинг и ответственное лицо за производство
CSL Behring GmbH
Эмиль-фон-Беринг-Штрассе 76
35041 Марбург
Германия
Вы можете запросить дополнительную информацию о этом лекарственном средстве, обратившись к местному представителю владельца разрешения на маркетинг:
Бельгия/Белгique/Бельгия CSL Behring NV Тел: +32 15 28 89 20 | Литва CentralPharma Communications UAB Тел: +370 5 243 0444 |
| Люксембург/Люксбург CSL Behring NV Тел: +32 15 28 89 20 |
Чешская Республика CSL Behring s.r.o. Тел: +420 702 137 233 | Венгрия CSL Behring Kft. Тел: +36 1 213 4290 |
Дания CSL Behring AB Тел: +46 8 544 966 70 | Мальта AM Mangion Ltd. Тел: +356 2397 6333 |
Германия CSL Behring GmbH Тел: +49 6190 75 84810 | Нидерланды CSL Behring BV Тел: +31 85 111 96 00 |
Эстония CentralPharma Communications OÜ Тел: +372 601 5540 | Норвегия CSL Behring AB Тел: +46 8 544 966 70 |
Греция CSL Behring ΕΠΕ Тел: +30 210 7255 660 | Австрия CSL Behring GmbH Тел: +43 1 80101 1040 |
Испания CSL Behring S.A. Тел: +34 933 67 1870 | Польша CSL Behring Sp.z o.o. Тел: +48 22 213 22 65 |
Франция CSL Behring S.A. Тел: +33 –(0)-1 53 58 54 00 | Португалия CSL Behring Lda Тел: +351 21 782 62 30 |
Хорватия Marti Farm d.o.o. Тел: +385 1 5588297 | Румыния Prisum Healthcare S.R.L. Тел: +40 21 322 0171 |
Ирландия CSL Behring GmbH Тел: +49 6190 75 84700 Исландия CSL Behring AB Тел: +46 8 544 966 70 | Словения Emmes Biopharma Global s.r.o. podružnica v Sloveniji Тел: +386 41 42 0002 Словакия CSL Behring Slovakia s.r.o. Тел: +421 911 653 862 |
Италия CSL Behring S.p.A. Тел: +39 02 34964 200 | Финляндия CSL Behring AB Тел: +46 8 544 966 70 |
Кипр CSL Behring ΕΠΕ Тел: +30 210 7255 660 | Швеция CSL Behring AB Тел: +46 8 544 966 70 |
Латвия CentralPharma Communications SIA Тел: +371 6 7450497 | |
Дата последнего пересмотра этой инструкции:{MM/ГГГГ}
Подробная информация о этом лекарственном средстве доступна на сайте Европейского агентства по лекарственным средствам: http://www.ema.europa.eu.
----------------------------------------------------------------------------------------------------------
Эта информация предназначена только для медицинских специалистов:
Мониторинг лечения
Во время лечения рекомендуется контролировать уровни фактора VIII, чтобы определить дозу, которая должна быть введена, и частоту инъекций. Реакции пациентов на фактор VIII могут варьироваться, что демонстрирует, что у них разные периоды полувыведения и скорости восстановления. Возможно, что доза, основанная на весе тела, должна быть скорректирована у пациентов с недостаточным или избыточным весом. В случае проведения крупных хирургических вмешательств крайне важно точно контролировать терапию замены с помощью анализа коагуляции (активности плазменного фактора VIII).
При использовании одностадийного коагуляционного теста на основе активированного частичного тромбопластинового времени (АЧТТ) in vitroдля определения активности фактора VIII в образцах крови пациентов результаты активности плазменного фактора VIII могут быть существенно затронуты как типом реактива АЧТТ, так и эталонным стандартом, используемым в тесте. Также могут возникать значительные расхождения между результатами, полученными в одностадийном коагуляционном тесте на основе АЧТТ, и результатами, полученными в хромогенном тесте согласно Европейской фармакопее. Это особенно важно при смене лаборатории или реактивов, используемых в тесте.
Активность плазменного фактора VIII у пациентов, получающих АФСТИЛУ, с помощью хромогенного теста или одностадийного коагуляционного теста должна быть контролируема, чтобы руководить введенной дозой и частотой повторных инъекций. Результат хромогенного теста более точно отражает клинический гемостатический потенциал АФСТИЛЫ, поэтому это предпочтительный метод. Результат одностадийного коагуляционного теста занижает уровень активности фактора VIII по сравнению с результатом хромогенного теста примерно на 45%. Если используется одностадийный коагуляционный тест, результат умножается на коэффициент пересчета 2 для определения уровня активности фактора VIII пациента.
Дозировка
Доза и продолжительность терапии замены зависят от тяжести дефицита фактора VIII, местоположения и степени кровотечения, а также клинического состояния пациента.
Количество введенных единиц фактора VIII выражается в международных единицах (МЕ), соответствующих текущему стандарту ВОЗ для препаратов с фактором VIII. Активность плазменного фактора VIII выражается в процентах (относительно нормальной человеческой плазмы) или, предпочтительно, в международных единицах (относительно международного стандарта для плазменного фактора VIII).
Одна международная единица (МЕ) активности фактора VIII равна количеству фактора VIII, присутствующего в 1 мл нормальной человеческой плазмы.
Назначение мощности определяется с помощью хромогенного субстратного теста.
Уровни плазменного фактора VIII можно контролировать с помощью хромогенного субстратного теста или одностадийного коагуляционного теста.
Лечение по требованию
Расчет необходимой дозы фактора VIII основан на эмпирическом факте, что 1 МЕ фактора VIII на килограмм веса тела увеличивает плазменную активность фактора VIII на 2 МЕ/дл.
Требуемая доза определяется по следующей формуле: Доза (МЕ) = вес тела (кг) x желаемое увеличение фактора VIII (МЕ/дл или % от нормального уровня) x 0,5 (МЕ/кг на МЕ/дл)
Доза и частота введения всегда устанавливаются в зависимости от клинической эффективности, наблюдаемой в каждом случае.
В случае следующих геморрагических событий активность плазменного фактора VIII не должна быть ниже установленного уровня плазменной активности (в % от нормального уровня или МЕ/дл) в течение соответствующего периода. Следующая таблица может быть использована в качестве руководства по дозировке при геморрагических эпизодах и хирургии:
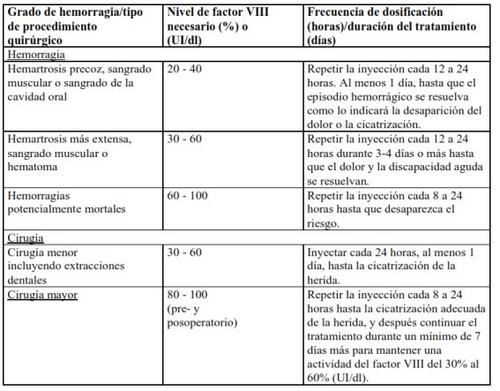
Профилактическое лечение
Рекомендуемая первоначальная схема лечения составляет 20-50 МЕ/кг АФСТИЛЫ, вводимых 2 или 3 раза в неделю. Схема может быть скорректирована в зависимости от реакции пациента.
Педиатрическое население
Рекомендуемая первоначальная схема лечения для детей (от 0 до <12 лет) составляет 30-50 МЕ кг АФСТИЛЫ, вводимых 2 или 3 раза в неделю. Возможно, что детям возрасте <12 лет потребуются более частые высокие дозы из-за высокого клиренса, наблюдаемого этой возрастной группе.< p>
У подростков в возрасте 12 лет и старше рекомендуемые дозы такие же, как и для взрослых.
Население пожилого возраста
В клинических исследованиях АФСТИЛЫ не были включены пациенты в возрасте 65 лет и старше.
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- Производитель
- СоставCLORURO DE SODIO (16,4 mg mg), SACAROSA (6 mg mg)
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги АФСТИЛА 3000 МЕ ПОРОШОК И РАСТВОРИТЕЛЬ ДЛЯ ПРИГОТОВЛЕНИЯ ИНЪЕКЦИОННОГО РАСТВОРАФорма выпуска: ИНЪЕКЦИОННЫЙ РАСТВОР, 1000 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: Takeda Manufacturing Austria AgТребуется рецептФорма выпуска: ИНЪЕКЦИОННЫЙ РАСТВОР, 1500 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: Takeda Manufacturing Austria AgТребуется рецептФорма выпуска: ИНЪЕКЦИОННЫЙ РАСТВОР, 1000 МЕ - после восстановления в 2 мл воды для инъекций доза составляет 500 МЕ/млАктивное вещество: фактор свертывания крови VIIIПроизводитель: Takeda Manufacturing Austria AgТребуется рецепт





