ADVATE 1500 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION

How to use ADVATE 1500 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
Introduction
Package Leaflet: Information for the User
ADVATE250UI powder andsolvent for solution for injection
ADVATE500UI powder andsolvent for solution for injection
ADVATE1000UI powder andsolvent for solution for injection
ADVATE1500UI powder andsolvent for solution for injection
Octocog alfa (recombinant human coagulation factor VIII)
Read all of this leaflet carefully before you start using this medicine because it contains important information for you.
- Keep this leaflet, you may need to read it again.
- If you have any further questions, ask your doctor or pharmacist.
- This medicine has been prescribed for you only. Do not pass it on to others. It may harm them, even if their signs of illness are the same as yours.
- If you get any side effects, talk to your doctor or pharmacist. This includes any possible side effects not listed in this leaflet. See section 4.
Contents of the pack and other information
- What is ADVATE and what is it used for
- What you need to know before you use ADVATE
- How to use ADVATE
- Possible side effects
- Storage of ADVATE
- Contents of the pack and further information
1. What is ADVATE and what is it used for
ADVATE contains the active substance octocog alfa, a recombinant human coagulation factor VIII produced by DNA technology. Factor VIII is necessary for blood to clot and to stop bleeding. In patients with haemophilia A, factor VIII is missing or does not work properly (hereditary absence of factor VIII).
ADVATE is used to treat and prevent bleeding in patients of all ages with haemophilia A (a hereditary bleeding disorder caused by the absence of factor VIII).
ADVATE is prepared without adding any human or animal derived protein in the entire manufacturing process.
2. What you need to know before you use ADVATE
Do not use ADVATE
- if you are allergic (hypersensitive) to octocog alfa or any of the other ingredients of this medicine (listed in section 6).
- if you are allergic to mouse or hamster proteins
If you are not sure if you are allergic, consult your doctor.
Warnings and precautions
Consult your doctor before you start using ADVATE. Inform your doctor if you have been previously treated with medicines containing factor VIII, especially if you developed inhibitors, as there may be a high risk that this will happen again. Inhibitors are antibodies that block factor VIII and reduce the effectiveness of ADVATE for bleeding control. The development of inhibitors is a known complication in the treatment of haemophilia A. If your bleeding is not controlled with ADVATE, consult your doctor immediately.
There is a small risk that you may experience a severe allergic reaction (anaphylaxis) to ADVATE. You should be aware that the first symptoms of an allergic reaction are rash, itching, hives, itching all over, swelling of the lips and tongue, difficulty breathing, wheezing, tightness in the chest, feeling of general discomfort and dizziness. These symptoms can be a warning of anaphylactic shock, which can also cause severe dizziness, loss of consciousness and severe breathing difficulties.
If you experience any of these symptoms, stop using the medicine immediately and consult a doctor. Severe symptoms, including difficulty breathing and (nearly) fainting, require rapid emergency treatment.
Patients who develop factor VIII inhibitors
The formation of inhibitors (antibodies) is a known complication that can occur during treatment with all factor VIII medicines. These inhibitors, especially in large quantities, prevent the treatment from working properly, so you and your child will be carefully monitored for the development of such inhibitors. If your bleeding or your child's bleeding is not controlled with ADVATE, consult your doctor immediately.
Children and adolescents
The warnings and precautions mentioned apply to adults and children (from 0 to 18 years of age).
Using ADVATE with other medicines
Tell your doctor if you are using, have recently used or might use any other medicines.
Pregnancy andbreast-feeding
If you are pregnant or breast-feeding, think you may be pregnant or are planning to have a baby, ask your doctor for advice before using this medicine.
Driving and using machines
Treatment with ADVATE has no influence on the ability to drive and use machines.
ADVATE contains sodium
This medicine contains 0.45 mmol of sodium (10 mg) per vial, which should be taken into consideration in patients on a low-sodium diet.
Incorrect administration of ADVATE
Incorrect administration (injection into an artery or outside a vein) should be avoided as it may cause mild and short-term reactions at the injection site, such as bruising and redness.
3. How to use ADVATE
Treatment with ADVATE will be started by a doctor who has experience in the treatment of patients with haemophilia A.
Your doctor will calculate your dose of ADVATE (in international units or IU) based on your condition, body weight and whether it is to be used for prevention or treatment of bleeding. The frequency of administration will depend on how ADVATE works for you. Replacement therapy with ADVATE is usually a lifelong treatment.
Follow exactly the administration instructions for this medicine given by your doctor. If you are unsure, consult your doctor again.
Prevention of bleeding
The usual dose of octocog alfa is 20 to 40 IU per kg body weight, administered every 2 or 3 days. However, in some cases, especially in younger patients, more frequent administration of injections or higher doses may be required.
Treatment of bleeding
The dose of octocog alfa is calculated based on your body weight and the desired factor VIII levels. The factor VIII levels to be achieved will depend on the severity and location of the bleeding.
Dose (IU) = body weight (kg) x desired increase in factor VIII (% of normal) x 0.5
If you think that the effect of ADVATE is too weak, consult your doctor.
Your doctor will perform the necessary laboratory tests to ensure that you have adequate factor VIII levels. This is especially important if you are going to have major surgery.
Use in children and adolescents(from 0 to 18 years of age)
For the treatment of bleeding, the dose in children does not differ from that in adult patients. To prevent bleeding in children under 6 years of age, doses of 20 to 50 IU per kg body weight 3 to 4 times a week are recommended. Administration of ADVATE in children (intravenously) does not differ from administration in adults. A central venous access device (CVAD) may be necessary to allow for frequent infusions of factor VIII products.
Due to the reduced injection volume of reconstituted ADVATE in 2 ml, the time to react to hypersensitivity reactions during an injection is further reduced. Therefore, caution is advised during injection of reconstituted ADVATE in 2 ml, especially in children.
How ADVATE is administered
ADVATE is usually injected into a vein (intravenously) by your doctor or nurse. You or another person can also administer the injection of ADVATE, but only after receiving appropriate training. Detailed instructions for administration are described at the end of this leaflet.
If you use more ADVATE than you should
Follow exactly the administration instructions for this medicine given by your doctor. Consult your doctor if you are unsure. If you inject more ADVATE than you should, consult your doctor as soon as possible.
If you forget to use ADVATE
Do not inject a double dose to make up for forgotten doses. Administer the next injection as scheduled and continue as instructed by your doctor.
If you stop using ADVATE
Do not stop using ADVATE without consulting your doctor.
If you have any further questions on the use of this medicine, ask your doctor.
4. Possible side effects
Like all medicines, this medicine can cause side effects, although not everybody gets them.
If you experience sudden and severe allergic reactions(anaphylactic reactions), stop the injection immediately. Contact your doctor immediately if you have any of the following initial symptoms of allergic reactions:
- rash, itching, hives, itching all over,
- swelling of the lips and tongue,
- difficulty breathing, wheezing, tightness in the chest,
- feeling of general discomfort,
- dizziness and loss of consciousness.
Severe symptoms, such as difficulty breathing and (nearly) fainting, require rapid emergency treatment.
In children who have not been previously treated with factor VIII medicines, inhibitor antibodies (see section 2) may occur very frequently (more than 1 in 10 patients); however, in patients who have been previously treated with factor VIII (more than 150 days of treatment), the risk is infrequent (less than 1 in 100 patients). If this happens, the medicines you or your child are taking may stop working properly and you or your child may experience persistent bleeding. In this case, contact your doctor immediately.
Very common side effects(may affect more than 1 in 10 patients)
Factor VIII inhibitors (in children who have not been previously treated with factor VIII medicines).
Common side effects(may affect up to 1 in 10 patients)
Headache and fever
Uncommon side effects(may affect up to 1 in 100 patients)
Factor VIII inhibitors (in patients who have been previously treated with factor VIII [more than 150 days of treatment]), dizziness, flu-like illness, fainting, irregular heartbeats, red spots associated with itching, chest discomfort, injection site bruising, injection site reaction, itching, increased sweating, unusual taste in the mouth, hot flushes, migraines, memory loss, chills, diarrhoea, nausea, vomiting, difficulty breathing, sore throat, infection of the lymphatic vessels, paleness, eye inflammation, rash, excessive sweating, inflammation of feet and legs, decreased red blood cell count, increased monocytes (a type of white blood cell) and pain in the upper abdomen or lower chest.
Related to surgery
catheter-related infection, decreased red blood cell count, swelling of the limbs and joints, prolonged bleeding after drain removal, decreased factor VIII levels and postoperative haematoma
Related to central venous access devices (CVAD)
Catheter-related infection, systemic infection and local blood clot at the catheter site.
Side effects with unknown frequency(cannot be estimated from the available data)
Potentially life-threatening reactions (anaphylaxis) and other allergic reactions (hypersensitivity), general disorders (fatigue, lack of energy).
Additional side effects in children
In addition to the development of inhibitors in previously untreated paediatric patients and catheter-related complications, no age-specific differences in side effects were observed in clinical trials.
Reporting of side effects
If you experience any side effects, talk to your doctor or pharmacist. This includes any possible side effects not listed in this leaflet. You can also report side effects directly via the national reporting system listed in Appendix V. By reporting side effects you can help provide more information on the safety of this medicine.
5. Storage of ADVATE
Keep this medicine out of the sight and reach of children.
Do not use this medicine after the expiry date which is stated on the carton after EXP. The expiry date refers to the last day of the month stated.
Store in a refrigerator (2°C to 8°C).
Do not freeze.
Until the expiry date, the blister with the medicine can be stored at room temperature (up to 25°C) for a single period not exceeding 6 months. In this case, this medicine expires at the end of this 6-month period or on the expiry date printed on the blister, whichever is earlier. Please note the date of the end of the 6-month period on the carton. The medicine cannot be refrigerated again after storage at room temperature.
Store the blister with the medicine in the outer carton to protect it from light.
This medicine is for single use only. Dispose of any unused solution properly.
Use the medicine immediately after complete dissolution of the powder.
Do not refrigerate the medicine after preparation.
Medicines should not be disposed of via wastewater or household waste. Ask your pharmacist how to dispose of medicines no longer required. These measures will help protect the environment.
6. Container Contents and Additional Information
Composition of ADVATE
- The active ingredient is octocog alfa (human coagulation factor VIII produced by recombinant DNA technology). Each vial of powder contains nominally 250, 500, 1000, or 1500 IU of octocog alfa.
- The other components are mannitol, sodium chloride, histidine, trehalose, calcium chloride, tromethamine, polysorbate 80, and glutathione (reduced)
Solvent vial: 2 ml of sterile water for injectable preparations
Appearance of the Product andContainer Contents
ADVATE is a white to off-white friable powder.
After reconstitution, the solution is transparent, colorless, and free of foreign particles.
Marketing Authorization Holder
Takeda Manufacturing Austria AG
Industriestrasse 67
A-1221 Vienna
Tel: +800 66838470
E-mail: [email protected]
Manufacturers
Baxalta Belgium Manufacturing SA
Boulevard René Branquart 80
B-7860 Lessines
Belgium
Date of Last Revision of this Leaflet
Detailed information on this medicinal product is available on the European Medicines Agency website: http://www.ema.europa.eu/.
--------------------------------------------------------------------------------------------------------------------
Instructions for Preparation andAdministration
ADVATE must not be mixed with other medicines or solvents.
It is strongly recommended to record the name and batch number of the product each time ADVATE is administered.
Instructions for Reconstitution
- Do not use after the expiry date stated on the labels and on the container.
- Do not use if the blister cap is not perfectly sealed.
- Do not refrigerate the preparation after reconstitution.
- If the medicine is in the refrigerator, take the sealed blister (containing vials of powder and pre-loaded solvent with the reconstitution system) out of the refrigerator and let it stand at room temperature (between 15°C and 25°C).
- Wash your hands with soap and warm water.
- Open the ADVATE packaging by removing the cap. Remove the BAXJECT III system from the blister.
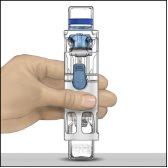
- Place ADVATE on a flat surface with the solvent vial on top (Fig. 1). The solvent vial has a blue stripe. Do not remove the blue protector until instructed to do so later.
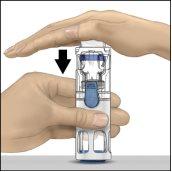
- While holding ADVATE with one hand in the BAXJECT III system, press the solvent vial firmly with the other hand until the system is fully contracted and the solvent enters the ADVATE vial (Fig. 2). Do not tilt the system until the transfer is complete.
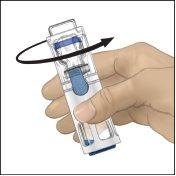
- Check that the solvent transfer is complete. Gently swirl until all material is dissolved. Ensure that the ADVATE powder is completely dissolved; if not, the reconstituted solution will not pass through the filter of the equipment. The medicine dissolves quickly (usually in less than 1 minute). After reconstitution, the solution must be transparent, colorless, and free of foreign particles.
Fig.1 | Fig.2 | Fig.3 |
|
|
|
Instructions for Injection
Aseptic technique is required during administration.
Administration requires the use of a luer-lock syringe.
Important Note:
- Do not attempt to administer the injection unless you have received special training from your doctor or nurse.
- Inspect the prepared solution for particles or discoloration before administration (the solution must be transparent, colorless, and free of foreign particles).
Do not use ADVATE if the solution is not totally transparent or not completely dissolved.
- Remove the blue protector from the BAXJECT III system. Do not introduce air into the syringe. Connect the syringe to the BAXJECT III system.
- Invert the system (the vial with the reconstituted solution on top). Introduce the reconstituted solution into the syringe by slowly pulling the plunger back.
- Disconnect the syringe.
- Connect a winged infusion needle to the syringe. Inject intravenously. The solution should be administered slowly, at a rate determined by the patient's level of comfort, not exceeding 10 ml per minute. The pulse should be taken before and during the administration of ADVATE. If a significant increase in pulse is observed, the administration rate should be reduced or the injection temporarily interrupted, normally allowing the symptoms to disappear immediately (see section 4 "Possible Adverse Effects").
- Dispose of unused solution properly.
--------------------------------------------------------------------------------------------------------------------
This information is intended only for healthcare professionals:
On-demand Treatment
In the case of subsequent hemorrhagic episodes, factor VIII activity should not be lower than the given plasma activity level (in % of normal or IU/dl) during the corresponding period. The following table can be used as a dosing guide for hemorrhagic episodes and surgery.
The dose and frequency of administration should be adapted to the individual clinical response. In certain circumstances (e.g., presence of a low inhibitor titre), higher doses than those calculated using the formula may be necessary.
Severity of Hemorrhage / Type of Surgical Procedure | Required Factor VIII Level (% orIU/dl) | Dose Frequency (hours) / Duration of Therapy (days) |
Hemorrhage Early hemarthrosis or muscle or oral hemorrhage. More extensive hemarthrosis, muscle hemorrhage, or hematoma. Life-threatening hemorrhage. | 20 – 40 30 – 60 60 – 100 | Repeat injection every 12 to 24 hours (every 8 to 24 hours in patients under 6 years of age) for at least 1 day until the hemorrhagic episode, as indicated by pain, is resolved or healing is achieved. Repeat injection every 12-24 hours (every 8 to 24 hours in patients under 6 years of age) for 3 to 4 days or more, until pain and acute disability cease. Repeat injection every 8 to 24 hours (every 6 to 12 hours in patients under 6 years of age) until the danger has passed. |
Surgery MinorIncluding dental extraction. Major | 30 – 60 80 – 100 (pre- and post-operative) | Every 24 hours (every 12 to 24 hours in patients under 6 years of age), for at least 1 day, until healing is achieved. Repeat injection every 8-24 hours (every 6 to 24 hours in patients under 6 years of age) until adequate wound healing is achieved, and then for at least another 7 days of therapy to maintain a factor VIII activity of 30% to 60% (IU/dl). |
- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to ADVATE 1500 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTIONDosage form: INJECTABLE, 1,000 IUActive substance: coagulation factor VIIIManufacturer: Takeda Manufacturing Austria AgPrescription requiredDosage form: INJECTABLE, 1500 IUActive substance: coagulation factor VIIIManufacturer: Takeda Manufacturing Austria AgPrescription requiredDosage form: INJECTABLE, 1000 IU - after reconstitution in 2 ml of water for injections, the dose is 500 IU/mlActive substance: coagulation factor VIIIManufacturer: Takeda Manufacturing Austria AgPrescription required
Online doctors for ADVATE 1500 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION
Discuss questions about ADVATE 1500 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions