ZYCLARA 3,75% CREME

Pergunte a um médico sobre a prescrição de ZYCLARA 3,75% CREME

Como usar ZYCLARA 3,75% CREME
Introdução
Prospecto: Informação para o paciente
Zyclara 3,75% creme
imiquimode
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que relê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Zyclara e para que é utilizado
- O que precisa saber antes de começar a usar Zyclara
- Como usar Zyclara
- Possíveis efeitos adversos
- Conservação de Zyclara
- Conteúdo do envase e informações adicionais
1. O que é Zyclara e para que é utilizado
Zyclara 3,75% creme contém a substância ativa imiquimode.
Este medicamento é prescrito para o tratamento da queratose actínica em adultos, que é um Modificador de Resposta Imune (para estimular o sistema imunológico humano).
Este medicamento estimula o seu próprio sistema imunológico para produzir substâncias naturais que contribuem para combater a queratose actínica.
As queratoses actínicas aparecem como zonas de pele rugosa presentes em pessoas que estiveram expostas a grande quantidade de luz solar ao longo da vida. Estas zonas podem ser da mesma cor que a sua pele, ou serem grisáceas, rosadas, vermelhas ou marrons. Podem ser planas e escamosas, ou elevadas, rugosas, duras e verrugosas.
Este medicamento deve ser usado exclusivamente em queratoses actínicas do rosto ou do couro cabeludo, se o seu médico decidir que é o tratamento mais adequado para si.
2. O que precisa saber antes de começar a usar Zyclara
Não use Zyclara
- se é alérgico ao imiquimode ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6).
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar Zyclara:
- se utilizou anteriormente este medicamento ou outro preparado similar, em uma concentração diferente.
- se padece transtornos autoimunes.
- se teve um transplante de órgão.
- se tem um recuento sanguíneo anormal.
Instruções gerais durante o tratamento
- Se foi submetido recentemente a tratamento cirúrgico ou farmacológico, espere até que a zona a tratar tenha cicatrizado antes de usar este medicamento.
- Evite o contato com olhos, lábios e fossas nasais. Em caso de contato acidental, elimine o creme lavando a zona com água.
- Utilize o creme apenas de forma externa (sobre a pele do rosto ou couro cabeludo).
- Não use uma quantidade de creme maior do que a recomendada pelo seu médico.
- Não cubra a zona tratada com vendas ou outros elementos após ter aplicado Zyclara.
- Se desenvolver desconforto excessivo na zona tratada, retire o creme com um sabão neutro e água. Uma vez que as molestias tenham remitido, pode retomar o tratamento da forma recomendada. O creme não deve ser aplicado mais de uma vez ao dia.
- Não utilize lâmpadas solares nem solários, e evite, na medida do possível, a luz do sol durante o tratamento com este medicamento. Se sair ao ar livre durante o dia, utilize protetor solar e vista roupas protetoras, bem como um chapéu de aba larga.
Reações cutâneas locais
Enquanto utilizar Zyclara, pode experimentar reações cutâneas locais devido à forma como o medicamento atua sobre a sua pele. Estas reações podem indicar que o medicamento está a atuar da forma prevista.
Durante a utilização de Zyclara e até à cura, a zona de tratamento pode apresentar um aspecto claramente diferente do da pele normal. Existe também a possibilidade de que uma inflamação pré-existente piore temporariamente.
Este medicamento também pode provocar sintomas semelhantes aos da gripe (incluindo cansaço, náuseas, febre, dores musculares e articulares, e calafrios) antes ou durante a aparência das reações cutâneas locais.
Se apresentar sintomas gripais ou sensação de mal-estar ou reações cutâneas locais intensas, pode tomar um período de descanso de vários dias. Pode retomar o tratamento com creme de imiquimode após a reação cutânea se ter moderado. No entanto, não deve prolongar o ciclo de tratamento de 2 semanas devido às doses perdidas ou aos períodos de descanso.
A intensidade das reações cutâneas locais tende a ser mais baixa no segundo ciclo do que no primeiro ciclo de tratamento com Zyclara.
A resposta ao tratamento não pode ser avaliada adequadamente até à resolução das reações cutâneas locais. Deve continuar o tratamento da forma prescrita.
Este medicamento pode revelar e tratar queratoses actínicas que não tenham sido vistas ou percebidas previamente, e que posteriormente podem desaparecer. A aplicação deve continuar durante a totalidade do ciclo de tratamento, mesmo que todas as queratoses actínicas pareçam ter desaparecido.
Crianças e adolescentes
Este medicamento não deve ser administrado a crianças menores de 18 anos, porque não foi estabelecida a segurança e eficácia em pacientes menores dessa idade. Não há dados disponíveis sobre o uso de imiquimode em crianças e adolescentes.
Outros medicamentos e Zyclara
Informa ao seu médico ou farmacêutico se está a tomar, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Informa ao seu médico antes de iniciar o tratamento se recebe medicamentos imunossupressores que inibem o sistema imunológico.
Evite o uso concomitante de Zyclara e qualquer outro creme de imiquimode na mesma área de tratamento.
Gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
O seu médico avaliará os riscos e os benefícios de utilizar Zyclara durante a gravidez. Os estudos em animais não indicam efeitos nocivos diretos ou indiretos na gravidez.
Desconhece-se se o imiquimode passa para o leite materno. Não deve usar Zyclara se está a amamentar ou tem previsto amamentar. O seu médico decidirá se deve interromper a amamentação ou se deve interromper o tratamento com Zyclara.
Condução e uso de máquinas
A influência deste medicamento sobre a capacidade para conduzir e usar máquinas é nula ou insignificante.
Zyclara contém parahidroxibenzoato de metilo, parahidroxibenzoato de propilo, álcool cetílico, álcool estearílico e álcool benzílico.
Pode produzir reações alérgicas (possivelmente retardadas) porque contém parahidroxibenzoato de metilo (E 218) e parahidroxibenzoato de propilo (E 216).
Este medicamento pode produzir reações locais na pele (como dermatite de contacto) porque contém álcool cetílico e álcool estearílico.
Este medicamento contém 5 mg de álcool benzílico em cada envelope. O álcool benzílico pode provocar reações alérgicas e irritação local moderada.
3. Como usar Zyclara
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico. Não utilize este medicamento até que o seu médico lhe tenha ensinado a forma correta de fazê-lo.
Este medicamento apenas deve ser usado para as queratoses actínicas do rosto e couro cabeludo.
Dosagem
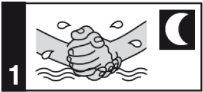
Aplique este medicamento sobre a zona afetada uma vez ao dia, imediatamente antes de deitar-se.
A dosagem diária máxima é de 2 envelopes (500 mg = 2 envelopes de 250 mg cada).
Este medicamento não deve ser aplicado sobre zonas de tamanho maior que todo o rosto ou o couro cabeludo alopécico.
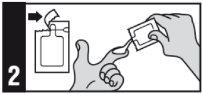
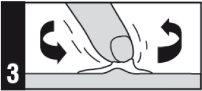
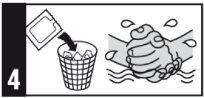
Forma de administração
|
|
|
|
|
|
|
|
|
|
|
|
Duração do tratamento
O tratamento começa com uma aplicação diária durante duas semanas, seguida de uma pausa sem aplicação durante duas semanas, e termina com uma aplicação diária durante duas semanas novamente.
Se usar mais Zyclara do que deve
Se aplicou demasiado creme, retire o excesso lavando a zona com água e sabão neutro.
Quando as reações cutâneas tiverem remitido, pode retomar o tratamento segundo o programa regular recomendado. O creme não deve ser aplicado mais de uma vez ao dia.
Se engolir acidentalmente este medicamento, entre em contato imediatamente com o seu médico.
Se esquecer de usar Zyclara
Se esquecer de uma dose de Zyclara, espere até a noite seguinte para aplicá-la e, a seguir, prosiga com o regime habitual. O creme não deve ser aplicado mais de uma vez ao dia. Cada ciclo de tratamento não deve durar mais de duas semanas, mesmo que tenha omitido algumas doses.
Se interromper o tratamento com Zyclara
Consulte o seu médico antes de suspender o tratamento com Zyclara.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Pedir assistência médica imediatamente se aparecer qualquer um destes efeitos adversos graves durante o uso deste medicamento:
Reações cutâneas graves (frequência não conhecida), com lesões cutâneas ou manchas na pele que se iniciam como pequenas zonas de cor vermelha e evoluem até alcançar o aspecto de pequenas dianas, possivelmente com sintomas como picazón, febre, mal-estar geral, dores articulares, problemas de visão, sensação de queimadura, dores ou picazón oculares e úlceras bucais. Se sofrer estes distúrbios, interrompa o uso deste medicamento e informe imediatamente o seu médico.
Em algumas pessoas, observou-se uma descida da fórmula sanguínea (frequência não conhecida). Este facto poderia aumentar a sua susceptibilidade a sofrer infecções, desenvolver hematomas ou provocar cansaço. Se perceber qualquer um destes sintomas, informe o seu médico.
Alguns pacientes que padecem de transtornos autoimunes podem experimentar agravamento da sua doença. Consulte o seu médico se experimentar qualquer alteração durante o tratamento com Zyclara.
Se houver presença de pus ou outro sinal de infecção na pele (frequência não conhecida), consulte o seu médico.
Muitos dos efeitos secundários deste medicamento devem-se à sua ação local sobre a pele. As reações cutâneas locais podem indicar que o medicamento está a atuar da forma prevista. Se a sua pele reagir mal ou sofrer desconforto excessivo durante o uso deste medicamento, suspenda a aplicação do creme e lave a zona com água e um sabão neutro. Seguidamente, entre em contato com o seu médico ou farmacêutico, que pode aconselhá-lo a interromper a aplicação deste medicamento durante alguns dias (ou seja, realizar um breve descanso durante o tratamento).
Foram comunicados os seguintes efeitos adversos com imiquimode:
Muito frequentes(pode afetar mais de 1 em cada 10 pessoas)
- Vermelhidão da pele, crostas, descamação cutânea, supuração, secura da pele, inchaço cutâneo, úlceras cutâneas e redução da pigmentação cutânea no local de aplicação.
Frequentes(pode afetar até 1 em cada 10 pessoas)
- Outras reações adicionais no local de aplicação, por exemplo, inflamação da pele, picazón, dor, sensação de queimadura, irritação e exantema cutâneo
- Glândulas inflamadas
- Cefaleias
- Tontura
- Perda de apetite
- Náuseas
- Diarréia
- Vómitos
- Sintomas semelhantes aos da gripe
- Febre
- Dor
- Dores musculares e articulares
- Dor torácica
- Insónia
- Cansaço
- Infecção viral (herpes simples)
- Aumento da glicose no sangue
Pouco frequentes(pode afetar até 1 em cada 100 pessoas)
- Alterações na zona de aplicação, por exemplo, sangramento, pequenas zonas inchadas na pele, inflamação, formigamento, aumento da sensibilidade ao toque, formação de cicatrizes, sensação de calor, lesões da pele, bolhas ou pústulas
- Debilidade
- Calafrios
- Falta de energia (letargia)
- Desconforto
- Tumefação do rosto
- Lombalgia
- Dor de extremidades
- Nariz entupido
- Dor de garganta
- Irritação dos olhos
- Inchaço das pálpebras
- Depressão
- Irritabilidade
- Boca seca
- Dor abdominal
Raros(pode afetar até 1 em cada 1.000 pessoas)
- Surto de doenças autoimunes (uma doença autoimune é uma doença causada por uma resposta imunológica anormal)
- Reações cutâneas afastadas do local de aplicação
Frequência não conhecida(não pode ser estimada a partir dos dados disponíveis)
- Mudanças de cor da pele
Alguns pacientes experimentaram mudanças de cor da pele na zona sobre a qual se aplicou Zyclara. Embora estas mudanças tendam a melhorar com o tempo, em alguns pacientes podem ser permanentes.
- Perda de cabelo
Um número reduzido de pacientes experimentou perda de cabelo na zona de tratamento ou imediatamente adjacente.
- Elevação das enzimas hepáticas
Foram relatados aumentos das enzimas hepáticas.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
.
5. Conservação de Zyclara
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e no envase exterior após CAD.
A data de validade é o último dia do mês que se indica.
Não conserve a uma temperatura superior a 25°C.
Uma vez abertos, os envelopes não devem ser reutilizados.
Os medicamentos não devem ser jogados nos deságues nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Zyclara
- O princípio ativo é imiquimode. Cada sobre contém 9,375 mg de imiquimode em 250 mg de crema (100 mg de crema contêm 3,75 mg de imiquimode).
- Os demais componentes são: ácido isoesteárico, álcool benzílico, álcool cetílico, álcool estearílico, parafina branca leve, polissorbato 60, estearato de sorbitano,glicerol,parahidroxibenzoato de metilo (E 218),parahidroxibenzoato de propilo (E 216),goma xantana, água purificada (ver também a seção 2 “Zyclara contém parahidroxibenzoato de metilo, parahidroxibenzoato de propilo, álcool cetílico, álcool estearílico e álcool benzílico”).
Aspecto de Zyclara e conteúdo do envase
- Cada sobre de Zyclara 3,75% crema contém 250 mg de uma crema de cor branca a ligeiramente amarelada, de aspecto uniforme.
- Cada envase contém 14, 28 ou 56 sobres de um só uso de poliéster/poliétileno de baixa densidade branco/lâmina de alumínio.
Pode ser que apenas alguns tamanhos de envase sejam comercializados.
Título da autorização de comercialização
Viatris Healthcare Limited
Damastown Industrial Park
Mulhuddart
Dublin 15
DUBLIN
Irlanda
Responsável pela fabricação
Swiss Caps GmbH
Grassingerstraße 9
83043 Bad Aibling
Alemanha
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização:
Bélgica Mylan EPD bvba/sprl Terhulpsesteenweg, 6A B-1560 Hoeilaart Tel: +32 2 658 61 00 | Luxemburgo Mylan EPD bvba/sprl Terhulpsesteenweg, 6A B-1560 Hoeilaart Tel: +32 2 658 61 00 |
Bulgária ?????? ???? ???.: +359 2 44 55 400 | Hungria Mylan EPD Kft. 1138 Budapeste Váci út 150 Tel: +36 1 465 2100 |
República Checa Viatris CZ s.r.o. Tel: +420 222 004 400 | Malta V.J. Salomone Pharma Limited Upper Cross Road Marsa, MRS 1542 Tel: +356 21 22 01 74 |
Dinamarca Viatris ApS Borupvang 1 2750 Ballerup Tlf: +45 28 11 69 32 | Países Baixos Mylan Healthcare B.V. Krijgsman 20 1186 DM Amstelveen Tel: +31 (0)20 426 3300 |
Alemanha Viatris Healthcare GmbH Lütticher Straße 5 53842 Troisdorf Tel: +49 800 0700 800 | Noruega Viatris AS Hagaløkkveien 26 1383 Asker Tlf: +47 66 75 33 00 |
Estônia Meda Pharma SIA Liivalaia 13/15 11018 Tallinn Tel: +372 62 61 025 | Áustria Mylan Österreich GmbH Guglgasse 15 1110 Viena Tel: + 43 (0)1 86 390 0 |
Grécia Viatris Hellas Ltd Tel: +30 210 010 0002 | Polônia Mylan Healthcare Sp. z.o.o. ul. Postepu 21B 02-676 Varsóvia Tel: +48 22 546 6400 |
Espanha Viatris Pharmaceuticals, S.L.U. Tel: +34 900 102 712 | Portugal Viatris Healthcare, Lda. Av. D. João II, Edifício Atlantis, nº 44C – 7.3 e 7.4 1990-095 Lisboa Tel: +351 214 127 200 |
França Viatris Médical 1 bis place de la Défense – Tour Trinity 92400 Courbevoie Tél: +33 (0)1 40 80 15 55 | Romênia BGP PRODUCTS SRL Tel.: +40 372 579 000 |
Croácia Viatris Hrvatska d.o.o. Koranska 2 10 000 Zagreb Tel: +385 1 2350 599 | Eslovênia Viatris d.o.o. Tel: +386 1 23 63 180 |
Irlanda Mylan Ireland Limited Tel: +353 1 8711600 | República Eslovaca Viatris Slovakia s.r.o. Tel: +421 2 32 199 100 |
Islândia Icepharma hf. Sími: +354 540 8000 | Finlândia Viatris Oy Vaisalantie 2-8/Vaisalavägen 2-8 02130 Espoo/Esbo Puh/Tel: +358 20 720 9555 |
Itália Mylan Italia Via Vittor Pisani, 20 20124 Milão Tel: +39 0261246921 | Suécia Viatris AB Box 23033 104 35 Estocolmo +46 (0) 8 630 19 00 |
Chipre Βαρν?βας Χατζηπαναγ?ς Λτδ Λεωφ. Γι?ννου Κρανιδι?τη 226 ΤK 2234, Λατσι?, Λευκωσ?α Τηλ.: +357 22207700 | Reino Unido (Irlanda do Norte) Mylan IRE Healthcare Limited Tel: +353 18711600 |
Letônia Meda Pharma SIA 101 Mukusalas str. Riga LV-1004 Talr: +371 67616137 | |
Lituânia Meda Pharma SIA Žalgirio str. 90-100 Vilnius LT-09303 Tel. + 370 52051288 |
Data da última revisão deste prospecto: (MM/AAAA)
A informação detalhada deste medicamento está disponível na página Web da Agência Europeia de Medicamentos: http://www.ema.europa.eu.

Quanto custa o ZYCLARA 3,75% CREME em Espanha em 2025?
O preço médio do ZYCLARA 3,75% CREME em dezembro de 2025 é de cerca de 66.11 EUR. Os valores podem variar consoante a região, a farmácia e a necessidade de receita. Confirme sempre com uma farmácia local ou fonte online para obter informações atualizadas.
- País de registo
- Preço médio em farmácia66.11 EUR
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ZYCLARA 3,75% CREMEForma farmacêutica: CREME, 50 mg/gSubstância ativa: imiquimodFabricante: Viatris Healthcare LimitedRequer receita médicaForma farmacêutica: CREME, 50 mg/gSubstância ativa: imiquimodFabricante: Viatris Healthcare LimitedRequer receita médicaForma farmacêutica: CREME, 5 %Substância ativa: imiquimodFabricante: Mibe Pharma Espana S.L.Requer receita médica
Alternativas a ZYCLARA 3,75% CREME noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ZYCLARA 3,75% CREME em Polónia
Alternativa a ZYCLARA 3,75% CREME em Ukraine
Médicos online para ZYCLARA 3,75% CREME
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ZYCLARA 3,75% CREME – sujeita a avaliação médica e regras locais.