
Como usar TRANSLARNA 1000 mg GRÂNULOS PARA SUSPENSÃO ORAL
Introdução
Prospecto: Informação para o paciente
Translarna 125 mg granulado para suspensão oral
Translarna 250 mg granulado para suspensão oral
Translarna 1.000 mg granulado para suspensão oral
atalureno
Este medicamento está sujeito a seguimento adicional, o que agilizará a detecção de nova informação sobre a sua segurança. Pode contribuir comunicando os efeitos adversos que possa ter. A parte final da seção 4 inclui informação sobre como comunicar estes efeitos adversos.
Leia todo o prospecto detenidamente antes de começar a tomar este medicamento, porque contém informação importante para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas a si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Translarna e para que é utilizado
- O que precisa saber antes de começar a tomar Translarna
- Como tomar Translarna
- Possíveis efeitos adversos
- Conservação de Translarna
- Conteúdo do envase e informação adicional
1. O que é Translarna e para que é utilizado
Translarna é um medicamento que contém o princípio ativo atalureno.
Translarna é utilizado para o tratamento da distrofia muscular de Duchenne devido a um defeito genético que afeta a função normal dos músculos.
Translarna é utilizado para tratar pacientes de 2 anos de idade e mais velhos que podem caminhar.
O seu médico deve ter realizado testes a si ou ao seu filho antes de começar o tratamento com Translarna para confirmar que a sua doença é adequada para este medicamento.
Como actua Translarna?
A distrofia muscular de Duchenne está causada por alterações genéticas que produzem uma anomalia de uma proteína muscular chamada distrofina, a qual é necessária para que os músculos funcionem adequadamente. Translarna torna possível a produção de distrofina funcional e contribui para que os músculos funcionem adequadamente.
2. O que precisa saber antes de começar a tomar Translarna
Não tome Translarna
- se é alérgico a atalureno ou a qualquer um dos outros componentes deste medicamento (incluídos na seção 6).
- se está a receber antibióticos como gentamicina, tobramicina ou estreptomicina por via intravenosa.
Advertências e precauções
O seu médico deve ter realizado um análise de sangue que confirme que a sua doença é adequada para o tratamento com Translarna. Se si tiver algum problema de rim, o seu médico realizará reconhecimentos periódicos dos seus rins.
Se tiver insuficiência renal grave (VFGe <30 ml min) ou se está a receber diálise porque os seus rins não funcionam (nefropatia terminal), o seu médico determinará tratamento com translarna é adequado para si.< p>
O seu médico verificará os níveis de lípidos (gorduras como o colesterol e os triglicéridos) no seu sangue e a função renal cada 6 ou 12 meses. Se si estiver a tomar medicamentos corticosteroides, o seu médico reverá a sua tensão arterial cada 6 meses.
Crianças e adolescentes
Não dê este medicamento a crianças menores de 2 anos ou que pesem menos de 12 kg, porque ainda não foi testado neste grupo de pacientes.
Outros medicamentos e Translarna
Informa o seu médico se está a utilizar, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento. Em concreto, não tome Translarna com antibióticos gentamicina, tobramicina ou estreptomicina administrados por via intravenosa. Podem afectar a sua função renal.
Deve informar o seu médico se está a tomar algum dos seguintes medicamentos:
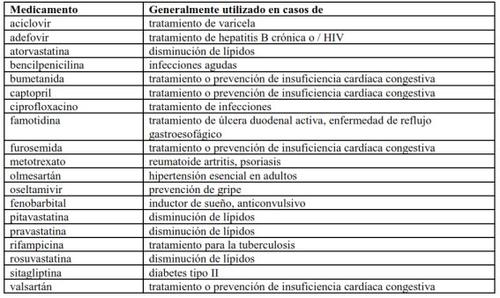
Alguns desses medicamentos não foram testados em administração conjunta com Translarna, e o seu médico pode decidir controlá-lo estreitamente.
Gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que pode estar grávida ou tem intenção de engravidar, consulte o seu médico antes de utilizar este medicamento. Se engravidar enquanto está a tomar Translarna, consulte o seu médico imediatamente, porque não se recomenda tomar Translarna durante a gravidez ou a amamentação.
Condução e uso de máquinas
Se sentir tontura, não conduza nem utilize maquinaria.
3. Como tomar Translarna
Siga exactamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
Translarna está disponível em sobres com as seguintes concentrações: 125 mg, 250 mg e 1.000 mg de atalureno por sobre. O seu médico ou farmacêutico indicar-lhe-á o número exacto de sobres e qual concentração deve tomar em cada momento.
A sua dose de Translarna depende do seu peso corporal. A dose recomendada é de 10 mg/kg de peso corporal pela manhã, 10 mg/kg de peso corporal ao meio-dia e 20 mg/kg de peso corporal à noite (somando uma dose diária total de 40 mg/kg de peso corporal).
Este medicamento é tomado por via oral misturado em líquido ou com um alimento semissólido.
Não deve abrir o sobre até o momento em que o vai a tomar e utilize o conteúdo completo do sobre. Todo o conteúdo do sobre deve ser misturado com pelo menos 30 ml de líquido (água, leite, sumo de fruta) ou 3 colheres de sopa de alimento semissólido (iogurte ou compota de maçã). Misture bem a dose preparada antes de a tomar. Pode aumentar a quantidade de líquido ou alimento semissólido se assim o preferir.
Tabela de posologia
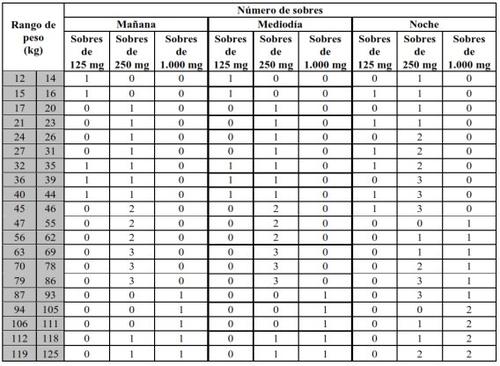
Tome Translarna por via oral 3 vezes ao dia, pela manhã, ao meio-dia e à noite. Deve existir um intervalo de 6 horas entre a dose da manhã e a dose do meio-dia, de 6 horas entre a dose do meio-dia e a dose da noite, e de 12 horas entre a dose da noite e a primeira dose do dia seguinte. Por exemplo, pode tomar Translarna pela manhã às 7:00 com o pequeno-almoço, ao meio-dia às 13:00 com o almoço e de novo pela tarde hacia as 19:00 com o jantar.
Beba água ou outros líquidos com regularidade para evitar a desidratação enquanto estiver a tomar Translarna.
Se tomar mais Translarna do que deve
Se tomou mais Translarna do que a dose recomendada, contacte o seu médico.
Pode experimentar cefaleia, náuseas, vómitos ou diarreia.
Se esquecer de tomar Translarna
Se esqueceu de tomar Translarna e passaram menos de 3 horas desde o momento da toma habitual da manhã ou do meio-dia, ou menos de 6 horas desde a da noite, ainda pode tomar a dose. Lembre-se de tomar a seguinte dose à sua hora.
Se esqueceu a dose e passaram mais de 3 horas desde a toma habitual da manhã ou do meio-dia, ou mais de 6 horas desde a da noite, não tome a dose. Mas tome as seguintes doses à sua hora.
Não tome uma dose dupla para compensar as doses esquecidas. É importante que tome a dose correcta. Translarna pode não ser tão eficaz para tratar os seus sintomas se tomar mais da dose recomendada.
Se interromper o tratamento com Translarna
Não deixe de tomar Translarna sem consultar o seu médico.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram. Depois de tomar Translarna pode experimentar um ou vários dos seguintes efeitos adversos:
Efeitos adversos muito frequentes (podem afectar mais de 1 de cada 10 pacientes):
- Vómitos
Efeitos adversos frequentes (podem afectar até 1 de cada 10 pacientes):
- Perda do apetite
- Níveis elevados de triglicéridos no sangue
- Dor de cabeça
- Náuseas
- Perda de peso
- Pressão arterial alta
- Tosse
- Sangramento nasal
- Prisão de ventre
- Gases
- Molestias no estômago
- Dor de estômago
- Erupção
- Dor de braços ou pernas
- Dor no peito
- Micção involuntária
- Sangue na urina
- Febre
Frequência não conhecida (não pode ser estimada a partir dos dados disponíveis):
- Aumento em lípidos sanguíneos
- Aumento em testes de função renal
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, pode contribuir para fornecer mais informação sobre a segurança deste medicamento.
5. Conservação de Translarna
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no embalagem e no sobre após “CAD”. A data de validade é o último dia do mês que se indica.
Não requer condições especiais de conservação.
Tome cada dose preparada imediatamente após a sua preparação. Se a dose preparada for mantida refrigerada (2 - 8 °C) deve ser descartada se não for utilizada nas 24 horas seguintes à preparação ou nas 3 horas seguintes se for mantida à temperatura ambiente (15 - 30 °C).
Os medicamentos não devem ser jogados fora por esgotos ou lixo. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Translarna
Translarna está disponível em 3 concentrações, que contêm respectivamente 125 mg, 250 mg e 1.000 mg do princípio ativo, chamado atalureno. Os outros componentes (excipientes) são: polidextrosa (E1200), macrogol, poloxâmero, manitol (E421), crospovidona, hidroxietil celulosa, aroma artificial de baunilha, (maltodextrina, aromatizantes artificiais e glicol de propileno), sílica, coloidal (E551) e estearato de magnésio.
Aspecto do produto e conteúdo do envase
Translarna é um granulado de cor entre branco e esbranquiçado para suspensão oral em sobres.
Translarna está disponível em envases que contêm 30 sobres.
Titular da autorização de comercialização e responsável pela fabricação
PTC Therapeutics International Limited
5º andar
3 Grand Canal Plaza
Grand Canal Street Upper
Dublin 4
D04 EE70
Irlanda
Pode solicitar mais informação sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Responsável pela fabricação
Almac Pharma Services
22 Seagoe Industrial Estate
Craigavon BT63 5QD Reino Unido
PTC Therapeutics International Limited
5º andar
3 Grand Canal Plaza
Grand Canal Street Upper
Dublin 4
D04 EE70
Irlanda
Almac Pharma Services (Irlanda) Limited
Finnabair Industrial Estate
Dundalk, Co. Louth, A91 P9KD
Irlanda
Data da última revisão deste prospecto:
Este medicamento foi autorizado com uma «autorização condicional». Esta modalidade de autorização significa que se espera obter mais informação sobre este medicamento.
A Agência Europeia de Medicamentos reverá a informação nova sobre este medicamento pelo menos uma vez por ano e este prospecto será actualizado quando necessário
A informação detalhada sobre este medicamento está disponível no site da Agência Europeia de Medicamentos: http://www.ema.europa.eu. Também existem ligações a outras páginas web sobre doenças raras e medicamentos órfãos.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a TRANSLARNA 1000 mg GRÂNULOS PARA SUSPENSÃO ORALForma farmacêutica: SOLUÇÃO/SUSPENSÃO ORAL, 125mgSubstância ativa: atalurenFabricante: Ptc Therapeutics International LimitedRequer receita médicaForma farmacêutica: SOLUÇÃO/SUSPENSÃO ORAL, 250mgSubstância ativa: atalurenFabricante: Ptc Therapeutics International LimitedRequer receita médicaForma farmacêutica: SOLUÇÃO/SUSPENSÃO ORAL, 8,86 mg/mlSubstância ativa: givinostatFabricante: Italfarmaco S.P.A.Requer receita médica
Alternativas a TRANSLARNA 1000 mg GRÂNULOS PARA SUSPENSÃO ORAL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a TRANSLARNA 1000 mg GRÂNULOS PARA SUSPENSÃO ORAL em Ukraine
Médicos online para TRANSLARNA 1000 mg GRÂNULOS PARA SUSPENSÃO ORAL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de TRANSLARNA 1000 mg GRÂNULOS PARA SUSPENSÃO ORAL – sujeita a avaliação médica e regras locais.






