Como usar SKYRIZI 360 mg SOLUÇÃO INJETÁVEL EM CARTUCHO
Introdução
Prospecto: informação para o paciente
Skyrizi 180mg solução injetável em cartucho
Skyrizi 360 mg solução injetável em cartucho
risancizumab
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Skyrizi e para que é utilizado
- O que precisa saber antes de começar a usar Skyrizi
- Como usar Skyrizi
- Possíveis efeitos adversos
- Conservação de Skyrizi
- Conteúdo do envase e informações adicionais
1. O que é Skyrizi e para que é utilizado
Skyrizi contém o princípio ativo risancizumab.
Skyrizi é utilizado para tratar pacientes adultos com:
- doença de Crohn de moderada a grave
- colite ulcerosa de moderada a grave
Como funciona Skyrizi
Este medicamento actua bloqueando uma proteína do organismo chamada “IL-23” que provoca inflamação.
Doença de Crohn
A doença de Crohn é uma doença inflamatória do aparelho digestivo. Se tem doença de Crohn ativa, é possível que primeiro lhe administrem outros medicamentos. Se estes medicamentos não funcionam suficientemente bem, será administrado Skyrizi para o tratamento da sua doença de Crohn.
Colite ulcerosa
A colite ulcerosa é uma doença inflamatória do intestino grosso. Se tem colite ulcerosa ativa, é possível que primeiro lhe administrem outros medicamentos. Se estes medicamentos não funcionam suficientemente bem ou se não pode tomá-los, será administrado Skyrizi para tratar a sua colite ulcerosa.
Skyrizi reduz a inflamação e, por isso, pode ajudar a reduzir os sinais e sintomas da sua doença.
2. O que precisa saber antes de começar a usar Skyrizi
Não use Skyrizi
- se é alérgico a risancizumab ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
- se tem uma infecção que o seu médico considera importante, por exemplo, tuberculose ativa.
Advertências e precauções
Consulte o seu médico, farmacêutico ou enfermeiro antes de começar a usar Skyrizi e durante o tratamento:
- se padece uma infecção atualmente ou se tem uma infecção que reaparece.
- se padece tuberculose (TB).
- se recebeu recentemente ou tem previsto receber uma vacina. Certas vacinas não devem ser administradas durante o tratamento com Skyrizi.
É importante que o seu médico ou enfermeiro conserve uma cópia do número de lote de Skyrizi.
Cada vez que receber um novo envase de Skyrizi, o seu médico ou enfermeiro deve anotar a data e o número de lote (que aparece no envase após “Lote”).
Reações alérgicas
Consulte o seu médico ou solicite atenção médica de imediato se advertir algum sinal de reação alérgica enquanto recebe Skyrizi, por exemplo:
- dificuldade para respirar ou engolir
- inchaço do rosto, lábios, língua ou garganta
- coceira intensa na pele, com uma erupção vermelha ou bolhas
Crianças e adolescentes
Skyrizi não é recomendado em crianças e adolescentes menores de 18 anos de idade, porque não se estudou o uso de Skyrizi neste grupo de idade.
Outros medicamentos e Skyrizi
Informa o seu médico, farmacêutico ou enfermeiro:
- se está utilizando, utilizou recentemente ou poderia ter que utilizar qualquer outro medicamento.
- se se vacinou recentemente ou tem previsto vacinar-se. Certas vacinas não devem ser administradas durante o tratamento com Skyrizi.
Em caso de dúvida, consulte o seu médico, farmacêutico ou enfermeiro antes de usar Skyrizi e durante o tratamento.
Gravidez, anticoncepção e amamentação
Se está grávida, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico antes de utilizar este medicamento. É necessário que o faça porque não se sabe como afetará este medicamento ao bebê.
Se é uma mulher que pode engravidar, deve utilizar anticoncepcionais enquanto estiver em tratamento com este medicamento e durante um mínimo de 21 semanas após a sua última dose de Skyrizi.
Se está em período de amamentação ou tem intenção de amamentar um bebê, consulte o seu médico antes de utilizar este medicamento.
Condução e uso de máquinas
É pouco provável que Skyrizi afete a sua capacidade para conduzir e usar máquinas.
Skyrizi contém sódio
Este medicamento contém menos de 1 mmol de sódio (23 mg) por frasco; isto é, é essencialmente “isento de sódio”.
3. Como usar Skyrizi
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte de novo o seu médico ou farmacêutico.
Este medicamento é administrado mediante uma injeção sob a pele (chamada “injeção subcutânea”).
Quanto Skyrizi utilizar
Vai começar o tratamento com Skyrizi a uma dose inicial que lhe será administrada pelo seu médico ou enfermeiro mediante gotejamento no braço (perfusão intravenosa).
Doses iniciais
Quanto? | Quando? | |
Doença de Crohn | 600 mg | Quando o seu médico indicar |
600 mg | 4 semanas após a 1.ª dose | |
600 mg | 4 semanas após a 2.ª dose |
Colite ulcerosa | Quanto? | Quando? |
1 200 mg | Quando o seu médico indicar | |
1 200 mg | 4 semanas após a 1.ª dose | |
1 200 mg | 4 semanas após a 2.ª dose |
Posteriormente, receberá Skyrizi mediante uma injeção sob a pele.
Doses de manutenção
Doença de Crohn | Quanto? | Quando? |
1.ª dose de manutenção | 360 mg | 4 semanas após a última dose inicial (na semana 12) |
Doses seguintes | 360 mg | Cada 8 semanas, começando após a 1.ª dose de manutenção |
Colite ulcerosa | Quanto? | Quando? |
1.ª dose de manutenção | 180 mg ou 360 mg | 4 semanas após a última dose inicial (na semana 12) |
Doses seguintes | 180 mg ou 360 mg | Cada 8 semanas, começando após a 1.ª dose de manutenção |
Si e o seu médico, farmacêutico ou enfermeiro decidirão se se poderia injetar este medicamento si mesmo. Não deve injetar este medicamento si mesmo a menos que o seu médico, farmacêutico ou enfermeiro lhe tenham ensinado como fazer. Também é possível que lhe administre a injeção um cuidador que tenha aprendido a fazê-lo.
Leia a seção 7 “Instruções de uso” no final deste prospecto antes de se aplicar a injeção de Skyrizi.
Se usar mais Skyrizi do que deve
Se utilizou mais Skyrizi do que deve ou se administraram a dose antes do prescrito, consulte o seu médico.
Se esquecer de usar Skyrizi
Se esquecer de se administrar Skyrizi, deve injetar uma dose assim que se lembrar. Em caso de dúvida, consulte o seu médico.
Se interromper o tratamento com Skyrizi
Não deixe de utilizar Skyrizi sem falar antes com o seu médico. Se interromper o tratamento, os seus sintomas podem reaparecer.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Efeitos adversos graves
Consulte o seu médico ou solicite atenção médica de imediato se tiver algum sintoma de infecção grave, por exemplo:
- febre, sintomas pseudogripais, suores noturnos
- sensação de cansaço ou dificuldade para respirar, tos persistente
- calor, vermelhidão e dor na pele ou uma erupção cutânea dolorosa com bolhas
Seu médico decidirá se pode continuar utilizando Skyrizi.
Outros efeitos adversos
Informa o seu médico, farmacêutico ou enfermeiro se notar algum dos seguintes efeitos adversos.
Muito frequentes:podem afetar mais de 1 de cada 10 pessoas
- infecções das vias respiratórias altas com sintomas como dor de garganta e congestão nasal
Frequentes:podem afetar até 1 de cada 10 pessoas
- sensação de cansaço
- infecção de fungos na pele
- reações no local de injeção (como vermelhidão ou dor)
- coceira
- dor de cabeça
- erupção
- eczema
Pouco frequentes:podem afetar até 1 de cada 100 pessoas
- pequenos bolhas vermelhos na pele
- urticárias
Comunicação de efeitos adversos
Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Skyrizi
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta do cartucho e na caixa exterior após EXP.
Conservar na geladeira (entre 2 ºC e 8 ºC). Não congelar.
Se necessário, também pode conservar o cartucho fora da geladeira (a uma temperatura máxima de 25 °C) durante um máximo de 24 horas.
Conservar o cartucho no embalagem original para protegê-lo da luz.
Não utilize este medicamento se o líquido estiver turvo ou contiver escamas ou partículas grandes.
Cada injetor corporal com cartucho é para um único uso.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Skyrizi
O princípio ativo é risankizumab.
Skyrizi 180 mg solução injetável em cartucho
- Cada cartucho contém 180 mg de risankizumab em 1,2 ml de solução.
- Os demais componentes são acetato de sódio trihidrato, ácido acético, trealose dihidrato, polissorbato 20 e água para preparações injetáveis.
Skyrizi 360 mg solução injetável em cartucho
- Cada cartucho contém 360 mg de risankizumab em 2,4 ml de solução.
- Os demais componentes são acetato de sódio trihidrato, ácido acético, trealose dihidrato, polissorbato 20 e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Skyrizi é um líquido transparente de incolor a cor amarela contido em um cartucho. O líquido pode conter partículas diminutas transparentes ou brancas.
Cada envase contém 1 cartucho e 1 injetor corporal.
Título da autorização de comercialização e responsável pela fabricação
AbbVie Deutschland GmbH & Co. KG
Knollstrasse
67061 Ludwigshafen
Alemanha
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização:
Bélgica AbbVie SA Tel: +32 10 477811 | Lituânia AbbVie UAB Tel: +370 5 205 3023 |
| Luxemburgo AbbVie SA Bélgica Tel: +32 10 477811 |
República Checa AbbVie s.r.o. Tel: +420 233 098 111 | Hungria AbbVie Kft. Tel: +36 1 455 8600 |
Dinamarca AbbVie A/S Tlf: +45 72 30-20-28 | Malta V.J.Salomone Pharma Limited Tel: +356 22983201 |
Alemanha AbbVie Deutschland GmbH & Co. KG Tel: 00800 222843 33 (gratuito) Tel: +49 (0) 611 / 1720-0 | Países Baixos AbbVie B.V. Tel: +31 (0)88 322 2843 |
Estônia AbbVie OÜ Tel: +372 623 1011 | Noruega AbbVie AS Tlf: +47 67 81 80 00 |
Grécia AbbVie ΦΑΡΜΑΚΕΥΤΙΚΗ Α.Ε. Τηλ: +30 214 4165 555 | Áustria AbbVie GmbH Tel: +43 1 20589-0 |
Espanha AbbVie Spain, S.L.U. Tel: +34 91 384 09 10 | Polônia AbbVie Sp. z o.o. Tel: +48 22 372 78 00 |
França AbbVie Tél: +33 (0) 1 45 60 13 00 | Portugal AbbVie, Lda. Tel: +351 (0)21 1908400 |
Croácia AbbVie d.o.o. Tel: +385 (0)1 5625 501 | Romênia AbbVie S.R.L. Tel: +40 21 529 30 35 |
Irlanda AbbVie Limited Tel: +353 (0)1 4287900 | Eslovênia AbbVie Biofarmacevtska družba d.o.o. Tel: +386 (1)32 08 060 |
Islândia Vistor hf. Tel: +354 535 7000 | Eslováquia AbbVie s.r.o. Tel: +421 2 5050 0777 |
Itália AbbVie S.r.l. Tel: +39 06 928921 | Finlândia AbbVie Oy Puh/Tel: +358 (0)10 2411 200 |
Chipre Lifepharma (Z.A.M.) Ltd Τηλ: +357 22 34 74 40 | Suécia AbbVie AB Tel: +46 (0)8 684 44 600 |
Letônia AbbVie SIA Tel: +371 67605000 |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos: http://www.ema.europa.eu.
A informação detalhada e atualizada sobre este produto está disponível a seguir ou no embalagem exterior digitalizando o código QR por meio de um smartphone. A mesma informação também está disponível no seguinte site: www.skyrizi.eu
Código QR a incluir
Para solicitar uma cópia deste prospecto em
- Instruções de uso
Leia toda a seção 7 antes de utilizar Skyrizi
Injetor corporal de Skyrizi
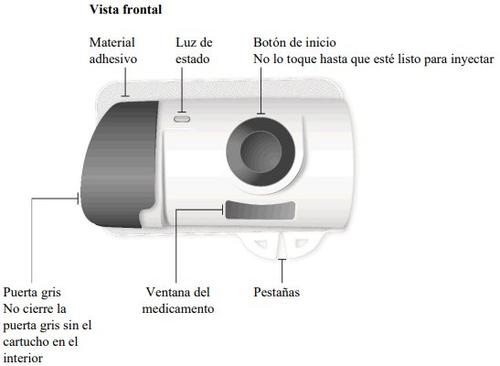
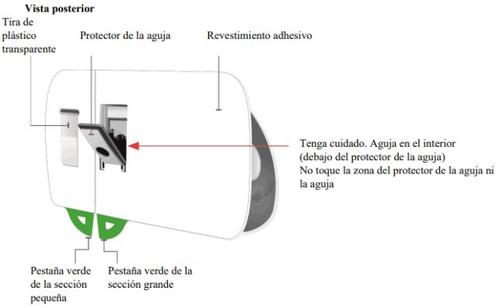
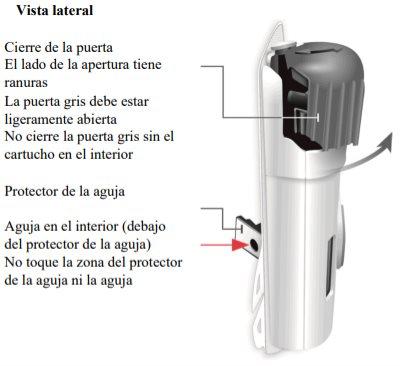
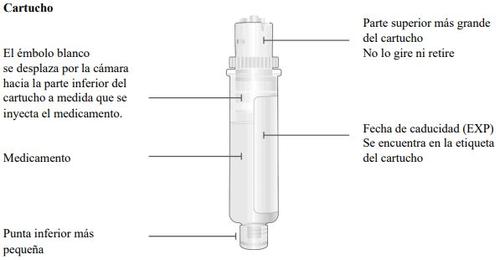
Informação importante que deve conhecer antes da injeção de Skyrizi
- Você deve ter recebido treinamento sobre como injetar Skyrizi antes de administrar uma injeção. Se precisar de ajuda, consulte seu médico, farmacêutico ou enfermeiro
- Marque as datas em um calendário para saber quando é a vez de injetar Skyrizi
- O injetor corporal de uso único é projetado para uso exclusivamente com o cartucho de Skyrizi
- Mantenha Skyrizi em seu embalagem original para proteger o medicamento da luz até o momento de usá-lo
- Retire a caixa da geladeira e deixe-a em temperatura ambiente, longe da luz solar direta, por pelo menos 45 e até 90 minutosantes da injeção
- Nãodeixe que o injetor corporal se molhe com água ou com qualquer outro líquido
- Nãotoque o botão de início até que coloque o injetor corporal carregado com o cartucho sobre a pele e esteja pronto para injetar
- Únicamente pode pressionar o botão de início umavez
- Durante o processo de injeção, deve limitar a atividade física. Pode realizar atividades físicas moderadas, como andar, esticar ou dobrar
- Nãoretarde a injeção do medicamento uma vez carregado o cartucho limpo no injetor corporal. Se esperar, o medicamento secará e o injetor corporal deixará de funcionar
- Nãoinjete o medicamento se o líquido da janela de inspeção estiver turvo ou contiver escamas ou partículas grandes. O líquido deve ser transparente a cor amarela e pode conter partículas diminutas transparentes ou brancas
- Nãoagite a caixa, o cartucho ou o injetor corporal
- Nãoreutilize o cartucho ou o injetor corporal
Devolva este medicamento à farmácia
- após a data de validade (EXP) indicada
- se o líquido se congelou em algum momento (mesmo se descongelou)
- se o cartucho ou o injetor corporal se caíram ou danificaram
- se as perfurações da caixa estão quebradas
- se a cobertura de papel branco da bandeja não está ou se quebrou
Siga os seguintes passos cada vez que usar Skyrizi
PASSO 1: Prepare-se | ||
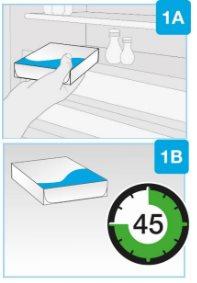
| Retire a caixa da geladeira e deixe-a em temperatura ambiente, longe da luz solar direta, durante pelo menos 45 e até 90 minutosantes da injeção.
| |
Contenedor para resíduos especiais
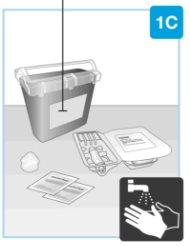
| Reúna todos os materiais e lave as mãos Sobre uma superfície lisa e limpa, coloque o seguinte:
Lave e seque as mãos. | |
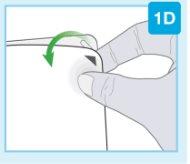
| Retire o selo de papel branco da bandeja
| |
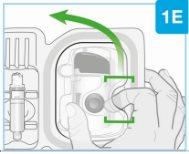
| Levante a cobertura de plástico
| |
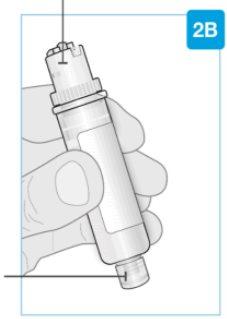
Parte superior maior do cartucho | Inspeccione o cartucho Retire com cuidado o cartucho da bandeja de plástico.
Verifique o cartucho
| |
Ponta inferior menor |
| |
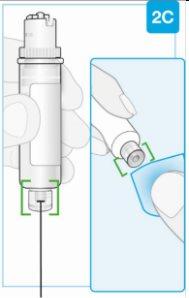
Ponta inferior menor | Limpe a ponta inferior menor do cartucho Localize a ponta inferior menor do cartucho
| |
Limpe o centro da ponta inferior menor | ||
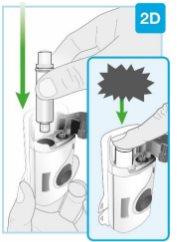
Insira em linha reta “clic”
| Carregue o cartucho limpo no injetor corporal
Certifique-se de proceder com o próximo passo imediatamente. Se esperar, o medicamento secará. | |
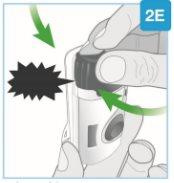
“estalo” | Feche a porta cinza Gire a porta cinza para a esquerda, luego aperte firmemente e ouvirá um “estalo” ao fechar a porta cinza
| |
PASSO 3: Preparação da injeção | ||
Zonas de injeção
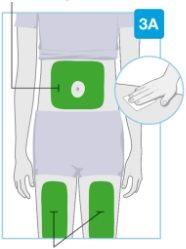
Zonas de injeção | Escolha e limpe o local de injeção Escolha uma das 3 zonas para aplicar a injeção:
Nãoinjete em zonas da pele com dobras ou proeminências naturais, pois o injetor corporal pode cair durante o uso. Antes da injeção, limpe o local de injeção com uma toalheta impregnada em álcool fazendo movimentos circulares.
| |
Seção pequena Seção grande
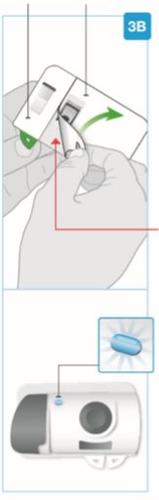
| Aguja no interior (debaixo do protetor da aguja) Injetor ativado A luz de estado pisca em azul | Desprenda ambas as abas para que fique exposto o adesivo cutâneo Volte ao injetor corporal para localizar as duas abas verdes
Retire a seção grande utilizando a aba verde para que fique exposto o adesivo cutâneo Retire a seção pequena utilizando a aba verde para que fique exposto o adesivo cutâneo. Dessa forma, removerá a tira de plástico transparente e ativará o injetor corporal.
O injetor corporal de Skyrizi deve ser colocado sobre a pele e a injeção deve ser iniciada nos 30 minutos seguintes à remoção das abas verdes; caso contrário, não funcionará. Certifique-se de proceder com o próximo passo imediatamente. |
| Se a luz de estado piscar em vermelho, o injetor corporal não funciona corretamente. Não continue usando. Consulte seu médico, farmacêutico ou enfermeiro para que o ajudem. Se o injetor corporal estiver grudado em seu corpo, retire-o com cuidado da pele. | |
|
Injeção no abdômen e coxa marcadas com pontos verdes setas indicam movimento de um dispositivo aplicador cilíndrico">
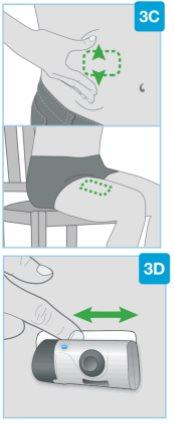
Prepare o injetor corporal para sua colocação
- Para a barriga (abdômen), mova e segure a pele para criar uma superfície firme e plana para a injeção a pelo menos 5 cm de distância do umbigo. Certifique-se de sentar-se em posição ereta para evitar os dobras e proeminências da pele.
- Não é necessário puxar a pele para aplanar a parte da frente da coxa esquerda ou direita.
Certifique-se de colocar o injetor corporal de maneira que possa ver a luz de estado azul.
Coloque o injetor corporal sobre a pele
- Quando a luz azul piscar, o injetor corporal estará pronto. Coloque o injetor corporal sobre a pele limpa com a luz de estado visível
- Nãocoloque o injetor corporal sobre a roupa. Coloque-o apenas sobre a pele nua.
- Passe um dedo ao redor do material adesivo para fixá-lo
- Nãomova nem ajuste o injetor corporal após tê-lo colocado sobre a pele
Prossiga imediatamente para o próximo passo.
PASSO 4: Injeção de Skyrizi
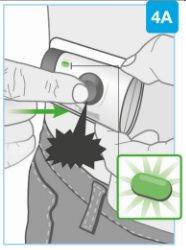
“clic”
Inicie a injeção
Pressione firmemente o botão gris de início e solte
- Ouça um “clic” e pode sentir um pinchazo da agulha
- Verifique a luz de estado quando o injetor corporal emitir um sinal sonoro
- Depois de iniciar a injeção, a luz de estado piscará continuamente em verde
- Uma vez iniciada a injeção, ouvirá sons de bombeio enquanto o injetor corporal administra o medicamento
Nãocontinue utilizando o injetor corporal se a luz de estado piscar em vermelho. Retire-o com cuidado da pele se a luz de estado piscar em vermelho. Se isso ocorrer, informe seu médico, farmacêutico ou enfermeiro.
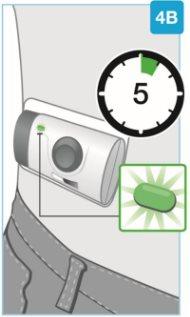
Aguarde até que termine a injeção
- Pode levar até 5 minutos para administrar a dose completa do medicamento. O injetor corporal se deterá automaticamente quando terminar a injeção
- Durante a injeção, a luz de estado seguirá piscando em verde
- Durante a injeção, ouvirá sons de bombeio enquanto o injetor corporal segue administrando o medicamento
- Durante a injeção, podem ser realizadas atividades físicas moderadas, como andar, esticar ou dobrar.
Nãosiga utilizando o injetor corporal se a luz de estado piscar em vermelho. Retire-o com cuidado da pele se a luz de estado piscar em vermelho. Se isso ocorrer, informe seu médico, farmacêutico ou enfermeiro.
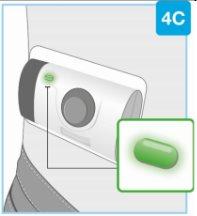
A injeção terminou quando:
- O injetor corporal se detém por si só
- Ouça um sinal sonoro e a luz de estado muda para verde fixo. Se a luz de estado mudou para verde fixo, significa que a injeção terminou
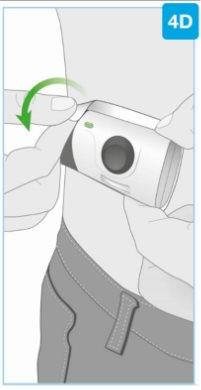
Retire o injetor corporal
- Nãocoloque os dedos na parte posterior do injetor corporal quando o retirar da pele
- Uma vez terminada a injeção, agarre a esquina do adesivo para despegar com cuidado o injetor corporal da pele
- Evite tocar o protetor da agulha ou a agulha na parte posterior do injetor corporal
- Depois de retirar o injetor corporal, ouvirá vários sinais sonoros e a luz de estado se apagará
- O protetor da agulha cobrirá a agulha quando se retirar o injetor corporal da pele
- É normal ver algumas pequenas gotas de líquido na pele após retirar o injetor corporal
- Pressione com uma bola de algodão ou uma gaze sobre o local de injeção e mantenha pressionado durante 10 segundos.
- Nãoesfregue o local de injeção
- É normal que haja um ligeiro sangramento no local de injeção
Prossiga com o próximo passo.
PASSO 5: Finalização
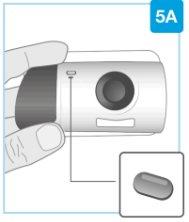
Verifique o injetor corporal
Inspeccione a janela do medicamento e a luz de estado.
Verifique que o êmbolo branco preenche toda a janela do medicamento e que a luz verde fixa se apaga, o que lhe indica que se injetou todo o medicamento.
- Se o êmbolo branco não preencher a janela, informe seu médico, farmacêutico ou enfermeiro
Contenedor para resíduos especiais
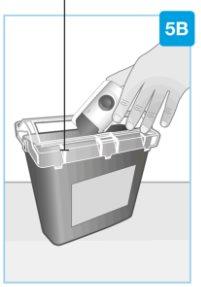
Eliminação
Jogue o injetor corporal usado em um contenedor para resíduos especiais imediatamente após seu uso.
- O injetor corporal contém pilhas, componentes eletrônicos e uma agulha
- Deixe o cartucho no injetor corporal.
- Nãojogue o injetor corporal usado no lixo doméstico
- Seu médico, farmacêutico ou enfermeiro lhe explicarão como devolver o contenedor para resíduos especiais quando estiver cheio. Pode haver diretrizes locais para sua eliminação
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a SKYRIZI 360 mg SOLUÇÃO INJETÁVEL EM CARTUCHOForma farmacêutica: INJETÁVEL, 150 mgSubstância ativa: risankizumabFabricante: Abbvie Deutschland Gmbh & Co. KgRequer receita médicaForma farmacêutica: INJETÁVEL, 150 mgSubstância ativa: risankizumabFabricante: Abbvie Deutschland Gmbh & Co. KgRequer receita médicaForma farmacêutica: INJETÁVEL, 180 mgSubstância ativa: risankizumabFabricante: Abbvie Deutschland Gmbh & Co. KgRequer receita médica
Alternativas a SKYRIZI 360 mg SOLUÇÃO INJETÁVEL EM CARTUCHO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a SKYRIZI 360 mg SOLUÇÃO INJETÁVEL EM CARTUCHO em Ukraine
Médicos online para SKYRIZI 360 mg SOLUÇÃO INJETÁVEL EM CARTUCHO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de SKYRIZI 360 mg SOLUÇÃO INJETÁVEL EM CARTUCHO – sujeita a avaliação médica e regras locais.