SHINGRIX pó e suspensão para suspensão injetável

Pergunte a um médico sobre a prescrição de SHINGRIX pó e suspensão para suspensão injetável

Como usar SHINGRIX pó e suspensão para suspensão injetável
Introdução
Prospecto: informação para o utilizador
Shingrix pó e suspensão para suspensão injetável
vacina contra o herpes zóster (recombinante, adjuvada)
Leia todo o prospecto atentamente antes de começar a receber esta vacina, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que o ler novamente.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Shingrix e para que é utilizado
- O que precisa saber antes de receber Shingrix
- Como é administrado Shingrix
- Possíveis efeitos adversos
- Conservação de Shingrix
- Conteúdo do envase e informação adicional
1. O que é Shingrix e para que é utilizado
Para que é utilizado Shingrix
Shingrix é uma vacina que ajuda a proteger os adultos contra o herpes zóster (culebrilha) e contra a neuralgia pós-herpética (NPH), a dor de longa duração que segue ao herpes zóster devido a um dano nos nervos.
Shingrix é administrado a:
- adultos a partir de 50 anos de idade;
- adultos a partir de 18 anos de idade que têm um maior risco de sofrer de herpes zóster.
Shingrix não pode ser utilizado para prevenir a varicela.
O que é o herpes zóster
- O herpes zóster é uma erupção com vesículas, frequentemente dolorosa. Geralmente aparece em uma zona limitada do corpo e pode durar várias semanas.
- O herpes zóster é causado pelo mesmo vírus que causa a varicela.
- Depois de ter sofrido de varicela, o vírus que a causou permanece no seu corpo, nas células nervosas.
- Às vezes, após muitos anos, se o seu sistema imunológico (as defesas naturais do corpo) se debilitar (devido à idade, a uma doença ou a um medicamento que está a tomar), o vírus pode causar herpes zóster.
Complicações relacionadas com o herpes zóster
O herpes zóster pode provocar complicações.
A complicação mais frequente associada ao herpes zóster é:
- dor de longa duração devido a um dano nos nervos – chamada neuralgia pós-herpética ou NPH. Uma vez que as vesículas do herpes zóster desaparecem, pode ter dor durante meses ou anos e pode ser grave.
Outras complicações do herpes zóster são:
- cicatrizes onde houve vesículas
- infecções da pele, fraqueza, paralisia muscular e perda de audição ou visão – estas são menos frequentes.
Como funciona Shingrix
Shingrix permite que o seu corpo lembre o vírus que causa o herpes zóster. Isso ajuda ao seu sistema imunológico (as defesas naturais do corpo) a estar preparado para combater o vírus e protegê-lo contra o herpes zóster e suas complicações.
2. O que precisa saber antes de receber Shingrix
Não lhe deve ser administrado Shingrix se
- se é alérgico ao princípio ativo ou a algum dos outros componentes desta vacina (incluídos na secção 6). Os sinais de uma reação alérgica podem incluir: erupção cutânea com picazão, dificuldade para respirar e inchaço do rosto ou língua.
Não lhe deve ser administrado Shingrix se lhe aplicar alguma das condições acima. Se não tiver certeza, consulte o seu médico ou farmacêutico.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a receber Shingrix se:
- tiver uma infecção grave com temperatura alta (febre). Nesses casos, pode ser necessário adiar a vacinação até que se tenha recuperado. Uma infecção menor, como um resfriado, não deve ser um problema, mas consulte primeiro o seu médico;
- tiver um problema de coagulação ou apresentar hematomas com facilidade.
Se lhe aplicar alguma das condições acima (ou não tiver certeza), consulte o seu médico ou farmacêutico antes de que lhe seja administrado Shingrix.
Antes ou depois de qualquer injeção, pode ocorrer um desmaio, por isso deve informar o seu médico ou enfermeiro se já desmaiou em ocasiões anteriores após a administração de uma injeção.
Shingrix não pode ser utilizado como tratamento se já tiver herpes zóster ou complicações associadas a este.
Como com todas as vacinas, pode ser que Shingrix não proteja completamente todos os vacinados.
Consulte o seu médico se, após receber Shingrix, experimentar inflamação temporária dos nervos que produz dor, fraqueza e paralisia (chamada síndrome de Guillain-Barré). Foi notificado um ligeiro aumento do risco de sofrer de síndrome de Guillain-Barré (estimado em 3 casos adicionais por milhão de doses administradas) após receber Shingrix em pessoas a partir dos 65 anos de idade.
Outros medicamentos e Shingrix
Informa o seu médico ou farmacêutico se está a utilizar, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento, incluindo medicamentos sem prescrição, ou se lhe foi administrada recentemente qualquer outra vacina.
Shingrix pode ser administrado ao mesmo tempo que outras vacinas, como a vacina inativada não adjuvada contra a gripe sazonal, a vacina antineumocócica polissacarídica 23-valente, a vacina antineumocócica conjugada 13-valente, a vacina antidiftérica, antitetânica e antitossina (componente acelular) de teor antigénico reduzido ou a vacina de ARNm contra o COVID-19. Será utilizado um local de injeção distinto para cada vacina.
É mais provável que sofra febre e/ou calafrios quando se administra Shingrix ao mesmo tempo que a vacina antineumocócica polissacarídica 23-valente.
É mais provável que sofra calafrios, cansaço, febre, desconforto estomacal e digestivo (incluindo náuseas, vómitos, diarreia e/ou dor de estômago), dor de cabeça, dor muscular ou dor nas articulações quando se lhe administra uma vacina de ARNm contra o COVID-19 ao mesmo tempo que Shingrix.
Gravidez e lactação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de que lhe seja administrada esta vacina.
Condução e uso de máquinas
Alguns dos efeitos mencionados na secção 4 “Possíveis efeitos adversos” podem afetar temporariamente a capacidade para conduzir ou utilizar máquinas. Não conduza ou maneje máquinas se não se sentir bem.
Shingrix contém polissorbato 80, sódio e potássio
Este medicamento contém 0,08 mg de polissorbato 80 por dose. Os polissorbatos podem causar reações alérgicas. Informe o seu médico se tiver alguma alergia conhecida.
Este medicamento contém menos de 1 mmol de sódio (23 mg) por dose; isto é, é essencialmente “isento de sódio”.
Este medicamento contém potássio, menos de 1 mmol (39 mg) por dose; isto é, é essencialmente “isento de potássio”.
3. Como é administrado Shingrix
- Shingrix é administrado por injeção no músculo (normalmente na parte superior do braço).
- Receberá 2 injeções com 2 meses de diferença. Se for necessário flexibilidade no esquema de vacinação, a segunda dose pode ser administrada entre 2 e 6 meses após a primeira dose.
Dependendo do seu estado de saúde, o seu médico também pode recomendar que receba a segunda injeção 1 mês após a primeira.
- Será informado sobre quando deve voltar para receber a segunda dose de Shingrix.
Certifique-se de que completa o programa de vacinação. Isso maximizará a proteção oferecida por Shingrix.
Pode ser administrado Shingrix mesmo que já tenha sido vacinado com a vacina viva atenuada contra o herpes zóster. Para mais informações, consulte o seu médico.
4. Possíveis efeitos adversos
Como todos os medicamentos, esta vacina pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Efeitos adversos notificados durante os ensaios clínicos e após a comercialização de Shingrix:
Muito frequentes(podem ocorrer em mais de 1 de cada 10 doses de vacina):
- dor de cabeça
- sintomas de estômago e digestivos (que incluem náuseas, vómitos, diarreia e/ou dor de estômago)
- dor muscular (mialgia)
- dor, vermelhidão e inchaço na zona de injeção
- sensação de cansaço
- calafrios
- febre.
Frequentes(podem ocorrer até em 1 de cada 10 doses de vacina):
- picazão na zona de injeção (prurito)
- malestar geral.
Pouco frequentes(podem ocorrer até em 1 de cada 100 doses de vacina):
- inchaço dos gânglios do pescoço, axilas ou ingles
- dor nas articulações.
Raros(podem ocorrer até em 1 de cada 1 000 doses de vacina):
- reações alérgicas, incluindo erupção, habão urticarial (urticária), inchaço do rosto, língua ou garganta que pode causar dificuldade para engolir ou respirar (angioedema).
A maioria desses efeitos adversos é de intensidade leve a moderada e de curta duração.
Os adultos imunocomprometidos entre 18 e 49 anos de idade podem ter mais efeitos adversos do que os adultos imunocomprometidos com 50 anos de idade ou mais.
Os adultos entre 50 e 69 anos de idade podem ter mais efeitos adversos do que os adultos com 70 anos de idade ou mais.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Shingrix
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e no envase. A data de validade é o último dia do mês que é indicado.
Conservar em frigorífico (entre 2 ºC e 8 ºC). Não congelar.
Conservar no embalagem original para protegê-lo da luz.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, você ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Shingrix
- Os princípios ativos são:
Após a reconstituição, uma dose (0,5 ml) contém: Glicoproteína E como componente antigénico2 do vírus da varicela zóster1 | 50 microgramas |
1 vírus da varicela zóster = VVZ | |
2 adjuvada com AS01B que contém: extrato da planta Quillaja saponariaMolina, fração 21 (QS-21) | 50 microgramas |
3-O-desacil-4’-monofosforil lípido A (MPL) de Salmonella minnesota | 50 microgramas |
A glicoproteína E é uma proteína presente no vírus da varicela zóster. Esta proteína não é infecciosa. O adjuvante (AS01B) é utilizado para potenciar a resposta do corpo à vacina. |
- Os outros componentes são:
- Pó:sacarose, polissorbato 80 (E 433), dihidrogenofosfato de sódio dihidratado (E 339), fosfato dipotássico (E 340).
- Suspensão:dioleoil fosfatidilcolina (E 322), colesterol, cloreto de sódio, fosfato disódico anidro (E 339), dihidrogenofosfato de potássio (E 340) e água para preparações injetáveis.
Ver secção 2 “Shingrix contém polissorbato 80, sódio e potássio”.
Aspecto do produto e conteúdo do envase
Pó e suspensão para suspensão injetável. O pó é branco.
A suspensão é um líquido opalescente, de incoloro a marrom claro.
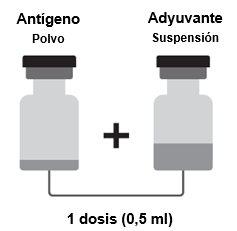
Um envase de Shingrix contém:
- Pó (antígeno) para 1 dose em um frasco
- Suspensão (adjuvante) para 1 dose em um frasco.
Shingrix está disponível em envases de 1 frasco com pó e 1 frasco com suspensão ou em envases de 10 frascos com pó e 10 frascos com suspensão.
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Bélgica
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
België/Belgique/Belgien GlaxoSmithKline Pharmaceuticals s.a./n.v. Tél/Tel: + 32 (0) 10 85 52 00 | Lietuva GlaxoSmithKline Biologicals SA Tel: +370 80000334 |
| Luxembourg/Luxemburg GlaxoSmithKline Pharmaceuticals s.a./n.v. Belgique/Belgien Tél/Tel: + 32 (0) 10 85 52 00 |
Ceská republika GlaxoSmithKline s.r.o. Tel: + 420 2 22 00 11 11 | Magyarország GlaxoSmithKline Biologicals SA Tel.: +36 80088309 |
Danmark GlaxoSmithKline Pharma A/S Tlf.: + 45 36 35 91 00 | Malta GlaxoSmithKline Biologicals SA Tel: + 356 80065004 |
Deutschland GlaxoSmithKline GmbH & Co. KG Tel: + 49 (0)89 360448701 | Nederland GlaxoSmithKline BV Tel: + 31 (0)33 2081100 |
Eesti GlaxoSmithKline Biologicals SA Tel: +372 8002640 | Norge GlaxoSmithKline AS Tlf: + 47 22 70 20 00 |
Ελλ?δα GlaxoSmithKline Μονοπρ?σωπη A.E.B.E Τηλ: + 30 210 68 82 100 | Österreich GlaxoSmithKline Pharma GmbH Tel: + 43 (0)1 97075 0 |
España GlaxoSmithKline, S.A. Tel: + 34 900 202 700 | Polska GSK Services Sp. z o.o. Tel.: + 48 (22) 576 9000 |
France Laboratoire GlaxoSmithKline Tél: + 33 (0) 1 39 17 84 44 Hrvatska GlaxoSmithKline Biologicals SA Tel.: + 385 800787089 | Portugal GlaxoSmithKline - Produtos Farmacêuticos, Lda. Tel: + 351 21 412 95 00 România GlaxoSmithKline Biologicals SA Tel: +40 800672524 |
Ireland GlaxoSmithKline (Ireland) Ltd Tel: + 353 (0)1 495 5000 | Slovenija GlaxoSmithKline Biologicals SA Tel: + 386 80688869 |
Ísland Vistor hf. Sími: +354 535 7000 | Slovenská republika GlaxoSmithKline Biologicals SA Tel.: + 421 800500589 |
Italia GlaxoSmithKline S.p.A. Tel: + 39 (0)45 7741 111 | Suomi/Finland GlaxoSmithKline Oy Puh/Tel: + 358 10 30 30 30 |
Κ?προς GlaxoSmithKline Biologicals SA Τηλ: + 357 80070017 | Sverige GlaxoSmithKline AB Tel: + 46 (0)8 638 93 00 |
Latvija GlaxoSmithKline Biologicals SA Tel: + 371 80205045 |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos: https://www.ema.europa.eu.
------------------------------------------------------------------------------------------------------------------------
Esta informação é destinada apenas a profissionais de saúde:
Shingrix é apresentado em um frasco com uma tampa removível marrom que contém o pó (antígeno) e um frasco com uma tampa removível azul-verde que contém a suspensão (adjuvante).
O pó e a suspensão devem ser reconstituídos antes da administração.
|
O pó e a suspensão devem ser examinados visualmente para observar se existe alguma partícula estranha e/ou variação do aspecto físico. Se for observada alguma dessas circunstâncias, não reconstituir a vacina.
Como preparar Shingrix:
Shingrix deve ser reconstituído antes da sua administração.
- Retirar todo o conteúdo do frasco que contém a suspensão com a seringa, usando uma agulha adequada (21G a 25G).
- Adicionar todo o conteúdo da seringa ao frasco que contém o pó.
- Agitar suavemente até que o pó se dissolva completamente.
A vacina reconstituída é um líquido opalescente, de incoloro a marrom claro.
A vacina reconstituída deve ser examinada de forma visual para observar se existe alguma partícula estranha e/ou variação do aspecto físico. Se for observada alguma dessas circunstâncias, não administrar a vacina.
Após a reconstituição, a vacina deve ser utilizada de imediato; se não for possível, a vacina deve ser armazenada em frigorífico (entre 2 °C e 8 °C). Deve ser descartada se não for utilizada em um período de 6 horas.
Antes da administração:
- Retirar todo o conteúdo do frasco que contém a vacina reconstituída com a seringa.
- Trocar a agulha de forma que se use uma nova agulha para administrar a vacina.
A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele será realizada de acordo com a regulamentação local.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a SHINGRIX pó e suspensão para suspensão injetávelForma farmacêutica: INJETÁVEL, -Substância ativa: varicella, live attenuatedFabricante: Glaxosmithkline S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, mínimo de 1350 UFP/0.5 ml doseSubstância ativa: varicella, live attenuatedFabricante: Schering Plough S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 60 microgramas/dose + 60 microgramas/doseSubstância ativa: respiratory syncytial virus vaccinesFabricante: Pfizer Europe Ma EeigRequer receita médica
Médicos online para SHINGRIX pó e suspensão para suspensão injetável
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de SHINGRIX pó e suspensão para suspensão injetável – sujeita a avaliação médica e regras locais.