
PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO
Pergunte a um médico sobre a prescrição de PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO

Como usar PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO
Introdução
Prospecto: informação para o utilizador
Prolastina 4000 mg pó e dissolvente para solução para perfusão
Prolastina 5000 mg pó e dissolvente para solução para perfusão
Princípio ativo: alfa1-antitripsina humana
Leia todo o prospecto atentamente antes de começar a usar este medicamento,pois contém informações importantes para si.
- Conserva este prospecto, pois pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, pois pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Prolastina e para que é utilizada
- O que necessita saber antes de começar a usar Prolastina
- Como usar Prolastina
- Possíveis efeitos adversos
- Conservação de Prolastina
- Conteúdo do envase e informação adicional
1. O que é Prolastina e para que é utilizada
Prolastina pertence a um grupo de medicamentos denominados “Inibidores de proteasas”.
A alfa1-antitripsina é um componente normal do sangue humano, cuja função consiste em inibir a atividade de alguns enzimas como as elastasas que podem danificar os pulmões. Quando há uma deficiência hereditária de alfa1-antitripsina, há um desequilíbrio entre a alfa1-antitripsina e as elastasas. Isso pode levar a uma destruição progressiva do tecido pulmonar e desenvolver um enfisema pulmonar. O enfisema pulmonar é um alargamento anormal do pulmão, acompanhado por destruição do tecido pulmonar. Prolastina está indicada para restaurar o equilíbrio entre alfa1-antitripsina e as elastasas no pulmão, e em consequência, evitar um maior deterioramento no enfisema pulmonar.
Prolastina é utilizada como tratamento crónico em certo tipo de pacientes com déficit de alfa1-antitripsina, conforme determinado pelo seu médico.
2. O que necessita saber antes de começar a usar Prolastina
Não use Prolastina
- Se é alérgico (hipersensível) à alfa1-antitripsina ou a qualquer um dos outros componentes de Prolastina (incluídos na seção 6).
- Se tem déficit de certas imunoglobulinas, conhecidas como IgA, pois podem desenvolver reações alérgicas graves que podem desembocar, mesmo, em choque anafilático.
Advertências e precauções
- Consulte o seu médico, farmacêutico ou enfermeiro antes de começar a usar Prolastina.
- Comunique ao seu médico se padece insuficiência cardíaca grave (falta cardíaca). Será necessário ter extrema precaução, pois Prolastina pode produzir um aumento transitório do volume de sangue.
Reações alérgicas (hipersensibilidade)
Raramente podem ocorrer reações de hipersensibilidade a Prolastina, embora se lhe tenham administrado previamente inibidores de alfa1-antitripsina humanos e os tenha tolerado bem.
O seu médico informá-lo-á sobre os sintomas das reações alérgicas e dir-lhe-á o que deve fazer em caso de que os experimente (ver também a seção 4).
Se experimentar qualquer sintoma de uma reação alérgica de hipersensibilidade durante a perfusão do medicamento, avise o seu médico ou enfermeiro imediatamente.
Informação sobre segurança com respeito ao risco de infecções
Para prevenir a transmissão de doenças infecciosas devidas ao uso de medicamentos derivados de sangue ou plasma humanos, são tomadas medidas padrão que incluem:
- a seleção cuidadosa dos doadores de sangue e plasma para garantir a exclusão de doadores com risco de padecer infecções,
- a análise de cada doação e mistura de plasmas para detectar possíveis vírus ou infecções
- a inclusão de etapas no processo de fabricação para inativar/eliminar vírus.
Apesar disso, quando se administram medicamentos derivados de sangue ou plasma humano, a possibilidade de transmissão de agentes infecciosos não pode ser excluída totalmente. Isso também se refere a vírus e outros patógenos emergentes ou de natureza desconhecida.
Estes procedimentos são considerados eficazes contra vírus envoltos, como o vírus da imunodeficiência humana (VIH), o vírus da hepatite B e o da hepatite C. Os procedimentos de inativação/eliminação podem ter um valor limitado para vírus não envoltos, tais como o vírus da hepatite A ou o parvovirus B19. A infecção pelo parvovirus B19 pode ter consequências graves em mulheres grávidas (infecção fetal), e em pacientes com imunodeficiência ou com eritropoiese aumentada (por exemplo, em caso de anemia hemolítica).
Se receber tratamento crónico com medicamentos derivados de plasma humano (como os inibidores de proteasas), é recomendável que seja vacinado contra a hepatite A e B.
Recomenda-se encarecidamente que cada vez que se lhe administre Prolastina se anote o nome e o número de lote do medicamento; isso permite fazer um seguimento dos pacientes que receberam cada lote de produto.
Tabagismo
Como a eficácia de Prolastina é comprometida pela presença de fumo de tabaco nos pulmões, recomenda-se que os pacientes abandonem o hábito de fumar.
Crianças e adolescentes
Não há experiência sobre o uso de Prolastina em crianças ou adolescentes com menos de 18 anos de idade.
Outros medicamentos e Prolastina
Não são conhecidas interações entre Prolastina e outros medicamentos.
Comunique ao seu médico ou farmacêutico se está tomando, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Gravidez e amamentação
Consulte o seu médico ou farmacêutico antes de usar um medicamento.
Não se dispõe de ensaios clínicos controlados sobre o uso deste medicamento durante a gravidez. Informe o seu médico se está grávida ou acha que pode estar.
Desconhece-se se Prolastina passa para o leite materno, por isso não deve ser administrada a mulheres em período de amamentação.
Consulte o seu médico se se encontra em período de amamentação.
Condução e uso de máquinas
Não se observaram efeitos sobre a capacidade para conduzir ou utilizar máquinas.
Prolastina contémsódio
Prolastina 4000 mg contém aproximadamente 441,6 mg de sódio (componente principal do sal de mesa/para cozinhar).
Prolastina 5000 mg contém aproximadamente 552,0 mg de sódio (componente principal do sal de mesa/para cozinhar).
No caso de um paciente de 75 kg de peso corporal, a dose recomendada equivale a 24,84% da ingestão diária máxima de sódio recomendada para um adulto. Consulte o seu médico ou farmacêutico se lhe foi recomendado seguir uma dieta baixa em sal (sódio).
3. Como usar Prolastina
Após reconstituir a solução com o dissolvente incluído no envase, Prolastina deve ser administrada por perfusão intravenosa. Um médico especialista em doença pulmonar obstrutiva crónica supervisionará as primeiras perfusões com Prolastina.
Tratamento domiciliar
Depois das primeiras perfusões, um profissional de saúde também pode administrar Prolastina, mas apenas após ter recebido uma formação adequada. Se o seu médico decidir que você é apto para tal tratamento domiciliar, assegurará que seja fornecida a formação adequada ao profissional de saúde com respeito a:
- como preparar e administrar a solução reconstituída para perfusão (ver as instruções ilustradas no final deste prospecto,
- como manter o produto estéril (técnicas assépticas de perfusão),
- como realizar o registo do tratamento,
- como identificar os efeitos adversos, incluindo os sintomas das reações alérgicas e as medidas que devem ser tomadas em caso de que se manifestem tais efeitos (ver também a seção 4).
Dose
A quantidade de Prolastina que lhe é administrada baseia-se no seu peso corporal. Recomenda-se administrar uma dose semanal de 60 mg do princípio ativo por kg de peso corporal (no caso de um paciente de 75 kg de peso, esta dose equivale a 180 ml da solução reconstituída para perfusão e contém 25 mg de inibidor de alfa1-antitripsina (humana) por ml), que normalmente é suficiente para manter os níveis de proteção do inibidor de alfa1-antitripsina para evitar o agravamento do enfisema pulmonar.
O seu médico indicar-lhe-á a duração do seu tratamento, pois até à data não se estabeleceu a necessidade de limitar a duração do tratamento.
Se tiver a impressão de que o efeito de Prolastina é demasiado forte ou fraco, consulte o seu médico ou farmacêutico.
Se usar mais Prolastina do que deve
Até à data, desconhecem-se os efeitos de uma sobredose.
- Avise o seu médico ou profissional de saúde se acredita que usou mais Prolastina do que deve para que tome as medidas adequadas.
- Em caso de sobredose ou administração acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone 91 562 04 20, indicando o medicamento e a quantidade administrada.
Se esquecer de usar Prolastina
- Consulte o seu médico se a dose esquecida deve ser administrada.
- Não administre uma dose dupla para compensar a perfusão esquecida.
Se interromper o tratamento com Prolastina
Se se interromper o tratamento com Prolastina, a sua doença pode agravar-se. Consulte o seu médico imediatamente se desejar interromper o tratamento com Prolastina.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Se os efeitos adversos se apresentarem durante a perfusão de Prolastina, deverá suspender ou interromper a perfusão, dependendo da natureza e da gravidade do efeito adverso.
Possíveis efeitos adversos graves
Raramente podem ocorrer reações de hipersensibilidade(podem afetar até uma de cada 1.000 pessoas), em alguns casos muito raros, estas reações podem ocorrer como reações de anafilaxia de qualquer tipo (podem afetar até uma de cada 10.000 pessoas), embora não se tenham experimentado sintomas de alergia em perfusões anteriores.
Avise o seu médico ou enfermeiro imediatamentese observar qualquer um dos seguintes sintomas:
- erupção, sarpullido, picazón,
- dificuldade para engolir,
- inchaço na face ou na boca,
- vermelhidão,
- dificuldade para respirar (dispnéia),
- queda da pressão arterial,
- alteração do ritmo cardíaco,
- arrepios
O seu médico ou profissional de saúde decidirá se deve diminuir ou interromper a perfusão e iniciar o tratamento adequado, conforme necessário.
Em caso de tratamento domiciliar interrompa a perfusão imediatamentee entre em contacto com o seu médico ou profissional de saúde.
Durante o tratamento com Prolastina, foram observados os seguintes efeitos adversos:
Pouco frequentes (podem afetar até uma de cada 100 pessoas):
- Arrepios, febre, sintomas semelhantes aos da gripe, dor no peito.
- Sarpullido (urticária).
- Tontura, aturdimiento, dor de cabeça.
- Dificuldade para respirar (dispnéia).
- Erupções cutâneas.
- Náuseas.
- Dor nas articulações (artralgia).
Raros (podem afetar até uma de cada 1.000 pessoas):
- Reações alérgicas.
- Pulso rápido (taquicardia).
- Pressão arterial baixa (hipotensão).
- Pressão arterial alta (hipertensão).
- Dor nas costas.
Muito raros (podem afetar até uma de cada 10.000 pessoas):
- Choque anafilático.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Prolastina
Não conservar a temperatura superior a 25°C.
Não congelar.
Não refrigerar a solução após a sua reconstituição. A solução reconstituída deve ser utilizada sempre nas 3 horas seguintes à sua preparação. O produto não utilizado deve ser eliminado. Não jogue qualquer medicamento pelo esgoto nem com o lixo doméstico. Pergunte ao seu farmacêutico como pode eliminar os medicamentos que já não utilize. Estas medidas ajudarão a proteger o meio ambiente.
Mantenha fora da vista e do alcance das crianças.
Não use este medicamento após a data de validade que aparece na etiqueta do frasco e na caixa.
6. Conteúdo do envase e informação adicional
Composição de Prolastina
- O princípio ativo é alfa1-antitripsina humana (derivada de sangue ou plasma humano).
- Os demais componentes são cloreto de sódio, dihidrogénio fosfato de sódio, água para preparações injetáveis (dissolvente/diluente).
Aspecto do produto e conteúdo do envase
Alfa1-antitripsina humana é um pó de cor branca ou amarela pálida ou marrom pálida ou uma massa friável.
Uma vez reconstituída com água para preparações injetáveis, a solução deve ser entre transparente e ligeiramente opalescente, incolor, verde pálida, amarela pálida ou marrom pálida e livre de partículas visíveis.
1 ml da solução reconstituída contém 25 mg de alfa1-antitripsina humana.
Um envase individual contém:
Prolastina 4000 mg pó e dissolvente para solução para perfusão:
- 1 frasco com pó que contém 4000 mg de alfa1-antitripsina humana.
- 1 frasco com 160 ml de dissolvente (água para preparações injetáveis).
- 1 dispositivo de transferência para a reconstituição.
Prolastina 5000 mg pó e dissolvente para solução para perfusão:
- 1 frasco com pó que contém 5000 mg de alfa1-antitripsina humana.
- 1 frasco com 200 ml de dissolvente (água para preparações injetáveis).
- 1 dispositivo de transferência para a reconstituição.
Titular da autorização de comercialização e responsável pela fabricação
Titular:
Grifols Deutschland GmbH
Colmarer Straße 22
60528 Frankfurt
Alemanha
Telefone: +49 69/660 593 100
Email: [email protected]
Fabricante:
Instituto Grifols, S.A.
Can Guasch, 2 – Parets del Vallès
08150 Barcelona
Espanha
Representante Local:
Instituto Grifols, S.A.
Can Guasch, 2 - Parets del Vallès
08150 Barcelona
Espanha
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu com os seguintes nomes:
Prolastin [4000 mg/5000 mg]: Áustria, Irlanda, Itália, França, Alemanha, Grécia, Holanda, Polônia, Portugal,
Prolastina [4000 mg/5000 mg]: Dinamarca, Finlândia, Noruega, Espanha, Suécia,
Pulmolast [4000 mg/5000 mg]: Bélgica.
Data da última revisão deste prospecto: Setembro 2023.
A informação detalhada e atualizada deste medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.es/
Esta informação está destinada a profissionais de saúde e a pacientes aptos para tratamento domiciliário.
Preparação da solução reconstituída para perfusão:
- Empregue condições assépticas (limpeza e desinfecção) para manter a esterilidade. Reconstitua o medicamento em uma superfície de trabalho plana durante a preparação da solução.
- Certifique-se de que os frascos de Prolastina em pó e de dissolvente (água para preparações injetáveis estéril) estão à temperatura ambiente (20-25ºC).
- Retire a cápsula protetora tanto do frasco de Prolastina como do frasco de dissolvente e limpe os bordos do colo e os tampões com uma toalhita com álcool. Deixe que os tampões de borracha sequem.
|
|
|
|
|
|
- Se for necessário mais de um frasco de produto para alcançar a dose requerida, repita as instruções anteriores utilizando o envase adicional que contém um novo adaptador de transferência. Não reutilize o adaptador.
A dissolução total deve ser obtida em aproximadamente 15 minutos para as apresentações de 4000 mg e 5000 mg de Prolastina.
Somente devem ser utilizadas soluções entre transparentes e ligeiramente opalescentes, incolores, verde pálida, amarela pálida ou marrom pálida e livres de partículas visíveis. Prolastina não deve ser misturada com outras soluções para perfusão. A solução reconstituída deve ser usada sempre dentro de 3 horas após sua preparação.
A solução reconstituída deve ser administrada mediante perfusão intravenosa lenta, com um equipamento de perfusão (não incluído) adequado. A velocidade de perfusão deve ser inferior a 0,08 ml por kg de peso corporal por minuto (equivalente a 6 ml por minuto para um paciente de 75 kg de peso).
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃOForma farmacêutica: PERFURAÇÃO INJETÁVEL, 1000 mgSubstância ativa: alfa1 antitrypsinFabricante: Instituto Grifols S.A.Requer receita médicaForma farmacêutica: PERFURAÇÃO INJETÁVEL, 1000 mg alfa 1 antitripsinaSubstância ativa: alfa1 antitrypsinFabricante: Grifols Deutschland GmbhRequer receita médicaForma farmacêutica: PERFURAÇÃO INJETÁVEL, 5.000 mgSubstância ativa: alfa1 antitrypsinFabricante: Grifols Deutschland GmbhRequer receita médica
Alternativas a PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO em Polónia
Alternativa a PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO em Ukraine
Médicos online para PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de PROLASTINA 4.000 MG PÓ E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO – sujeita a avaliação médica e regras locais.





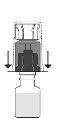 encaixe. Evite girá-lo.
encaixe. Evite girá-lo.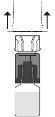
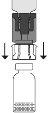 Empurre-o com o terminal transparente/branco do adaptador reto para baixo, sem girá-lo, até que a ponta perfure o tampão e encaixe.
Empurre-o com o terminal transparente/branco do adaptador reto para baixo, sem girá-lo, até que a ponta perfure o tampão e encaixe.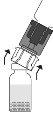 Devido ao vácuo no frasco de pó, a transferência de dissolvente se iniciará automaticamente. Espere até que se complete a transferência do dissolvente. Retire o adaptador com o frasco de dissolvente conectado em um ângulo aproximado de 45°.
Devido ao vácuo no frasco de pó, a transferência de dissolvente se iniciará automaticamente. Espere até que se complete a transferência do dissolvente. Retire o adaptador com o frasco de dissolvente conectado em um ângulo aproximado de 45°.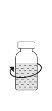 Gire suavemente o frasco de Prolastina até que o pó se dissolva completamente. Não agite para evitar a formação de espuma. Não toque o tampão. Administre o produto com uma técnica asséptica.
Gire suavemente o frasco de Prolastina até que o pó se dissolva completamente. Não agite para evitar a formação de espuma. Não toque o tampão. Administre o produto com uma técnica asséptica.









