Como usar ILUMETRI 100 mg SOLUÇÃO INJETÁVEL EM SERINGA PREENCHIDA
Introdução
Prospecto: informação para o utilizador
Ilumetri 100mg solução injetável em seringa pré-carregada
tildrakizumab
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Ilumetri e para que é utilizado
- O que precisa saber antes de começar a usar Ilumetri
- Como usar Ilumetri
- Possíveis efeitos adversos
- Conservação de Ilumetri
- Conteúdo do envase e informação adicional
1. O que é Ilumetri e para que é utilizado
Ilumetri contém o princípio ativo tildrakizumab. Tildrakizumab pertence a um grupo de medicamentos denominados inibidores de interleucinas (IL).
Este medicamento actua bloqueando a actividade de uma proteína chamada IL-23, uma substância que se encontra no organismo e participa nas respostas inflamatórias e imunitárias normais e que está presente em grandes quantidades em doenças como a psoríase.
Ilumetri é utilizado para tratar uma afecção da pele chamada psoríase em placas, em adultos com doença de moderada a grave.
O uso de Ilumetri beneficiará-o porque produz melhorias nas lesões da pele e reduz os sintomas.
2. O que precisa saber antes de começar a usar Ilumetri
Não use Ilumetri:
- Se é alérgico a tildrakizumab ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- Se tem uma infecção que o seu médico considera importante, por exemplo, tuberculose activa, que é uma doença infecciosa que afeta principalmente os pulmões.
Advertências e precauções
Consulte o seu médico, farmacêutico ou enfermeiro antes de começar a usar Ilumetri:
- Se sofre reacções alérgicas com sintomas como opressão no peito, sibilancias, inchaço da face, dos lábios ou da garganta, não se injete mais Ilumetri e contacte o seu médico de imediato.
- Se actualmente padece uma infecção ou se contrai infecções de longa duração ou de forma repetida.
- Se foi vacinado recentemente ou tem previsto vacinar-se.
Se não tem a certeza de se encontra em alguma das circunstâncias anteriores, consulte o seu médico, farmacêutico ou enfermeiro antes de utilizar Ilumetri.
Cada vez que receber um novo envase de Ilumetri, é importante que anote a data e o número do lote (que aparece no envase após “Lote”) e que guarde esta informação num local seguro.
Vigilância de infecções e reacções alérgicas
É possível que Ilumetri possa causar efeitos adversos graves, como por exemplo infecções e reacções alérgicas. Deve estar atento aos signos destas afecções enquanto utiliza Ilumetri.
Deixe de usar Ilumetri e informe o seu médico ou solicite atenção médica de imediato se observar signos que indiquem uma possível infecção grave ou uma reacção alérgica (ver secção 4. Possíveis efeitos adversos).
Crianças e adolescentes
Não se recomenda o uso de Ilumetri em crianças e adolescentes menores de 18 anos de idade, porque ainda não foi avaliado neste grupo de pacientes.
Outros medicamentos e Ilumetri
Informa o seu médico ou farmacêutico se está a utilizar, utilizou recentemente ou poderia ter que utilizar qualquer outro medicamento. Isto inclui vacinas e medicamentos imunossupressores (medicamentos que afetam o sistema imunitário).
Não devem administrar-lhe certos tipos de vacinas (vacinas de micróbios vivos) enquanto utiliza Ilumetri. Não há dados disponíveis sobre o uso simultâneo de Ilumetri e de vacinas vivas.
Gravidez, amamentação e fertilidade
É preferível evitar o uso de Ilumetri durante a gravidez. Desconhece-se os efeitos deste medicamento nas mulheres grávidas.
Se é uma mulher em idade fértil, é recomendável que não fique grávida e deve usar um método anticonceptivo eficaz enquanto receber tratamento com Ilumetri e durante um mínimo de 17 semanas após terminar o tratamento.
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Condução e uso de máquinas
A influência de Ilumetri sobre a capacidade para conduzir e utilizar máquinas é nula ou insignificante.
Ilumetri contém polissorbatos
Este medicamento contém 0,5 mg de polissorbato 80 (E 433) em cada seringa pré-carregada, equivalente a 0,5 mg/ml. Os polissorbatos podem causar reacções alérgicas. Informe o seu médico se tem alguma alergia conhecida.
3. Como usar Ilumetri
Ilumetri deve ser utilizado sob a direcção e supervisão de um médico com experiência no diagnóstico e tratamento da psoríase.
Siga exactamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte de novo o seu médico ou farmacêutico. Este medicamento é para um só uso.
A dose recomendada de Ilumetri é de 100 mg em injeção subcutânea nas semanas 0 e 4 e cada 12 semanas em diante.
Se é um paciente com carga elevada da doença ou com um peso corporal superior a 90 kg, é possível que o seu médico lhe recomende uma dose de 200 mg.
O seu médico decidirá a duração do tratamento com Ilumetri.
Depois de ter aprendido correctamente a técnica da injeção subcutânea, pode injetar Ilumetri por si mesmo se o médico considerar apropriado.
Para consultar as instruções sobre como injetar Ilumetri, leia as “Instruções de uso” que se encontram no final deste prospecto.
Consulte o seu médico quando lhe tocarão as injeções e as visitas de seguimento.
Uso em crianças e adolescentes
Não foi estabelecida ainda a segurança e eficácia de Ilumetri em crianças e adolescentes menores de 18 anos de idade, por isso não se recomenda o uso de Ilumetri em crianças e adolescentes.
Se usar mais Ilumetri do que deve
Se se administrou mais Ilumetri do que devia ou a dose se administrou antes do que indica a receita do médico, informe o seu médico.
Se esquecer de usar Ilumetri
Se se esqueceu ou se saltou uma injeção de Ilumetri, administre a dose o mais breve possível. A continuación, reinicie a administração ao intervalo habitual.
Se interromper o tratamento com Ilumetri
A decisão de interromper o tratamento com Ilumetri deve tomar-se junto com o seu médico. É possível que os seus sintomas reapareçam ao interromper o tratamento.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Efeitos adversos graves
Se notar algum dos seguintes sintomas, contacte o seu médicoimediatamente:
- Inchaço da face, dos lábios ou da garganta
- Dificuldade para respirar
Estes podem ser signos de uma reacção alérgica.
Outros efeitos adversos
A maioria dos seguintes efeitos adversos são leves. Se algum dos seguintes efeitos adversos se tornar intenso, informe o seu médico ou farmacêutico.
Muito frequentes(podem afectar mais de 1 em cada 10 pessoas)
- Infecções das vias respiratórias altas
Frequentes(podem afectar até 1 em cada 10 pessoas)
- Gastroenterite
- Náuseas
- Diarréia
- Dor na zona de injeção
- Dor de costas
- Dor de cabeça
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Ilumetri
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de caducidade que aparece na caixa e na etiqueta da seringa pré-carregada após CAD ou EXP. A data de caducidade é o último dia do mês que se indica.
Conserva o medicamento na caixa original para protegê-lo da luz. Não agite.
Conserva em frigorífico (entre 2 °C e 8 °C). Não congele.
Depois de sacar a seringa pré-carregada do frigorífico, espere 30 minutos, aproximadamente, para que a solução de Ilumetri na seringa atinja a temperatura ambiente (máximo 25 °C). Não aqueça de nenhuma outra forma.
Não utilize se o líquido contém partículas visíveis, está turvo ou é claramente castanho.
Uma vez sacado do frigorífico, não conserve tildrakizumab a mais de 25 °C nem o refrigere de novo.
No espaço provido na caixa exterior, anote a data em que sacou o medicamento do frigorífico e a data de eliminação que corresponda. Utilize a seringa antes de que tenham decorrido 30 dias desde que a sacou do frigorífico ou antes de que atinja a data de caducidade, o que ocorrer primeiro.
Os medicamentos não devem ser deitados por os desgoues nem para a lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Ilumetri
- O princípio ativo é tildrakizumab. Cada seringa precarregada contém 100 mg de tildrakizumab.
- Os outros componentes são L-histidina, hidrocloruro de L-histidina monohidrato, polissorbato 80 (E 433), sacarose e água para preparações injetáveis.
Aspecto deIlumetrie conteúdo do envase
Ilumetri 100 mg solução injetável (injeção) em seringa precarregada é uma solução transparente ou ligeiramente opalescente, entre incolora e ligeiramente amarela.
Ilumetri 100 mg solução injetável (injeção) em seringa precarregada está disponível em envases unitários com 1 seringa precarregada e em envases com 2 seringas precarregadas.
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Titular da autorização de comercialização
Almirall, S.A.
Ronda General Mitre, 151
08022 Barcelona, Espanha
Responsável pela fabricação
SUN Pharmaceuticals Industries (Europe) B.V.
Polarisavenue 87
2132JH Hoofddorp, Países Baixos
Indústrias Farmacêuticas Almirall, S.A.
Ctra. de Martorell 41-61
08740 Sant Andreu de la Barca, Barcelona, Espanha
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Bélgica/Bélgica/Bélgica/ Luxemburgo/Luxemburgo Almirall N.V. Tel: +32 (0)2 771 86 37 | Itália Almirall SpA Tel: +39 02 346181 |
Estônia/Grécia/ Espanha/ Croácia/ Chipre/Letônia/Lituânia/ Hungria/ Malta/ Romênia/ Eslovênia Almirall, S.A. Tel: +34 93 291 30 00 | Países Baixos Almirall B.V. Tel: +31 (0)30 711 15 10 |
República Tcheca/República Eslovaca Almirall s.r.o Tel: +420 739 686 638 | |
Dinamarca/ Noruega/ Suécia Almirall ApS Tel: +45 70 25 75 75 | Áustria Almirall GmbH Tel: +43 (0)1/595 39 60 |
Alemanha Almirall Hermal GmbH Tel: +49 (0)40 72704-0 | Polônia Almirall Sp.z o. o. Tel.: +48 22 330 02 57 |
França Almirall SAS Tel: +33(0)1 46 46 19 20 | Portugal Amgen Biofarmacêutica, Lda. Tel: +351 21 4220606 |
Irlanda Almirall, S.A. Tel: +353 1800 849322 | Finlândia Orion Pharma Tel: +358 10 4261 |
Islândia Vistor hf. Tel: +354 535 70 00 |
Data da última revisão deste prospecto: 06/2024
Outras fontes de informação
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos https://www.ema.europa.eu/.
INSTRUÇÕES DE USO
Antes de usar as seringas precarregadas:
Pontos importantes que você deve conhecer
- Antes de usar as seringas precarregadas de Ilumetri, leia e siga atentamente todas as instruções passo a passo. Guarde as instruções de uso e consulte-as quando necessário.
- As seringas precarregadas não devem ser agitadas.
- Leia o prospecto de Ilumetri para obter mais informações sobre o medicamento.
DESCRIÇÃO DO PRODUTO
A seringa precarregada de Ilumetri tem este aspecto:
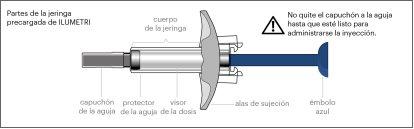
PREPARAÇÃO
- Saia do envase da geladeira (se o conservar na geladeira)
- Certifique-se de que a dose da seringa corresponde à prescrita pelo seu médico.
- Para uma dose de 100 mg, é necessária uma seringa, e para uma dose de 200 mg, duas seringas.
- Saia da geladeira a caixa e coloque-a sem abrir em uma superfície de trabalho limpa e plana.
- Espera 30 minutos (se o conservar na geladeira)
- Deixe a seringa precarregada na caixa exterior (com a tampa fechada) à temperatura ambiente durante 30 minutos.
- Inspeccione o medicamento
- Saia a seringa precarregada da caixa quando estiver pronto para a injeção.
- Verifique a data de validade que figura na caixa de cartão e na seringa precarregada e descarte-a se a data já tiver passado.
- NÃO remova o capuchão da agulha até que esteja pronto para administrar a injeção.
- Antes da administração de Ilumetri, inspecione-o visualmente para detectar a presença de partículas e um cambio de cor.
- Ilumetri é uma solução transparente ou ligeiramente opalescente, entre incolora e ligeiramente amarela.
- NÃO o utilize se o líquido contiver partículas visíveis ou se a seringa estiver danificada. É possível que haja bolhas de ar; não há necessidade de eliminá-las.
- NÃO utilize o produto se ele tiver caído sobre uma superfície dura ou estiver danificado.
- Reúna todos os materiais que você precisa
- Sobre uma superfície de trabalho limpa e bem iluminada, coloque o seguinte:
- comprimidos impregnados em álcool
- bolita de algodão ou gaze
- curativo
- recipiente para descartar objetos cortantes
- Lave as mãos
- Lave bem as mãos com água e sabão.
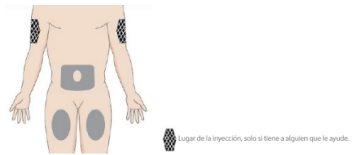
- Escolha o local da injeção
- Escolha um local para administrar a injeção onde a pele esteja saudável e seja de fácil acesso, como por exemplo o abdômen, os quadris ou a parte superior do braço.
- NÃO administre a injeção nos 5 cm ao redor do umbigo nem em zonas de pele com sensibilidade, hematomas, enrubescimento anormal, endurecimento ou lesões de psoríase.
- NÃO injete em cicatrizes, estrias nem vasos sanguíneos.
- A parte superior do braço só é adequada se a injeção for administrada por outra pessoa.
- Alterne os locais de injeção em cada administração.
- Em caso de que a sua dose seja de 200 mg (2 seringas precarregadas de 100 mg), escolha um local diferente para a segunda injeção.
- Limpe o local da injeção
- Limpe o local da injeção com um comprimido impregnado em álcool e deixe que a pele seque.
- Não toque esta zona novamente antes de administrar a injeção.
INJEÇÃO
Se a sua dose for de 200 mg, você precisará usar 2 seringas precarregadas cada vez que administrar o medicamento.
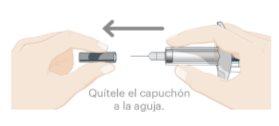
- Remova o capuchão da agulha
- Enquanto segura o corpo da seringa precarregada, remova o capuchão da agulha como mostrado e descarte-o. É possível que você veja 1 ou 2 gotas de líquido, é normal.
- NÃO toque no êmbolo azul ainda.
- NÃO utilize o produto se a seringa precarregada ou a agulha estiverem dobradas.
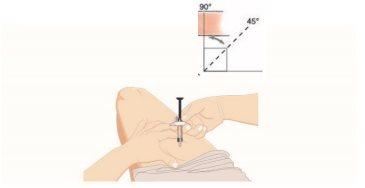
- Pellizque a pele e insira a agulha
- Pellizque suavemente a pele no local da injeção escolhido.
- Insira toda a agulha na pele que está pellizcada entre os dedos, em um ângulo de 45 a 90graus.
- NÃO coloque o dedo no êmbolo enquanto está inserindo a agulha.
- Segure firmemente a seringa precarregada.
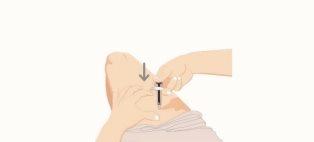
- Administre a injeção
- Uma vez inserida a agulha, solte suavemente a pele.
- Empurre o êmbolo azul para baixo até que chegue ao topo. Dessa forma, é ativado um mecanismo de segurança que garante a total retracção da agulha uma vez administrada a injeção.
- Se o êmbolo azul chegar ao topo, não pode mais se mover e não há derramamento, uma dose completa foi administrada.
- Remova a seringa utilizada
- Remova completamente a agulha da pele antes de soltar o êmbolo azul.
- Depois de soltar o êmbolo azul, o bloqueio de segurança atrairá a agulha para o protetor da agulha.
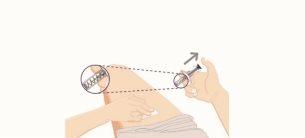
- Descarte a seringa utilizada em um recipiente para descartar objetos cortantes de forma imediata após o uso e antes de injetar uma segunda seringa, se necessário.
- Se houver algum líquido residual ou um pouco de sangue, limpe o local da injeção com uma bolita de algodão ou uma gaze enquanto aplica pressão. Se considerar necessário, pode usar um curativo para cobrir a zona de injeção.
- Repita o procedimento com a segunda seringa em uma zona de pele diferente se for administrar uma dose de 200 mg.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ILUMETRI 100 mg SOLUÇÃO INJETÁVEL EM SERINGA PREENCHIDAForma farmacêutica: INJETÁVEL, 100 mgSubstância ativa: tildrakizumabFabricante: Almirall S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 100 mgSubstância ativa: tildrakizumabFabricante: Almirall S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 200 mgSubstância ativa: tildrakizumabFabricante: Almirall S.A.Requer receita médica
Médicos online para ILUMETRI 100 mg SOLUÇÃO INJETÁVEL EM SERINGA PREENCHIDA
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ILUMETRI 100 mg SOLUÇÃO INJETÁVEL EM SERINGA PREENCHIDA – sujeita a avaliação médica e regras locais.