
CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEA

Pergunte a um médico sobre a prescrição de CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEA

Como usar CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEA
Introdução
Prospecto: informação para o utilizador
Cutaquig 165mg/mlsolução para injeção subcutânea
Inmunoglobulina normal humana (IgSC)
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Cutaquig e para que se utiliza
- O que necessita saber antes de começar a usar Cutaquig
- Como usar Cutaquig
- Posíveis efeitos adversos
- Conservação de Cutaquig
- Conteúdo do envase e informação adicional
1. O que é Cutaquig e para que se utiliza
O que é Cutaquig
Cutaquig pertence a uma classe de medicamentos chamados «inmunoglobulinas normais humanas». As inmunoglobulinas também são conhecidas como anticorpos e são proteínas que se encontram no sangue de pessoas saudáveis. Os anticorpos fazem parte do sistema imunitário (as defesas naturais do organismo) e ajudam o seu corpo a combater as infecções.
Como funciona Cutaquig
Cutaquig contém inmunoglobulinas que foram preparadas a partir de sangue de pessoas saudáveis. O medicamento funciona exatamente da mesma forma que as inmunoglobulinas que se encontram de forma natural no seu sangue.
Para que se usa Cutaquig
Cutaquig se utiliza em pacientes que não têm suficientes anticorpos para combater as infecções e, por tanto, tendem a sofrer infecções frequentes. A administração regular de doses suficientes de Cutaquig pode aumentar os níveis de inmunoglobulinas anormalmente baixos do seu sangue até uns níveis normais (tratamento de restituição).
Cutaquig se prescreve a adultos e crianças (de idades entre 0 e 18 anos) nas seguintes situações:
Tratamento de pacientes que nasceram com uma menor capacidade ou com uma incapacidade para produzir anticorpos (imunodeficiência primária).
Pacientes com deficiência adquirida de anticorpos (imunodeficiência secundária) devido a doenças e/ou tratamentos específicos e que experimentam infecções graves ou recorrentes.
2. O que necessita saber antes de começar a usar Cutaquig
Não use Cutaquig:
- se é alérgico à inmunoglobulina normal humana ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
NÃO injete Cutaquig em um vaso sanguíneo.
Advertências e precauções:
Consulte o seu médico ou farmacêutico antes de começar a usar Cutaquig.
Pode que, sem saber, seja alérgico (hipersensível) às inmunoglobulinas.
As reações alérgicas verdadeiras, como a queda repentina da tensão arterial ou o choque anafilático (uma queda brusca da tensão arterial com outros sintomas como inchação da garganta, dificuldade para respirar e erupção cutânea) são pouco frequentes, mas se podem produzir de maneira ocasional, mesmo se recebeu inmunoglobulinas humanas com anterioridade e as tolerou bem. Se podem produzir especialmente se não tem suficiente quantidade de inmunoglobulina tipo A (IgA) no sangue (deficiência de IgA) e tem anticorpos contra a IgA.
- Informa ao seu médico ou profissional de saúde antes do tratamento para saber se tem uma deficiência de inmunoglobulina tipo A (IgA). Cutaquig contém quantidades residuais de IgA que poderiam causar uma reação alérgica.
Nestes casos pouco frequentes, se podem produzir reações alérgicas, como uma queda repentina da tensão arterial ou um choque (ver também a seção 4).
Os sinais e sintomas dessas reações alérgicas pouco frequentes incluem
- Sensação de desvanecimento, tontura ou fraqueza
- Erupção cutânea e picazón, inchação da boca ou garganta, dificuldade para respirar, sibilancias
- Ritmo cardíaco anómalo, dor no peito, coloração azulada dos lábios ou dos dedos de mãos e pés
- Visão borrosa
Se observa esses sinais durante a perfusão de Cutaquig, informe ao seu médico de imediato.
Ele ou ela decidirá se diminui a velocidade da perfusão ou se a detém por completo.
- Informa ao seu médico se tem antecedentes de doença cardíaca ou doença dos vasos sanguíneos, ou coágulos sanguíneos, sangue espessa ou se esteve imóvel durante algum tempo. Estas coisas podem aumentar o seu risco de ter um coágulo de sangue após usar Cutaquig. Além disso, comunique ao seu médico quais medicamentos está usando, porque alguns medicamentos, como os que contêm estrógenos (por exemplo, as píldoras anticonceptivas), podem aumentar o seu risco de desenvolver um coágulo de sangue. Põe-se em contacto com o seu médico imediatamente se, após receber Cutaquig, experimenta sinais e sintomas como respiração difícil, dor no peito, dor e inchação de uma extremidade, fraqueza ou entorpecimento em um lado do corpo.
- Põs-se em contacto com o seu médico se, após receber Cutaquig, experimenta os seguintes sinais e sintomas: dor de cabeça intensa, rigidez no pescoço, sonolência, febre, fotofobia, náuseas e vómitos. Estes poderiam ser sinais de meningite asséptica. O seu médico decidirá se são necessários mais análises e se se deve continuar com Cutaquig.
- Cutaquig contém anticorpos do grupo sanguíneo que podem causar a destruição dos glóbulos vermelhos e, por lo tanto, anemia (número baixo de glóbulos vermelhos).
O seu profissional de saúde evitará possíveis complicações assegurando-se:
- de que o senhor não é sensível à inmunoglobulina normal humana
O medicamento deve ser perfundido lentamente no início. Deve-se seguir estreitamente a velocidade de perfusão recomendada que se indica na seção 3.
- de que se lhe controla cuidadosamente para detectar qualquer sintoma durante o período de perfusão, especialmente se:
- Recebe inmunoglobulina humana normal pela primeira vez
- Tem mudado de um medicamento diferente para Cutaquig
- Tem transcorrido um longo intervalo de tempo (mais de oito semanas) desde a última perfusão
Nestes casos, se recomenda que se lhe vigie durante a primeira perfusão e durante uma hora após. Se os pontos anteriores não se aplicam no seu caso, se recomenda que o observem durante, pelo menos, 20 minutos após a administração.
Crianças e adolescentes
As advertências e precauções enumeradas se aplicam tanto a adultos como a crianças.
Uso de Cutaquig com outros medicamentos
- Informa ao seu médico ou farmacêutico se está utilizando, utilizou recentemente ou pudesse ter que utilizar qualquer outro medicamento.
- Não deve misturar Cutaquig com qualquer outro medicamento.
- Antes da vacinação, informa ao médico encarregado de vaciná-lo sobre o seu tratamento com Cutaquig. Cutaquig (como todas as soluções de inmunoglobulina normal humana) pode interferir com o efeito de algumas vacinas de vírus vivos como o sarampo, a rubéola, as paperas ou a varicela. Por lo tanto, após receber Cutaquig, é possível que deba esperar até 3 meses antes de receber a sua vacina atenuada. No caso da vacinação contra o sarampo, esta circunstância pode persistir durante um ano.
- Prova de glicose no sangue
Alguns tipos de sistemas de análise de glicose no sangue (denominados glicómetros) interpretam de forma errónea a maltose contida em Cutaquig como glicose. Isto pode provocar leituras elevadas de glicose falsas durante uma perfusão ou um período de cerca de 15 horas após finalizar a perfusão e, como consequência, a inapropriada administração de insulina, dando lugar a uma hipoglicemia (ou seja, o descenso do nível de açúcar no sangue) que poderia provocar a morte. Do mesmo modo, os casos de hipoglicemia autêntica podem não ser tratados, se o estado hipoglicémico for mascarado por falsas leituras elevadas de glicose.
Como consequência, ao administrar Cutaquig ou outros produtos que contenham maltose, a medição da glicose no sangue deve ser realizada com um sistema de análise que utilize um método específico para a glicose. Os sistemas baseados nos métodos da glicose desidrogenase pirroloquinolinaquinona (GDH PQQ) ou a glicose-corante-oxidorredutase não devem ser utilizados.
Deve revisar-se detenidamente a informação do produto do sistema de análise de glicose no sangue, incluindo a das tiras reativas, para determinar se o sistema é apropriado para utilizar com produtos parenterais que contenham maltose. Em caso de dúvida, consulte o médico que o está tratando para determinar se o sistema de análise de glicose que está utilizando é apropriado para utilizar com produtos parenterais que contenham maltose.
Uso de Cutaquig com alimentos, bebidas e álcool
Não se observaram efeitos.
Gravidez, lactação e fertilidade
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico ou farmacêutico antes de utilizar este medicamento. Este produto só deve ser utilizado durante a gravidez ou a lactação após consultar o seu médico ou farmacêutico.
Não se realizaram estudos clínicos com Cutaquig em mulheres grávidas. No entanto, os medicamentos que contêm inmunoglobulinas se têm utilizado em mulheres grávidas e em período de lactação durante anos, e não se observaram efeitos nocivos no desenvolvimento da gravidez nem no bebê.
Se está amamentando e recebe Cutaquig, as inmunoglobulinas do medicamento também se podem encontrar no leite materno. Por lo tanto, o seu bebê pode estar protegido de certas infecções.
A experiência com as inmunoglobulinas sugere que não se esperam efeitos nocivos sobre a fertilidade.
Condução e uso de máquinas
A capacidade para conduzir e utilizar máquinas pode ser afetada por algumas reações adversas associadas a Cutaquig. Os pacientes que experimentem reações adversas durante o tratamento devem esperar a que se resolvam antes de conduzir ou utilizar máquinas.
Cutaquig contém Sódio
Este medicamento contém 33,1 mg de sódio (componente principal da sal de mesa/para cozinhar) por frasco de 48 ml e 13,8 mg por frasco de 20 ml. Isto equivale ao 1,7 % e 0,7 % respectivamente da ingestão diária máxima recomendada de sódio para um adulto.
Informação sobre a composição de Cutaquig
Cutaquig é feito de plasma sanguíneo humano (esta é a parte líquida do sangue). Quando os medicamentos são feitos de sangue ou plasma humanos, se aplicam certas medidas para evitar que as infecções se transmitam aos pacientes. Estas incluem:
- seleção cuidadosa dos doadores de sangue e plasma para garantir que se exclua os que correm risco de ser portadores de infecções,
- análise de cada doação e dos grupos de plasma para detectar sinais de vírus/infecções,
- a inclusão de passos no processamento do sangue ou do plasma que podem desativar ou eliminar vírus.
Apesar destas medidas, quando se administram medicamentos preparados a partir de sangue ou plasma humano, não se pode excluir totalmente a possibilidade de transmitir uma infecção. Isto também se aplica a qualquer vírus desconhecido ou emergente ou outros tipos de infecções.
As medidas tomadas se consideram eficazes contra vírus com envoltura, como o vírus de imunodeficiência humana (VIH, o vírus que causa a SIDA), o vírus da hepatite B e o vírus da hepatite C.
As medidas tomadas podem ter um valor limitado contra vírus sem envoltura, como o vírus da hepatite A e o parvovirus B19.
As inmunoglobulinas não se têm associado a infecções por hepatite A ou parvovirus B19, talvez porque os anticorpos contra estas infecções, que se encontram contidos no produto, são protectores.
Recomenda-se encarecidamente que cada vez que receba uma dose de Cutaquig, se registrem o nome e o número de lote do medicamento para manter um registo dos lotes utilizados (consulte também o Anexo I: Directrizes sobre a administração).
3. Como usar Cutaquig
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte de novo o seu médico ou farmacêutico.
Cutaquig deve ser administrado por baixo da pele (administração subcutânea ou s.c.).
O tratamento será iniciado pelo seu médico ou enfermeiro com experiência no tratamento de pacientes com um sistema imunitário débil.
Uma vez que o médico/enfermeiro tenha encontrado a dose e a velocidade de perfusão adequadas para si e uma vez que tenha recebido as primeiras perfusões sob supervisão, pode ser permitido que o senhor se administre o tratamento em sua casa ou que o seu cuidador (capacitado) o administre. O seu médico ou enfermeiro com experiência em guiar os pacientes no tratamento domiciliário, se assegurará de que o senhor ou o seu cuidador recebam formação e informação precisa sobre
- a técnica de perfusão sem germes (asséptica)
- o uso do dispositivo de perfusão (se necessário)
- o manutenção de um diário de tratamento
- o que medidas tomar em caso de efeitos adversos graves (consulte também a seção 4).
Assim que possa tratar-se a si mesmo, e se não têm aparecido efeitos adversos durante o tratamento, é possível que o seu médico lhe permita continuar o tratamento em casa.
Posologia
O seu médico determinará a sua dose individual e a velocidade de perfusão, e adaptará a dose especialmente para si, tendo em conta o seu peso, qualquer tratamento anterior que tenha recebido e a sua resposta ao tratamento. Siga sempre as instruções do seu médico.
Tratamento de restituição em síndromes de imunodeficiência primária:
O seu médico determinará se necessita de uma dose de carga (para adultos e crianças) de pelo menos 1,2 a 3,0 ml/kg de peso corporal dividida em vários dias. Após isso, receberá Cutaquig de forma regular, desde diariamente até cada duas semanas. A dose acumulada por mês será de aproximadamente 2,4 a 4,8 ml/kg de peso corporal. O seu profissional de saúde pode ajustar a sua dose dependendo da sua resposta ao tratamento.
Tratamento de restituição em imunodeficiências secundárias:
A dose recomendada de Cutaquig é uma dose mensal acumulada de 1,2 – 2,4 ml/kg administrada a intervalos repetidos (aproximadamente uma vez por semana). Pode ser necessário injetar cada dose individual em diferentes locais anatómicos. O seu profissional de saúde pode ajustar a dose em função da sua resposta ao tratamento.
Não mude a dose ou o intervalo de administração sem consultar o seu médico. Se acredita que deve receber Cutaquig com maior ou menor frequência, fale com o seu médico. Se acredita que esqueceu uma dose, fale com o seu médico o mais rápido possível.
Forma e via de administração
Seleção do(s) local(is) das perfusões:
As zonas recomendadas para a perfusão subcutânea de Cutaquig são o abdômen, os músculos da coxa, a parte superior dos braços ou a zona superior da perna/quadris. Podem ser usados múltiplos locais para as perfusões subcutâneas ao mesmo tempo. O número de locais de perfusão é ilimitado, mas estes devem ter uma separação de pelo menos 5 cm. Rote os locais com cada administração segundo o recomende o seu médico ou enfermeiro.
A quantidade perfundida por local é variável, mas se recomenda dividir grandes volumes de perfusão (>30 ml) e realizar a perfusão em vários locais. Em lactentes e crianças, os locais de perfusão podem mudar cada 5 a 15 ml.
Velocidade de perfusão:
O seu médico determinará a velocidade de perfusão adequada para si tendo em conta a sua dose individual, a frequência de dosagem e a tolerabilidade do produto.
A velocidade de perfusão inicial recomendada é de 15 ml/h/local se não recebeu antes tratamento com IGSC. Se já está em tratamento com IGSC e vai mudar para Cutaquig, se recomenda utilizar as velocidades de administração empregadas anteriormente para as perfusões iniciais. Para as perfusões posteriores, se se tolera bem, pode aumentar gradualmente a velocidade de perfusão em aproximadamente 10 ml/h/local cada 2-4 semanas em adultos (≥ 40 kg) e em até 10 ml/h/local cada 4 semanas em pacientes pediátricos (<40 kg).< p>
A partir de então, se tolera as perfusões iniciais à dose completa por local e à velocidade máxima, pode considerar um aumento da velocidade de perfusão para as perfusões subsequentes até alcançar um fluxo máximo de 67,5 ml/h/local para adultos (≥ 40 kg) e 25 ml/h/local para pacientes pediátricos (<40 kg).< p>
A seguir se proporcionam as instruções detalhadas para o uso.
Cutaquig está destinado apenas para a administração subcutânea (por baixo da pele). Não injete em um vaso sanguíneo.
Use Cutaquig apenas em casa quando o seu profissional de saúde lhe tenha ensinado e capacitado adequadamente.
Siga passo a passo as instruções de administração que se encontram no final do prospecto (Anexo I) e utilize uma técnica asséptica/estéril ao administrar Cutaquig.
Ao preparar a perfusão use luvas, se lhe indicaram que o faça.
Uso em crianças e adolescentes
Para crianças e adolescentes (de 0 a 18 anos) se aplicam as mesmas indicações, doses e frequência de perfusão que em adultos.
Se usa mais Cutaquig do que deve
Se pensa que se perfundiu demasiado Cutaquig, ponha-se em contacto com o seu profissional de saúde o mais rápido possível.
Se esqueceu de usar Cutaquig
Se esqueceu de uma dose, informe disso ao seu médico ou profissional de saúde tão rápido quanto possível. Não se perfunda uma dose dupla de Cutaquig para compensar a dose esquecida.
4. Possíveis efeitos adversos
Tal como todos os medicamentos, este medicamento pode produzir efeitos adversos, como arrepios, dor de cabeça, tonturas, febre, vómitos, reacções alérgicas, náuseas, dor nas articulações, tensão arterial baixa e dor moderada na parte baixa das costas, embora nem todas as pessoas os sofram.
Certos efeitos adversos, como dor de cabeça, arrepios ou dores corporais, podem reduzir-se ao diminuir a velocidade de perfusão.
Não se observaram reacções adversas graves relacionadas com os medicamentos nos sujeitos tratados com Cutaquig durante os estudos clínicos que avaliaram a sua segurança.
Pode ser que seja alérgico (hipersensível) às imunoglobulinas e se podem produzir reacções alérgicas, como uma queda repentina da tensão arterial e, em casos isolados, choque. Os médicos são conscientes destes possíveis efeitos adversos e o vigiarão durante e após as perfusões iniciais.
Informa ao seu médico imediatamente se observa algum dos seguintes sintomas:
- Sensação de desvanecimento, tontura ou fraqueza
- Erupção cutânea e picazón, inchação da boca ou garganta, dificuldade para respirar, sibilancias
- Ritmo cardíaco anómalo, dor no peito, coloração azulada dos lábios ou dos dedos das mãos e pés
- Visão borrosa
Quando usar Cutaquig em sua casa, pode realizar a perfusão na presença do seu cuidador, que o ajudará a observar os sinais de uma reação alérgica. Em caso de qualquer sintoma de uma reação alérgica, detenha a perfusão e busque ajuda se necessário.
Consulte também a seção 2 deste prospecto acerca do risco de reacções alérgicas.
Os seguintes efeitos adversos são muito frequentes (podem afectar a mais de 1 de cada 10 perfusões):
- Reacções no local da injeção, como vermelhidão, inchação, picazón e malestar.
Os seguintes efeitos adversos são pouco frequentes (podem afectar entre mais de 1 de cada 1.000 e menos de 1 de cada 100 perfusões):
- Dor de cabeça
- GANAS de vomitar
- Cansaço
Os seguintes efeitos adversos são raros (podem afectar a mais de 1 em 10.000 perfusões):
- Tonturas
- Dor abdominal
- Distensão abdominal
- Vómitos
- Arcadas
- Dor muscular
- Dor nas articulações
- Febre
- Arrepios
- Malestar no peito
- Doença semelhante à gripe
- Dor
- Sensação de malestar geral
- Análise de sangue positivos para anticorpos
- Resultados irregulares nos análises de sangue que mostram a destruição dos glóbulos vermelhos
- Aumento da hemoglobina
- Aumento da creatinina no sangue
- Erupção
- Reacções na pele
- Níveis elevados de certas enzimas do fígado chamadas transaminases
Outros efeitos adversos que não se produziram nos estudos clínicos, mas que também se têm notificado, são:
- Hipersensibilidade (por exemplo, eritema, urticária)
- Aumento da tensão arterial
- Problemas devidos à formação de coágulos sanguíneos nos vasos sanguíneos (por exemplo, trombose venosa profunda, acidente vascular cerebral)
- Coágulos nos vasos sanguíneos (consulte também a seção 2 “Advertências e precauções”)
- Picazón
- Dor nas costas
Efeitos adversos observados com medicamentos semelhantes
Se têm observado os seguintes efeitos adversos adicionais com a perfusão de imunoglobulina normal humana subcutânea. É possível que alguém que use este medicamento possa experimentá-los.
- Palidez
- Arrepios
- Diarréia
- Dor no local da injeção
- Verdelhidão rápida do pescoço/rosto
- Sensação de calor
- Sensação de frio
- Fraqueza
- Opresão na garganta
- Dificuldade para respirar
- Sintomas semelhantes ao asma
- Tosse
- Inchação do rosto
- Um síndroma chamado meningite asséptica (consulte também a seção 2 “Advertências e precauções”)
Informa ao seu médico imediatamente se apresenta algum dos seguintes sintomas. Podem ser sinais de um problema grave.
- Dor de cabeça intensa com náuseas, vómitos, rigidez do pescoço, febre e sensibilidade à luz. Estes podem ser sinais de uma inflamação não infecciosa, temporária e reversível das membranas que rodeiam o cérebro e a medula espinhal (meningite).
- Dor, inchação, calor, vermelhidão, ou presença de um bulto nas pernas ou nos braços, respiração difícil inexplicável, dor no peito ou malestar que piora com a respiração profunda, pulso rápido inexplicável, entorpecimento ou fraqueza de um lado do corpo, confusão repentina ou problemas para falar. Estes podem ser sinais de um coágulo de sangue.
Podem ocorrer efeitos adversos como estes mesmo quando tenha recebido imunoglobulina humana anteriormente e a tenha tolerado bem.
Consulte também a seção 2 para obter informações adicionais sobre as circunstâncias que aumentam o risco de efeitos adversos.
Comunicação de efeitos adversos
Se experimenta qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano: www.notificaRAM.es
Ao comunicar efeitos adversos, pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Cutaquig
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que figura na etiqueta e no invólucro após CAD. A data de validade é o último dia do mês que se indica.
Conservar em frigorífico (2 °C – 8 °C). Não congelar. Conservar o frasco no invólucro exterior para protegê-lo da luz.
Dentro do seu período de validade, o produto pode ser conservado a temperatura ambiente (não conservar a mais de 25 °C) até um máximo de 9 meses, sem refrigerar novamente durante este período, e deve ser deitado fora se não for utilizado após este período.
Após a primeira abertura, o produto deve ser utilizado imediatamente.
Não use Cutaquig se a solução estiver turva ou contiver partículas.
Os medicamentos não devem ser deitados fora pelos esgotos nem para o lixo. Pergunte ao seu farmacêutico como deitar fora os invólucros e os medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do invólucro e informações adicionais
Composição de Cutaquig
O princípio ativo é imunoglobulina normal humana 165 mg/ml (pelo menos 95 % é imunoglobulina G)
- IgG1 ……….. 71 %
- IgG2 ……….. 25 %
- IgG3 ……….. 3 %
- IgG4 ……….. 2 %
Os outros excipientes são maltose, polissorbato 80 e água para preparações injetáveis.
O conteúdo máximo de IgA é de 300 microgramas/ml
Cutaquig contém ≤30 mmol/l de sódio
Aspecto do produto e conteúdo do invólucro
Cutaquig é uma solução injetável.
A solução é transparente e incolor.
Durante a conservação, o líquido pode tornar-se ligeiramente opalescente e amarelo pálido.
Cutaquig está disponível como:
6, 10, 12, 20, 24 ou 48 ml de solução em um frasco (vidro tipo I) com um tampão de borracha de bromobutilo: tamanho do invólucro de 1, 10 ou 20 frascos
Pode ser que apenas alguns tamanhos de invólucros estejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização:
Octapharma, S.A.
Av. Castilla, 2 (P.E. San Fernando)
Ed. Dublín - 2ª Planta
28830 San Fernando de Henares
Madrid
Espanha
Fabricantes:
Octapharma Pharmazeutika Produktionsges.m.b.H.
Oberlaaer Strasse 235
1100 Viena
Áustria
Octapharma AB Lars Forssells gata 23 112 75 Estocolmo Suécia
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu com os seguintes nomes:
Alemanha, Áustria, Bélgica, Bulgária, Croácia, Dinamarca, Eslováquia, Eslovénia, Espanha, Estónia, Finlândia, França, Hungria, Irlanda, Islândia, Itália, Letónia, Lituânia, Luxemburgo, Malta, Noruega, Países Baixos, Polónia, Portugal, Reino Unido (Irlanda do Norte), República Checa, Roménia, Suécia: | Cutaquig® |
Data da última revisão deste prospecto: 11/2023.
Anexo I: Directrizes sobre a administração
- Preparar o número necessário de frascos de Cutaquig
- Se estiver armazenado em frigorífico, coloque os frascos a temperatura ambiente pelo menos 90 minutos antes da perfusão.
- Não aqueça os frascos nem os coloque no micro-ondas.
- Não agite os frascos para evitar a formação de espuma.
- Preparar-se para a perfusão
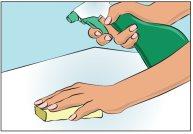 Escolha e prepare uma área de trabalho limpa com toalhetes antisépticos ou solução desinfectante (Figura 1).
Escolha e prepare uma área de trabalho limpa com toalhetes antisépticos ou solução desinfectante (Figura 1).

- Reúna o seu equipamento de perfusão:
- Bomba de perfusão (opcional) e seringa(s) compatível(s)
- Agulha (para extrair o produto do frasco)
- Conjunto de perfusão
- Tubo de perfusão e conector em Y (se necessário)
- Álcool e toalhetes com álcool/toalhetes antisépticos
- Gaze ou adesivo transparente e fita adesiva
- Recipiente para objetos cortantes
- Diário e caneta de tratamento
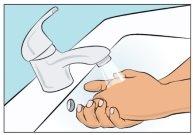
- Lave bem as mãos e deixe-as secar (Figura 2). Use gel desinfectante como lhe foi mostrado durante a formação.
- Se necessário, programe a bomba de acordo com o manual do usuário e como o seu profissional de saúde lhe mostrou durante a formação.
- Verificar e abrir os frascos
- Inspeccione cuidadosamente cada frasco para:
- Corrigir a dose etiquetada de acordo com a sua receita.
- Verificar o aspecto da solução (deve ser transparente e incolor a amarelo pálido ou marrom claro).
- Certificar-se de que a tampa protectora não está quebrada nem falta.
- Verificar a data de validade e o número do lote.
- Não use a solução se estiver turva ou contiver partículas.
- Retire a cápsula de fecho protectora.
- Desinfete o tampão de borracha com um pano antiséptico e deixe-o secar (Figura 3).


- Preparar e encher a seringa
- Abra a seringa e a agulha estéreis.
- Conecte a agulha à seringa enroscando-a.
- Puxe o êmbolo para encher a seringa com ar que deve ser aproximadamente igual à quantidade de solução necessária do frasco.
- Insira a agulha no frasco e coloque o frasco boca abaixo. Injete ar: certifique-se de que a ponta da agulha não esteja dentro da solução para evitar a formação de espuma.
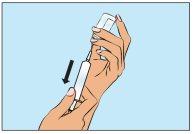 A seguir, certificando-se de que a agulha permaneça sempre na solução, extraia lentamente o Cutaquig (Figura 4).
A seguir, certificando-se de que a agulha permaneça sempre na solução, extraia lentamente o Cutaquig (Figura 4).

- Retire a agulha do frasco.
- É possível que este procedimento deva ser repetido se precisar de vários frascos para a dose calculada.
- Quando terminar, retire a agulha e coloque-a imediatamente no recipiente para objetos cortantes.
- Continue imediatamente com o próximo passo, pois a solução de IgG deve ser usada imediatamente.
- Preparar a bomba de perfusão e o tubo (opcional)
- Siga as instruções do fabricante para preparar a bomba de perfusão.
- Para carregar o tubo de administração, coloque a seringa cheia no tubo de perfusão e pressione suavemente o êmbolo para encher o tubo com Cutaquig e para eliminar todo o ar. (Figura 5).
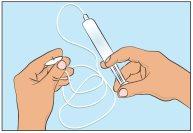

- Decidir os sítios de perfusão e inserir a(s) agulha(s) de perfusão
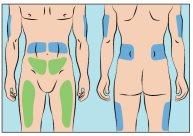 Cutaquig pode ser perfundido nas seguintes zonas: abdômen, coxa, parte superior do braço e/ou parte superior da perna/zona da anca (Figura 6).
Cutaquig pode ser perfundido nas seguintes zonas: abdômen, coxa, parte superior do braço e/ou parte superior da perna/zona da anca (Figura 6).

- Os sítios de perfusão devem ter uma separação de pelo menos 5 cm.
- Use diferentes sítios de perfusão aos que usou para a administração anterior.
- Evite inserir a agulha em cicatrizes, tatuagens, estrias ou zonas onde a pele esteja lesionada/inflamada/vermelha.
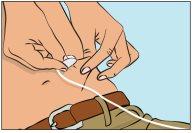
- Pegue a pele entre o polegar e o dedo indicador ao redor do local da injeção (Figura 7), retire com cuidado a cobertura da agulha e insira a agulha na pele (Figura 8). O ângulo da agulha dependerá do tipo de equipamento de perfusão que se utiliza.
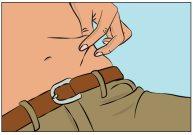


- Verificar a perfusão
- A solução não deve ser perfundida em um vaso sanguíneo.
- Fixe a agulha no lugar colocando uma gaze estéril e uma fita adesiva ou um adesivo transparente (Figura 9).
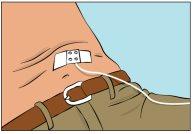

- Iniciar a perfusão
- Inicie a perfusão. Se estiver utilizando uma bomba de perfusão para a administração, siga as instruções do fabricante.
- Registrar a perfusão
- Em cada frasco de Cutaquig, encontrará uma etiqueta descolável com os detalhes do número do lote. Cole esta etiqueta no diário de tratamento do seu paciente ou no livro de registro de perfusão. Registre os detalhes da dose, a data, a hora, a localização do local de perfusão e qualquer infecção, efeitos secundários ou outros comentários relacionados com esta perfusão.
- Após finalizar a perfusão
- Retire suavemente a(s) agulha(s) e coloque-a(s) imediatamente no recipiente para objetos cortantes.
- Se necessário, pressione com um pequeno pedaço de gaze no local onde a agulha penetrinou e aplique um adesivo.
- Elimine todos os suprimentos descartáveis usados, bem como qualquer produto não utilizado e o(s) frasco(s) vazio(s) segundo as recomendações do seu profissional de saúde e de acordo com os requisitos locais.
Organize e armazene de forma segura todo o equipamento reutilizável (por exemplo, a bomba) até a próxima perfusão.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEAForma farmacêutica: INJETÁVEL, 200 mg/mlSubstância ativa: immunoglobulins, normal human, for extravascular adm.Fabricante: Baxalta Innovations GmbhRequer receita médicaForma farmacêutica: INJETÁVEL, 200 mg/mlSubstância ativa: immunoglobulins, normal human, for extravascular adm.Fabricante: Csl Behring GmbhRequer receita médicaForma farmacêutica: INJETÁVEL, 200 mg proteína plasmática humana/mlSubstância ativa: immunoglobulins, normal human, for extravascular adm.Fabricante: Csl Behring GmbhRequer receita médica
Alternativas a CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEA noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEA em Polónia
Alternativa a CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEA em Ukraine
Médicos online para CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEA
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de CUTAQUIG 165 mg/ml SOLUÇÃO PARA INJEÇÃO SUBCUTÂNEA – sujeita a avaliação médica e regras locais.














