
Tisseel
Pergunte a um médico sobre a prescrição de Tisseel

Como usar Tisseel
Folheto para o utilizador: informação
TISSEEL – Soluções para preparar adesivo tecidual
Fibrinogénio humano, trombina humana, aprotinina sintética, cloreto de cálcio di-hidratado
Deve ler atentamente o conteúdo do folheto antes de aplicar o medicamento, pois contém informações importantes para o doente.
- Deve conservar este folheto para o poder reler se necessário.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Se o doente apresentar algum efeito indesejado, incluindo qualquer efeito indesejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto:
- 1. O que é TISSEEL e para que é utilizado
- 2. Informações importantes antes de aplicar TISSEEL
- 3. Como aplicar TISSEEL
- 4. Efeitos indesejados possíveis
- 5. Como conservar TISSEEL
- 6. Conteúdo da embalagem e outras informações
1. O que é TISSEEL e para que é utilizado
O que é TISSEEL
TISSEEL é um adesivo tecidual bifásico, composto por duas soluções, solução de proteínas adesivas e solução de trombina. A solução Tisseel contém fibrinogénio e trombina. São duas proteínas do sangue necessárias para a coagulação do sangue. Quando estas proteínas se misturam durante a aplicação, formam um coágulo no local onde o cirurgião o aplica.
Para que é utilizado TISSEEL
TISSEEL é utilizado como tratamento de apoio, quando as técnicas cirúrgicas padrão não são suficientemente eficazes:
para melhorar a hemostase;
como adesivo tecidual, facilitando a cicatrização de feridas ou como material de selagem de suturas em cirurgia vascular e gastrointestinal;
para colar tecidos, por exemplo, fixar enxertos de pele.
TISSEEL é eficaz mesmo em doentes que recebem medicamentos com heparina que inibem a coagulação.
2. Informações importantes antes de aplicar TISSEEL
Quando não aplicar TISSEEL:
- em caso de alergia (hipersensibilidade) a qualquer um dos componentes ativos ou a qualquer um dos outros componentes do medicamento.
- para tratar hemorragias arteriais ou venosas maciças. A aplicação exclusiva de TISSEEL não é recomendada nessa situação.
- TISSEEL não deve ser injetado em vasos sanguíneos (veias ou artérias). Como o TISSEEL forma coágulos no local de aplicação, a injeção de TISSEEL pode causar a formação de um coágulo no vaso. Se esse coágulo for transportado pelo sangue, pode levar a complicações que ameaçam a vida.
- TISSEEL não é indicado para substituir suturas na pele para fechar a ferida operatória.
Precauções e advertências
Antes de iniciar o tratamento com TISSEEL, deve discutir com o médico, farmacêutico ou enfermeiro.
Deve ter cuidado ao aplicar TISSEEL devido à possibilidade de reações alérgicas de hipersensibilidade.
Os primeiros sinais de reação alérgica podem incluir:
- rubor passageiro da pele
- prurido
- erupção cutânea
- náuseas, vômitos
- mal-estar geral
- calafrios
- pressão no peito
- inchaço dos lábios e língua
- dificuldades respiratórias/apneia
- queda da pressão arterial
- aumento ou diminuição da frequência cardíaca
Se ocorrer algum desses sintomas, a aplicação deve ser interrompida imediatamente. Em caso de sintomas graves, deve-se iniciar o tratamento de emergência.
Deve ter cuidado ao aplicar TISSEEL, pois contém uma proteína sintética chamada aprotinina. Mesmo que essa proteína seja administrada em quantidades pequenas e apenas na superfície da ferida, há risco de reação anafilática grave. Esse risco parece ser maior em doentes que receberam TISSEEL ou aprotinina anteriormente, mesmo que tenha sido bem tolerado. Por isso, deve-se registrar na história clínica do doente as informações sobre a administração de aprotinina ou produtos que contenham aprotinina. Como a aprotinina sintética é estruturalmente idêntica à aprotinina bovina, deve-se considerar cuidadosamente a aplicação de TISSEEL em doentes com alergia a proteínas bovinas.
Deve ter cuidado ao aplicar TISSEEL, pois a administração inadvertida em um vaso sanguíneo pode levar a complicações que ameaçam a vida devido à entrada de coágulos no sistema circulatório.
A administração intravascular, especialmente em doentes sensíveis, pode aumentar a probabilidade e a gravidade de reações de hipersensibilidade aguda.
Durante as operações de cirurgia cardíaca, o médico deve ter cuidado para não injetar TISSEEL em um vaso sanguíneo. É igualmente importante evitar a injeção na mucosa nasal devido ao risco de formação de coágulos sanguíneos nas artérias ao redor dos olhos.
- pois há risco de dano tecidual local em caso de injeção de TISSEEL no tecido.
- para evitar a colagem de tecidos em locais indesejados. Por isso, antes da aplicação, deve-se verificar se as áreas do corpo fora do local de aplicação do produto estão suficientemente protegidas.
- pois a espessura excessiva do coágulo formado pode afetar negativamente a eficácia do produto e o processo de cicatrização da ferida. Por isso, o TISSEEL deve ser aplicado apenas em uma camada fina.
Deve ter cuidado ao aplicar o adesivo de fibrina com gás comprimido.
Durante a aplicação de dispositivos de spray equipados com regulador de pressão para aplicar adesivos de fibrina tecidual, foi observado um raro ocorrer de embolia aérea ou gasosa que ameaça a vida ou causa a morte
(consistindo na entrada de ar no sistema circulatório, o que pode levar a um risco grave para a saúde ou a vida).
Parece estar relacionado ao uso do dispositivo de spray com configurações de pressão maiores do que as recomendadas e (ou)
muito perto da superfície do tecido. O risco parece ser maior quando os adesivos de fibrina tecidual são pulverizados com ar, em vez de com CO.
Por isso, não se pode excluir a ocorrência de tal evento devido à pulverização do produto TISSEEL em feridas abertas tratadas cirurgicamente.
O dispositivo de spray e a ponta adicional foram acompanhados de instruções de uso com as recomendações do fabricante sobre os intervalos de pressão e a distância da superfície do tecido durante a pulverização.
O produto TISSEEL deve ser administrado estritamente de acordo com as instruções e apenas com os dispositivos recomendados para o uso deste produto.
Durante a pulverização do produto TISSEEL, deve-se monitorar as alterações da pressão arterial, frequência cardíaca, saturação de oxigênio no sangue arterial e concentração final de CO, devido à possibilidade de ocorrência de embolia aérea ou gasosa (ver ponto 2).
No caso da produção de medicamentos a partir de sangue humano ou plasma, são tomadas medidas para prevenir a transmissão de infecções para os doentes. Isso inclui:
- seleção rigorosa dos doadores de sangue e plasma, para garantir que os grupos de risco de infecção sejam excluídos
- verificação de doações individuais de sangue e pools de plasma coletado para vírus ou infecções
- inclusão de etapas no processo de tratamento do sangue ou plasma que possam inativar ou remover vírus.
Apesar dessas medidas, quando os medicamentos produzidos a partir de sangue humano ou plasma são administrados, não se pode excluir completamente a possibilidade de transmissão de infecção. Isso inclui vírus desconhecidos e recentemente descobertos, bem como outros patógenos.
As medidas tomadas são consideradas eficazes contra vírus envelopados, como o vírus da imunodeficiência humana (HIV), vírus da hepatite B e vírus da hepatite C, bem como contra o vírus da hepatite A não envelopado. As medidas tomadas podem ter valor limitado contra alguns vírus não envelopados, como o parvovirus B19.
A infecção por parvovirus B19 pode ser grave em mulheres grávidas (infecção fetal) e em pessoas com sistema imunológico debilitado ou com certos tipos de anemia (por exemplo, esferocitose congênita ou anemia hemolítica).
O médico pode recomendar que o doente considere a vacinação contra a hepatite viral A e B, se o doente receber adesivo de fibrina repetidamente.
É altamente recomendável que, a cada administração de TISSEEL, se documente o nome e o número de lote do medicamento usando a etiqueta autoadesiva anexa, que deve ser colocada na história clínica do doente.
TISSEEL e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o doente está tomando atualmente ou recentemente, bem como sobre os medicamentos que o doente planeja tomar, mesmo que sejam disponíveis sem prescrição.
Não são conhecidas interações de TISSEEL com outros produtos medicinais.
Como outros produtos comparáveis ou soluções de trombina, o produto pode ser denaturado pelo efeito de soluções que contenham álcool, iodo ou metais pesados (por exemplo, soluções desinfetantes).
Antes da aplicação do produto, deve-se limpar a superfície com esses tipos de substâncias.
As informações sobre os preparados que contenham celulose oxidada estão no ponto Preparação para a aplicação .
TISSEEL com alimentos e bebidas
Deve perguntar ao médico. O médico decidirá se o doente pode comer e beber antes da aplicação de TISSEEL.
Gravidez, amamentação e fertilidade
Se a doente estiver grávida ou amamentando, suspeitar que possa estar grávida ou planejar ter um filho, deve consultar o médico ou farmacêutico antes de aplicar este medicamento. O médico decidirá se o TISSEEL pode ser aplicado durante a gravidez ou amamentação.
Condução de veículos e operação de máquinas
TISSEEL não afeta a capacidade de conduzir veículos ou operar máquinas.
TISSEEL contém Polissorbato 80
O Polissorbato 80 pode causar reações locais na pele, como dermatite de contato.
3. Como aplicar TISSEEL
O produto TISSEEL pode ser aplicado apenas por cirurgiões experientes que tenham sido treinados para isso.
Antes da aplicação do produto TISSEEL, a superfície da ferida deve ser seca, usando técnicas padrão (por exemplo, troca de curativos, gaze, uso de dispositivos de aspiração).
Não se deve usar ar comprimido ou gás para secar a superfície.
O TISSEEL só pode ser pulverizado em superfícies visíveis.
Durante a aplicação do produto TISSEEL com um dispositivo de spray, deve-se seguir as recomendações do fabricante sobre a pressão e a distância da superfície do tecido, de acordo com os intervalos fornecidos abaixo:
| Procedimento cirúrgico | Conjunto de spray a ser utilizado | Ponta de aplicação a ser utilizada | Regulador de pressão a ser utilizado | Distância recomendada da superfície do tecido | Pressão recomendada de pulverização |
| Ferida aberta | Conjunto de spray Tisseel/Artiss | nd. | EasySpray | 10–15 cm | 1,5– 2,0 bar (21,5– 28,5 psi) |
| Conjunto de spray Tisseel/Artiss — embalagem de 10 unidades | nd. | EasySpray | |||
| Procedimentos laparoscópicos/ minimamente invasivos | nd. | Ponta de aplicação Duplospray MIS 20 cm | Regulador Duplospray MIS 1,5 bar | 2–5 cm | 1,2– 1,5 bar (18– 22 psi) |
| Ponta de aplicação Duplospray MIS 30 cm | |||||
| Ponta de aplicação Duplospray MIS 40 cm | |||||
| Conjunto de spray Set 360 Ponta de aplicação endoscópica com Snap Lock | |||||
| Conjunto de spray Set 360 Ponta de aplicação endoscópica com faixa de segurança | |||||
| Ponta de aplicação intercambiável | |||||
Durante a pulverização do produto TISSEEL, deve-se monitorar as alterações da pressão arterial, frequência cardíaca, saturação de oxigênio no sangue arterial e concentração final de CO, devido à possibilidade de ocorrência de embolia aérea ou gasosa (ver ponto 2).
A dose do adesivo aplicado é determinada com base nas necessidades individuais.
A dose depende de vários fatores, incluindo o tipo de procedimento cirúrgico, o tamanho da superfície a ser colada, o método de aplicação escolhido e a quantidade de aplicação. O médico decidirá a quantidade necessária e aplicará uma camada fina e uniforme na superfície-alvo. Se a quantidade aplicada não parecer suficiente, a aplicação do adesivo pode ser repetida.
Durante a aplicação do produto TISSEEL, um coágulo se forma rapidamente. Deve-se evitar aplicar uma nova camada sobre a camada existente do medicamento TISSEEL, pois a nova camada não se unirá à camada existente. Deve-se evitar aplicar separadamente o componente com proteínas adesivas e o componente que contém trombina.
Nos estudos clínicos, as doses individuais administradas variaram de 4 a 20 ml. Em alguns procedimentos (por exemplo, lesões hepáticas traumáticas ou tratamento de queimaduras extensas), pode ser necessário usar volumes maiores.
Como diretriz para a colagem de superfícies, pode-se considerar que 1 conjunto de adesivo TISSEEL 2 ml (ou seja, 1 ml de solução de proteínas adesivas mais 1 ml de solução de trombina) é suficiente para cobrir uma área de pelo menos 10 cm².
Quando o TISSEEL é aplicado por pulverização, a mesma quantidade será suficiente para cobrir áreas maiores.
Para evitar a formação excessiva de granuloma e garantir a absorção gradual do adesivo tecidual solidificado, deve-se aplicar camadas finas de TISSEEL.
Para garantir a mistura adequada dos componentes da solução de proteínas adesivas e da solução de trombina, deve-se extrair as primeiras gotas do produto da agulha de aplicação antes da aplicação.
Uso de dose maior do que a recomendada de TISSEEL
O TISSEEL é usado apenas durante a operação cirúrgica. O médico determina a quantidade necessária. Não são conhecidos casos de superdose.
Em caso de dúvidas sobre o uso do medicamento, deve-se consultar o médico ou farmacêutico.
Uso em crianças
A segurança e eficácia do medicamento em crianças não foram estabelecidas.
4. Efeitos indesejados possíveis
Como qualquer medicamento, este medicamento pode causar efeitos indesejados, embora não ocorram em todos.
Se algum dos efeitos indesejados se agravar ou ocorrer algum efeito indesejado não mencionado neste folheto, deve-se informar o médico ou farmacêutico.
Em doentes tratados com adesivo tecidual, podem ocorrer reações de hipersensibilidade ou reações alérgicas. Embora sejam muito raras, podem ser muito graves.
Os primeiros sinais de reação alérgica podem incluir:
- rubor passageiro da pele
- prurido
- erupção cutânea
- náuseas, vômitos
- dor de cabeça
- sonolência
- ansiedade
- formigamento e picada no local de aplicação
- zumbido nos ouvidos
- calafrios
- pressão no peito
- inchaço dos lábios, língua e garganta (o que pode causar dificuldades respiratórias e/ou deglutição)
- dificuldades respiratórias
- queda da pressão arterial
- aumento ou diminuição da frequência cardíaca
- perda de consciência devido à queda da pressão arterial
Em casos isolados, essas reações podem evoluir para reações alérgicas graves (anafilaxia).
Essas reações podem ocorrer especialmente quando o produto é usado repetidamente ou é administrado a doentes que já apresentaram hipersensibilidade à aprotinina ou a qualquer outro componente do produto.
Mesmo que o uso anterior do TISSEEL tenha sido bem tolerado, a administração subsequente do TISSEEL ou a injeção de aprotinina pode levar a reações alérgicas graves (anafiláticas).
A equipe que realiza o procedimento cirúrgico está ciente do risco dessas reações e, se ocorrerem os primeiros sinais de hipersensibilidade, a administração do TISSEEL será interrompida imediatamente. Sintomas graves podem exigir medidas de emergência.
A injeção de TISSEEL em tecidos moles pode causar dano tecidual local.
A injeção de TISSEEL em vasos sanguíneos (veias ou artérias) pode causar a formação de coágulos (trombose).
Como o TISSEEL é produzido a partir de plasma de doadores, não se pode excluir completamente o risco de infecção. No entanto, o fabricante toma várias medidas para reduzir esse risco (ver ponto 2).
Em casos raros, podem ocorrer anticorpos contra os componentes do adesivo tecidual.
Os seguintes efeitos indesejados foram observados no tratamento com TISSEEL:
Os efeitos indesejados foram avaliados de acordo com as seguintes categorias de frequência:
Muito frequentes: pode afetar mais de 1 em 10 pessoas
Frequentes: pode afetar até 1 em 10 pessoas
Pouco frequentes : pode afetar até 1 em 100 pessoas
Raros: pode afetar até 1 em 1000 pessoas
Muito raros: pode afetar até 1 em 10000 pessoas
Desconhecidos: a frequência não pode ser estimada com base nos dados disponíveis
| Local de ocorrência | Efeito indesejado | Frequência |
| Infecções e infestações | Infecção pós-operatória da ferida | Frequentes |
| Distúrbios do sangue e do sistema linfático | Aumento dos produtos de degradação da fibrina | Pouco frequentes |
| Distúrbios do sistema imunológico | Reações de hipersensibilidade | Pouco frequentes |
| Reações alérgicas (anafiláticas) | Pouco frequentes | |
| Choque anafilático | Pouco frequentes | |
| Sensação de zumbido, formigamento ou dormência da pele | Pouco frequentes | |
| Pressão no peito | Pouco frequentes | |
| Dificuldades respiratórias | Pouco frequentes | |
| Prurido | Pouco frequentes | |
| Rubor da pele | Pouco frequentes | |
| Distúrbios do sistema nervoso | Distúrbios da sensação | Frequentes |
| Distúrbios cardíacos | Aumento ou diminuição da frequência cardíaca | Pouco frequentes |
| Distúrbios vasculares | Trombose da veia braquial | Frequentes |
| Queda da pressão arterial | Raros | |
| Hematomas | Pouco frequentes | |
| Bolhas de gás no sistema vascular* | Desconhecidos | |
| Coágulos sanguíneos nas veias | Pouco frequentes | |
| Oclusão da artéria cerebral | Pouco frequentes |
| Distúrbios do sistema respiratório, torácico e mediastínico | Dispneia | Pouco frequentes |
| Distúrbios gastrointestinais | Náuseas | Pouco frequentes |
| Obstrução intestinal | Pouco frequentes | |
| Distúrbios da pele e do tecido subcutâneo | Erupção cutânea | Frequentes |
| Urticária | Pouco frequentes | |
| Distúrbio da cicatrização | Pouco frequentes | |
| Distúrbios musculoesqueléticos e do tecido conjuntivo | Dor nas extremidades | Frequentes |
| Distúrbios gerais e condições no local de administração | Dor | Frequentes |
| Febre | Frequentes | |
| Rubor | Desconhecidos | |
| Inchaço devido ao acúmulo de líquido no tecido corporal (edema) | Pouco frequentes | |
| Lesões, envenenamentos e complicações pós-procedimento | Dor relacionada ao procedimento | Pouco frequentes |
| Acúmulo de linfa ou outros líquidos corporais transparentes na área da ferida operatória (acúmulo de líquido seroso local) | Muito frequentes | |
| Inchaço rápido da pele, tecido subcutâneo, mucosa e camada submucosa (edema angioneurótico) | Pouco frequentes |
* A ocorrência de bolhas de gás ou ar no sistema vascular ocorreu quando os adesivos de fibrina tecidual foram aplicados usando dispositivos com ar comprimido ou gás; parece estar relacionada ao uso inadequado do dispositivo de spray (por exemplo, pressão mais alta do que a recomendada e/ou distância mais curta do que a recomendada da superfície do tecido).
Notificação de efeitos indesejados
Se ocorrer algum efeito indesejado, incluindo qualquer efeito indesejado não mencionado neste folheto, deve-se informar o médico ou enfermeiro.
Os efeitos indesejados podem ser notificados diretamente ao
Departamento de Monitoramento de Efeitos Indesejados de Produtos Medicinais da Agência Reguladora de Produtos Medicinais, Dispositivos Médicos e Produtos Biocidas
Al. Jerozolimskie 181C
02-222 Varsóvia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Site: https://smz.ezdrowie.gov.pl
Os efeitos indesejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos indesejados permite coletar mais informações sobre a segurança do medicamento.
5. Como conservar TISSEEL
O medicamento deve ser conservado em um local invisível e inacessível para crianças.
Não use este medicamento após o prazo de validade impresso na etiqueta.
Conservar e transportar congelado (a uma temperatura ≤-20°C) sem interrupção até o momento de uso.
Conservar a seringa no pacote de cartão externo para proteger da luz.
Conservação após a descongelação:
O produto em embalagem não aberta e descongelado a temperatura ambiente pode ser conservado a temperatura ambiente (não superior a 25°C) por até 72 horas.
Após a descongelação, não congele novamente ou coloque na geladeira!
Os medicamentos não devem ser jogados na canalização ou em recipientes de lixo doméstico. Deve-se perguntar ao farmacêutico como descartar os medicamentos que não são mais necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém TISSEEL
TISSEEL consiste em dois componentes:
Componente 1: Solução de proteínas adesivas
As substâncias ativas presentes em 1 ml de solução de proteínas adesivas são: fibrinogénio humano, 91 mg/ml, aprotinina sintética 3000 KIU/ml.
Os outros componentes são: albumina humana, L-histidina, amida do ácido nicotínico, citrato de sódio di-hidratado, polissorbato 80 (Tween 80), água para injeção.
Componente 2: Solução de trombina
As substâncias ativas presentes em 1 ml de solução de trombina são: trombina humana, 500 UI/ml, cloreto de cálcio di-hidratado, 40 μmol/ml
Os outros componentes são: albumina humana, cloreto de sódio, água para injeção.
| Após a mistura | 1 ml | 2 ml | 4 ml | 10 ml | |
| Componente 1: Solução de proteínas adesivas | Fibrinogénio humano | 45,5 mg | 91 mg | 182 mg | 455 mg |
| Aprotinina sintética | 1500 KIU | 3000 KIU | 6000 KIU | 15000 KIU | |
| Componente 2: Solução de trombina | Trombina humana | 250 UI | 500 UI | 1000 UI | 2500 UI |
| Cloreto de cálcio di-hidratado | 20 μmol | 40 μmol | 80 μmol | 200 μmol |
TISSEEL contém fator XIII humano, copurificado com o fibrinogénio humano, em quantidades de 0,6 – 5 UI/ml.
Como é TISSEEL e que embalagem contém
Soluções para preparar adesivo tecidual
A solução de proteínas adesivas e a solução de trombina são fornecidas em uma seringa de plástico para uso único.
As soluções congeladas são incolores a ligeiramente amareladas, opalescentes.
Após a descongelação, as soluções são incolores a ligeiramente amareladas.
TISSEEL está disponível nas seguintes embalagens:
Conteúdo da embalagem com seringa PRIMA
1 ml, 2 ml ou 5 ml de solução de proteínas adesivas e 1 ml, 2 ml ou 5 ml de solução de trombina em uma seringa de câmara dupla (de polipropileno) fechada com uma tampa e embalada em dois sacos com um dispositivo composto por 2 conectores e 4 agulhas de aplicação.
Conteúdo da embalagem com seringa AST
1 ml, 2 ml ou 5 ml de solução de proteínas adesivas e 1 ml, 2 ml ou 5 ml de solução de trombina em uma seringa de câmara dupla (de polipropileno) fechada com uma tampa e embalada em dois sacos com um dispositivo composto por 2 conectores, 4 agulhas de aplicação e 1 êmbolo duplo da seringa.
Tamanho da embalagem
TISSEEL está disponível nos seguintes tamanhos de embalagem: 1x 2 ml (1 ml + 1 ml), 1 x 4 ml (2 ml + 2 ml) e 1 x 10 ml (5 ml + 5 ml).
As soluções estão congeladas.
Nem todos os tipos de embalagens precisam estar disponíveis no mercado.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização:
Baxter Polska Sp. z o.o.
ul. Kruczkowskiego 8
00-380 Varsóvia
Fabricante
Takeda Manufacturing Austria AG
Industriestrasse 67
1221 Viena, Áustria
Este medicamento está autorizado para comercialização nos países membros da Área Econômica Europeia sob os seguintes nomes:
Áustria:
TISSEEL - Lösungen für einen Gewebekleber
Bulgária:
ТИСИЛ - разтвори за тъканно лепило
República Tcheca:
TISSEEL - roztoky pro lepidlo
França:
TISSEEL - solutions pour colle
Alemanha:
TISSEEL 2 ml
TISSEEL 4 ml
TISSEEL 10 ml
Grécia:
TISSEEL - Διαλύματα για στεγανοποιητικό
Malta:
TISSEEL - Solutions for sealant
Noruega:
TISSEEL
Polônia:
TISSEEL
Eslováquia:
TISSEEL - fibrínové lepidlo
Espanha:
TISSEEL - soluciones para adhesivo tisular
Data da última atualização do folheto janeiro de 2022
Informações destinadas apenas ao pessoal médico especializado (embalagem:
Seringa PRIMA):
Informações gerais
- Antes da aplicação do TISSEEL, deve-se proteger as áreas do corpo fora do local de aplicação do produto para evitar a colagem de tecidos em locais indesejados.
- Para evitar a aderência do adesivo de fibrina às luvas e instrumentos cirúrgicos, deve-se umedecê-los com solução salina fisiológica antes do contato.
- Como diretriz para a colagem de superfícies, pode-se considerar que 1 conjunto de adesivo TISSEEL 2 ml (ou seja, 1 ml de solução de proteínas adesivas mais 1 ml de solução de trombina) é suficiente para cobrir uma área de pelo menos 10 cm².
- A dose necessária depende do tamanho da superfície a ser colada.
- NÃO use os dois componentes do produto TISSEEL separadamente. Ambos os componentes devem ser usados juntos.
- Não exponha o produto TISSEEL a temperaturas acima de 37°C. NÃO submeta a micro-ondas.
- NÃO descongele o produto segurando-o na mão.
- NÃO use o produto TISSEEL até que esteja completamente descongelado e aquecido a uma temperatura de 33°C - 37°C.
- Remova a tampa protetora da seringa apenas após a descongelação e aquecimento. Para facilitar a remoção da tampa protetora da seringa, mova a tampa para a frente e para trás e, em seguida, remova a tampa da seringa.
- Remova todo o ar da seringa e, em seguida, fixe o conector e a agulha de aplicação.
Preparação para a aplicação
A solução de proteínas adesivas e a solução de trombina estão contidas em uma seringa pronta para uso. O produto é embalado em condições assépticas em dois sacos estéreis. O saco interno e seu conteúdo são estéreis, a menos que a integridade do saco externo da embalagem tenha sido comprometida. Usando técnica asséptica, transfira o saco interno estéril e seu conteúdo para uma área estéril.
A seringa pronta para uso pode ser descongelada E aquecida por um dos seguintes métodos:
- 1. Descongelação/aquecimento rápido (banho de água estéril) – método recomendado
- 2. Descongelação/aquecimento em banho de água não estéril
- 3. Descongelação/aquecimento em incubadora
- 4. A seringa pronta para uso também pode ser descongelada e armazenada a temperatura ambiente (não superior a 25°C) por até 72 horas. Antes do uso, é necessário aquecer.
- 1) Descongelação/aquecimento rápido (banho de água estéril) – método recomendado
Recomenda-se descongelar e aquecer ambos os componentes do adesivo usando um banho de água estéril a uma temperatura de 33°C - 37°C.
- A temperatura do banho de água não deve exceder 37°C. Para controlar o intervalo de temperatura específico, a temperatura da água deve ser verificada continuamente com um termômetro e a água substituída se necessário.
- Se o banho de água estéril for usado para a descongelação e aquecimento, retire a seringa do saco antes de colocá-la no banho de água estéril.
Instruções:
Transfira o saco interno para condições estéreis, retire a seringa pronta para uso do saco interno e coloque-a diretamente no banho de água estéril. Certifique-se de que o conteúdo da seringa pronta para uso esteja completamente submerso na água.
Tabela 1 – Seringa PRIMA: tempo mínimo de descongelação e aquecimento no banho de água estéril
| Tamanho da embalagem | Tempo mínimo de descongelação/aquecimento |
| 2 ml | 5 minutos |
| 4 ml | 5 minutos |
| 10 ml | 10 minutos |
- 2) Descongelação/aquecimento em banho de água não estéril
Instruções:
Coloque a seringa pronta para uso em ambos os sacos de proteção no banho de água fora da área estéril por um tempo adequado (ver Tabela 2). Certifique-se de que os sacos permaneçam submersos na água durante todo o tempo de descongelação. Após a descongelação, retire os sacos do banho de água, seque o saco externo e transfira o saco interno com a seringa pronta para uso e o êmbolo para a área estéril.
Tabela 2 - Seringa PRIMA: tempo mínimo de descongelação e aquecimento no banho de água não estéril
| Tamanho da embalagem | Tempo mínimo de descongelação | Tempo de aquecimento adicional |
| 2 ml | 15 minutos | 1,5– 2,0 bar (21,5– 28,5 psi) |
| 4 ml | 20 minutos | 1,2– 1,5 bar (18– 22 psi) |
| 10 ml | 35 minutos | 1,2– 1,5 bar (18– 22 psi) |
- 3) Descongelação/aquecimento em incubadora
Instruções:
Coloque a seringa pronta para uso em ambos os sacos de proteção na incubadora fora da área estéril por um tempo adequado (ver Tabela 3). Após a descongelação e aquecimento, retire os sacos da incubadora, remova o saco externo e transfira o saco interno com a seringa pronta para uso para a área estéril.
Tabela 3 – Seringa PRIMA: tempo mínimo de descongelação e aquecimento na incubadora
| Tamanho da embalagem | Tempo mínimo de descongelação/aquecimento |
| 2 ml | 40 minutos |
| 4 ml | 50 minutos |
| 10 ml | 90 minutos |
- 4) Descongelação em temperatura ambiente (não superior a 25°C) ANTES do aquecimento
Instruções:
Descongele a seringa pronta para uso em ambos os sacos de proteção a temperatura ambiente fora da área estéril por um tempo adequado (ver Tabela 4). Após a descongelação, para aquecer o produto para uso, aqueça-o no saco externo na incubadora.
Tabela 4 – Seringa PRIMA: tempo mínimo de descongelação em temperatura ambiente fora da área estéril e tempo de aquecimento adicional na incubadora a uma temperatura de 33°C - 37°C
| Tamanho da embalagem | Tempo mínimo de descongelação | Tempo de aquecimento |
| 2 ml | 80 minutos | + 11 minutos |
| 4 ml | 90 minutos | + 13 minutos |
| 10 ml | 160 minutos | + 25 minutos |
Após a descongelação a temperatura ambiente, o produto deve ser usado dentro de 72 horas após a retirada do congelador.
Estabilidade após a descongelação
Após a descongelação e aquecimento (a uma temperatura de 33°C a 37°C, métodos 1, 2 e 3), a estabilidade química e física do produto foi demonstrada por 12 horas a uma temperatura de 33°C a 37°C.
Para o produto descongelado a temperatura ambiente, em saco não aberto (método 4), a estabilidade química e física do produto foi demonstrada por 72 horas a uma temperatura não superior a 25°C.
Aqueça a uma temperatura de 33°C a 37°C imediatamente antes do uso.
Do ponto de vista microbiológico, o produto deve ser usado imediatamente após o aquecimento a uma temperatura de 33°C a 37°C, a menos que o método de abertura/descongelação exclua o risco de contaminação microbiológica.
Se o produto não for usado imediatamente, o usuário é responsável pelo tempo e condições de armazenamento.
Não re-congele ou coloque na geladeira após o início da descongelação.
Manejo do produto após a descongelação/antes da administração
Para obter a mistura ótima das duas soluções e a coagulação ótima do adesivo de fibrina, deve-se manter a temperatura de ambos os componentes do adesivo em 33°C - 37°C até a administração .
As soluções de proteínas adesivas e trombina devem ser transparentes ou ligeiramente opalescentes. Não use soluções turvas ou que contenham sedimentos. Os produtos descongelados devem ser inspecionados visualmente antes do uso para detectar partículas insolúveis e alterações da cor ou qualquer alteração na aparência física. Se ocorrer alguma dessas situações, a solução deve ser descartada.
A solução de proteínas adesivas descongelada deve ser um líquido ligeiramente viscoso. Se a solução estiver na forma de um gel solidificado, deve-se supor que tenha sido denaturada (provavelmente devido à interrupção da cadeia de frio de armazenamento ou superaquecimento durante o aquecimento). Nesse caso, NÃO use o TISSEEL sob nenhuma circunstância.
- Não retire a seringa de câmara dupla do saco de plástico até o momento do uso.
- Use o TISSEEL apenas após a descongelação completa e aquecimento (consistência líquida).
- Remova a tampa protetora da seringa apenas imediatamente antes da aplicação. Para facilitar a remoção da tampa protetora da seringa, mova a tampa para a frente e para trás e, em seguida, remova a tampa da seringa.
Administração com seringa PRIMA: Para aplicar o adesivo, conecte a seringa de câmara dupla pronta para uso contendo a solução de proteínas adesivas e a solução de trombina ao conector e à agulha de aplicação fornecidos no conjunto de dispositivos. O êmbolo comum da seringa de câmara dupla pronta para uso garante a administração de volumes iguais de ambos os componentes, que são misturados na agulha de aplicação e, em seguida, aplicados.
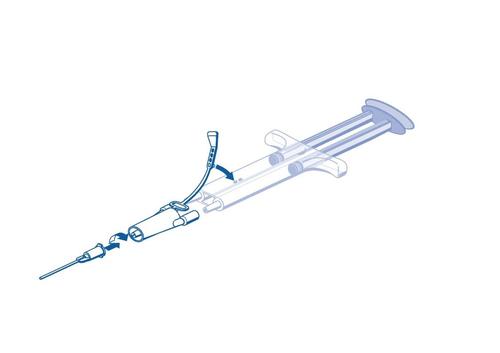
Faixa de segurança
Êmbolo duplo
Seringa de câmara dupla
Conector
Agulha de aplicação
- Remova todo o ar da seringa e, em seguida, fixe o conector e a agulha de aplicação.
- Ajuste o conector e fixe-o ao lado da seringa com a faixa de segurança.
- Conecte as saídas da seringa de câmara dupla pronta para uso ao conector, certificando-se de que estejam bem fixadas.
- Fixe o conector, fixando a faixa de segurança na seringa pronta para uso.
- Se a faixa de segurança for rompida, use o conector adicional fornecido no conjunto.
- Se não houver mais um conector adicional, o conjunto ainda pode ser usado, desde que se certifique de que a conexão seja segura e estanque.
- NÃO remova o ar do conector.
- Fixe a agulha de aplicação ao conector.
- NÃO remova o ar do conector ou da agulha de aplicação antes de iniciar a aplicação do adesivo, pois isso pode causar a obstrução da agulha.
Administração
Antes da aplicação do produto TISSEEL, a superfície da ferida deve ser seca, usando técnicas padrão (por exemplo, troca de curativos, gaze, uso de dispositivos de aspiração).
Não use ar comprimido ou gás para secar a superfície.
- Aplique a solução misturada de proteínas adesivas-trombina na superfície-alvo ou superfícies a serem coladas, pressionando suavemente a parte traseira do êmbolo comum.
- Em procedimentos cirúrgicos que exigem volumes mínimos de adesivo de fibrina, recomenda-se extrair e descartar as primeiras gotas do produto.
- Após a aplicação do TISSEEL, aguarde pelo menos 2 minutos para alcançar a polimerização suficiente.
Aviso:
Se a aplicação dos componentes do adesivo de fibrina for interrompida, a agulha pode ficar imediatamente entupida. Nesse caso, a agulha de aplicação deve ser substituída por uma nova apenas antes de reaplicar o adesivo. Se as saídas do conector estiverem entupidas, deve-se utilizar um conector adicional fornecido no pacote. Após a mistura dos componentes do adesivo de fibrina, a sua solidificação ocorre em poucos segundos - devido à alta concentração de trombina (500 UI/ml). O adesivo de fibrina pode ser aplicado também com outros dispositivos fabricados pela empresa BAXTER, que são especialmente adaptados para uso em endoscopia, procedimentos cirúrgicos minimamente invasivos ou para aplicar o preparado em superfícies grandes ou de difícil acesso. Ao utilizar esses dispositivos, deve-se seguir as instruções de uso. Preparados que contenham celulose oxidada não devem ser utilizados com o produto TISSEEL, pois o pH baixo afeta a atividade da trombina. Para certos usos, podem ser utilizados materiais biocompatíveis, como placas de colágeno, como suporte ou para reforço mecânico das uniões.
Aplicação do produto com um dispositivo de pulverização
Ao aplicar o produto TISSEEL com um dispositivo de pulverização, deve-se seguir as recomendações do fabricante em relação à pressão e à distância da pele, de acordo com os intervalos indicados abaixo:
| Valores recomendados de pressão e distância da pele, bem como dispositivos de pulverização para aplicar o produto TISSEEL | |||||
| Tratamento cirúrgico | Kit de pulverização a ser utilizado | Pontas do aplicador a serem utilizadas | Regulador de pressão a ser utilizado | Distância recomendada da pele alvo | Pressão recomendada de pulverização |
| Ferida aberta | Kit de pulverização Tisseel/Artiss | nd. | EasySpray | 10–15 cm | 1,5–2,0 bar (21,5–28,5 psi) |
| Kit de pulverização Tisseel/Artiss — embalagem de 10 unidades | nd. | EasySpray | |||
| Procedimentos laparoscópicos/minimamente invasivos | nd. | Aplikador Duplospray MIS 20 cm | Regulador Duplospray MIS 1,5 bar | 2–5 cm | 1,2–1,5 bar (18–22 psi) |
| Aplikador Duplospray MIS 30 cm | |||||
| Aplikador Duplospray MIS 40 cm | |||||
| Kit de pulverização 360 com aplicador endoscópico com Snap Lock | |||||
| Kit de pulverização 360 com aplicador endoscópico com faixa de segurança | |||||
| Ponta de aplicação substituível | |||||
Ao pulverizar o produto TISSEEL, deve-se monitorar as alterações na pressão arterial, frequência cardíaca, saturação de oxigênio no sangue arterial e concentração de CO no final da expiração, devido à possibilidade de ocorrência de embolia aérea ou gasosa (ver item 2).
No caso de administração do produto TISSEEL em um espaço fechado do tórax ou abdômen, recomenda-se o uso do aplicador DuploSpray MIS e do sistema de regulagem. Mais informações estão disponíveis nas instruções de uso do dispositivo DuploSpray MIS.
Remoção de resíduos
Qualquer resíduo não utilizado do produto medicinal ou seus resíduos deve ser removido de acordo com as regulamentações locais.
Informações destinadas apenas ao pessoal médico especializado (embalagem: seringa AST):
Informações gerais
- Antes de aplicar o TISSEEL, deve-se proteger as áreas do corpo que não são o local de aplicação do produto, para evitar a adesão de tecidos em locais indesejados.
- Para evitar a adesão do adesivo às luvas e instrumentos cirúrgicos, deve-se umedecê-los com solução salina antes do contato.
- Como diretriz para a adesão de superfícies, pode-se considerar que 1 kit de adesivo TISSEEL de 2 ml (ou seja, 1 ml de solução de proteínas adesivas mais 1 ml de solução de trombina) é suficiente para cobrir uma área de pelo menos 10 cm².
- A dose necessária depende do tamanho da superfície a ser aderida.
- NÃO use os dois componentes do produto TISSEEL separadamente. Ambos os componentes devem ser usados juntos.
- NÃO expor o produto TISSEEL a temperaturas acima de 37°C. NÃO submeter ao micro-ondas.
- NÃO descongelar o produto segurando-o na mão.
- NÃO usar o produto TISSEEL até que esteja completamente descongelado e aquecido a uma temperatura de 33°C a 37°C.
- Remover a tampa protetora da seringa apenas após o descongelamento e aquecimento.
- Remover todo o ar da seringa e, em seguida, fixar o conector e a agulha de aplicação.
Preparação para uso
A solução de proteínas adesivas e a solução de trombina estão contidas em uma seringa pronta para uso. O produto é embalado em condições assépticas em dois sacos estéreis. O saco interno e seu conteúdo são estéreis, a menos que a integridade do saco externo tenha sido comprometida. Com técnica estéril, o saco interno estéril e seu conteúdo devem ser transferidos para uma área estéril. A seringa pronta para uso pode ser descongelada e aquecida por um dos seguintes métodos:
- 1. Descongelamento/aquecimento rápido (banho de água estéril) – método recomendado
- 2. Descongelamento/aquecimento em banho de água não estéril
- 3. Descongelamento/aquecimento em incubadora
- 4. A seringa pronta para uso também pode ser descongelada e armazenada em temperatura ambiente (não excedendo 25°C) por até 72 horas. Antes do uso, é necessário aquecer.
- 1) Descongelamento/aquecimento rápido (banho de água estéril) – método recomendado
Recomenda-se descongelar e aquecer ambos os componentes do adesivo usando um banho de água estéril a uma temperatura de 33°C a 37°C.
- A temperatura do banho de água não deve exceder 37°C. Para controlar o intervalo de temperatura específico, a temperatura da água deve ser verificada continuamente com um termômetro e a água substituída se necessário.
- Se um banho de água estéril for usado para descongelar e aquecer, a seringa deve ser removida do saco antes de ser colocada no banho de água estéril.
Instruções:
Transferir o saco interno para condições estéreis, remover a seringa pronta para uso do saco interno e colocá-la diretamente no banho de água estéril. Certificar-se de que o conteúdo da seringa pronta para uso esteja completamente submerso na água. Tabela 1 – Seringa AST: tempo mínimo de descongelamento e aquecimento em banho de água estéril. Tempo mínimo de descongelamento/aquecimento. Tamanho do pacote. 33°C a 37°C, banho de água estéril. Produto removido dos sacos. 2 ml. 5 minutos. 4 ml. 5 minutos. 10 ml. 12 minutos.
- 2) Descongelamento/aquecimento em banho de água não estéril
Instruções:
Colocar a seringa pronta para uso em ambos os sacos protetores no banho de água fora da área estéril por um tempo adequado (ver Tabela 2). Deve-se certificar de que os sacos permaneçam submersos na água durante todo o tempo de descongelamento. Após o descongelamento, remover os sacos do banho de água, secar o saco externo e transferir o saco interno com a seringa pronta para uso e o êmbolo para a área estéril. Tabela 2 - Seringa AST: tempo mínimo de descongelamento e aquecimento em banho de água não estéril. Tempo mínimo de descongelamento/aquecimento. Tamanho do pacote. 33°C a 37°C, banho de água não estéril. Produto nos sacos. 2 ml. 30 minutos. 4 ml. 40 minutos. 10 ml. 80 minutos.
- 3) Descongelamento/aquecimento em incubadora
Instruções:
Colocar a seringa pronta para uso em ambos os sacos protetores na incubadora fora da área estéril por um tempo adequado (ver Tabela 3). Após o descongelamento/aquecimento, remover os sacos da incubadora, remover o saco externo e transferir o saco interno com a seringa pronta para uso para a área estéril. Tabela 3 – Seringa AST: tempo mínimo de descongelamento e aquecimento em incubadora. Tempo mínimo de descongelamento/aquecimento. Tamanho do pacote. 33°C a 37°C, incubadora. Produto nos sacos. 2 ml. 40 minutos. 4 ml. 85 minutos. 10 ml. 105 minutos.
- 4) Descongelamento em temperatura ambiente (não excedendo 25°C) ANTES do aquecimento
Instruções:
Descongelar a seringa pronta para uso em ambos os sacos protetores em temperatura ambiente fora da área estéril por um tempo adequado (ver Tabela 4). Após o descongelamento, para aquecer o produto para uso, aquecê-lo no saco externo na incubadora. Tabela 4 – Seringa AST: tempo mínimo de descongelamento em temperatura ambiente fora da área estéril e tempo adicional de aquecimento na incubadora a uma temperatura de 33°C a 37°C. Tempo de aquecimento antes do uso. Tempo mínimo de descongelamento. Para uma temperatura de 33°C a 37°C na incubadora após o descongelamento em temperatura ambiente. Produto em temperatura ambiente. Produto nos sacos. 2 ml. 60 minutos. + 15 minutos. 4 ml. 110 minutos. + 25 minutos. 10 ml. 160 minutos. + 35 minutos. Após o descongelamento em temperatura ambiente, o produto deve ser usado dentro de 72 horas após a remoção do congelador.
Estabilidade após o descongelamento
Após o descongelamento e aquecimento (a uma temperatura de 33°C a 37°C, métodos 1, 2 e 3), a estabilidade química e física do produto foi demonstrada por 12 horas a uma temperatura de 33°C a 37°C. Para o produto descongelado em temperatura ambiente, no saco não aberto (método 4), a estabilidade química e física do produto foi demonstrada por 72 horas a uma temperatura não excedendo 25°C. Aquecer a uma temperatura de 33°C a 37°C imediatamente antes do uso. Do ponto de vista microbiológico, o produto deve ser usado imediatamente após o aquecimento a uma temperatura de 33°C a 37°C, a menos que o método de abertura/descongelamento exclua o risco de contaminação microbiológica. Se o produto não for usado imediatamente, o usuário é responsável pelo tempo e condições de armazenamento. Não deve ser recongelado ou colocado na geladeira após o início do descongelamento.
Manuseio do produto após o descongelamento/antes da administração
Para obter a mistura ótima das duas soluções e a solidificação ótima do adesivo de fibrina, deve-se manter a temperatura de ambos os componentes do adesivo em 33°C - 37°C até a aplicação. A solução de proteínas adesivas e a solução de trombina devem ser transparentes ou ligeiramente opalescentes. Não deve ser usado se as soluções estiverem turvas ou contiverem sedimentos. Os produtos descongelados devem ser submetidos a uma inspeção visual antes do uso para detectar a presença de partículas insolúveis ou alterações na cor ou no aspecto físico. Se ocorrer alguma dessas situações, a solução deve ser descartada. A solução de proteínas adesivas descongelada deve ser um líquido ligeiramente viscoso. Se a solução tiver a forma de um gel solidificado, deve-se supor que ela tenha sofrido denaturação (provavelmente devido à interrupção da cadeia de frio de armazenamento ou superaquecimento durante o aquecimento). Nesse caso, NÃO deve ser usado o TISSEEL sob nenhuma circunstância.
- Não remover a seringa do saco até o momento do uso.
- Usar o TISSEEL apenas após o descongelamento e aquecimento completo (consistência líquida).
- Remover a tampa protetora da seringa apenas antes da aplicação.
Administração com a seringa AST:Para aplicar o adesivo, conectar a seringa de dois compartimentos pronta para uso, preenchida com a solução de proteínas adesivas e a solução de trombina, ao conector e à agulha de aplicação fornecidos no kit de dispositivos. O êmbolo comum da seringa de dois compartimentos pronta para uso, fornecido no kit de dispositivos, assegura a administração de volumes iguais de ambos os componentes, que são então misturados na agulha de aplicação e aplicados. Instruções de uso da seringa AST
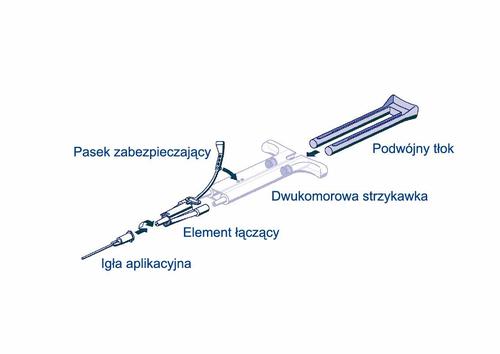
- Remover todo o ar da seringa e, em seguida, fixar o conector e a agulha de aplicação.
- Ajustar o conector e fixá-lo ao lado da seringa com a faixa de segurança.
- Conectar as saídas da seringa de dois compartimentos pronta para uso ao conector, certificando-se de que estejam devidamente fixadas.
- Fixar o conector, prendendo a faixa de segurança à seringa de dois compartimentos pronta para uso.
- Se a faixa de segurança for rompida, usar o conector adicional fornecido no kit.
- Se não houver conector adicional, o kit ainda pode ser usado, desde que se certifique de que a conexão seja segura e estanque.
- NÃO remover o ar do conector.
- Fixar a agulha de aplicação ao conector.
- NÃO remover o ar do conector ou da agulha de aplicação antes de iniciar a aplicação do adesivo, pois isso pode causar entupimento da agulha.
Administração
Antes de aplicar o produto TISSEEL, a superfície da ferida deve ser seca, usando técnicas padrão (por exemplo, trocando curativos, gazes, usando dispositivos de sucção). Não deve ser usado ar comprimido ou gás para secar a superfície.
- Aplique a solução mista de proteína adesiva-trombina na superfície alvo ou nas superfícies a serem unidas, pressionando suavemente a parte traseira do êmbolo comum.
- Em procedimentos cirúrgicos que exigem volumes mínimos de adesivo de fibrina, recomenda-se extrair e descartar as primeiras gotas do produto.
- Após a aplicação do TISSEEL, aguarde pelo menos 2 minutos para alcançar a polimerização adequada.
Aviso:
Se a aplicação dos componentes do adesivo de fibrina for interrompida, a agulha pode ficar imediatamente entupida. Nesse caso, a agulha de aplicação deve ser substituída por uma nova apenas antes de reaplicar o adesivo. Se as saídas do conector estiverem entupidas, deve-se utilizar um conector adicional fornecido no pacote. Após a mistura dos componentes do adesivo de fibrina, a sua solidificação ocorre em poucos segundos - devido à alta concentração de trombina (500 UI/ml). O adesivo de fibrina pode ser aplicado também com outros dispositivos fabricados pela empresa BAXTER, que são especialmente adaptados para uso em endoscopia, procedimentos cirúrgicos minimamente invasivos ou para aplicar o preparado em superfícies grandes ou de difícil acesso. Ao utilizar esses dispositivos, deve-se seguir as instruções de uso. Preparados que contenham celulose oxidada não devem ser utilizados com o produto TISSEEL, pois o pH baixo afeta a atividade da trombina. Para certos usos, podem ser utilizados materiais biocompatíveis, como placas de colágeno, como suporte ou para reforço mecânico das uniões.
Aplicação do produto com um dispositivo de pulverização
Valores recomendados de pressão e distância da pele, bem como dispositivos de pulverização para aplicar o produto TISSEEL
Kit de pulverização a ser utilizado. Pontas do aplicador a serem utilizadas. Regulador de pressão a ser utilizado. Distância recomendada da pele alvo. Pressão recomendada de pulverização. Tratamento cirúrgico. Kit de pulverização Tisseel/Artiss. nd. EasySpray. 1,5–2,0 bar (21,5–28,5 psi). Ferida aberta. 10–15 cm. Kit de pulverização Tisseel/Artiss — embalagem de 10 unidades. nd. EasySpray. Regulador Duplospray MIS 1,5 bar. Aplicador Duplospray MIS 20 cm. Aplicador Duplospray MIS 30 cm. Aplicador Duplospray MIS 40 cm. Kit de pulverização 360 com aplicador endoscópico com Snap Lock. Kit de pulverização 360 com aplicador endoscópico com faixa de segurança. Ponta de aplicação substituível. 1,2–1,5 bar (18–22 psi). Procedimentos laparoscópicos/minimamente invasivos. nd. 2–5 cm.
| Ao aplicar o produto TISSEEL com um dispositivo de pulverização, deve-se seguir as recomendações do fabricante em relação à pressão e à distância da pele, de acordo com os intervalos indicados abaixo: | ||
| przestrzegać zaleceń producenta dotyczących ciśnienia oraz odległości od tkanki zgodnie z zakresami podanymi poniżej: | ||
| zakresami podanymi poniżej: | ||
| Ao pulverizar o produto TISSEEL, deve-se monitorar as alterações na pressão arterial, frequência cardíaca, saturação de oxigênio no sangue arterial e concentração de CO no final da expiração, devido à possibilidade de ocorrência de embolia aérea ou gasosa (ver item 2). | |
| wystąpienia zatoru powietrznego lub gazowego (patrz punkt 2). | |
| wystąpienia zatoru powietrznego lub gazowego (patrz punkt 2). | |
| No caso de administração do produto TISSEEL em um espaço fechado do tórax ou abdômen, recomenda-se o uso do aplicador DuploSpray MIS e do sistema de regulagem. Mais informações estão disponíveis nas instruções de uso do dispositivo DuploSpray MIS. | |
| zastosowanie aplikatora DuploSpray MIS oraz systemu regulującego. Dalsze informacje w instrukcji użycia urządzenia DuploSpray MIS. | |
| zastosowanie aplikatora DuploSpray MIS oraz systemu regulującego. Dalsze informacje w instrukcji użycia urządzenia DuploSpray MIS. | |
| Remoção de resíduos | |
| Qualquer resíduo não utilizado do produto medicinal ou seus resíduos deve ser removido de acordo com as regulamentações locais. | |
| lokalnymi przepisami. | |
- País de registo
- Requer receita médicaNão
- Fabricante
- ImportadorTakeda Manufacturing Austria AG
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a TisseelForma farmacêutica: Solução, 100 mg/mlSubstância ativa: acetylcysteineFabricante: Lek Pharmaceuticals d.d.Requer receita médicaForma farmacêutica: Solução, 10 mg/mlSubstância ativa: calcium folinateFabricante: Fresenius Kabi Austria GmbHRequer receita médicaForma farmacêutica: Solução, 10 mg/mlSubstância ativa: calcium folinateRequer receita médica
Médicos online para Tisseel
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Tisseel – sujeita a avaliação médica e regras locais.














