
Como usar Pomalidomide Glenmark
Folheto de informação para o doente
Pomalidomida Glenmark, 1 mg, cápsulas duras
Pomalidomida Glenmark, 2 mg, cápsulas duras
Pomalidomida Glenmark, 3 mg, cápsulas duras
Pomalidomida Glenmark, 4 mg, cápsulas duras
Pomalidomida
É esperado que o medicamento Pomalidomida Glenmark cause defeitos congénitos graves e possa levar à morte do feto.
- Não deve tomar o medicamento se estiver grávida ou se pode estar grávida.
- Deve seguir os conselhos sobre contracepção apresentados neste folheto.
Deve ler atentamente o folheto antes de tomar o medicamento, pois contém informações importantes para si.
- Deve guardar este folheto para o poder reler se necessário.
- Se tiver alguma dúvida, deve consultar o seu médico, farmacêutico ou enfermeira.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que os sintomas da sua doença sejam os mesmos.
- Se ocorrerem algum efeitos secundários, incluindo qualquer efeito secundário não mencionado neste folheto, deve informar o seu médico, farmacêutico ou enfermeira. Ver secção 4.
Índice do folheto
- 1. O que é o medicamento Pomalidomida Glenmark e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Pomalidomida Glenmark
- 3. Como tomar o medicamento Pomalidomida Glenmark
- 4. Efeitos secundários possíveis
- 5. Como conservar o medicamento Pomalidomida Glenmark
- 6. Conteúdo do pacote e outras informações
1. O que é o medicamento Pomalidomida Glenmark e para que é utilizado
O que é o medicamento Pomalidomida Glenmark
O medicamento Pomalidomida Glenmark contém a substância ativa "pomaldomida". Este medicamento é semelhante ao talidomida e pertence a um grupo de medicamentos que afetam o sistema imunológico (a defesa natural do organismo).
Para que é utilizado o medicamento Pomalidomida Glenmark
O medicamento Pomalidomida Glenmark é utilizado para tratar adultos com um tipo de cancro chamado "mieloma múltiplo".
O medicamento Pomalidomida Glenmark é utilizado em conjunto com:
- dois outros medicamentos- bortezomibe (um tipo de medicamento utilizado na quimioterapia) e dexametasona (um medicamento anti-inflamatório) em doentes que já receberam pelo menos um outro tipo de tratamento que contenha lenalidomida. ou
- um outro medicamento- dexametasona em doentes com mieloma múltiplo que se agravou, apesar de terem recebido pelo menos dois outros tipos de tratamento que contenham lenalidomida e bortezomibe.
O que é o mieloma múltiplo
O mieloma múltiplo é um tipo de cancro que ataca um tipo de glóbulos brancos (chamados células plasmáticas). Estas células crescem de forma descontrolada e acumulam-se na medula óssea, o que pode danificar os ossos e os rins.
Na prática, o mieloma múltiplo é incurável. No entanto, o tratamento pode aliviar os sintomas objetivos e subjetivos da doença ou fazer com que desapareçam por um período de tempo. Isto é designado por "resposta" ao tratamento.
Como funciona o medicamento Pomalidomida Glenmark
O medicamento Pomalidomida Glenmark funciona de várias maneiras:
- inibindo o crescimento das células do mieloma;
- estimulando o sistema imunológico para atacar as células cancerígenas;
- inibindo a formação de vasos sanguíneos que fornecem sangue às células cancerígenas.
Benefícios do tratamento com o medicamento Pomalidomida Glenmark e bortezomibe e dexametasona
O medicamento Pomalidomida Glenmark, quando utilizado em conjunto com bortezomibe e dexametasona, pode atrasar o crescimento do mieloma múltiplo:
- O medicamento Pomalidomida Glenmark utilizado com bortezomibe e dexametasona atrasou a recorrência do mieloma múltiplo por 11 meses - em comparação com 7 meses nos doentes que receberam apenas bortezomibe e dexametasona.
Benefícios do tratamento com o medicamento Pomalidomida Glenmark e dexametasona
O medicamento Pomalidomida Glenmark, quando utilizado em conjunto com dexametasona, pode atrasar o crescimento do mieloma múltiplo:
- O medicamento Pomalidomida Glenmark utilizado com dexametasona atrasou a recorrência do mieloma múltiplo por 4 meses - em comparação com 2 meses nos doentes que receberam apenas dexametasona.
2. Informações importantes antes de tomar o medicamento Pomalidomida Glenmark
Quando não tomar o medicamento Pomalidomida Glenmark
- se estiver grávida, se suspeitar que possa estar grávida ou se planeia ter um filho, pois é esperado que o medicamento Pomalidomida Glenmark seja prejudicial ao feto (os homens e as mulheres que tomam este medicamento devem ler a secção "Gravidez, contracepção e amamentação - informação para homens e mulheres" abaixo).
- se puder engravidar, a menos que utilize todos os métodos de contracepção necessários (ver secção "Gravidez, contracepção e amamentação - informação para homens e mulheres"). Se puder engravidar, o médico que prescreve o medicamento verificará que as medidas necessárias foram tomadas e fornecerá uma confirmação à paciente.
- se tiver alergia à pomalidomida ou a qualquer um dos outros componentes deste medicamento (listados na secção 6). Se suspeitar que tem alergia a este medicamento, deve consultar um médico para aconselhamento. Se não tiver a certeza se alguma das situações acima se aplica a si, deve consultar um médico, farmacêutico ou enfermeira antes de começar a tomar o medicamento Pomalidomida Glenmark.
Precauções e advertências
Antes de começar a tomar o medicamento Pomalidomida Glenmark, deve discutir com o seu médico, farmacêutico ou enfermeira se:
- alguma vez teve coágulos sanguíneos no passado. Durante o tratamento com o medicamento Pomalidomida Glenmark, existe um risco aumentado de formação de coágulos sanguíneos nos vasos sanguíneos e arteriais. O médico pode prescrever um tratamento adicional (por exemplo, warfarina) ou reduzir a dose do medicamento Pomalidomida Glenmark para diminuir o risco de formação de coágulos sanguíneos.
- alguma vez teve uma reação de hipersensibilidade, como erupções cutâneas, coceira, inchaço, tonturas ou dificuldades respiratórias ao tomar medicamentos semelhantes com os nomes "talidomida" e "lenalidomida".
- teve um ataque cardíaco, tem insuficiência cardíaca, tem dificuldades respiratórias ou é fumador, tem hipertensão ou níveis elevados de colesterol.
- tem lesões tumorais generalizadas no organismo, incluindo a medula óssea. Estas lesões podem levar a uma situação em que os tumores se desintegrem e ocorram níveis anormais de substâncias químicas, o que pode levar a insuficiência renal. O doente também pode experimentar alterações no ritmo cardíaco. Esta condição é designada por "síndrome de lise tumorale".
- tem ou teve neuropatia (dano nervoso que causa formigamento ou dor nas mãos ou pés).
- tem ou teve infecção por vírus da hepatite B. O tratamento com o medicamento Pomalidomida Glenmark pode reativar o vírus em doentes previamente infectados, levando a uma recorrência da infecção. O médico deve verificar se o doente foi previamente infectado com o vírus da hepatite B.
- teve ou tem algum dos seguintes sintomas: erupções cutâneas no rosto ou erupções cutâneas generalizadas, vermelhidão da pele, febre alta, sintomas semelhantes à gripe, linfonodos aumentados (sintomas de uma reação cutânea grave designada por "síndrome de hipersensibilidade a medicamentos" ou "reação adversa a medicamentos com eosinofilia e sintomas sistémicos" (DRESS) ou "síndrome de Stevens-Johnson" ou "necrólise epidérmica tóxica" (TEN)). Ver também a secção 4.
Deve lembrar que os doentes com mieloma múltiplo tratados com pomalidomida podem desenvolver outros tipos de cancro. Por isso, o médico responsável deve avaliar cuidadosamente os benefícios e riscos associados à prescrição deste medicamento ao doente.
Em qualquer momento do tratamento ou após o seu término, deve informar imediatamente o médico ou a enfermeira se ocorrerem:
- alterações na visão, perda de visão ou visão dupla;
- dificuldades em falar;
- fraqueza nos braços ou pernas;
- alterações na marcha ou problemas de equilíbrio;
- formigamento persistente, diminuição da sensibilidade ou perda de sensibilidade;
- perda de memória ou desorientação.
Estes sintomas podem indicar uma doença cerebral grave e potencialmente fatal designada por "leucoencefalopatia multifocal progressiva" (LMP). Se estes sintomas ocorreram antes de tomar o medicamento Pomalidomida Glenmark, deve informar o médico sobre qualquer alteração nos sintomas.
Após o término do tratamento, todas as cápsulas não utilizadas devem ser devolvidas à farmácia que as aceita.
Gravidez, contracepção e amamentação - informação para homens e mulheres
Como mencionado, durante o tratamento com o medicamento Pomalidomida Glenmark, devem ser seguidas as condições do programa de prevenção da gravidez.
As mulheres que tomam o medicamento Pomalidomida Glenmark não devem engravidar, e as parceiras dos homens tratados com pomalidomida também não devem engravidar, pois é esperado que o medicamento seja prejudicial ao feto. O doente e a sua parceira devem utilizar métodos de contracepção eficazes durante o tratamento com este medicamento.
Mulheres
Não deve tomar o medicamento Pomalidomida Glenmark se estiver grávida, se suspeitar que possa estar grávida ou se planeia ter um filho, pois é esperado que o medicamento seja prejudicial ao feto. Antes de começar o tratamento, a paciente deve informar o médico se pode engravidar, mesmo que considere isso improvável.
Se a paciente puder engravidar:
- deve utilizar métodos de contracepção eficazes durante pelo menos 4 semanas antes de começar o tratamento, durante todo o tratamento e pelo menos 4 semanas após o término do tratamento. A paciente deve discutir com o médico qual é o método de contracepção mais adequado para si.
- em cada prescrição do medicamento, o médico responsável verificará se a paciente entendeu todas as medidas necessárias para evitar a gravidez.
- o médico responsável prescreverá testes de gravidez antes do tratamento, não menos frequentemente do que a cada 4 semanas durante o tratamento e após pelo menos 4 semanas após o término do tratamento.
Se, apesar das medidas de prevenção, a paciente engravidar:
- deve interromper imediatamente o tratamento e informar o médico.
Amamentação
Não se sabe se o medicamento Pomalidomida Glenmark passa para o leite materno. Se a paciente estiver a amamentar ou planeia amamentar, deve informar o médico. O médico responsável informará a paciente se deve interromper ou continuar a amamentação.
Homens
O medicamento Pomalidomida Glenmark passa para o sêmen humano.
- Se a parceira do homem estiver grávida ou puder engravidar, o homem deve utilizar preservativos durante todo o tratamento e por 7 dias após o término do tratamento.
- Se a parceira do homem engravidar enquanto o homem estiver a tomar o medicamento Pomalidomida Glenmark, deve informar imediatamente o médico. A parceira também deve consultar um médico.
O doente não deve doar sêmen durante o tratamento e por 7 dias após o término do tratamento.
Doação de sangue e exames de sangue
Durante o tratamento e por 7 dias após o término do tratamento, o doente não deve doar sangue.
Antes e durante o tratamento com o medicamento Pomalidomida Glenmark, o médico responsável prescreverá regularmente exames de sangue ao doente. Isto é necessário porque o medicamento pode causar uma diminuição no número de glóbulos brancos (que ajudam a combater infecções) e uma diminuição no número de plaquetas (que ajudam a prevenir hemorragias).
O médico responsável prescreverá exames de sangue:
- antes do tratamento;
- semanalmente durante as primeiras 8 semanas de tratamento;
- após isso, pelo menos uma vez por mês, enquanto o doente estiver a tomar o medicamento Pomalidomida Glenmark.
O médico responsável pode alterar a dose do medicamento Pomalidomida Glenmark ou interromper o tratamento com base nos resultados dos exames de sangue do doente. O médico responsável também pode alterar a dose ou interromper o tratamento com base no estado geral de saúde do doente.
Crianças e adolescentes
O medicamento Pomalidomida Glenmark não é recomendado para uso em crianças e adolescentes com menos de 18 anos.
Pomalidomida Glenmark e outros medicamentos
Deve informar o médico, farmacêutico ou enfermeira sobre todos os medicamentos que está a tomar atualmente ou recentemente, bem como sobre qualquer medicamento que planeia tomar, pois o medicamento Pomalidomida Glenmark pode afetar a ação de outros medicamentos. Além disso, outros medicamentos podem afetar a ação do medicamento Pomalidomida Glenmark.
Antes de tomar o medicamento Pomalidomida Glenmark, deve informar o médico, farmacêutico ou enfermeira, em particular, se estiver a tomar algum dos seguintes medicamentos:
- alguns medicamentos antifúngicos, como o ketconazol;
- alguns antibióticos (por exemplo, ciprofloxacino, enoxacina);
- alguns medicamentos antidepressivos, como a fluvoxamina.
Condução de veículos e operação de máquinas
Durante o tratamento com o medicamento Pomalidomida Glenmark, algumas pessoas podem sentir fadiga, tonturas, desmaio, confusão ou diminuição da vigilância. Se ocorrerem estes sintomas, o doente não deve conduzir veículos, utilizar ferramentas ou operar máquinas.
O medicamento Pomalidomida Glenmark contém sódio
O medicamento contém menos de 1 mmol (23 mg) de sódio por cápsula, o que significa que o medicamento é considerado "sem sódio".
3. Como tomar o medicamento Pomalidomida Glenmark
O medicamento Pomalidomida Glenmark deve ser prescrito por um médico com experiência no tratamento de mieloma múltiplo.
Este medicamento deve ser sempre tomado de acordo com as instruções do médico. Se tiver alguma dúvida, deve consultar o médico, farmacêutico ou enfermeira.
Quando tomar o medicamento Pomalidomida Glenmark com outros medicamentos
Medicamento Pomalidomida Glenmark com bortezomibe e dexametasona
- Deve ler os folhetos de informação dos medicamentos bortezomibe e dexametasona para obter mais informações sobre a sua utilização e efeitos.
- O medicamento Pomalidomida Glenmark, bortezomibe e dexametasona são utilizados em ciclos de tratamento. Cada ciclo dura 21 dias (3 semanas).
- Deve ler a tabela abaixo para verificar quais medicamentos deve tomar em cada dia do ciclo de 3 semanas:
POM:Pomalidomida Glenmark; BOR: bortezomibe; DEX: dexametasona
Ciclos de 1 a 8 Ciclos de 9 e subsequentes
Nome do medicamento Nome do medicamento
Dia POM BOR DEX Dia POM BOR DEX
1
√
√
√
1
√
√
√
2
√
√
2
√
√
3
√
3
√
4
√
√
√
4
√
5
√
√
5
√
6
√
6
√
7
√
7
√
8
√
√
√
8
√
√
√
9
√
√
9
√
√
10
√
10
√
11
√
√
√
11
√
12
√
√
12
√
13
√
13
√
14
√
14
√
15
15
16
16
17
17
18
18
19
19
20
20
21
21
- Após o término de cada ciclo de 3 semanas, deve começar um novo ciclo.
Medicamento Pomalidomida Glenmark apenas com dexametasona
- Deve ler o folheto de informação do medicamento dexametasona para obter mais informações sobre a sua utilização e efeitos.
- O medicamento Pomalidomida Glenmark e dexametasona são utilizados em ciclos de tratamento. Cada ciclo dura 28 dias (4 semanas).
- Deve ler a tabela abaixo para verificar quais medicamentos deve tomar em cada dia do ciclo de 4 semanas:
POM:Pomalidomida Glenmark; DEX: dexametasona
Nome do medicamento
Dia POM DEX
1
√
√
2
√
3
√
4
√
5
√
6
√
7
√
8
√
√
9
√
10
√
11
√
12
√
13
√
14
√
15
√
√
16
√
17
√
18
√
19
√
20
√
21
√
22
√
23
24
25
26
27
28
- Após o término de cada ciclo de 4 semanas, deve começar um novo ciclo.
Qual é a dose do medicamento Pomalidomida Glenmark que deve tomar com outros medicamentos
Medicamento Pomalidomida Glenmark com bortezomibe e dexametasona
- A dose inicial recomendada do medicamento Pomalidomida Glenmark é de 4 mg por dia.
- A dose inicial recomendada do bortezomibe será determinada pelo médico com base no peso e altura do doente (1,3 mg/m² de área de superfície corporal).
- A dose inicial recomendada da dexametasona é de 20 mg por dia. No entanto, se o doente tiver mais de 75 anos, a dose inicial recomendada é de 10 mg por dia.
Medicamento Pomalidomida Glenmark apenas com dexametasona
- A dose do medicamento Pomalidomida Glenmark é de 4 mg por dia.
- A dose inicial recomendada da dexametasona é de 40 mg por dia. No entanto, se o doente tiver mais de 75 anos, a dose inicial recomendada é de 20 mg por dia.
O médico pode reduzir a dose do medicamento Pomalidomida Glenmark, bortezomibe ou dexametasona, ou interromper o tratamento com um ou mais destes medicamentos com base nos resultados dos exames de sangue do doente, no seu estado geral de saúde, na utilização de outros medicamentos (por exemplo, ciprofloxacino, enoxacina e fluvoxamina) e se ocorrerem efeitos secundários devido ao tratamento (em particular, erupções cutâneas ou inchaço).
Se o doente tiver doença renal ou hepática, o médico responsável verificará cuidadosamente o estado de saúde do doente durante o tratamento com este medicamento.
Como tomar o medicamento Pomalidomida Glenmark
- Não deve partir, abrir ou mastigar as cápsulas. Se o pó de uma cápsula danificada entrar em contato com a pele, deve lavar a pele imediatamente com sabão e água.
- O pessoal médico, os cuidadores e os membros da família devem utilizar luvas de borracha descartáveis ao manusear o blister ou a cápsula. As luvas devem ser removidas cuidadosamente para evitar a exposição da pele, colocadas em um saco plástico fechado e eliminadas de acordo com as regulamentações locais. Em seguida, deve lavar as mãos com sabão e água. As mulheres grávidas ou que suspeitam que possam estar grávidas não devem manusear o blister ou a cápsula.
- As cápsulas devem ser engolidas inteiras, com um pouco de água.
- As cápsulas podem ser tomadas com ou sem alimentos.
- As cápsulas devem ser tomadas mais ou menos à mesma hora todos os dias.
Para remover a cápsula do blister, deve pressionar a cápsula apenas de um lado e empurrá-la através da folha de alumínio. Não deve pressionar o centro da cápsula, pois isso pode danificá-la.
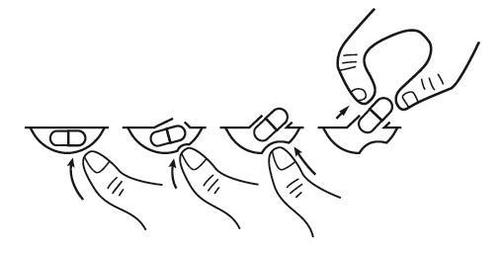
Se o doente tiver doença renal e estiver a fazer diálise, o médico aconselhará sobre como e quando tomar o medicamento Pomalidomida Glenmark.
Duração do tratamento com o medicamento Pomalidomida Glenmark
Deve continuar os ciclos de tratamento até que o médico decida interromper o tratamento.
Uso de uma dose maior do que a recomendada do medicamento Pomalidomida Glenmark
Se tomar uma dose maior do que a recomendada do medicamento Pomalidomida Glenmark, deve informar imediatamente o médico ou ir ao hospital. Deve levar o pacote do medicamento consigo.
Omissão de uma dose do medicamento Pomalidomida Glenmark
Se esquecer de tomar uma dose do medicamento Pomalidomida Glenmark no dia em que deve tomar, deve tomar a próxima cápsula de acordo com o esquema de dosagem estabelecido. Não deve tomar uma dose dupla para compensar a dose omitida.
Se tiver alguma dúvida adicional sobre a utilização deste medicamento, deve consultar o médico ou farmacêutico.
4. Efeitos secundários possíveis
Como qualquer medicamento, o medicamento Pomalidomida Glenmark pode causar efeitos secundários, embora não todos os doentes os experimentem.
Efeitos secundários graves
Se ocorrerem algum dos seguintes efeitos secundários graves, deve interromper o tratamento com o medicamento Pomalidomida Glenmark e consultar imediatamente o médico – pode ser necessário um tratamento imediato.
- febre, calafrios, dor de garganta, tosse, úlceras na boca ou qualquer outro sintoma de infecção (devido à diminuição do número de glóbulos brancos que ajudam a combater infecções)
- hemorragia ou hematomas sem causa aparente, incluindo hemorragia nasal, intestinal ou gástrica (devido ao efeito do medicamento nas células sanguíneas chamadas plaquetas)
- respiração rápida, pulsação rápida, febre e calafrios, produção de urina muito pequena ou ausência de urina, náuseas e vômitos, confusão, perda de consciência (devido a uma infecção sanguínea designada por septicemia ou choque séptico)
- diarreia grave, persistente ou com sangue (também com dor abdominal ou febre) causada por bactérias designadas por Clostridium difficile
- dor no peito ou dor nas pernas e inchaço, especialmente nas pernas e tornozelos (causados por coágulos sanguíneos)
- falta de ar (devido a infecções graves no peito, pneumonia, insuficiência cardíaca ou coágulos sanguíneos)
- inchaço da face, lábios, língua e garganta, que podem causar dificuldades respiratórias (devido a reações alérgicas graves designadas por angioedema e reação anafilática)
- alguns tipos de cancro de pele (carcinoma de células escamosas e carcinoma basocelular), que podem causar alterações na pele ou o crescimento de tumores na pele. Se o doente notar alguma alteração na pele enquanto estiver a tomar o medicamento Pomalidomida Glenmark, deve informar o médico o mais rápido possível.
- reação de reativação do vírus da hepatite B, que pode causar icterícia, urina escura, dor abdominal no lado direito, febre, náuseas e vômitos. Se o doente notar algum desses sintomas, deve consultar imediatamente o médico.
- erupções cutâneas generalizadas, febre alta, linfonodos aumentados e envolvimento de outros órgãos (erupção cutânea medicamentosa com eosinofilia e sintomas sistémicos, também designada por DRESS ou síndrome de hipersensibilidade a medicamentos, necrólise epidérmica tóxica ou síndrome de Stevens-Johnson). Se ocorrerem estes sintomas, deve interromper imediatamente o tratamento com o medicamento Pomalidomida Glenmark e consultar um médico ou procurar assistência médica imediatamente. Ver também a secção 2.
Se ocorrerem algum dos efeitos secundários graves acima, deve interromper o tratamento com o medicamento Pomalidomida Glenmark e consultar imediatamente o médico– pode ser necessário um tratamento imediato.
Outros efeitos secundários
Muito comuns(podem ocorrer em mais de 1 em cada 10 doentes):
- falta de ar (dispneia)
- infecções pulmonares (pneumonia e bronquite)
- infecções do nariz, seios e garganta causadas por bactérias ou vírus
- sintomas semelhantes à gripe (gripe)
- diminuição do número de glóbulos vermelhos, que pode causar anemia, levando a fadiga e fraqueza
- baixos níveis de potássio no sangue (hipocalemia), que podem causar fraqueza, cãibras musculares, dor muscular, palpitações, formigamento ou dormência, falta de ar, alterações de humor
- altos níveis de açúcar no sangue
- batimento cardíaco rápido e irregular (fibrilação atrial)
- perda de apetite
- constipação, diarreia ou náuseas
- vômitos
- dor abdominal
- fadiga
- dificuldades em dormir ou manter o sono
- tonturas, tremores
- cãibras musculares, fraqueza muscular
- dor óssea, dor nas costas
- formigamento, sensação de queimadura ou dor nas mãos ou pés (neuropatia periférica sensorial)
- inchaço do corpo, incluindo inchaço das mãos e pés
- erupções cutâneas
- infecção do trato urinário, que pode causar ardor ao urinar ou necessidade de urinar com frequência
Comuns(podem ocorrer em até 1 em cada 10 doentes):
- quedas
- hemorragia cerebral
- diminuição da capacidade de movimento ou sensação nas mãos, braços, pés e pernas devido a danos nos nervos (neuropatia periférica sensorial e motora)
- formigamento, coceira e sensação de queimadura na pele (parestesias)
- sensação de vertigem que dificulta manter a posição ereta e caminhar
- inchaço devido à retenção de líquidos
- urticária
- coceira na pele
- herpes zóster
- ataque cardíaco (dor no peito que se irradia para os braços, pescoço, mandíbula, suor, falta de ar, náuseas ou vômitos)
- dor no peito, infecção no peito
- hipertensão
- pancitopenia (diminuição do número de glóbulos vermelhos, glóbulos brancos e plaquetas), que pode causar fadiga, fraqueza, falta de ar e maior risco de infecções e hemorragias. O doente pode sentir-se cansado, fraco e ter dificuldades respiratórias.
- diminuição do número de linfócitos (um tipo de glóbulos brancos), frequentemente devido a uma infecção (linfopenia)
- baixos níveis de magnésio no sangue (hipomagnesemia), que podem causar fadiga, fraqueza geral, cãibras musculares, irritabilidade e levar a baixos níveis de cálcio no sangue (hipocalcemia), que podem causar formigamento ou dormência nas mãos, pés ou lábios, cãibras musculares, fraqueza muscular, tonturas, confusão
- baixos níveis de fosfato no sangue (hipofosfatemia), que podem causar fraqueza muscular e irritabilidade ou confusão
- altos níveis de cálcio no sangue (hipercalcemia), que podem causar lentidão dos reflexos e fraqueza muscular
- altos níveis de potássio no sangue, que podem causar arritmias cardíacas
- baixos níveis de sódio no sangue, que podem causar fadiga e confusão, tremores musculares, convulsões (ataques epilépticos) ou coma
- altos níveis de ácido úrico no sangue, que podem levar a gota
- hipotensão, que pode causar tonturas ou desmaio
- dor ou secura na boca
- alterações no paladar
- inchaço abdominal
- confusão
- depressão
- perda de consciência, desmaio
- turvação da visão (catarata)
- lesão renal
- incapacidade de urinar
- anormalidades nos exames de função hepática
- dor pélvica
- perda de peso
Menos comuns(podem ocorrer em até 1 em cada 100 doentes):
- acidente vascular cerebral
- hepatite, que pode causar coceira na pele, icterícia, urina clara, dor abdominal no lado direito, febre, náuseas e vômitos
- destruição de células tumorais, levando à liberação de substâncias tóxicas no sangue (síndrome de lise tumorale). Isso pode levar a problemas renais.
- hipotireoidismo, que pode causar fadiga, letargia, fraqueza muscular, batimento cardíaco lento, ganho de peso
Frequência desconhecida(não pode ser estimada a partir dos dados disponíveis):
- rejeição do transplante de órgão miąższowy (como coração ou fígado)
Notificação de efeitos secundários
Se ocorrerem algum efeito secundário, incluindo qualquer efeito secundário não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeira. Os efeitos secundários podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Secundários de Medicamentos da Agência Reguladora de Medicamentos:
Al. Jerozolimskie 181C, 02-222 Varsóvia
telefone: +48 22 49 21 301, fax: +48 22 49 21 309
site da internet: https://smz.ezdrowie.gov.pl
Os efeitos secundários também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos secundários pode ajudar a obter mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Pomalidomida Glenmark
O medicamento deve ser conservado em um local seguro e fora do alcance das crianças.
Não deve utilizar este medicamento após o término da validade impresso no blister e na caixa de cartão após EXP. A data de validade é o último dia do mês indicado.
Não há requisitos especiais para a conservação do medicamento.
Não deve utilizar o medicamento Pomalidomida Glenmark se notar qualquer dano ou sinal de abertura do pacote.
Os medicamentos não devem ser jogados na canalização ou nos lixeiras domésticas. Após o término do tratamento, todas as cápsulas não utilizadas devem ser devolvidas à farmácia que as aceita. Este procedimento ajudará a proteger o meio ambiente.
6. Conteúdo do pacote e outras informações
O que contém o medicamento Pomalidomida Glenmark
- A substância ativa é a pomalidomida.
- Os outros componentes são celulose microcristalina, maltodextrina e estearato de sódio.
Pomalidomida Glenmark, 1 mg, cápsulas duras:
- Cada cápsula contém 1 mg de pomalidomida.
- A cápsula contém: gelatina, dióxido de titânio (E 171), óxido de ferro amarelo (E 172), óxido de ferro vermelho (E 172) e tinta branca.
- A tinta de impressão contém: lacas, dióxido de titânio (E 171), propilenoglicol.
Pomalidomida Glenmark, 2 mg, cápsulas duras:
- Cada cápsula contém 2 mg de pomalidomida.
- A cápsula contém: gelatina, dióxido de titânio (E 171), óxido de ferro amarelo (E 172), óxido de ferro vermelho (E 172) e tinta branca.
- A tinta de impressão contém: lacas, dióxido de titânio (E 171), propilenoglicol.
Pomalidomida Glenmark, 3 mg, cápsulas duras:
- Cada cápsula contém 3 mg de pomalidomida.
- A cápsula contém: gelatina, dióxido de titânio (E 171), óxido de ferro amarelo (E 172), óxido de ferro vermelho (E 172), índigo carmim (E 132) e tinta branca.
- A tinta de impressão contém: lacas, dióxido de titânio (E 171), propilenoglicol.
Pomalidomida Glenmark, 4 mg, cápsulas duras:
- Cada cápsula contém 4 mg de pomalidomida.
- A cápsula contém: gelatina, dióxido de titânio (E 171), óxido de ferro amarelo (E 172), óxido de ferro vermelho (E 172), índigo carmim (E 132), eritrosina (E 127) e tinta branca.
- A tinta de impressão contém: lacas, dióxido de titânio (E 171), propilenoglicol.
Como é o medicamento Pomalidomida Glenmark e que contenções o pacote tem
O medicamento Pomalidomida Glenmark 1 mg cápsulas duras (cápsulas): cápsula dura de gelatina com corpo amarelo e tampa vermelha, com impressão branca "PLM 1" ao longo do eixo do corpo da cápsula.
O medicamento Pomalidomida Glenmark 2 mg cápsulas duras (cápsulas): cápsula dura de gelatina com corpo laranja e tampa vermelha, com impressão branca "PLM 2" ao longo do eixo do corpo da cápsula.
O medicamento Pomalidomida Glenmark 3 mg cápsulas duras (cápsulas): cápsula dura de gelatina com corpo turquesa e tampa vermelha, com impressão branca "PLM 3" ao longo do eixo do corpo da cápsula.
O medicamento Pomalidomida Glenmark 4 mg cápsulas duras (cápsulas): cápsula dura de gelatina com corpo azul escuro e tampa vermelha, com impressão branca "PLM 4" ao longo do eixo do corpo da cápsula.
Tamanhos de embalagem disponíveis:
Cada embalagem contém 14, 21 ou 21x1 cápsulas em uma caixa de cartão.
Nem todos os tamanhos de embalagem podem estar disponíveis.
Titular da autorização de comercialização
Glenmark Pharmaceuticals s.r.o.
Hvězdova 1716/2b
140 78 Praga 4
República Checa
Fabricante
Glenmark Pharmaceuticals s.r.o.
Fibichova 143
566 17 Vysoké Mýto
República Checa
Synthon Hispania S.L.
Calle De Castello 1
Sant Boi De Liobregat
08830 Barcelona
Espanha
Synthon B.V.
Microweg 22
Nijmegen
6545 CM Gelderland
Países Baixos
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu sob os seguintes nomes:
| Estado membro | Nome do medicamento |
| Países Baixos | Pomalidomida Glenmark 1 mg cápsulas duras Pomalidomida Glenmark 2 mg cápsulas duras Pomalidomida Glenmark 3 mg cápsulas duras Pomalidomida Glenmark 4 mg cápsulas duras |
| Dinamarca | Pomalidomida Glenmark |
| Finlândia | Pomalidomida Glenmark |
| Itália | Pomalidomida Glenmark 1 mg cápsulas duras Pomalidomida Glenmark 2 mg cápsulas duras Pomalidomida Glenmark 3 mg cápsulas duras Pomalidomida Glenmark 4 mg cápsulas duras |
| Noruega | Pomalidomida Glenmark |
| Polônia | Pomalidomida Glenmark |
| Suécia | Pomalidomida Glenmark |
Para obter mais informações sobre este medicamento, deve contactar o representante local do titular da autorização de comercialização:
Glenmark Pharmaceuticals Sp. z o. o.
ul. Dziekońskiego 3
00-728 Varsóvia
Email: [email protected]
Data da última revisão do folheto:
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorGlenmark Pharmaceuticals s.r.o. Synthon B.V. Synthon Hispania S.L.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Pomalidomide GlenmarkForma farmacêutica: Cápsulas, 3 mgSubstância ativa: pomalidomideRequer receita médicaForma farmacêutica: Cápsulas, 4 mgSubstância ativa: pomalidomideRequer receita médicaForma farmacêutica: Cápsulas, 2 mgSubstância ativa: pomalidomideRequer receita médica
Alternativas a Pomalidomide Glenmark noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Pomalidomide Glenmark em Hiszpania
Alternativa a Pomalidomide Glenmark em Ukraina
Médicos online para Pomalidomide Glenmark
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Pomalidomide Glenmark – sujeita a avaliação médica e regras locais.






