
Fragmin

Pergunte a um médico sobre a prescrição de Fragmin

Como usar Fragmin
Folheto informativo para o doente
FRAGMIN
2 500 UI anti-Xa/0,2 ml, solução para injeção
FRAGMIN
5 000 UI anti-Xa/0,2 ml, solução para injeção
FRAGMIN
7 500 UI anti-Xa/0,3 ml, solução para injeção
FRAGMIN
10 000 UI anti-Xa/0,4 ml, solução para injeção
FRAGMIN
12 500 UI anti-Xa/0,5 ml, solução para injeção
FRAGMIN
15 000 UI anti-Xa/0,6 ml, solução para injeção
FRAGMIN
18 000 UI anti-Xa/0,72 ml, solução para injeção
Dalteparina sódica
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder reler se necessário.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode ser prejudicial para outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento Fragmin e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Fragmin
- 3. Como tomar o medicamento Fragmin
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Fragmin
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Fragmin e para que é utilizado
O Fragmin é um medicamento anticoagulante, na forma de dalteparina sódica. A dalteparina sódica é
uma heparina de baixo peso molecular. A ação anticoagulante da dalteparina está relacionada com a sua
capacidade de potenciar a inibição do fator Xa e da trombina.
O medicamento Fragmin é indicado para uso em doentes adultos com mais de 18 anos em:
- Tratamento da trombose venosa profunda aguda.
- Doença coronária instável (por exemplo, angina de peito de repouso, infarto do miocárdio sem bloqueio Q).
- Tratamento crónico da doença venosa tromboembólica sintomática (trombose venosa profunda proximal e embolia pulmonar) com o objetivo de reduzir a recorrência da doença tromboembólica em doentes com cancro.
- Prevenção da coagulação sanguínea em circulação extracorpórea, por exemplo, durante a hemodiálise e a hemofiltrção na insuficiência renal aguda ou crónica.
- Prevenção da trombose associada a cirurgia.
- Prevenção da trombose em doentes imobilizados por razões médicas: com insuficiência cardíaca congestiva na classe III ou IV da NYHA ou insuficiência respiratória aguda, com infecção aguda, com doença reumática aguda ou doença inflamatória intestinal aguda e pelo menos um fator de risco adicional para a trombose venosa profunda, por exemplo, idade superior a 75 anos, obesidade, cancro, história de trombose venosa profunda.
O medicamento Fragmin é indicado para uso em crianças a partir de 1 mês de idade em:
- Tratamento da trombose sanguínea nos vasos (doença venosa tromboembólica (DVT)) em crianças e jovens a partir de 1 mês de idade.
2. Informações importantes antes de tomar o medicamento Fragmin
Quando não tomar o medicamento Fragmin
- se o doente tiver alergia à dalteparina sódica ou a outra heparina de baixo peso molecular, ou heparina não fracionada, ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6);
- mais de 100 000/µl ou mm3;
- sangramento ativo, por exemplo, gastrointestinal ou cerebral;
- distúrbios da coagulação com curso grave;
- endocardite bacteriana aguda ou subaguda;
- lesões recentes ou cirurgia no sistema nervoso central, olhos e/ou ouvidos. Devido ao risco aumentado de sangramento, não devem ser administradas doses elevadas de dalteparina sódica (por exemplo, doses utilizadas no tratamento da trombose venosa profunda, embolia pulmonar ou doença coronária instável) a doentes que tenham sido submetidos a anestesia espinhal ou epidural, ou a outros procedimentos que exijam punção lombar.
Precauções e advertências
Antes de iniciar o tratamento com o medicamento Fragmin, deve discutir com o médico ou farmacêutico.
- Nos doentes antes da anestesia espinhal (epidural ou subaracnoide) ou punção lombar. Os doentes que recebem medicamentos anticoagulantes, como heparinas de baixo peso molecular ou heparinoides, para prevenir complicações tromboembólicas, estão em risco de desenvolver um hematoma epidural ou subaracnoide, que pode causar paralisia prolongada ou permanente. O risco de tais complicações aumenta se forem introduzidos cateteres permanentes no espaço epidural para administração de medicamentos anestésicos e se forem administrados medicamentos que afetam a hemostase, como anti-inflamatórios não esteroides, inibidores da agregação plaquetária e outros medicamentos anticoagulantes. Parece que a punção traumática ou repetida do espaço epidural ou lombar também aumenta o risco. Os doentes devem ser monitorizados, verificando frequentemente o seu estado, tendo em conta os sintomas objetivos e subjetivos que indiciam alterações neurológicas. Nos doentes com:
Troca de medicamentos
A dalteparina não pode ser utilizada como substituto (unidade por unidade) da heparina não fracionada,
outras heparinas de baixo peso molecular ou polissacarídeos sintéticos. Cada um desses medicamentos
difere no que respeita às matérias-primas utilizadas, processo de fabrico e propriedades físico-químicas,
biológicas e clínicas, o que leva a diferenças na dosagem, e possivelmente também na eficácia clínica e
segurança. Cada um desses medicamentos é único e exige que sejam seguidas as instruções individuais
do médico para a sua administração.
Crianças
O medicamento Fragmin não deve ser utilizado em recém-nascidos com menos de 1 mês de idade.
Interacções com outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou
recentemente, bem como sobre os medicamentos que planeia tomar.
Alguns medicamentos podem afetar a ação do medicamento Fragmin, bem como o Fragmin pode
reduzir a eficácia de outros medicamentos tomados ao mesmo tempo.
O tratamento trombolítico (dissolvente de coágulos) ou alguns medicamentos que afetam a coagulação
sanguínea podem aumentar o risco de sangramento se forem administrados com o medicamento Fragmin:
- aspirina (ácido acetilsalicílico);
- medicamentos que inibem a agregação plaquetária (utilizados para reduzir a agregação das plaquetas sanguíneas e diminuir o risco de formação de coágulos sanguíneos);
- medicamentos trombolíticos (utilizados para dissolver coágulos sanguíneos);
- anti-inflamatórios não esteroides (AINE) (medicamentos utilizados no tratamento de condições inflamatórias);
- antagonistas dos receptores GP IIb/IIIa (medicamentos que afetam a agregação plaquetária, utilizados no tratamento de doenças cardíacas);
- antagonistas da vitamina K e outros tipos de medicamentos anticoagulantes;
- dextrans (utilizados em algumas lágrimas artificiais).
Medicamentos que aumentam a ação do medicamento Fragmin:
- medicamentos utilizados para diluir o sangue (dipiridamol);
- alguns medicamentos utilizados no tratamento da gota (por exemplo, sulfinpirazon, probenecida);
- alguns medicamentos diuréticos (por exemplo, ácido etacrínico);
- soluções administradas para aumentar o volume sanguíneo;
- medicamentos citostáticos (utilizados no tratamento do cancro).
Medicamentos que podem reduzir a ação do medicamento Fragmin:
- medicamentos utilizados no tratamento de alergias e resfriados (por exemplo, medicamentos antihistamínicos);
- medicamentos utilizados no tratamento da insuficiência cardíaca e doenças cardiovasculares (por exemplo, medicamentos que contenham digital, como a digoxina, digitoxina);
- antibióticos da classe das tetraciclinas, utilizados no tratamento de infecções bacterianas;
- vitamina C (por exemplo, contida em medicamentos vitamínicos).
Outros medicamentos que podem afetar a ação do medicamento Fragmin:
- medicamentos utilizados no tratamento da angina de peito (por exemplo, nitroglicerina administrada por via intravenosa);
- antibióticos, como as penicilinas administradas em doses elevadas, utilizados no tratamento de infecções bacterianas;
- medicamentos utilizados na prevenção e tratamento da malária (por exemplo, quinina);
- nicotina ingerida devido ao tabagismo ou preparados que facilitam a cessação do tabagismo.
Deve lembrar que, se o doente estiver a ser tratado com o medicamento Fragmin devido a doença coronária instável, o médico pode ajustar a dose de ácido acetilsalicílico (aspirina).
As recomendações de dosagem para crianças baseiam-se em experiências clínicas; os dados provenientes
de estudos clínicos são demasiado limitados para que o médico possa ajustar a dose adequada de medicamento Fragmin.
Gravidez, amamentação e fertilidade
Se a paciente estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planeiar ter um filho,
deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Gravidez
O medicamento deve ser utilizado durante a gravidez apenas se for absolutamente necessário.
Amamentação
Quantidades pequenas de dalteparina sódica passam para o leite materno. Não se pode excluir o risco
para as crianças amamentadas. O medicamento Fragmin deve ser utilizado durante a amamentação,
tendo em conta os benefícios da amamentação para a criança e os benefícios da terapêutica para a mãe.
Fertilidade
Não há dados que indiquem um efeito do medicamento Fragmin na fertilidade.
Condução de veículos e utilização de máquinas
O Fragmin não afeta a capacidade de conduzir veículos ou utilizar máquinas.
O medicamento Fragmin contém sódio
O Fragmin 2 500 UI anti-Xa/0,2 ml, Fragmin 5 000 UI anti-Xa/0,2 ml, Fragmin 7 500 UI anti-Xa/0,3 ml,
Fragmin 10 000 UI anti-Xa/0,4 ml, Fragmin 12 500 UI anti-Xa/0,5 ml, Fragmin 15 000 UI anti-Xa/0,6 ml
e Fragmin 18 000 UI anti-Xa/0,72 ml contêm menos de 1 mmol (23 mg) de sódio por seringa pré-cheia,
ou seja, os medicamentos são considerados «livres de sódio». Os doentes em dieta com baixo teor de sódio
e os pais cujos filhos estão a ser tratados com o medicamento Fragmin podem ser informados de que
estes medicamentos são essencialmente «livres de sódio».
Este medicamento pode ser diluído com soluções que contenham sódio . Deve informar o médico se o doente
ou a criança está em dieta com baixo teor de sódio.
3. Como tomar o medicamento Fragmin
Este medicamento deve ser sempre utilizado de acordo com as instruções do médico ou farmacêutico.
Em caso de dúvida, deve consultar o médico ou farmacêutico.
O medicamento Fragmin é administrado por via subcutânea, intravenosa ou extracorpórea (no circuito
de diálise).
Não administrar o medicamento Fragmin por via intramuscular.
No tratamento da trombose sanguínea, o medicamento Fragmin é administrado por via subcutânea.
Se o doente estiver a ser submetido a diálise ou hemofiltração (processos utilizados para purificar o
sangue), o medicamento Fragmin é administrado por via intravenosa ou para o tubo de diálise.
A dalteparina pode ser misturada com solução isotónica de cloreto de sódio (9 mg/ml) ou glicose
(50 mg/ml) em frascos de vidro e recipientes de plástico.
Dosagem e modo de administração Tratamento da trombose venosa profunda aguda
O medicamento Fragmin pode ser administrado por via subcutânea uma ou duas vezes por dia.
Durante o tratamento com o medicamento Fragmin, pode ser iniciada a administração concomitante de
antagonistas da vitamina K. O medicamento Fragmin é administrado até que os níveis dos factores da
coagulação (factores: II, VII, IX, X) diminuam para um nível terapêutico. Isso ocorre geralmente após
cerca de 5 dias de tratamento combinado. É possível o tratamento ambulatorial com as mesmas doses
utilizadas no hospital.
- A dose de 200 UI/kg de peso corporal por via subcutânea uma vez por dia. Não é necessário o
monitorização da ação anticoagulante. Não deve ser administrada uma dose única diária superior a
18 000 UI.
Administração uma vez por dia
A dose de 200 UI/kg de peso corporal por via subcutânea uma vez por dia. A monitorização da ação
anticoagulante não é necessária. Não deve ser administrada uma dose única diária superior a 18 000 UI.
A dosagem com seringa pré-cheia de uso único pode ser determinada com base na tabela abaixo.
| Peso corporal (kg) | Dose |
| 10 000 UI |
| 12 500 UI |
| 15 000 UI |
| 83 e mais | 18 000 UI |
Administração duas vezes por dia
Alternativamente, pode ser utilizada uma dose de 100 UI/kg de peso corporal por via subcutânea duas
vezes por dia. Geralmente, não é necessário o monitorização da ação anticoagulante, mas deve ser
considerada em doentes especiais (ver ponto 2: Precauções e advertências). O sangue deve ser
coletado no momento do pico da concentração plasmática do medicamento (3 a 4 horas após a injeção
subcutânea). As concentrações plasmáticas recomendadas variam entre 0,5 e 1,0 UI anti-Xa/ml.
Prevenção da coagulação sanguínea em circulação extracorpórea, por exemplo, durante a hemodiálise e a hemofiltrção na insuficiência renal aguda ou crónica
O medicamento Fragmin deve ser administrado para o linha arterial do aparelho de diálise ou por via
intravenosa, escolhendo o esquema de dosagem mais adequado abaixo descrito.
- Doentes com insuficiência renal crónica e sem risco aumentado de sangramentoNesses doentes, geralmente são necessários ajustes pequenos na dose, por isso não é necessário o monitorização frequente da atividade anti-Xa. Em doentes com:
Prevenção da trombose associada a cirurgia
O medicamento Fragmin deve ser administrado por via subcutânea. A monitorização da ação anticoagulante
geralmente não é necessária. Se for realizada a monitorização, o sangue deve ser coletado no momento
do pico da concentração plasmática do medicamento (3 a 4 horas após a injeção subcutânea). As
concentrações plasmáticas recomendadas variam entre 0,1 e 0,4 UI anti-Xa/ml.
Cirurgia geral
Deve ser escolhida a dosagem adequada entre as abaixo indicadas.
- Doentes com risco de complicações tromboembólicas2 500 UI por via subcutânea 2 horas antes da cirurgia e 2 500 UI por via subcutânea todas as manhãs após a cirurgia até que o doente seja mobilizado (geralmente por 5 a 7 dias ou mais).
- Doentes com fatores de risco adicionais para complicações tromboembólicas (por exemplo, cancro)Administrar o medicamento Fragmin até que o doente seja mobilizado (geralmente por 5 a 7 dias ou mais).
- 1. Início da administração do medicamento no dia anterior à cirurgia: 5 000 UI por via subcutânea à noite antes da cirurgia. Após a cirurgia, administrar 5 000 UI por via subcutânea todas as noites.
- 2. Início da administração do medicamento no dia da cirurgia: 2 500 UI por via subcutânea 2 horas antes da cirurgia e 2 500 UI por via subcutânea 8 a 12 horas depois, mas não antes de 4 horas após o fim da cirurgia. Após a cirurgia, a partir do dia seguinte, administrar 5 000 UI por via subcutânea todas as manhãs.
Prevenção da trombose venosa profunda aguda em doentes imobilizados por razões médicas
A dose recomendada de medicamento Fragmin é de 5 000 UI uma vez por dia. O tratamento com dalteparina
sódica é realizado até ao fim do período de imobilização do doente, por 14 dias ou mais. A monitorização
da ação anticoagulante geralmente não é necessária.
Duração do tratamento
A prevenção da trombose em doentes com risco significativamente aumentado de tromboembolia, temporariamente imobilizados devido a doença grave, como insuficiência cardíaca, insuficiência respiratória ou infecção grave, deve ser realizada até que o doente seja completamente mobilizado. O período de tratamento é determinado com base no estado do doente e geralmente dura 14 dias.
Modo de administração
A gota no final da agulha deve ser removida antes da injeção, pois a entrada da dalteparina sódica no
cano da injeção pode causar um hematoma superficial ou, raramente, irritação local.
Para saber como administrar o medicamento, ver abaixo Como administrar o medicamento Fragmin
Fragmin. Doença coronária instável (angina de peito instável e infarto do miocárdio sem bloqueio Q)
Geralmente, não é necessário o monitorização da ação anticoagulante, mas deve ser considerada em
doentes especiais (ver ponto 2: Precauções e advertências). O sangue deve ser coletado no momento
do pico da concentração plasmática do medicamento (3 a 4 horas após a injeção subcutânea). As
concentrações plasmáticas recomendadas variam entre 0,5 e 1,0 UI anti-Xa/ml. Recomenda-se a
administração concomitante de ácido acetilsalicílico (em dose de 75 a 325 mg/dia). Administrar o
medicamento Fragmin na dose de 120 UI/kg de peso corporal por via subcutânea a cada 12 horas até
uma dose máxima de 10 000 UI/12 horas. Continuar o tratamento até que o estado clínico do doente
se estabilize (geralmente por pelo menos 6 dias) ou mais tempo, se o médico considerar necessário. Em
seguida, recomenda-se o tratamento prolongado com a dose fixa de medicamento Fragmin até que seja
realizada a revascularização (por exemplo, intervenções percutâneas ou pontagem de arteria coronária).
O medicamento não deve ser administrado por mais de 45 dias. A dose de medicamento Fragmin é
determinada com base no sexo e peso corporal do doente.
- Nas mulheres com peso corporal inferior a 80 kg e nos homens com peso corporal inferior a 70 kg, deve
ser administrada uma dose de 5 000 UI por via subcutânea a cada 12 horas. - Nas mulheres com peso corporal igual ou superior a 80 kg e nos homens com peso corporal igual ou
superior a 70 kg, deve ser administrada uma dose de 7 500 UI por via subcutânea a cada 12 horas.
Tratamento crónico da doença venosa tromboembólica sintomática (trombose venosa profunda proximal e embolia pulmonar) com o objetivo de reduzir a recorrência da doença tromboembólica em doentes com cancro
Mês 1
Durante os primeiros 30 dias de tratamento, o medicamento Fragmin deve ser administrado uma vez por
dia, por via subcutânea, na dose de 200 UI/kg de peso corporal. A dose diária total não deve exceder
18 000 UI.
Meses 2-6
O medicamento Fragmin deve ser administrado uma vez por dia, por via subcutânea, na dose de cerca
de 150 UI/kg de peso corporal. O tamanho da dose do medicamento administrado com a seringa
pré-cheia de uso único é determinado com base na tabela abaixo.
Ajuste da dose em caso de trombocitopenia induzida pela quimioterapia
Nos estudos clínicos, foram utilizados os seguintes princípios de dosagem:
Em caso de trombocitopenia induzida pela quimioterapia com contagem de plaquetas inferior a 50 000/
mm3, deve ser suspensa a administração do medicamento Fragmin até que a contagem de plaquetas retorne a um valor superior a 50 000/mm3. Se a contagem de plaquetas estiver entre 50 000 e 100 000/mm3, a dose do medicamento Fragmin deve ser reduzida em 17% a 33% da dose inicial (com base no peso corporal do doente). Quando a contagem de plaquetas retornar a um valor ≥ 100 000/mm3, deve ser retomada a dose completa do medicamento Fragmin.
Tabela 1. Redução da dose do medicamento Fragmin em caso de trombocitopenia entre 50 000 – 100 000/mm3, dosagem com seringas pré-cheias de uso único
Insuficiência renal
Em caso de insuficiência renal grave definida como uma concentração de creatinina superior a 3 vezes o
limite superior da normalidade, a dose do medicamento Fragmin deve ser ajustada para manter a concentração terapêutica de anti-Xa em 1 UI/ml (faixa 0,5-1,5 UI/ml), medida 4-6 horas após a injeção. Se a concentração de anti-Xa estiver abaixo ou acima da faixa terapêutica, a dose do medicamento Fragmin deve ser aumentada ou reduzida, respectivamente. A determinação da concentração de anti-Xa deve ser repetida após a administração de 3-4 injeções na dose ajustada. Este esquema de ajuste da dose deve ser repetido até que a concentração de anti-Xa atinja o valor terapêutico.
| Peso corporal (kg) | Dose do medicamento Fragmin (UI) |
| ≤56 | 7 500 |
| 10 000 |
| 12 500 |
| 15 000 |
| ≥99 | 18 000 |
| Peso corporal (kg) | Dose planeada do medicamento Fragmin (UI) | Dose reduzida do medicamento Fragmin (UI) | Redução média da dose (%) |
| ≤56 | 7 500 | 5 000 | 33 |
| 10 000 | 7 500 | 25 |
| 12 500 | 10 000 | 20 |
| 15 000 | 12 500 | 17 |
| ≥99 | 18 000 | 15 000 | 17 |
Uso em crianças e jovens
Tratamento da trombose sanguínea nos vasos (doença venosa tromboembólica (DVT))
As doses recomendadas dependem do peso corporal e da idade da criança e serão calculadas pelo
médico. O médico informará sobre a dose individualizada do medicamento Fragmin com base nesses
critérios. Não deve alterar a dosagem e o esquema de tratamento sem consultar o médico.
Abaixo estão indicadas as doses iniciais recomendadas para crianças e jovens com base na sua idade:
Crianças com idade entre 1 mês e menos de 2 anos:150 UI/kg de peso corporal duas vezes por dia.
Crianças com idade entre 2 anos e menos de 8 anos:125 UI/kg de peso corporal duas vezes por dia.
Crianças com idade entre 8 anos e menos de 18 anos:100 UI/kg de peso corporal duas vezes por dia.
A ação do medicamento Fragmin é monitorizada após a administração da dose inicial e, em seguida, a dose
será ajustada com base nos resultados dos exames de sangue.
Como administrar o medicamento Fragmin
O medicamento Fragmin é administrado por via subcutânea. Nesta parte do folheto, é explicado como
administrar o medicamento Fragmin a si mesmo ou à sua criança. Deve seguir estas instruções apenas
após ter sido treinado pelo médico. Se tiver alguma dúvida sobre o que fazer, deve contactar imediatamente
o médico. Deve injetar (administrar) a dose do medicamento Fragmin nos horários do dia recomendados
pelo médico.
Se for necessário diluir o medicamento Fragmin antes da administração às crianças, deve ser feito por
pessoal médico qualificado. Deve seguir as instruções do médico sobre como e quando administrar o
medicamento diluído.
Deve realizar as seguintes ações
Passo 1: Preparação da seringa pré-cheia para a injeção do medicamento Fragmin.
Deve remover a tampa da seringa pré-cheia. Na seringa pré-cheia, aparecerá uma bolha de ar. Deve
ignorá-la. É importante não pressionar o êmbolo antes da injeção, pois parte do medicamento pode ser
perdida. A seringa pré-cheia está pronta para a injeção. Deve passar para o passo 2.
Seringa pré-cheia com sistema de segurança para a agulha Needle-Trap
O sistema de segurança para a agulha Needle-Trap foi projetado para evitar que a agulha seja removida
após a administração correta do medicamento Fragmin. Consiste em um dispositivo de plástico de
segurança fixado à etiqueta da seringa. Serve para evitar picadas acidentais após a administração correta
do medicamento Fragmin. O sistema de segurança para a agulha Needle-Trap consiste em uma aba de
plástico (manípulo) disposta paralelamente à agulha, fixada firmemente à etiqueta do cilindro da seringa.
Para ativar o sistema de segurança, deve:
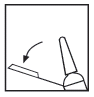
Deve levantar a seringa, segurar a extremidade do manípulo de plástico da agulha e afastá-lo da capa (ver
Fig. 1).
Fig. 1
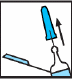
Deve remover a tampa de borracha azul da agulha, puxando-a com um movimento reto (ver Fig. 2).
Fig. 2
Na seringa pré-cheia, pode ser observada uma bolha de ar. Deve ignorá-la. É importante não pressionar
o êmbolo antes da injeção, pois parte do medicamento pode ser perdida. As bolhas de ar nas seringas
pré-cheias de uso único não devem ser expulsas antes da injeção, pois isso pode levar à perda de
medicamento e, consequentemente, à redução da dose. A seringa pré-cheia está pronta para a injeção.
Deve passar para o passo 2.
Passo 2: Escolha e preparação do local da injeção subcutânea
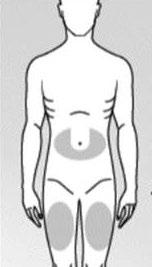
Deve escolher um dos locais de injeção recomendados abaixo (ver áreas sombreadas na Fig. 3):
Área em forma de «U» ao redor do umbigo.
Lado do meio da coxa.
Fig. 3
- Cada vez que administrar a dose, deve injetá-la em um local diferente.
- Não deve injetar em locais onde a pele esteja sensível, com hematomas, vermelha ou dura. Deve evitar
áreas com cicatrizes. - Se a pessoa adulta ou a criança tiver psoríase, não deve injetar o medicamento diretamente em nenhuma
placa elevada, grossa, vermelha ou descamativa na pele (lesões de psoríase). - Deve lavar e secar as mãos.
- Deve limpar o local da injeção com um novo cotonete embebido em álcool, fazendo movimentos circulares.
A pele deve estar completamente seca. Não deve tocar novamente nessa área antes de fazer a injeção.
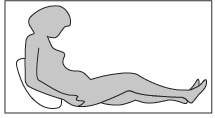
Passo 3: Adotar a posição correta
O adulto ou a criança deve sentar-se ou deitar-se para a injeção subcutânea profunda. Se o doente estiver
a administrar a injeção a si mesmo, deve sentar-se em uma posição confortável, de modo a poder ver
a sua barriga (ver Fig. 4).
Fig. 4
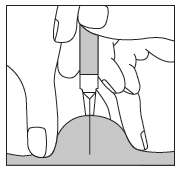
Passo 4:
Com o polegar e o dedo indicador, deve segurar uma dobra da pele com uma mão. Com a outra mão, deve
segurar a seringa como se fosse um lápis. Este será o local da injeção.
Passo 5:
Quando administrar o medicamento Fragmin a um adulto ou a si mesmo, deve segurar a seringa
pré-cheia sobre a dobra da pele, em ângulo reto (ou seja, verticalmente, como no esquema, e não em
ângulo). Deve inserir a agulha na pele até que a agulha seja completamente introduzida (ver Fig. 5).
Fig. 5
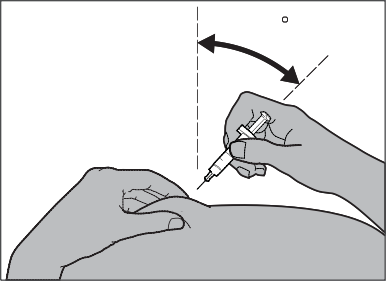
Quando administrar o medicamento Fragmin a uma criança, deve inserir a agulha na pele com um
movimento rápido e curto, em ângulo de 45° a 90° (ver Fig. 6).
Fig. 6
Passo 6:
Deve pressionar o êmbolo até o final com um movimento lento e constante, para administrar a dose
correta. Durante a injeção, deve continuar a segurar a dobra da pele e, em seguida, soltá-la e retirar a
agulha.
Se houver sangramento no local da injeção, deve aplicar uma pressão suave. Não deve friccionar o local
da injeção, pois isso pode causar hematomas. Deve aplicar um cotonete no local da injeção por 10
segundos. Pode ocorrer um sangramento leve. Não deve friccionar o local da injeção. O local da injeção
pode ser coberto com um curativo.
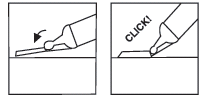
| Passo 6: Se a seringa tiver um sistema de segurança para a agulha, deve ativar a segurança da agulha | |
| agulha | |
| Deve colocar o manípulo de plástico sobre uma superfície dura e estável e, com uma mão, girar o cilindro da seringa para cima, na direção da agulha, empurrando a agulha para a capa, onde ficará bloqueada no seu lugar (ver Fig. 7 | |
| Deve continuar a dobrar a agulha até que a seringa ultrapasse um ângulo de 45 graus com a superfície plana, para que fique permanentemente inutilizada (ver Fig. 8 | |
Fig. 7 Fig. 8
Passo 7:
Deve descartar a seringa pré-cheia e a agulha no recipiente para objetos perfurantes. Deve manter o
recipiente para objetos perfurantes em um local inacessível a outras pessoas. Quando o recipiente para
objetos perfurantes estiver quase cheio, deve descartá-lo de acordo com as instruções ou contactar o
médico ou a enfermeira.
A dose será ajustada com base na idade e no peso corporal da criança. Em crianças mais novas, pode
ser necessária uma dose ligeiramente maior de medicamento Fragmin por quilograma de peso corporal do
que em adultos. O médico ajustará a dose adequada para o doente. Para monitorar a ação do medicamento
Fragmin durante o tratamento, o pessoal médico pode coletar uma amostra de sangue.
Uso do medicamento Fragmin em doentes com distúrbios da função renal e hepática
O medicamento requer cuidado ao ser utilizado em doentes com distúrbios da função renal e hepática (ver
ponto 2: Precauções e advertências).
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não em todas as pessoas. Os efeitos não desejados são classificados por frequência.
Frequente(pode ocorrer em até 1 em 10 pessoas)
- Trombocitopenia leve e reversível (tipo I)
- Sangramento
- Aumento transitório da atividade da aminotransferase (enzimas hepáticas, AspAT, AlAT)
- Hematoma subcutâneo no local da injeção
- Dor no local da injeção
Pouco frequente(pode ocorrer em até 1 em 100 pessoas)
- Hipersensibilidade
Raro(pode ocorrer em até 1 em 1.000 pessoas)
- Necrose da pele
- Alopecia transitória
Frequência desconhecida(não pode ser estimada com base nos dados disponíveis)
- Trombocitopenia imunológica induzida por heparina (tipo II, com ou sem complicações trombóticas)
- Reações anafiláticas
- Sangramentos intracranianos (alguns com resultado fatal)
- Sangramentos na cavidade abdominal (alguns com resultado fatal)
- Erupções cutâneas
- Hematoma subaracnoide ou epidural
Os produtos de heparina podem causar hipoaldosteronismo (caracterizado por uma redução na secreção de aldosterona, um hormônio da cortex adrenal), o que pode levar a um aumento nos níveis de potássio no sangue (hiperpotassemia). Raramente, especialmente em pacientes com insuficiência renal crônica e diabetes, pode ocorrer hiperpotassemia clinicamente significativa. No caso de uso prolongado do Fragmin, existe o risco de osteoporose. Estima-se que os efeitos não desejados em crianças sejam os mesmos que em adultos, no entanto, existem apenas dados limitados sobre a ocorrência de possíveis efeitos não desejados durante o tratamento prolongado em crianças.
Notificação de efeitos não desejados
Se ocorrerem qualquer sintomas não desejados, incluindo possíveis sintomas não desejados não listados nesta bula, deve-se informar o médico ou farmacêutico. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Medicamentos da Agência Reguladora de Medicamentos, Dispositivos Médicos e Produtos Biocidas Al. Jerozolimskie 181C 02-222 Varsóvia Tel.: +48 22 49 21 301 Fax: +48 22 49 21 309 Site: https://smz.ezdrowie.gov.pl Os efeitos não desejados também podem ser notificados ao representante do titular da autorização de comercialização ou ao próprio titular. A notificação de efeitos não desejados permitirá a coleta de mais informações sobre a segurança do medicamento.
5. Como armazenar o Fragmin
O medicamento deve ser armazenado em um local seguro e inacessível às crianças. As seringas pré-cheias devem ser armazenadas a uma temperatura abaixo de 25°C. Não use este medicamento após a data de validade impressa na embalagem. A data de validade é o último dia do mês indicado. Do ponto de vista microbiológico, o medicamento deve ser usado imediatamente. Se não for usado imediatamente, o usuário é responsável pelo tempo e condições de armazenamento durante o uso. Os medicamentos não devem ser jogados na canalização ou em lixeiras domésticas. É necessário perguntar ao farmacêutico como descartar os medicamentos que não são mais usados. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o Fragmin
- A substância ativa do medicamento é a dalteparina sódica. A potência é expressa em unidades internacionais (UI) anti-Xa, de acordo com o primeiro Padrão Internacional para Heparinas de Baixo Peso Molecular.
- Os outros componentes são:
Como é o Fragmin e o que contém a embalagem
A solução injetável está disponível em seringas pré-cheias com agulha contendo uma dose única do medicamento (vidro de classe I) com uma capa de agulha (borracha), um êmbolo (borracha clorobutila), um pistão (polipropileno ou poliestireno) com (ou sem) um dispositivo de segurança para a agulha. A capa da agulha pode conter látex.
| Nr | Volume | Dalteparina sódica (Dalteparinum natricum) |
| 0,2 ml | 2.500 UI anti-Xa |
| 0,2 ml | 5.000 UI anti-Xa |
| 0,3 ml | 7.500 UI anti-Xa |
| 0,4 ml | 10.000 UI anti-Xa |
| 0,5 ml | 12.500 UI anti-Xa |
| 0,6 ml | 15.000 UI anti-Xa |
| 0,72 ml | 18.000 UI anti-Xa |
| Nr | Dose/Volume | Substâncias auxiliares |
| 2.500 UI anti-Xa/0,2 ml | cloreto de sódio, hidróxido de sódio ou ácido clorídrico (ajuste de pH 5-7,5), água para injeção |
| 5.000 UI anti-Xa/0,2 ml | hidróxido de sódio ou ácido clorídrico (ajuste de pH 5-7,5), água para injeção |
| 7.500 UI anti-Xa/0,3 ml | hidróxido de sódio ou ácido clorídrico (ajuste de pH 5-7,5), água para injeção |
| 10.000 UI anti-Xa/0,4 ml | hidróxido de sódio ou ácido clorídrico (ajuste de pH 5-7,5), água para injeção |
| 12.500 UI anti-Xa/0,5 ml | hidróxido de sódio ou ácido clorídrico (ajuste de pH 5-7,5), água para injeção |
| 15.000 UI anti-Xa/0,6 ml | hidróxido de sódio ou ácido clorídrico (ajuste de pH 5-7,5), água para injeção |
| 18.000 UI anti-Xa/0,72 ml | hidróxido de sódio ou ácido clorídrico (ajuste de pH 5-7,5), água para injeção |
Nem todos os tamanhos de embalagem podem estar disponíveis no mercado.
Titular da autorização de comercialização
Pfizer Europe MA EEIG Boulevard de la Plaine 17 1050 Bruxelas Bélgica
Fabricante
2.500 UI anti-Xa/0,2 ml; 5.000 UI anti-Xa/0,2 ml; 7.500 UI anti-Xa/0,3 ml Pfizer Manufacturing Belgium NV Rijksweg 12, 2870 Puurs-Sint-Amands Bélgica Catalent France Limoges S.A.S. Z.I. Nord, 53 rue de Dion Bouton 87280 Limoges França 10.000 UI anti-Xa/0,4 ml, 12.500 UI anti-Xa/0,5 ml; 15.000 UI anti-Xa/0,6 ml; 18.000 UI anti-Xa/0,72 ml Pfizer Manufacturing Belgium NV Rijksweg 12, 2870 Puurs-Sint-Amands Bélgica Para obter informações mais detalhadas sobre este medicamento, por favor, contate o representante local do titular da autorização de comercialização: Pfizer Polska Sp. z o.o. tel. 22 335 61 00
Data da última atualização da bula: 06/2025
Informações detalhadas e atualizadas sobre este produto podem ser obtidas digitalizando o código QR presente na embalagem externa usando um dispositivo móvel. As mesmas informações também estão disponíveis no endereço URL: https://pfi.sr/ulotka-fragmin e no site da Agência Reguladora de Medicamentos, Dispositivos Médicos e Produtos Biocidas http://www.urpl.gov.pl .
| Nr | Dose/Volume | Tipo e conteúdo da embalagem |
| 2.500 UI anti-Xa/0,2 ml | 10 seringas pré-cheias com agulha de 0,2 ml 20 seringas pré-cheias com agulha de 0,2 ml |
| 5.000 UI anti-Xa/0,2 ml | 10 seringas pré-cheias com agulha de 0,2 ml 20 seringas pré-cheias com agulha de 0,2 ml |
| 7.500 UI anti-Xa/0,3 ml | 10 seringas pré-cheias com agulha de 0,3 ml 20 seringas pré-cheias com agulha de 0,3 ml |
| 10.000 UI anti-Xa/0,4 ml | 5 seringas pré-cheias com agulha de 0,4 ml |
| 12.500 UI anti-Xa/0,5 ml | 5 seringas pré-cheias com agulha de 0,5 ml |
| 15.000 UI anti-Xa/0,6 ml | 5 seringas pré-cheias com agulha de 0,6 ml |
| 18.000 UI anti-Xa/0,72 ml | 5 seringas pré-cheias com agulha de 0,72 ml |
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorCatalent France Limoges S.A.S Z.I. Nord Pfizer Manufacturing Belgium NV
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a FragminForma farmacêutica: Solução, 2500 UI anti-Xa/0,2 mlSubstância ativa: dalteparinRequer receita médicaForma farmacêutica: Solução, 5000 UI anti-Xa/0.2 mlSubstância ativa: dalteparinRequer receita médicaForma farmacêutica: Solução, 7500 UI anti-Xa/0,3 mlSubstância ativa: dalteparinRequer receita médica
Alternativas a Fragmin noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Fragmin em Espanha
Médicos online para Fragmin
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Fragmin – sujeita a avaliação médica e regras locais.














