
Beriate 1000

Pergunte a um médico sobre a prescrição de Beriate 1000

Como usar Beriate 1000
FOLHETO INCLUÍDO NA EMBALAGEM: INFORMAÇÃO PARA
UTILIZADOR
Beriate
Beriate 250, 250 UI. Pó e solvente para solução injectável/infusão
Beriate 500, 500 UI. Pó e solvente para solução injectável/infusão
Beriate 1000, 1000 UI. Pó e solvente para solução injectável/infusão
Beriate 2000, 2000 UI. Pó e solvente para solução injectável/infusão
Fator VIII humano
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder reler se necessário.
- Se tiver alguma dúvida, deve consultar o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si. Não o deve dar a outros.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o seu médico ou farmacêutico. Ver ponto 4.
Índice do folheto:
- 1. O que é o medicamento Beriate e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Beriate
- 3. Como tomar o medicamento Beriate
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Beriate
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Beriate e para que é utilizado
O que é o Beriate?
Beriate é um pó e um solvente. A solução reconstituída é administrada por via intravenosa sob a forma de injeção ou infusão.
Beriate é produzido a partir de plasma humano (parte líquida do sangue) e contém fator VIII humano. É utilizado para a prevenção e tratamento de hemorragias causadas pela falta de fator VIII (hemofilia tipo A) no sangue. Pode também ser utilizado no tratamento de deficiência adquirida de fator VIII.
2. Informações importantes antes de tomar o medicamento Beriate
As seguintes secções contêm informações que deve considerar antes de tomar Beriate.
Quando não tomar o medicamento Beriate
- Se o doente tiver alergia (hipersensibilidade) ao princípio ativo (fator VIII humano) ou a qualquer um dos excipientes deste medicamento (listados no ponto 6).
Precauções e advertências
Identificabilidade
É especialmente recomendado que, em cada administração de Beriate ao doente, sejam registados na ficha de tratamento a data de administração do medicamento, o número de lote e o volume injectado.
Antes de iniciar o tratamento com Beriate, deve discutir com o seu médico ou farmacêutico.
- Podem ocorrer reacções de hipersensibilidade de tipo alérgico. Os doentes devem ser informados pelo médico sobre os sintomas precoces de reacção de hipersensibilidade,tais como urticária, erupção cutânea generalizada, sensação de aperto no peito, respiração sibilante, diminuição da pressão arterial e anafilaxia (reação alérgica grave que pode causar dificuldades respiratórias graves ou tonturas). Se ocorrerem tais sintomas, os doentes devem interromper imediatamente a administração do produto e contactar o seu médico.
- A formação de inibidores(anticorpos) é uma complicação conhecida que pode ocorrer durante o tratamento com todos os medicamentos que contenham fator VIII. Estes inibidores, especialmente em níveis elevados, interrompem o tratamento eficaz e o doente será monitorizado atentamente para a formação destes inibidores. Se a hemorragia no doente não for controlada adequadamente com o medicamento Beriate, deve informar imediatamente o seu médico.
- Se o doente tiver doença cardíaca pré-existente ou risco de doença cardíaca, deve informar o seu médico ou farmacêutico.
- Se for necessário um dispositivo de acesso venoso central (ang. central venous access device, CVAD) para a administração de Beriate, o médico deve considerar o risco de complicações associadas ao CVAD, incluindo infecções locais, bactérias no sangue (bacteriemia) e formação de coágulos nos vasos sanguíneos (trombose) no local de inserção do cateter.
O médico deve avaliar cuidadosamente os benefícios do tratamento com o medicamento Beriate em relação ao risco destas complicações.
Segurança em relação à transmissão de vírus
Em relação aos medicamentos produzidos a partir de sangue ou plasma humano, são tomadas medidas de prevenção para evitar a transmissão de infecções para os doentes.
Estas medidas incluem a seleção rigorosa dos doadores de sangue e plasma para excluir portadores de doenças infecciosas e a testagem de cada doação e pool de plasma para vírus/infeções.
Os fabricantes destes produtos também incluem procedimentos no processo de fabrico que inactivam ou removem vírus ou outros patógenos. Apesar da implementação destas medidas, não é possível excluir totally a possibilidade de transmissão de agentes infecciosos com medicamentos derivados de sangue ou plasma humano. Isto inclui vírus desconhecidos ou recentemente identificados e outros tipos de infecções.
As medidas de segurança são consideradas eficazes contra vírus envelopados, como o vírus da imunodeficiência humana (HIV, vírus que causa a SIDA), vírus da hepatite B e C (hepatite) e contra vírus não envelopados, como o vírus da hepatite A e parvovirus B19.
Se o doente receber regularmente ou em múltiplas ocasiões produtos derivados de plasma humano (por exemplo, fator VIII), o médico pode recomendar a vacinação contra a hepatite A e B.
Interacções com outros medicamentos
- Deve informar o seu médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou recentemente, ou que planeia tomar.
- Beriate não deve ser misturado com outros produtos medicinais, diluentes e solventes, excepto os recomendados pelo fabricante (ver ponto 6).
Gravidez, amamentação e fertilidade
- Se a doente estiver grávida ou a amamentar, ou suspeitar que possa estar grávida ou planeia ter um filho, deve consultar o seu médico ou farmacêutico antes de tomar este medicamento.
- O medicamento Beriate deve ser utilizado durante a gravidez e amamentação apenas se estritamente necessário.
- Não estão disponíveis dados sobre a fertilidade.
Condução de veículos e utilização de máquinas
O medicamento Beriate não afecta a capacidade de conduzir veículos ou utilizar máquinas.
Beriate contém sódio
Beriate 250 UI e 500 UI contém menos de 1 mmol de sódio (23 mg) por frasco, pelo que pode ser considerado essencialmente "livre de sódio".
Beriate 1000 UI e 2000 UI contém 27,55 mg de sódio (componente principal do sal de cozinha) por frasco. Isto é equivalente a 1,4% da dose diária máxima recomendada de sódio para um adulto.
3. Como tomar o medicamento Beriate
Este medicamento deve ser sempre administrado de acordo com as instruções do seu médico ou farmacêutico. Se tiver alguma dúvida, deve consultar o seu médico ou farmacêutico.
O tratamento da hemofilia A deve ser iniciado e supervisionado por um médico com experiência no tratamento desta doença.
Dose recomendada
A quantidade necessária de fator VIII e a duração do tratamento dependem de vários factores, tais como peso corporal, gravidade da doença, localização e intensidade da hemorragia ou necessidade de prevenir hemorragias durante uma operação ou exame.
Se for recomendado o tratamento com o medicamento Beriate em casa, o médico deve informar o doente sobre como injectar o medicamento e qual a dose a utilizar.
Deve seguir as instruções recebidas do seu médico ou enfermeiro do centro de tratamento de hemofilia.
Uso em crianças e adolescentes
A dose é determinada com base no peso corporal, utilizando o mesmo princípio que para os adultos.
Uso de uma dose maior do que a recomendada de medicamento Beriate
Não foram relatados sintomas de sobredosagem de FVIII.
Omissão de uma dose de Beriate
A próxima dose deve ser administrada imediatamente e continuar a ser administrada em intervalos regulares, de acordo com as instruções do médico. Não deve ser administrada uma dose dupla para compensar a dose omitida.
Reconstituição e administração Recomendações gerais:
- Deve misturar o pó com o solvente (parte líquida) e retirar do frasco em condições assépticas.
- A solução reconstituída deve ser transparente ou ligeiramente opalescente, ou seja, pode brilhar quando observada à luz. Por vezes, podem aparecer pequenos grumos ou partículas no frasco. O filtro que faz parte do dispositivo Mix2Vial remove as partículas sólidas. A filtração não afecta o cálculo da dose. Antes da administração, após a filtração e retirada do produto para a seringa (ver abaixo), a solução deve ser verificada visualmente para excluir a presença de pequenas partículas e descoloração. Não utilizar a solução se estiver turva ou contiver depósitos ou partículas na seringa.
- Após a transferência para a seringa, o produto deve ser utilizado imediatamente. Não deve ser armazenado o produto na seringa.
- Qualquer resíduo de produto não utilizado ou resíduos deve ser eliminado de acordo com as regulamentações locais e as instruções do médico.
Reconstituição:
Não abrindo os frascos, aquecer o pó Beriate e o solvente à temperatura ambiente ou temperatura corporal. Isto pode ser feito deixando os frascos cerca de uma hora à temperatura ambiente ou segurando-os nas mãos durante alguns minutos.
NÃO submeter os frascos a calor directo. O frasco não deve ser aquecido a uma temperatura superior à temperatura corporal (37ºC).
Remover cuidadosamente as tampas de protecção dos frascos com pó e solvente, limpar a superfície dos cortes de borracha com um algodão embebido em álcool e deixar secar antes de abrir o pacote com o Mix2Vial, e seguir as instruções abaixo.
- 1. Abrir o pacote do Mix2Vial removendo a tampa. Nãoretirar o Mix2Vial do blister!
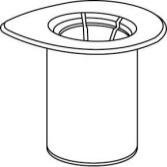
- 2. Colocar o frasco com solventesobre uma superfície plana e limpa e segurá-lo firmemente. Não retirar o conjunto Mix2Vial do blister. Pressionando a extremidade do conector azul para baixo, perfurar a tampa do frasco com solvente.
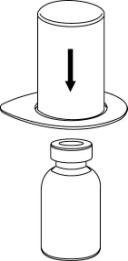
- 3. Retirar cuidadosamente o blister do conjunto Mix2Vial segurando a borda e puxando para cima. Deve ter atenção para apenas retirar o blister e não o conjunto Mix2Vial completo.
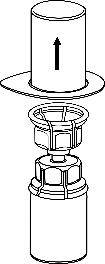
4 .Colocar o frasco com o produto sobre uma superfície plana e dura.
Inverter o frasco com solvente com o conjunto Mix2Vial ligado e, pressionando a extremidade do conector transparente para baixo, perfurar a tampa do frasco com o produto. O solvente fluirá automaticamente para o frasco com o produto.
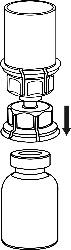
- 5. Segurando o frasco com o produto ligado ao conjunto Mix2Vial com uma mão e o frasco com solvente também ligado ao conjunto Mix2Vial com a outra mão, desrosquear cuidadosamente o conjunto em duas partes, girando em sentido contrário ao dos ponteiros do relógio. Retirar o frasco com solvente com o conector azul do conjunto Mix2Vial.
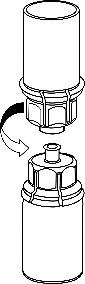
- 6. Fazer dissolver completamente o pó, movendo suavemente o frasco com o produto com o conector transparente ligado, com um movimento rotativo. Não agitar.
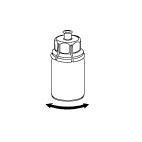
7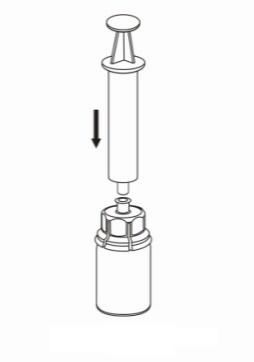 |
|
Retirada e administração:
- 8. Segurando o êmbolo da seringa pressionado, inverter o conjunto todo para cima e encher a seringa com a solução, puxando lentamente o êmbolo da seringa.
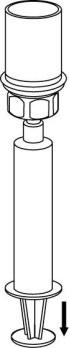
- 9. A solução agora está na seringa. Segurando firmemente o cilindro da seringa (com o êmbolo da seringa apontando para baixo), retirar o conector transparente do conjunto Mix2Vial da seringa, girando em sentido contrário ao dos ponteiros do relógio.
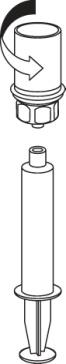
Introduzir a agulha na veia utilizando o conjunto fornecido para punções venosas. Deixar que o sangue flua até o final do tubo. Ligar a seringa à extremidade rosqueada do conjunto de punção venosa. De acordo com as instruções do médico, deve injetar lentamentea solução reconstituída por via intravenosa. A velocidade de injeção ou infusão não deve exceder 2 ml por minuto. Deve ter atenção para que o sangue não entre na seringa que contém o produto.
Se for necessário administrar um volume maior, também pode ser feito por infusão. Para isso, deve transferir o produto reconstituído para um conjunto de infusão aprovado para uso. A infusão deve ser feita de acordo com as instruções do médico.
Deve estar atento ao aparecimento de qualquer efeito não desejado. Se tal efeito puder estar relacionado com a administração de Beriate, a injeção ou infusão deve ser interrompida (ver também ponto 2).
Se tiver alguma dúvida adicional sobre a utilização deste medicamento, deve consultar o seu médico ou farmacêutico.
4. Efeitos não desejados
Como todos os medicamentos, este medicamento pode causar efeitos não desejados, embora não todos os doentes os experimentem.
Se ocorrer algum dos seguintes sintomas, deve informar imediatamente o seu médico ou serviço de emergência, ou o departamento de tratamento de hemofilia no hospital mais próximo:
- Sintomas de angioedema, tais como
- inchaço do rosto, língua ou garganta
- dificuldade em engolir
- urticária e dificuldade em respirar Estes efeitos não desejados foram observados muito raramente (podem ocorrer em menos de 1 em 10 000 doentes) e, em alguns casos, podem levar a reacções alérgicas graves (anafilaxia), com choque incluído.
- Falta de eficácia do tratamento (hemorragias persistentes). Em crianças não tratadas anteriormente com medicamentos que contenham fator VIII, anticorpos neutralizantes (ver ponto 2) podem ocorrer muito frequentemente (em mais de 1 em 10 doentes). No entanto, em doentes que foram tratados anteriormente com fator VIII (mais de 150 dias de tratamento), o risco é pouco frequente (em menos de 1 em 100 doentes). Se tal acontecer, os medicamentos do doente podem deixar de funcionar correctamente e o doente pode apresentar hemorragia persistente. Se tal acontecer, deve contactar imediatamente o seu médico.
Outros efeitos não desejados:
- Reacções alérgicas (hipersensibilidade), que podem incluir:
- queimadura e picada no local da injeção ou infusão
- arrepios, calafrios, erupção cutânea generalizada, bolhas
- dor de cabeça
- diminuição da pressão arterial, ansiedade, aceleração do ritmo cardíaco, sensação de aperto no peito, respiração sibilante
- sensação de fadiga (letargia)
- náuseas, vómitos
- formigamento Estes efeitos não desejados foram observados muito raramente e, em alguns casos, podem levar a reacções alérgicas graves (anafilaxia), com choque incluído.
- Foi observada, muito raramente, uma elevação da temperatura corporal.
Efeitos não desejados em crianças e adolescentes
A frequência, tipo e gravidade das reacções adversas em crianças são semelhantes aos dos adultos
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o seu médico ou farmacêutico ou enfermeiro.
Os efeitos não desejados podem ser notificados directamente para o Departamento de Monitorização de Efeitos Não Desejados de Medicamentos da Agência Nacional de Medicamentos e Produtos de Saúde
Rua Alexandre Herculano, 46 - 7º
1250-008 Lisboa
Telefone: +351 21 792 35 00
Fax: +351 21 792 35 99
Sítio da Internet: https://www.infarmed.pt/
Os efeitos não desejados também podem ser notificados para o titular da autorização de introdução no mercado.
A notificação de efeitos não desejados é importante, pois permite a recolha de mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Beriate
Não utilizar este medicamento após o prazo de validade impresso na etiqueta e na caixa após a abreviatura (EXP). O prazo de validade é o último dia do mês indicado.
O número do lote é registado na etiqueta e na caixa após a abreviatura (Lote).
- Conservar no frigorífico (2°C - 8°C ).
- Durante o prazo de validade, Beriate pode ser conservado a uma temperatura não superior a 25°C durante um período total de 1 mês. Os períodos individuais de conservação a temperatura ambiente devem ser registados nos registos de tratamento, de modo a que o período total de conservação a esta temperatura não exceda 1 mês.
- Beriate não contém conservante e é desejável a sua administração imediatamente após a reconstituição.
- Se o produto reconstituído não for administrado imediatamente, o seu período de conservação no frasco não deve exceder 8 horas à temperatura ambiente. Após a transferência para a seringa, o produto deve ser utilizado imediatamente.
- Não congelar.
- Conservar o recipiente no embalagem exterior para proteger da luz.
- O medicamento deve ser conservado fora do alcance e da vista das crianças.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Beriate Substância ativa do medicamento:
Beriate está disponível sob a forma de pó (contendo nominalmente 250 UI, 500 UI, 1000 UI ou 2000 UI de fator VIII humano por frasco) e parte líquida (solvente). A solução reconstituída é para injeção ou infusão.
Beriate 250/500/1000 reconstituído com 2,5 ml, 5 ml e 10 ml de água para injeção, respectivamente, contém cerca de 100 UI/ml de fator VIII humano.
Beriate 2000 deve ser reconstituído com 10 ml de água para injeção, e a solução resultante contém cerca de 200 UI/ml de fator VIII humano.
Outros componentes são:
Glicina, cloreto de cálcio, hidróxido de sódio (em quantidades pequenas) para ajustar o pH, sacarose, cloreto de sódio. Solvente:água para injeção 2,5 ml, 5 ml e 10 ml, respectivamente.
Que aspecto tem o medicamento Beriate e que embalagens estão disponíveis
Beriate é um pó branco e é fornecido com água para injeção.
A solução reconstituída deve ser transparente a ligeiramente opalescente, ou seja, pode brilhar quando segurada à luz, mas não deve conter partículas visíveis.
Embalagens disponíveis
Embalagem de 250 UI contendo:
1 frasco de pó
1 frasco de água para injeção de 2,5 ml
1 sistema de transferência 20/20 com filtro
Conjunto para administração (embalagem interior):
1 seringa de uso único de 5 ml
1 conjunto para punção venosa
2 algodões embebidos em álcool
1 penso não estéril
Embalagem de produto medicamentoso na dose de 500 UI contendo:
1 frasco de pó
1 frasco de água para injeção de 5 ml
1 sistema de transferência 20/20 com filtro
Conjunto para administração (embalagem interior):
1 seringa de uso único de 5 ml
1 conjunto para punção venosa
2 algodões embebidos em álcool
1 penso não estéril.
Embalagem de produto medicamentoso na dose de 1000 UI contendo:
1 frasco de pó
1 frasco de água para injeção de 10 ml
1 sistema de transferência 20/20 com filtro
Conjunto para administração (embalagem interior):
1 seringa de uso único de 10 ml
1 conjunto para punção venosa
2 algodões embebidos em álcool
1 penso não estéril.
Embalagem de produto medicamentoso na dose de 2000 UI contendo:
1 frasco de pó
1 frasco de água para injeção de 10 ml
1 sistema de transferência 20/20 com filtro
Conjunto para administração (embalagem interior):
1 seringa de uso único de 10 ml
1 conjunto para punção venosa
2 algodões embebidos em álcool
1 penso não estéril.
Nem todos os tamanhos de embalagem podem estar disponíveis.
Titular da autorização de introdução no mercado e fabricante
CSL Behring GmbH
Emil-von-Behring-Str. 76
35041 Marburg
Alemanha
Este medicamento está autorizado nos Estados-Membros do Espaço Económico Europeu sob os seguintes nomes:
Áustria:
Beriate 100 UI/ml Pó e solvente para solução injectável ou infusão (250 UI, 500 UI, 1000 UI)
Beriate 200 UI/ml Pó e solvente para solução injectável ou infusão (2000 UI)
Bulgária:
Beriate 250 UI Pó e solvente para solução injectável ou infusão
Beriate 500 UI Pó e solvente para solução injectável ou infusão
Beriate 1000 UI Pó e solvente para solução injectável ou infusão
Beriate 2000 UI Pó e solvente para solução injectável ou infusão
Croácia:
Beriate 250 UI Pó e solvente para solução injectável ou infusão
Beriate 500 UI Pó e solvente para solução injectável ou infusão
Beriate 1000 UI Pó e solvente para solução injectável ou infusão
Beriate 2000 UI Pó e solvente para solução injectável ou infusão
República Checa:
Beriate 250 UI, Beriate 500 UI, Beriate 1000 UI, Beriate 2000 UI
Estónia:
Beriate
Letónia:
Beriate 250 UI Pó e solvente para solução injectável ou infusão
Beriate 500 UI Pó e solvente para solução injectável ou infusão
Beriate 1000 UI Pó e solvente para solução injectável ou infusão
Beriate 2000 UI Pó e solvente para solução injectável ou infusão
Lituânia:
Beriate 250 UI Pó e solvente para solução injectável ou infusão
Beriate 500 UI Pó e solvente para solução injectável ou infusão
Beriate 1000 UI Pó e solvente para solução injectável ou infusão
Beriate 2000 UI Pó e solvente para solução injectável ou infusão
Alemanha:
Beriate 250, Beriate 500, Beriate 1000, Beriate 2000
Hungria:
Apresentações de Beriate 250, 500 e 1000:
BERIATE 100 UI/ml Pó e solvente para solução injectável ou infusão (250 UI, 500 UI, 1000 UI)
Apresentação 2000:
BERIATE 200 UI/ml Pó e solvente para solução injectável ou infusão (2000 UI)
Itália:
Beriate
Polónia:
Beriate 250
Beriate 500
Beriate 1000
Beriate 2000
Portugal:
Beriate
Roménia:
Beriate 250 UI Pó e solvente para solução injectável ou infusão
Beriate 500 UI Pó e solvente para solução injectável ou infusão
Beriate 1000 UI Pó e solvente para solução injectável ou infusão
Beriate 2000 UI Pó e solvente para solução injectável ou infusão
Espanha:
Beriate 250 UI Pó e solvente para solução injectável ou infusão
Beriate 500 UI Pó e solvente para solução injectável ou infusão
Beriate 1000 UI Pó e solvente para solução injectável ou infusão
Beriate 2000 UI Pó e solvente para solução injectável ou infusão
Eslováquia:
Beriate 250 UI
Beriate 500 UI
Beriate 1000 UI
Beriate 2000 UI
Eslovénia:
Beriate 250 UI Pó e solvente para solução injectável ou infusão
Beriate 500 UI Pó e solvente para solução injectável ou infusão
Beriate 1000 UI Pó e solvente para solução injectável ou infusão
Beriate 2000 UI Pó e solvente para solução injectável ou infusão
Data da última revisão do folheto: setembro de 2021
Informações destinadas apenas a profissionais de saúde:
Posologia
Monitorização do tratamento
Durante o tratamento, deve ser medida a actividade do fator VIII para determinar a dose adequada a administrar ao doente e a frequência das administrações repetidas.
A resposta individual dos doentes ao fator VIII pode variar, devido a diferentes níveis de recuperação e diferentes meias-vidas. A posologia com base no peso corporal pode necessitar de ajuste em doentes com peso corporal anormal. Em particular, em caso de intervenções cirúrgicas importantes, é necessário um controlo rigoroso da terapêutica de substituição através do monitorização do processo de coagulação (nível de actividade do fator VIII no plasma).
Os doentes devem ser monitorizados para a formação de inibidores do fator VIII. Ver também ponto 2.
A quantidade de unidades de fator VIII administradas ao doente é expressa em unidades internacionais (UI), que se referem aos padrões actuais da OMS para concentrados de fator VIII. A actividade do fator VIII no plasma é expressa como percentagem (em relação ao plasma normal humano) ou melhor, em UI (em relação aos padrões internacionais de fator VIII no plasma).
Uma unidade internacional de actividade do fator VIII é equivalente à actividade do fator VIII contida em 1 ml de plasma normal humano.
Tratamento de demanda
O cálculo da dose necessária de fator VIII baseia-se na observação empírica de que 1 UI de fator VIII por kg de peso corporal aumenta a actividade plasmática do fator VIII em cerca de 2% da actividade normal (2 UI/dl). A dose necessária é calculada utilizando a seguinte fórmula:
Dose necessária = peso corporal [kg] x aumento desejado do nível do fator VIII [% ou UI/dl] x 0,5.
A dose do produto e a frequência da sua administração devem ser sempre adaptadas individualmente, com base na eficácia clínica em cada doente.
Em caso de hemorragias, a actividade do fator VIII não deve diminuir abaixo dos valores indicados para a actividade no plasma (em % da norma ou UI/dl) durante o período de tempo correspondente. A tabela seguinte apresenta a posologia possível em caso de hemorragias e intervenções cirúrgicas:
| Tipo de hemorragia/ intervenção cirúrgica | Nível de fator VIII necessário (% ou UI/dl) | Frequência de administração (horas) / duração do tratamento (dias) |
| Hemorragias | ||
| Hemorragia menor nos joelhos, hemorragia muscular ou na boca | 20-40 | Repetir a cada 12 a 24 horas, durante pelo menos 1 dia, até que a dor e a hemorragia cessem ou até que a lesão seja tratada. |
| Hemorragia maior nos joelhos, hemorragia muscular ou hematoma | 30-60 | Repetir a administração a cada 12-24 horas durante 3 a 4 dias ou mais, até que a dor e a disfunção aguda cessem. |
| Hemorragias que ponham a vida em risco | 60-100 | Repetir a administração a cada 8 a 24 horas, até que o perigo tenha passado. |
| Intervenções cirúrgicas | ||
| Intervenções cirúrgicas menores, incluindo extração de dentes | 30-60 | A cada 24 horas, durante pelo menos 1 dia, até que a lesão seja tratada. |
| Intervenções cirúrgicas importantes | 80-100 (pré e pós-operatório) | Repetir a administração a cada 8 – 24 horas até que a ferida seja devidamente cicatrizada, seguida de tratamento terapêutico durante pelo menos 7 dias para manter a actividade do fator VIII em 30% - 60% (30-60 UI/dl, o que corresponde a 0,30-0,60 UI/ml). |
Profilaxia
No tratamento de longo prazo para prevenção de hemorragias em doentes com hemofilia tipo A grave, costuma-se administrar 20 a 40 UI de fator VIII por kg de peso corporal a intervalos de 2 a 3 dias. Em alguns casos, particularmente em doentes jovens, pode ser necessário um tratamento mais frequente ou doses maiores.
Crianças e adolescentes
A posologia em crianças depende do peso corporal, pelo que a dose é calculada com base no mesmo princípio que para os adultos. A frequência da administração deve ser sempre adaptada individualmente, com base na eficácia clínica. São relatados casos de tratamento de crianças com menos de 6 anos de idade.
Informações sobre as propriedades farmacológicas do VWF
Além do seu papel como proteína de transporte para o fator VIII, o fator de von Willebrand media a adesão das plaquetas ao local de lesão do vaso e desempenha um papel na agregação das plaquetas.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorCSL Behring GmbH
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Beriate 1000Forma farmacêutica: Pó, 2000 UISubstância ativa: coagulation factor VIIIFabricante: CSL Behring GmbHRequer receita médicaForma farmacêutica: Pó, 250 UISubstância ativa: coagulation factor VIIIFabricante: CSL Behring GmbHRequer receita médicaForma farmacêutica: Pó, 500 UISubstância ativa: coagulation factor VIIIFabricante: CSL Behring GmbHRequer receita médica
Alternativas a Beriate 1000 noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Beriate 1000 em Espanha
Alternativa a Beriate 1000 em Ukraine
Médicos online para Beriate 1000
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Beriate 1000 – sujeita a avaliação médica e regras locais.














