PROKAM 50 mg POWDER FOR INJECTABLE SOLUTION

How to use PROKAM 50 mg POWDER FOR INJECTABLE SOLUTION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
Introduction
Package Leaflet: Information for the Patient
Prokam50 mg powder for solution for injection
Cefuroxime
Read all of this leaflet carefully before this medicine is administered to you because it contains important information for you.
- Keep this leaflet, you may need to read it again. If you have any further questions, ask your doctor, pharmacist, or nurse.
- This medicine has been prescribed for you only. Do not pass it on to others. It may harm them, even if their signs of illness are the same as yours.
- If you get any side effects, talk to your doctor, pharmacist, or nurse. This includes any possible side effects not listed in this leaflet. See section 4.
Contents of the pack
- What is Prokam and what is it used for
- What you need to know before you are given Prokam
- How Prokam is administered
- Possible side effects
- Storage of Prokam
- Contents of the pack and further information
1. What is Prokam and what is it used for
- Prokam contains the active substance cefuroxime (as cefuroxime sodium), which belongs to a group of antibiotics called cephalosporins. Antibiotics are used to kill the bacteria or germs that cause infections.
Antibiotics are used to treat bacterial infections and do not work for viral infections such as flu or the common cold.
It is important to follow the instructions regarding the dose, administration interval, and duration of treatment indicated by your doctor.
Do not store or reuse this medicine. If you have any leftover antibiotic after finishing the treatment, return it to the pharmacy for proper disposal. Do not throw away medicines via wastewater or household waste.
- This medicine will be used if you are undergoing cataract surgery (opacity of the lens).
- In order to prevent eye infection, the ophthalmic surgeon will inject this medicine into your eye at the end of the cataract operation.
2. What you need to know before you are given Prokam
Do not useProkam
- If you are allergic (hypersensitive) to cefuroxime or any other antibiotic in the cephalosporin group.
Warnings and precautions
Tell your doctor, pharmacist, or nurse before starting to use Prokam:
Prokam is only administered as an injection into the eye (intracameral injection).
Prokam should only be administered under aseptic conditions (meaning cleanliness and absence of germs) typical of cataract surgery.
Each vial of Prokam should be used for a single patient.
Using Prokam with other medicines
Tell your doctor or pharmacist if you are using, have recently used, or might use any other medicines.
Pregnancy andbreast-feeding
- If you are pregnant or breastfeeding, think you may be pregnant, or plan to become pregnant, consult your doctor or pharmacist before this medicine is administered to you.
- Prokam will only be administered if the benefit outweighs the potential risks.
Prokam contains sodium
This medicine contains less than 1 mmol of sodium (23 mg) per dose, which is essentially "sodium-free".
3. How Prokam is administered
- Prokam injections will be administered by an ophthalmic surgeon at the end of cataract surgery.
- Prokam is presented as a sterile powder, which is dissolved in saline solution for injection before administration.
If you are given too much or too little Prokam
This medicine will be administered to you by a healthcare professional. If you think you have missed a dose or have received too much medicine, inform your doctor or nurse.
If you have any further questions on the use of this medicine, ask your doctor, pharmacist, or nurse.
In case of overdose or accidental ingestion, consult your doctor or pharmacist immediately or call the Toxicology Information Service, phone: 91 562 04 20, indicating the medicine and the amount ingested.
4. Possible side effects
Like all medicines, Prokam can cause side effects, although not everybody gets them.
The following side effects are very rare (may affect up to 1 in 10,000 people):
- Severe allergic reaction causing difficulty breathing or fainting.
The following side effect has been reported with an unknown frequency (cannot be estimated from the available data):
- Macular edema (blurred or distorted vision near or in the center of your field of vision).
Reporting of side effects
If you experience any side effects, talk to your doctor or pharmacist, even if it is a possible side effect not listed in this leaflet. You can also report side effects directly through the Spanish Medicines Monitoring System for human use: www.notificaram.es. By reporting side effects, you can help provide more information on the safety of this medicine.
5. Storage of Prokam
Keep this medicine out of the sight and reach of children.
Do not use this medicine after the expiry date which is stated on the label of the vial and the carton after EXP. The expiry date is the last day of the month stated.
Do not store above 25°C. Keep the vial in the outer packaging to protect it from light.
For single use only.
After reconstitution: the product should be used immediately.
Medicines should not be disposed of via wastewater or household waste. Ask your pharmacist how to dispose of medicines no longer required. This will help protect the environment.
6. Contents of the pack and further information
Composition ofProkam
The active substance is cefuroxime (as cefuroxime sodium).
Each vial contains 50 mg of cefuroxime.
After reconstitution, 0.1 ml of solution contains 1 mg of cefuroxime.
There are no other ingredients.
Appearance ofProkamand pack contents
Prokam is a white to almost white powder for solution for injection, contained in a glass vial.
Each box contains one, ten, or twenty vials, or ten vials along with ten sterile needles with a 5-micron filter. Only certain pack sizes may be marketed.
Marketing authorisation holder and manufacturer
Marketing authorisation holder:
LABORATOIRES THEA
12 rue Louis Blériot
63017 CLERMONT-FERRAND Cedex 2
France
Local representative:
Laboratorios THEA S.A.
C/ Enric Granados, nº 86-88, 2ª planta
08008 Barcelona
Manufacturer:
BIOPHARMA S.R.L.
Via Delle Gerbere, 22/30 Santa Palomba
00134 ROMA
Italy
or
LABORATOIRES THEA
12 rue Louis Blériot
63017 CLERMONT-FERRAND Cedex 2
France
This medicine is authorised in the Member States of the European Economic Area under the following names:
Austria, Belgium, Czech Republic, Denmark, Finland, France, Germany, Italy, Iceland, Luxembourg, Netherlands, Norway, Poland, Portugal, Romania, Slovakia, Slovenia, Sweden, United Kingdom …………………………………………………Aprokam
Cyprus, Greece, Spain…………………………………………………………..Prokam
Ireland…………………………………………………………………………….APROK
Date of last revision of thisleaflet:August 2019
Detailed and updated information on this medicine is available on the website of the Spanish Agency for Medicines and Health Products (AEMPS) http://www.aemps.gob.es/
This information is intended only for healthcare professionals:
Incompatibilities
There are no references to incompatibilities with products commonly used in cataract surgery in the literature. This medicine should not be mixed with other medicines, except for those mentioned below [sodium chloride 9 mg/ml (0.9%) solution for injection].
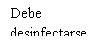
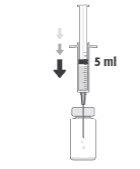
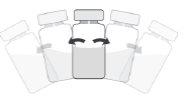
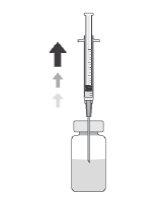
How to prepare and administer Prokam
Single-use vial, for intracameral use only.
After reconstitution, Prokam should be administered by intraocular injection into the anterior chamber of the eye (intracameral injection), by an ophthalmic surgeon, under the recommended aseptic conditions of cataract surgery.
The reconstituted solution should be inspected visually, and only used if it is a colorless to yellowish solution without visible particles.
After reconstitution, the product should be used immediately and not reused.
The recommended dose for cefuroxime is 1 mg in 0.1 ml of sodium chloride 9 mg/ml (0.9%) solution for injection.
DO NOT INJECT MORE THAN THE RECOMMENDED DOSE.
The vial is for single use.
Only one vial per patient. Attach the detachable label from the vial to the patient's documentation.
To prepare Prokamfor intracameral administration, follow these instructions: | |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
After use, discard any remaining reconstituted solution. Do not store it for later use. |
The disposal of unused medicine and all materials that have come into contact with it will be carried out in accordance with local regulations. Dispose of used needles in a puncture-resistant container.
- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to PROKAM 50 mg POWDER FOR INJECTABLE SOLUTIONDosage form: EYEDROP, 3.35 mg azithromycin dihydrateActive substance: azithromycinManufacturer: Laboratoires TheaPrescription requiredDosage form: EYE DROP, 0.3% gentamicinActive substance: gentamicinManufacturer: Ntc S.R.L.Prescription requiredDosage form: OPHTHALMIC GEL, 10 MG/GActive substance: fusidic acidManufacturer: Amdipharm LimitedPrescription required
Online doctors for PROKAM 50 mg POWDER FOR INJECTABLE SOLUTION
Discuss questions about PROKAM 50 mg POWDER FOR INJECTABLE SOLUTION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions