
BACEQ 150 MG and BACEQ 100 MG PROLONGED-RELEASE INJECTABLE SUSPENSION

How to use BACEQ 150 MG and BACEQ 100 MG PROLONGED-RELEASE INJECTABLE SUSPENSION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
Introduction
Package Leaflet: Information for the Patient
BACEQ 25 mg prolonged-release injectable suspension EFG
BACEQ 50 mg prolonged-release injectable suspension EFG
BACEQ 75 mg prolonged-release injectable suspension EFG
BACEQ 100 mg prolonged-release injectable suspension EFG
BACEQ 150 mg prolonged-release injectable suspension EFG
Initial Treatment Pack:
BACEQ 150 mg and BACEQ 100 mg prolonged-release injectable suspension EFG
Read the entire package leaflet carefully before starting to use this medication, as it contains important information for you.
Keep this package leaflet, as you may need to read it again.
- If you have any questions, ask your doctor or nurse.
- If you experience side effects, consult your doctor or nurse, even if they are not listed in this package leaflet. See section 4.
Contents of the Package Leaflet
- What is BACEQ and what is it used for
- What you need to know before starting to use BACEQ
- How to use BACEQ
- Possible side effects
- Storage of BACEQ
- Contents of the pack and further information
1. What is Paliperidone ratiopharm and what is it used for
BACEQ contains the active substance paliperidone, which belongs to the class of antipsychotic medications and is used as maintenance treatment for the symptoms of schizophrenia in adult patients stabilized with paliperidone or risperidone.
If you have shown a response to paliperidone or risperidone in the past and have mild or moderate symptoms, your doctor may initiate treatment with BACEQ without prior stabilization with paliperidone or risperidone.
Schizophrenia is a disorder with "positive" and "negative" symptoms. Positive means an excess of symptoms that are not normally present. For example, a person with schizophrenia may hear voices or see things that do not exist (called hallucinations), have false beliefs (called delusions), or have excessive distrust of others. Negative refers to the lack of behaviors or feelings that are normally present. For example, a person with schizophrenia may withdraw into themselves and not respond to any emotional stimuli or may have problems speaking in a clear and logical manner. People with this disorder may also feel depressed, anxious, guilty, or tense.
BACEQ can help alleviate the symptoms of your illness and prevent them from recurring.
2. What you need to know before starting to use Paliperidone ratiopharm
Do not usepaliperidone
- if you are allergic to paliperidone or any of the other components of this medication (listed in section 6);
- if you are allergic to any other antipsychotic medication, including risperidone.
Warnings and precautions
Consult your doctor, pharmacist, or nurse before starting to use BACEQ.
This medication has not been studied in elderly patients with dementia. However, elderly patients with dementia who are being treated with similar medications may have an increased risk of stroke or death (see section 4, possible side effects).
All medications have side effects, and some of the side effects of this medication may worsen the symptoms of other conditions. For this reason, it is essential that you discuss with your doctor any of the following conditions that may worsen during treatment with this medication:
- if you have Parkinson's disease
- if you have ever been diagnosed with a condition whose symptoms include elevated body temperature and muscle stiffness (also known as Neuroleptic Malignant Syndrome)
- if you have ever experienced abnormal movements of the tongue or face (Tardive Dyskinesia)
- if you have had low white blood cell counts in the past (which may or may not have been caused by other medications)
- if you are diabetic or have a tendency to diabetes
- if you have had breast cancer or a tumor in the pituitary gland of the brain
- if you have any heart condition or are receiving treatment for heart conditions that may make you more prone to a decrease in blood pressure
- if you have low blood pressure when standing up or getting up suddenly
- if you have epilepsy
- if you have kidney problems
- if you have liver problems
- if you have a prolonged and/or painful erection
- if you have difficulty controlling body temperature or are overheated
- if you have an abnormally high level of the hormone prolactin in your blood or if you have a tumor that may be dependent on prolactin
- if you or a family member has a history of blood clots, as antipsychotics have been associated with the formation of blood clots.
If you have any of these conditions, please consult your doctor, as it may be necessary to adjust your dose or monitor you for a period.
Because it has been rarely observed in patients treated with this medication that there is a dangerously low number of a type of white blood cells necessary to fight infections in the blood, your doctor may check your white blood cell count.
Even if you have previously tolerated oral paliperidone or risperidone, rare allergic reactions may occur after receiving paliperidone injections. Seek medical help immediately if you experience a skin rash, swelling of the throat, itching, or breathing problems, as these may be signs of a severe allergic reaction.
This medication may cause weight gain. Significant weight gain can negatively affect your health. Your doctor will regularly monitor your weight.
In patients treated with this medication, diabetes mellitus or worsening of pre-existing diabetes mellitus has been observed. Your doctor should check for signs of increased blood sugar. In patients with pre-existing diabetes mellitus, blood sugar should be regularly monitored.
Since this medication can reduce the urge to vomit, there is a possibility that it may mask the normal response of the body to the ingestion of toxic substances or other conditions.
During eye surgery for cataracts, the pupil (the black circle in the center of the eye) may not increase in size as needed. Additionally, the iris (the colored part of the eye) may become flaccid during surgery, which can cause eye damage. If you are considering eye surgery, make sure to inform your ophthalmologist that you are using this medication.
Children and adolescents
Do not use this medication in patients under 18 years of age.
Other medications and BACEQ
Tell your doctor if you are using, have recently used, or may need to use any other medication.
Taking this medication with carbamazepine (an antiepileptic and mood stabilizer) may require a change in your dose of this medication.
Since this medication acts primarily on the brain, interaction with other medications that also act on it may cause an exaggeration of side effects, such as drowsiness or other effects on the brain, such as other psychiatric medications, opioids, antihistamines, and sleep aids.
Since this medication can lower blood pressure, you should be careful if you use this medication with other medications that also lower blood pressure.
This medication may reduce the effect of medications for Parkinson's disease and restless legs syndrome (e.g., levodopa).
This medication may cause an abnormality in the electrocardiogram (ECG) that shows that it is necessary for an extended period for an electrical impulse to travel through a certain part of the heart (known as "prolongation of the QT interval"). Other medications that have this effect include some medications used to treat heart rhythm or to treat infections, in addition to other antipsychotics.
If you are prone to developing seizures, this medication may increase your chances of experiencing them. Other medications that have this effect include some medications used to treat depression or to treat infections, in addition to other antipsychotics.
BACEQ should be used with caution with medications that increase the activity of the central nervous system (psychostimulants such as methylphenidate).
Using BACEQ with alcohol
Alcohol should be avoided.
Pregnancy and breastfeeding
If you are pregnant or breastfeeding, think you may be pregnant, or plan to become pregnant, consult your doctor or pharmacist before using this medication. You should not use this medication during pregnancy unless you have discussed it with your doctor. The following symptoms may occur in newborn babies of mothers who have been treated with paliperidone in the last trimester of pregnancy (last three months of pregnancy): tremors, stiffness and/or muscle weakness, drowsiness, agitation, breathing problems, and difficulty feeding. If your baby develops any of these symptoms, you should contact your doctor.
This medication may pass from mother to child through breast milk and may harm the baby. Therefore, you should not breastfeed while using this medication.
Driving and using machines
During treatment with this medication, dizziness, extreme fatigue, and vision problems (see section 4) may occur. This should be taken into account when maximum attention is required, e.g., when driving or operating machines.
BACEQ contains sodium
This medication contains less than 1 mmol of sodium (23 mg) per dose; it is essentially "sodium-free".
3. How to use Paliperidone ratiopharm
Your doctor or another healthcare professional will administer this medication to you. Your doctor will tell you when to receive the next injection. It is essential that you do not miss any scheduled doses. If you cannot attend your appointment with the doctor, make sure to call them immediately to schedule another appointment as soon as possible.
You will receive the first injection (150 mg) and the second injection (100 mg) of this medication in the upper arm approximately one week apart. From then on, you will receive an injection (of 25 mg to 150 mg) in the upper arm or buttocks once a month.
If your doctor is switching you from risperidone long-acting injection to this medication, you will receive the first injection of this medication (of 25 mg to 150 mg) in the upper arm or buttocks at the next scheduled injection. From then on, you will receive an injection (of 25 mg to 150 mg) in the upper arm or buttocks once a month.
Depending on your symptoms, the doctor may increase or decrease the amount of medication you receive at the time of the monthly scheduled injection.
Patient with kidney problems
Your doctor may adjust the dose of this medication according to your renal function. If you have mild kidney problems, your doctor may give you a lower dose. You should not use this medication if you have moderate or severe kidney problems.
Elderly patients
Your doctor may reduce the dose of this medication if your kidney function is decreased.
If you use more BACEQ than you should
You will receive this medication under medical supervision; it is therefore unlikely that you will receive an excessive dose.
Patient who have received an overdose of paliperidone may experience the following symptoms: drowsiness or sedation, rapid heart rate, low blood pressure, abnormal electrocardiogram (ECG), or slow or abnormal movements of the face, body, arms, or legs.
If you stop using BACEQ
If you stop receiving your injections, the effects of the medication will be lost. You should not stop using this medication unless your doctor tells you to, as your symptoms may return.
If you have any further questions about the use of this medication, ask your doctor or pharmacist.
4. Possible Adverse Effects
Like all medicines, this medicine can cause adverse effects, although not all people suffer from them.
Tell your doctor immediately if:
- you have blood clots in the veins, especially in the legs (symptoms include swelling, pain, and redness of the leg), which can circulate through the blood vessels to the lungs, causing chest pain and difficulty breathing. If you notice any of these symptoms, seek medical advice immediately.
- you have dementia and experience a sudden change in your mental state or sudden weakness or numbness of the face, arms, or legs, especially on one side, or have difficulty speaking even for a short period. These may be signs of a stroke.
- you have fever, muscle stiffness, sweating, or a decrease in the level of consciousness (a condition known as "Neuroleptic Malignant Syndrome"). You may need immediate medical treatment.
- you are a man and experience a prolonged or painful erection. This is known as priapism. You may need immediate medical treatment.
- you experience involuntary rhythmic movements of the tongue, mouth, and face. It may be necessary to withdraw paliperidone.
- you have a severe allergic reaction characterized by fever, swelling of the mouth, face, lips, or tongue, difficulty breathing, itching, rash, and sometimes a drop in blood pressure (i.e., an "anaphylactic reaction"). Even if you have previously tolerated oral risperidone or paliperidone, allergic reactions have rarely appeared after receiving paliperidone injections.
- you are scheduled to undergo eye surgery, be sure to tell your ophthalmologist that you are taking this medicine. During eye surgery for cataracts, it is possible that the iris (the colored part of the eye) may become flaccid during surgery (known as "floppy iris syndrome"), which can cause eye damage.
- you have a dangerously low number of a type of white blood cell necessary to fight blood infections.
The following adverse effects may occur:
Very Common Adverse Effects: may affect more than 1 in 10 patients
- difficulty staying or falling asleep.
Common Adverse Effects: may affect up to 1 in 10 patients
- common cold symptoms, urinary tract infection, feeling like you have the flu
- paliperidone may increase the levels of a hormone called "prolactin" that is detected in blood tests (which may or may not cause symptoms). When symptoms of increased prolactin appear, they may include (in men) breast swelling, difficulty having or maintaining erections, or other sexual dysfunctions; (in women) breast tenderness, milk secretion from the breasts, loss of menstrual periods, or other problems with the cycle.
- increased blood sugar, weight gain, weight loss, decreased appetite
- irritability, depression, anxiety
- parkinsonism: This disease may include slow or altered movement, feeling of stiffness or tightness of the muscles (making jerky movements) and sometimes a feeling of "freezing" of movement that then restarts. Other signs of parkinsonism include walking slowly, dragging feet, tremors while resting, increased saliva and/or drooling, and loss of facial expressiveness.
- restlessness, feeling drowsy or less attentive
- distonia: It is a disorder that involves slow or continuous involuntary contraction of the muscles. Although any part of the body can be affected (and can cause abnormal postures), distonia often affects the muscles of the face, including abnormal movements of the eyes, mouth, tongue, or jaw.
- dizziness
- dykinesia: This disorder involves involuntary muscle movements and may include repetitive, spasmodic, or twisting movements, or spasms.
- tremors (agitation)
- headache
- rapid heartbeat
- increased blood pressure
- cough, nasal congestion
- abdominal pain, vomiting, nausea, constipation, diarrhea, indigestion, toothache
- increased liver transaminases in blood
- bone or muscle pain, back pain, joint pain
- absence of menstruation
- fever, weakness, fatigue (tiredness)
- a reaction at the injection site, including itching, pain, or swelling.
Uncommon Adverse Effects: may affect up to 1 in 100 patients
- pneumonia, chest infection (bronchitis), respiratory tract infection, nose infection, bladder infection, ear infection, fungal infection of the nails, tonsillitis, skin infection
- decrease in the number of white blood cells, decrease in a type of white blood cell that helps fight infections, anemia
- allergic reaction
- diabetes or worsening of diabetes, increased insulin (a hormone that controls blood sugar levels) in blood
- increased appetite
- loss of appetite that causes malnutrition and weight loss
- increased triglycerides in blood (fat), increased cholesterol in blood
- sleep disorder, euphoria (mania), decreased sexual desire, nervousness, nightmares
- late dykinesia (spasms or uncontrolled spasmodic movements of the face, tongue, or other parts of the body). Tell your doctor immediately if you experience involuntary rhythmic movements of the tongue, mouth, or face. It may be necessary to withdraw this medicine.
- fainting, restlessness that causes movement of body parts, dizziness when standing up, altered attention, speech problems, loss or alteration of taste, decreased skin sensitivity to pain or touch, tingling, pinching, or numbness of the skin
- blurred vision, eye infection or "red eye", dry eyes
- feeling that everything is spinning (vertigo), ringing in the ears, ear pain
- disruption of conduction between the upper and lower parts of the heart, anomaly in the electrical activity of the heart, prolongation of the QT interval in the heart, rapid heartbeat when standing up, slow heartbeat, anomalies in the heart's electrical tracing (electrocardiogram or ECG), feeling of fluttering or pounding in the chest (palpitations)
- decreased blood pressure, low blood pressure when standing up (therefore, some people taking this medicine may feel weak, dizzy, or may faint when getting up or sitting up suddenly)
- shortness of breath, sore throat, nosebleeds
- abdominal discomfort, stomach or intestine infection, difficulty swallowing, dry mouth
- excess gas or flatulence
- increased GGT (a liver enzyme called gamma-glutamyltransferase) in blood, increased liver enzymes in blood
- hives (or "urticaria"), itching, rash, hair loss, eczema, dry skin, redness of the skin, acne, abscesses under the skin
- increased CPK (creatine phosphokinase) in blood, an enzyme that is sometimes released with muscle breakdown
- muscle spasms, joint stiffness, muscle weakness
- urinary incontinence, frequent urination, pain when urinating
- erectile dysfunction, ejaculation disorder, absence of menstrual periods or other problems with the cycle (women), breast development in men, sexual dysfunction, breast pain, milk secretion from the breasts
- swelling of the face, mouth, eyes, or lips, swelling of the body, arms, or legs
- increased body temperature
- change in gait
- chest pain, chest discomfort, feeling of discomfort
- skin hardening
- falls.
Rare Adverse Effects: may affect up to 1 in 1,000 patients
- eye infection
- skin inflammation caused by mites, scaly scalp abscess with itching under the skin
- increased eosinophils (a type of white blood cell) in the blood
- decrease in platelets (blood cells that help stop bleeding)
- head agitation
- inadequate secretion of the hormone that controls urine volume
- sugar in the urine
- potentially fatal complications of uncontrolled diabetes
- decreased blood sugar
- excessive water intake
- lack of movement or response while awake (catatonia)
- confusion
- sleepwalking
- absence of emotions
- inability to achieve orgasm
- neuroleptic malignant syndrome (confusion, decreased or lost consciousness, high fever, and severe muscle stiffness), problems in the blood vessels of the brain, including sudden loss of blood flow to the brain (stroke or "mini" stroke), unresponsiveness to stimuli, loss of consciousness, decreased level of consciousness, seizures (epileptic crises), balance disorder
- abnormal coordination
- glaucoma (increased eye pressure)
- eye movement problems, eye rotation, hypersensitivity of the eyes to light, increased tearing, redness of the eyes
- atrial fibrillation (abnormal heart rhythm), irregular heartbeat
- blood clot in the lungs that causes chest pain and difficulty breathing. If you notice any of these symptoms, seek medical attention immediately.
- blood clots in the veins, especially in the legs (symptoms include swelling, pain, and redness of the leg). If you experience any of these symptoms, seek medical help immediately.
- flushing
- difficulty breathing during sleep (sleep apnea)
- pulmonary congestion, respiratory tract congestion
- crackling sounds in the lungs, wheezing
- pancreatitis, tongue swelling, fecal incontinence, very hard stools
- intestinal obstruction
- chapped lips
- drug-related skin rash, skin thickening, dandruff
- muscle fiber breakdown and muscle pain (rhabdomyolysis)
- joint swelling
- inability to urinate
- breast discomfort, breast gland growth, breast growth
- vaginal discharge
- priapism (a prolonged erection of the penis that may require surgical treatment)
- very low body temperature, chills, feeling of thirst,
- withdrawal symptoms from the medicine
- pus accumulation due to infection at the injection site, deep skin infection, cyst at the injection site, bruise at the injection site.
Frequency Not Known: cannot be estimated from the available data
- dangerously low number of a type of white blood cell necessary to fight infections
- severe allergic reaction characterized by fever, swelling of the mouth, face, lips, or tongue, difficulty breathing, itching, rash, and sometimes a drop in blood pressure
- dangerously excessive water intake
- sleep-related eating disorder
- diabetic coma
- decrease in oxygen in parts of the body (due to decreased blood flow)
- rapid, shallow breathing, pneumonia caused by aspiration of food, voice disorder
- absence of intestinal movement that causes obstruction
- yellow color of the skin and eyes (jaundice)
- severe skin rash with blisters and peeling of the skin that can start in and around the mouth, nose, eyes, and genitals and spread to other areas of the body (Stevens-Johnson syndrome or toxic epidermal necrolysis)
- severe allergic reaction with swelling that can affect the throat, causing difficulty breathing
- skin discoloration
- posture abnormality
- newborn babies, from mothers who have been treated with paliperidone during pregnancy, may experience adverse effects from the medicine and/or withdrawal symptoms, such as irritability, weak or sustained muscle contractions, restlessness, drowsiness, breathing problems, or difficulty feeding
- decreased body temperature
- dead skin cells at the injection site and ulcer at the injection site
Reporting of Adverse Effects
If you experience any type of adverse effect, consult your doctor or nurse, even if it is a possible adverse effect that is not listed in this leaflet. You can also report them directly through the Spanish Pharmacovigilance System for Human Use Medicines: https://www.notificaRAM.es. By reporting adverse effects, you can contribute to providing more information on the safety of this medicine.
5. Conservation of BACEQ
Keep this medicine out of the sight and reach of children.
Do not use this medicine after the expiration date that appears on the pre-filled syringe and on the carton after "CAD or EXP". The expiration date is the last day of the month indicated.
This medicine does not require any special storage conditions.
Medicines should not be thrown away in drains or trash. Deposit the containers and medicines you no longer need in the SIGRE Point of the pharmacy. In case of doubt, ask your pharmacist how to dispose of the containers and medicines you no longer need. This way, you will help protect the environment.
6. Container Contents and Additional Information
BACEQ Composition
The active ingredient is paliperidone
Each BACEQ 25 mg pre-filled syringe contains 39 mg of paliperidone palmitate in 0.25 ml.
Each BACEQ 50 mg pre-filled syringe contains 78 mg of paliperidone palmitate in 0.5 ml.
Each BACEQ 75 mg pre-filled syringe contains 117 mg of paliperidone palmitate in 0.75 ml.
Each BACEQ 100 mg pre-filled syringe contains 156 mg of paliperidone palmitate in 1 ml.
Each BACEQ 150 mg pre-filled syringe contains 234 mg of paliperidone palmitate in 1.5 ml
Initial Treatment Pack:
Each BACEQ 100 mg pre-filled syringe contains 156 mg of paliperidone palmitate in 1 ml.
Each BACEQ 150 mg pre-filled syringe contains 234 mg of paliperidone palmitate in 1.5 ml
The other components are:
polysorbate 20
macrogol 4000
citric acid monohydrate
disodium phosphate
sodium dihydrogen phosphate monohydrate
sodium hydroxide (for pH adjustment)
water for injectable preparations
Product Appearance and Container Contents
BACEQ is a white to off-white prolonged-release injectable suspension, which comes in a pre-filled syringe (prolonged-release injectable)
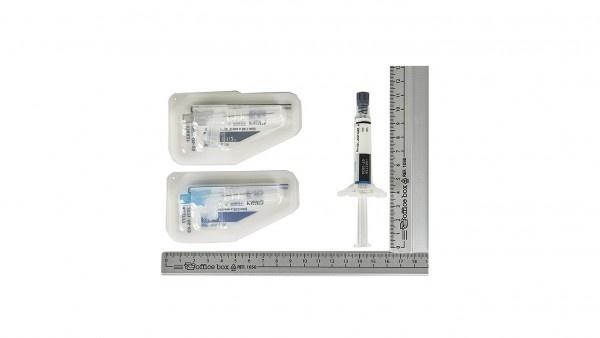
Each container contains 1 pre-filled syringe and 2 needles.
Initial Treatment Pack:
Each container contains 1 pack of BACEQ 150 mg and 1 pack of BACEQ 100 mg.
Only certain pack sizes may be marketed.
Marketing Authorization Holder and Manufacturer
Marketing Authorization Holder
Teva Pharma, S.L.U.
C/ Anabel Segura, 11, Edificio Albatros B, 1ª planta,
Alcobendas, 28108, Madrid (Spain)
Manufacturer:
Actavis Group PTC ehf.
Dalsharun 1
IS-220 Hafnarfjordur
Iceland
For further information about this medicinal product, please contact the local representative of the marketing authorization holder:
Laboratorios Farmacéuticos ROVI, S.A.
Julián Camarillo, 35
28037 – Madrid – Spain
This medicinal product is authorized in the Member States of the European Economic Area under the following names:
|
Date of the last revision of this leaflet:February 2024
Detailed information on this medicinal product is available on the website of the Spanish Agency for Medicines and Health Products (AEMPS) http://www.aemps.gob.es
This information is intended only for healthcare professionals and should be read in conjunction with the complete prescribing information (Summary of Product Characteristics).
The injectable suspension is for single use. It should be visually examined for any foreign particles before administration. Do not use the product if the syringe is not visually free of foreign particles.
The container contains a pre-filled syringe and two safety needles (one 22-gauge, 1½-inch [38.1 mm x 0.72 mm] needle and one 23-gauge, 1-inch [25.4 mm x 0.64 mm] needle) for intramuscular injection. BACEQ is also available in a treatment initiation pack that contains two pre-filled syringes (150 mg + 100 mg) and two additional safety needles.
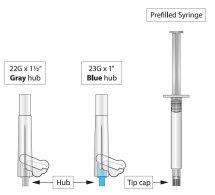
- Shake the syringe vigorously in a vertical position for at least 10 seconds to ensure a homogeneous suspension. Hold the syringe with the nozzle in a vertical position. Gently tap the syringe to ensure that all air bubbles rise to the top of the syringe
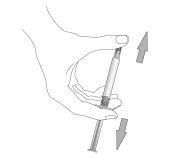
- Select the appropriate needle.
The first dose of BACEQ (150 mg) is administered on Day 1 in the DELTOID muscle using the needle for DELTOID injection. The second dose of BACEQ (100 mg) is also administered in the DELTOID muscle one week later (Day 8) using the needle for DELTOID injection.
If a patient is switched from prolonged-release injectable risperidone to BACEQ, the first injection of BACEQ (dose range of 25 mg to 150 mg) can be administered in the DELTOID muscle or the GLUTEAL muscle, using the appropriate needle for the injection site, at the time of the next scheduled injection.
Subsequently, monthly maintenance injections can be administered in either the DELTOID muscle or the GLUTEAL muscle using the appropriate needle for the injection site.
In the case of DELTOID injection, if the patient weighs <90 kg, use the 23-gauge, 1-inch (25.4 mm x 0.64 mm) needle (needle with blue hub); if patient weighs ≥ 90 22-gauge, 1½-inch (38.1 0.72 gray hub).< p>
In the case of GLUTEAL injection, use the 22-gauge, 1½-inch (38.1 mm x 0.72 mm) needle (needle with gray hub).
- While holding the syringe in a vertical position, remove the rubber protector from the nozzle with a twisting motion.
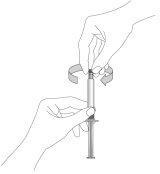
- Open the blister pack of the safety needle halfway. Hold the needle cover by the plastic paper. Hold the syringe with the nozzle pointing upwards. Attach the safety needle to the Luer connection of the syringe with a gentle twisting motion to avoid cracking or damaging the needle hub. Always check for signs of damage or leakage before administration.
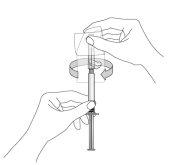
- Pull the sheath straight off to separate it from the needle. Do not twist the sheath, as the needle may become dislodged from the syringe.
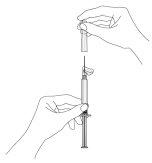
- Place the syringe with the needle in a vertical position to proceed with air elimination. Eliminate air from the syringe by carefully pushing the plunger forward until 3 drops of suspension foam are released from the syringe.
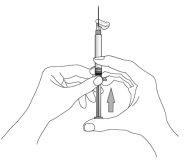
- Inject the entire contents slowly, deeply into the selected DELTOID or GLUTEAL muscle of the patient. Do not administer intravascularly or subcutaneously.
- Once the injection is complete, use your thumb or another finger (8a, 8b) or a flat surface (8c) to activate the needle protection system. The system is fully activated when a click is heard. Dispose of the syringe with the needle in an appropriate manner.
8.a
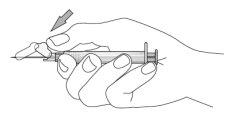
8b
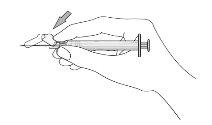
8c
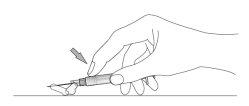
Disposal of unused medicinal products and all materials that have come into contact with them should be carried out in accordance with local regulations.
- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to BACEQ 150 MG and BACEQ 100 MG PROLONGED-RELEASE INJECTABLE SUSPENSIONDosage form: INJECTABLE, 50 mgActive substance: paliperidoneManufacturer: Teva Pharma S.L.U.Prescription requiredDosage form: INJECTABLE, 1000 mgActive substance: paliperidoneManufacturer: Janssen-Cilag International N.VPrescription requiredDosage form: INJECTABLE, 700 mgActive substance: paliperidoneManufacturer: Janssen-Cilag International N.VPrescription required
Online doctors for BACEQ 150 MG and BACEQ 100 MG PROLONGED-RELEASE INJECTABLE SUSPENSION
Discuss questions about BACEQ 150 MG and BACEQ 100 MG PROLONGED-RELEASE INJECTABLE SUSPENSION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions











