ASTARTE 0.25 mg/0.5 mL Injectable Solution in Pre-filled Syringe
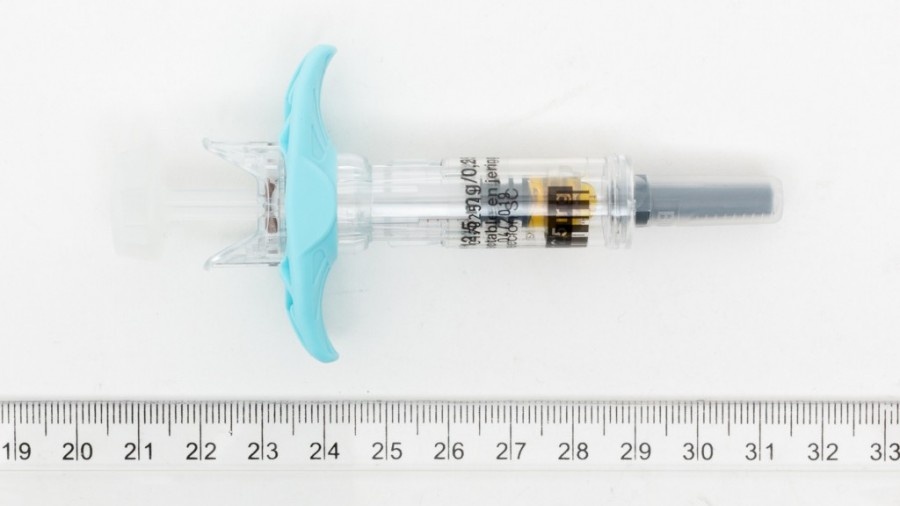

How to use ASTARTE 0.25 mg/0.5 mL Injectable Solution in Pre-filled Syringe
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
Introduction
Package Leaflet: Information for the User
Astarté 0.25 mg/0.5 ml solution for injection in a pre-filled syringe EFG
ganirelix
Read all of this leaflet carefully before you start using this medicine because it contains important information for you.
- Keep this leaflet, you may need to read it again.
- If you have any further questions, ask your doctor, pharmacist, or nurse.
- This medicine has been prescribed for you only. Do not pass it on to others. It may harm them, even if their signs of illness are the same as yours.
- If you get any side effects, talk to your doctor, pharmacist, or nurse. This includes any possible side effects not listed in this leaflet. See section 4.
Contents of the package leaflet
- What is Astarté and what is it used for
- What you need to know before you use Astarté
- How to use Astarté
- Possible side effects
- Storage of Astarté
- Contents of the pack and other information
1. What is Astarté and what is it used for
Astarté contains the active substance ganirelix and belongs to a group of medicines called “gonadotropin-releasing hormone antagonists” that act against the action of endogenous gonadotropin-releasing hormone (GnRH). GnRH regulates the release of gonadotropins (luteinizing hormone (LH) and follicle-stimulating hormone (FSH)). Gonadotropins play an important role in human fertility and reproduction. FSH is necessary in women for the growth and development of follicles in the ovaries. Follicles are small, rounded vesicles that contain the eggs. LH is necessary for the release of mature eggs from the ovarian follicles (i.e., ovulation). This medicine inhibits the action of GnRH, which causes the suppression of the release of LH in particular.
What ganirelix is used for
In women undergoing assisted reproduction techniques, such as in vitro fertilization (IVF) and other methods, premature ovulation may occasionally occur, which significantly reduces the likelihood of becoming pregnant. This medicine is used to prevent the premature release of LH, which can cause premature ovulation.
In clinical studies, ganirelix was used with recombinant follicle-stimulating hormone (FSH) or with corifollitropin alfa, a long-acting follicular stimulant.
2. What you need to know before you use Astarté
Do not use Astarté
- if you are allergic to ganirelix or any of the other ingredients of this medicine (listed in section 6).
- if you are hypersensitive to gonadotropin-releasing hormone (GnRH) or its analogs;
- if you have moderate or severe kidney or liver disease;
- if you are pregnant or breastfeeding.
Warnings and precautions
Consult your doctor, pharmacist, or nurse before starting treatment with this medicine
- if you have an active allergy, inform your doctor. Your doctor will decide, depending on the severity, if additional monitoring is needed during treatment. Allergic reactions have been observed, even after the first dose.
- allergic reactions, both generalized and local, including hives (urticaria), swelling of the face, lips, tongue, and/or throat that can cause difficulty breathing and/or swallowing (angioedema and/or anaphylaxis) (see also section 4). If you have an allergic reaction, stop using this medicine and seek medical attention immediately.
- during or after hormonal stimulation of the ovaries, ovarian hyperstimulation syndrome may develop. This syndrome is related to the gonadotropin stimulation procedure. We recommend that you read the package leaflet of the gonadotropin medicine that you have been prescribed.
- the incidence of congenital malformations (birth defects) after the use of assisted reproduction techniques may be slightly higher than after spontaneous conceptions. This slightly higher incidence is considered to be related to the characteristics of patients undergoing fertility treatments (e.g., woman's age, semen characteristics) and the higher incidence of multiple pregnancies (pregnancy with more than one baby at a time) recorded after the use of assisted reproduction techniques. The incidence of birth defects after the use of assisted reproduction techniques with this medicine is not different from the incidence with the use of other GnRH analogs in assisted reproduction techniques.
- there is a slight increase in the risk of an ectopic pregnancy (a pregnancy that develops outside the uterus) in women with damaged Fallopian tubes.
- the efficacy and safety of this medicine have not been established in women who weigh less than 50 kg or more than 90 kg. Consult your doctor for more information.
Children and adolescents
This medicine is not intended for use in children or adolescents.
Other medicines and Astarté
Inform your doctor or pharmacist if you are using, have recently used, or might use any other medicines.
Pregnancy, breastfeeding, and fertility
If you are pregnant or breastfeeding, think you may be pregnant, or plan to become pregnant, consult your doctor or pharmacist before using this medicine.
This medicine should be used during controlled ovarian stimulation for assisted reproduction techniques (ART).
Do not use this medicine during pregnancy and breastfeeding.
Driving and using machines
The effects on the ability to drive and use machines have not been studied.
This medicine contains sodium
This medicine contains less than 1 mmol of sodium (23 mg) per injection; i.e., it is essentially "sodium-free".
3. How to use Astarté
This medicine is used as part of the treatment in assisted reproduction techniques (ART), including in vitro fertilization (IVF).
You will administer the injections yourself, so your doctor should explain how to do it. Follow the administration instructions of this medicine exactly as indicated by your doctor or pharmacist. If you are in doubt, consult your doctor or pharmacist again.
Phase 1
Ovarian stimulation with follicle-stimulating hormone (FSH) or corifollitropin may start on the second or third day of your menstruation.
Phase 2
The contents of the syringe of this medicine (0.25 mg) should be injected once a day just under the skin, starting on the fifth or sixth day of stimulation. Depending on your ovarian response, your doctor may decide to start on another day.
This medicine and FSH should be administered approximately at the same time. However, these medicines should not be mixed and should be injected in different locations.
Daily treatment with this medicine should continue until there are enough follicles of adequate size.
Phase 3
The final maturation of the eggs in the follicles can be induced by administering human chorionic gonadotropin (hCG). The time between two injections of this medicine and between the last injection of this medicine and the injection of hCG should not exceed 30 hours, otherwise, premature ovulation (i.e., release of the eggs) may occur. Therefore, if the injection of this medicine is in the morning, treatment with this medicine should be maintained throughout the entire period of treatment with gonadotropin, including the day of ovulation induction. If the injection of this medicine is in the afternoon, the last injection of this medicine should be administered on the evening before the day of ovulation induction.
Instructions for use
- Injection site
This medicine comes in pre-filled syringes that contain a dose. The contents of the syringe should be injected slowly just under the skin, preferably in the thigh. Check the solution before use. Do not use the solution if it contains particles or is not transparent. You may notice air bubbles in the pre-filled syringe. This is to be expected and does not require the removal of the air bubbles. If you or your partner administer the injections, follow the instructions below carefully. Do not mix this medicine with other medicines.
- Preparing the injection site
Wash your hands thoroughly with water and soap. The injection site should be cleaned with a disinfectant (e.g., alcohol) to remove bacteria from the surface. Clean an area of about 5 cm around the injection point and let the disinfectant dry for at least one minute before injecting.
- Inserting the needle
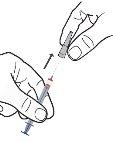
- Take 1 syringe from the packaging by holding it by the body. Do not hold the syringe by the plunger.
- Hold the syringe in a vertical positionand remove the needle cap without pressing or making rotational movements.
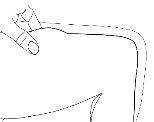
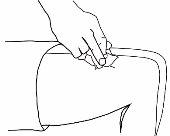
- Pinch a large area of skin between your index and thumb fingers.
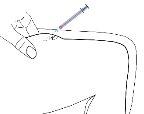
- Insert the needle into the base of the pinched skin at an angle of 45° with respect to the skin surface.
1 | 2 | 3 |
|
|
|
For each injection, the injection site should be varied.
- Checking the correct position of the needle
Gently pull back the plunger to check if the needle is correctly positioned.
If blood enters the syringe, it means that the tip of the needle has penetrated a blood vessel. If this happens, do not inject this medicine. Remove the syringe, cover the injection site with a swab with disinfectant, and press; it should stop bleeding within one or two minutes. Do not use this syringe and dispose of it properly. Start again with a new syringe.
- Injecting the solution
Once the needle is correctly positioned, press the plunger slowly and constantly to inject the solution correctly and avoid damaging the skin tissues.
- Removing the syringe
Remove the syringe quickly.
Press on the injection site with a swab with disinfectant. Use the pre-filled syringe only once.
If you use more Astarté than you should
Consult your doctor.
If you forget to use Astarté
If you realize that you have forgotten to inject a dose, administer it as soon as possible.
Do not take a double dose to make up for forgotten doses.
If you delay more than 6 hours (i.e., the interval between two injections is prolonged more than 30 hours), administer the dose as soon as possible and consult your doctor for advice.
If you stop treatment with Astarté
Do not stop using this medicine unless your doctor tells you to, as this may affect the outcome of your treatment.
If you have any further questions on the use of this medicine, ask your doctor, pharmacist, or nurse.
4. Possible side effects
Like all medicines, this medicine can cause side effects, although not everybody gets them.
Very common (may affect more than 1 in 10 women)
- Local reactions at the injection site (mainly redness, with or without swelling). The local reaction usually disappears within 4 hours after administration.
Uncommon (may affect up to 1 in 100 women)
- headache
- nausea (feeling sick)
- malaise (general feeling of being unwell)
Very rare (may affect up to 1 in 10,000 women)
- allergic reactions have been observed, even after the first dose
- rash
- facial swelling
- difficulty breathing (dyspnea)
- swelling of the face, lips, tongue, and/or throat, which can cause difficulty breathing and/or swallowing (angioedema and/or anaphylaxis)
- hives (urticaria).
Additionally, side effects related to controlled ovarian hyperstimulation have been observed, such as:
- abdominal pain,
- ovarian hyperstimulation syndrome (OHSS), (OHSS occurs when the ovaries react excessively to the fertility medicines you are taking)
- ectopic pregnancy (when the embryo develops outside the uterus)
- miscarriage (see the package leaflet of the FSH medicine you are using).
After the first dose of ganirelix, worsening of a pre-existing eczema has been reported in one patient.
Reporting of side effects
If you experience any side effects, talk to your doctor, pharmacist, or nurse, even if it is possible side effects not listed in this leaflet. You can also report side effects directly through the Spanish Pharmacovigilance System for Human Use Medicines: www.notificaram.es. By reporting side effects, you can help provide more information on the safety of this medicine.
5. Storage of Astarté
Keep this medicine out of the sight and reach of children.
Do not use this medicine after the expiry date which is stated on the label and carton after EXP. The expiry date is the last day of the month shown.
This medicine does not require any special storage conditions.
Inspect the syringe before use. The syringe should only be used if the solution is transparent and particle-free and the packaging is not damaged.
Medicines should not be disposed of via wastewater or household waste. Dispose of the packaging and medicines you no longer need in the SIGRE collection point at the pharmacy. If you are in doubt, ask your pharmacist how to dispose of the packaging and medicines you no longer need. This will help protect the environment.
6. Contents of the pack and other information
Composition of Astarté
- The active substance is ganirelix. Each pre-filled syringe contains 0.25 mg of ganirelix (as acetate) in 0.5 ml of aqueous solution.
- The other ingredients are glacial acetic acid, mannitol, and water for injections. The pH (a measure of acidity) may have been adjusted with sodium hydroxide and glacial acetic acid.
Appearance and packaging of the product
This medicine is a clear and colorless aqueous solution for injection. The solution is ready to use and should be administered subcutaneously.
This medicine is available in packs of 1 or 5 pre-filled syringes with injection needles (27 G), as specified below:
- 1 pre-filled syringe
- 5 pre-filled syringes
Not all pack sizes may be marketed.
Marketing authorization holder and manufacturer
GP-Pharm, S.A.
Pol. Ind. Els Vinyets – Els Fogars Sector 2
Carretera comarcal 244, km22
08777 Sant Quintí de Mediona, Barcelona
Spain
This medicine is authorized in the Member States of the European Economic Area under the following names:
Portugal: Astarté
Spain: Astarté 0.25 mg/0.5 ml solution for injection in a pre-filled syringe EFG
Date of last revision of this leaflet:08/2023
Detailed information on this medicine is available on the website of the Spanish Agency for Medicines and Health Products (AEMPS) http://www.aemps.gob.es/.
- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to ASTARTE 0.25 mg/0.5 mL Injectable Solution in Pre-filled SyringeDosage form: INJECTABLE, 0.25 mg/0.5 mgActive substance: ganirelixManufacturer: Sun Pharmaceutical Industries (Europe) B.V.Prescription requiredDosage form: INJECTABLE, 0.25 mg/0.5 mLActive substance: ganirelixManufacturer: Gedeon Richter Plc.Prescription requiredDosage form: INJECTABLE, UnknownActive substance: ganirelixManufacturer: Organon N.V.Prescription required
Online doctors for ASTARTE 0.25 mg/0.5 mL Injectable Solution in Pre-filled Syringe
Discuss questions about ASTARTE 0.25 mg/0.5 mL Injectable Solution in Pre-filled Syringe, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions