
Spiriva Respimat

Zapytaj lekarza o receptę na Spiriva Respimat

Jak stosować Spiriva Respimat
Ulotka dołączona do opakowania: informacja dla pacjenta
Spiriva Respimat, 2,5 mikrograma/dawkę odmierzoną, roztwór do inhalacji
Tiotropium
Należy uważnie zapoznać się z treścią ulotki przed przyjęciem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Spiriva Respimat i w jakim celu się go stosuje
- 2. Informacje ważne przed przyjęciem leku Spiriva Respimat
- 3. Jak przyjmować lek Spiriva Respimat
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Spiriva Respimat
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Spiriva Respimat i w jakim celu się go stosuje
Lek Spiriva Respimat ułatwia oddychanie pacjentom chorym na przewlekłą obturacyjną chorobę płuc
(POChP) lub astmę. POChP to przewlekła choroba płuc, która powoduje duszność i kaszel. POChP
jest związana z przewlekłym zapaleniem oskrzeli i rozedmą płuc. Astma jest przewlekłą chorobą
charakteryzującą się zapaleniem dróg oddechowych i ich zwężeniem.
POChP i astma są chorobami przewlekłymi, dlatego lek Spiriva Respimat należy przyjmować
codziennie, a nie tylko wtedy, gdy występują problemy z oddychaniem lub inne objawy. W leczeniu
astmy lek Spiriva Respimat należy przyjmować jako lek dodatkowy razem z tzw. kortykosteroidami
wziewnymi i długo działającymi beta-2-agonistami.
Spiriva Respimat to lek rozszerzający oskrzela o długotrwałym działaniu, który pomaga otworzyć
drogi oddechowe i ułatwia przedostawanie się powietrza do i z płuc. Regularne stosowanie leku
Spiriva Respimat może także pomóc w zmniejszeniu utrzymującej się duszności związanej z chorobą
i pomoże zmniejszyć skutki choroby odczuwalne w życiu codziennym. Codzienne stosowanie leku
Spiriva Respimat pomoże także zapobiec nagłemu, krótkotrwałemu zaostrzeniu objawów POChP,
które może trwać przez kilka dni.
Aby prawidłowo dawkować i stosować lek Spiriva Respimat, patrz punkt 3. Jak przyjmować lek
Spiriva Respimat oraz instrukcja dotycząca stosowania inhalatora wielokrotnego użytku Respimat (re-
usable) na końcu ulotki.
2. Informacje ważne przed przyjęciem leku Spiriva Respimat
Kiedy nie przyjmować leku Spiriva Respimat:
- jeśli pacjent ma uczulenie (nadwrażliwość) na tiotropium lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6),
- jeśli pacjent ma uczulenie (nadwrażliwość) na atropinę lub jej pochodne, np. ipratropium lub oksytropium.
Ostrzeżenia i środki ostrożności
Przed przyjęciem leku Spiriva Respimat należy skonsultować się z lekarzem lub farmaceutą.
Należy skonsultować się z lekarzem, jeżeli u pacjenta występują: jaskra z wąskim kątem przesączania,
problemy dotyczące gruczołu krokowego (prostaty) lub trudności z oddawaniem moczu.
Jeżeli u pacjenta występują problemy dotyczące nerek, należy skonsultować się z lekarzem.
Podczas inhalacji leku Spiriva Respimat należy uważać, aby lek nie dostał się do oczu, gdyż mogą
wtedy wystąpić: ból oka albo dyskomfort, niewyraźne widzenie, widzenie tęczowej obwódki wokół
źródła światła lub zmienione widzenie kolorów z towarzyszącym zaczerwienieniem oczu (tzn. jaskra
z wąskim kątem przesączania). Objawom niepożądanym dotyczącym oczu mogą towarzyszyć ból
głowy, nudności lub wymioty. Jeżeli lek dostał się do oczu, należy przemyć je ciepłą wodą, przerwać
stosowanie bromku tiotropiowego i natychmiast zgłosić się do lekarza w celu uzyskania dalszych
wskazówek.
Jeśli nasilą się problemy z oddychaniem lub wystąpi wysypka, obrzęk lub swędzenie, bezpośrednio po
inhalacji, należy przerwać stosowanie leku i natychmiast zgłosić się do lekarza.
Suchość błony śluzowej jamy ustnej występująca w czasie stosowania leku o działaniu
przeciwcholinergicznym, może po dłuższym czasie powodować próchnicę zębów, dlatego należy
pamiętać o utrzymaniu higieny jamy ustnej.
Lek Spiriva Respimat jest wskazany w podtrzymującym leczeniu przewlekłej obturacyjnej choroby
płuc lub astmy. Nie przyjmować tego leku do leczenia nagłych napadów duszności lub świszczącego
oddechu .W tym celu lekarz przepisze inny inhalator („lek doraźny”). Należy przestrzegać zaleceń
lekarza.
Jeśli pacjentowi zalecono stosowanie leku Spiriva Respimat w celu leczenia astmy, należy go
stosować jako lek dodatkowy do leczenia obejmującego kortykosteroid wziewny i długo działających
beta-2-agonistów. Należy kontynuować stosowanie kortykosteroidu wziewnego zgodnie z zaleceniami
lekarza, nawet jeśli pacjent poczuje się lepiej.
Jeśli pacjent przebył w czasie ostatnich 6 miesięcy zawał serca, doświadczył zaburzeń pracy serca lub
zagrażającego życiu nieregularnego bicia serca, lub ciężkiej niewydolności serca w ciągu ostatniego
roku, należy zawiadomić o tym lekarza. Pozwoli to zadecydować, czy lek Spiriva Respimat nadal jest
odpowiedni do stosowania.
Leku Spiriva Respimat nie należy stosować częściej niż raz na dobę.
Należy również skontaktować się z lekarzem, jeśli wystąpi uczucie trudności w oddychaniu.
Pacjenci z mukowiscydozą powinni poinformować lekarza, ponieważ lek Spiriva Respimat może
nasilać objawy mukowiscydozy.
Dzieci i młodzież
Lek Spiriva Respimat nie jest zalecany do stosowania u dzieci w wieku poniżej 6 lat.
Spiriva Respimat a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować, w tym o lekach wydawanych
bez recepty.
W szczególności należy poinformować lekarza lub farmaceutę o przyjmowaniu innych leków o
działaniu przeciwcholinergicznym, takich jak ipratropium czy oksytropium.
Nie zanotowano działań niepożądanych podczas przyjmowania leku Spiriva Respimat z innymi
lekami stosowanymi w leczeniu POChP i astmy, takimi jak doraźne leki wziewne (np. salbutamol),
metyloksantyny (np. teofilina), leki przeciwhistaminowe, leki mukolityczne (np. ambroksol), leki
przeciwleukotrienowe (np. montelukast), kromony, leki anty-IgE (np. omalizumab) i (lub) wziewne
lub doustne steroidy (np. budezonid, prednizolon).
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza, że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza przed zastosowaniem tego leku.
Nie należy przyjmować tego leku, chyba że na wyraźne zalecenie lekarza.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie przeprowadzono badań nad wpływem leku na zdolność prowadzenia pojazdów i obsługiwania
maszyn. Jeżeli wystąpią zawroty głowy lub niewyraźne widzenie, zdolność prowadzenia pojazdów
i obsługiwania maszyn może być zaburzona.
Spiriva Respimat zawiera chlorek benzalkoniowy
Ten lek zawiera 0,0011 mg chlorku benzalkoniowego w każdym rozpyleniu.
Chlorek benzalkoniowy może powodować świszczący oddech lub zaburzenia oddechowe (skurcz
oskrzeli), zwłaszcza u pacjentów z astmą.
3. Jak przyjmować lek Spiriva Respimat
Ten lek należy zawsze przyjmować zgodnie z zaleceniami lekarza lub farmaceuty. W razie
wątpliwości należy zwrócić się do lekarza lub farmaceuty.
Lek Spiriva Respimat przeznaczony jest wyłącznie do inhalacji.
Zalecana dawka leku dla pacjentów w wieku 6 lat i starszych to:
Lek Spiriva Respimat działa przez 24 godziny, dlatego należy go przyjmować RAZ NA DOBĘ,
w miarę możliwości o tej samej porze.
Przy każdym użyciu należy wykonać DWA ROZPYLENIA.
Ponieważ POChP i astma są chorobami przewlekłymi, lek Spiriva Respimat należy przyjmować
każdego dnia, a nie tylko w momencie wystąpienia problemów z oddychaniem. Nie należy
przekraczać zalecanej dawki.
Należy upewnić się, że prawidłowo stosuje się inhalator wielokrotnego użytku Respimat (re-usable).
Instrukcja dotycząca używania inhalatora wielokrotnego użytku Respimat (re-usable) jest
zamieszczona na końcu ulotki, patrz punkt „Instrukcja użycia inhalatora wielokrotnego użytku
Respimat (re-usable)”.
Stosowanie u dzieci i młodzieży
Lek Spiriva Respimat nie jest zalecany do stosowania u dzieci w wieku poniżej 6 lat, ze względu na
brak danych dotyczących bezpieczeństwa stosowania i skuteczności.
Przyjęcie większej niż zalecana dawki leku Spiriva Respimat
W razie przyjęcia większej dawki leku Spiriva Respimat niż dwa rozpylenia na dobę należy
natychmiast skontaktować się z lekarzem.
U pacjenta może zwiększyć się ryzyko wystąpienia objawów niepożądanych, takich jak suchość błony
śluzowej jamy ustnej, zaparcia, trudności w oddawaniu moczu, przyspieszenie akcji serca lub
niewyraźne widzenie.
Pominięcie przyjęcia leku Spiriva Respimat
W przypadku pominięcia zastosowania dawki (DWA ROZPYLENIA RAZ NA DOBĘ) należy przyjąć
pominiętą dawkę najszybciej jak to możliwe, ale nie należy stosować dwóch dawek jednocześnie lub
w tym samym dniu. Następną dawkę należy przyjąć o zwykłej porze.
Przerwanie przyjmowania leku Spiriva Respimat
Przed przerwaniem przyjmowania leku Spiriva Respimat należy poradzić się lekarza lub farmaceuty.
Po przerwaniu przyjmowania leku Spiriva Respimat mogą nasilić się objawy POChP i astmy.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku, należy zwrócić
się do lekarza lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Ocena działań niepożądanych została przeprowadzona na podstawie następującej konwencji częstości
występowania:
Często:
mogą wystąpić rzadziej niż u 1 na 10 pacjentów
Niezbyt często:
mogą wystąpić rzadziej niż u 1 na 100 pacjentów
Rzadko:
mogą wystąpić rzadziej niż u 1 na 1000 pacjentów
Częstość nieznana:
częstość nie może być określona na podstawie dostępnych danych
Poniższe działania niepożądane występowały u pacjentów przyjmujących lek i zostały uporządkowane
według częstości występowania jako występujące często, niezbyt często, rzadko lub z nieznaną
częstością.
| Działanie niepożądane | Częstość występowania POChP | Częstość występowania Astma |
| Suchość błony śluzowej jamy ustnej | Często | Niezbyt często |
| Chrypka (dysfonia) | Niezbyt często | Niezbyt często |
| Kaszel | Niezbyt często | Niezbyt często |
| Ból głowy | Niezbyt często | Niezbyt często |
| Zapalenie gardła | Niezbyt często | Niezbyt często |
| Bolesne oddawanie moczu (dyzuria) | Niezbyt często | Częstość nieznana |
| Zawroty głowy | Niezbyt często | Niezbyt często |
| Zakażenia grzybicze jamy ustnej i gardła (kandydoza jamy ustnej i gardła) | Niezbyt często | Niezbyt często |
| Trudności w oddawaniu moczu (zatrzymanie moczu) | Niezbyt często | Częstość nieznana |
| Zaparcia | Niezbyt często | Rzadko |
| Wysypka | Niezbyt często | Niezbyt często |
| Swędzenie (świąd) | Niezbyt często | Rzadko |
| Wzrost ciśnienia wewnątrzgałkowego | Rzadko | Częstość nieznana |
| Ciężkie reakcje alergiczne powodujące obrzęk warg i twarzy lub gardła (obrzęk naczynioruchowy) | Rzadko | Rzadko |
| Bezsenność | Rzadko | Niezbyt często |
| Nieregularne bicie serca (migotanie przedsionków, częstoskurcz nadkomorowy) | Rzadko | Częstość nieznana |
| Kołatanie serca | Rzadko | Niezbyt często |
| Krwawienie z nosa | Rzadko | Rzadko |
| Zapalenie języka | Rzadko | Częstość nieznana |
| Przyspieszone bicie serca (tachykardia) | Rzadko | Częstość nieznana |
| Ucisk w klatce piersiowej, z towarzyszącym kaszlem, świszczącym oddechem lub dusznością bezpośrednio po inhalacji (skurcz oskrzeli) | Rzadko | Niezbyt często |
| Trudności w przełykaniu (dysfagia) | Rzadko | Częstość nieznana |
| Działanie niepożądane | Częstość występowania POChP | Częstość występowania Astma |
| Widzenie tęczowej obwódki wokół źródła światła lub zmienione widzenie kolorów jednocześnie z zaczerwienieniem oczu (jaskra) | Rzadko | Częstość nieznana |
| Niewyraźne widzenie | Rzadko | Częstość nieznana |
| Zapalenie krtani | Rzadko | Częstość nieznana |
| Próchnica zębów | Rzadko | Częstość nieznana |
| Zapalenie dziąseł | Rzadko | Rzadko |
| Pokrzywka | Rzadko | Rzadko |
| Zakażenie skóry lub owrzodzenie skóry | Rzadko | Częstość nieznana |
| Sucha skóra | Rzadko | Częstość nieznana |
| Zakażenia dróg moczowych | Rzadko | Rzadko |
| Zgaga (choroba refluksowa przełyku) | Rzadko | Częstość nieznana |
| Nadwrażliwość, w tym reakcje natychmiastowe | Częstość nieznana | Rzadko |
| Zapalenie jamy ustnej | Częstość nieznana | Rzadko |
| Odwodnienie | Częstość nieznana | Częstość nieznana |
| Zapalenie zatok | Częstość nieznana | Częstość nieznana |
| Niedrożność jelit lub brak ruchów robaczkowych jelit (niedrożność jelit, w tym porażenna niedrożność jelit) | Częstość nieznana | Częstość nieznana |
| Nudności | Częstość nieznana | Częstość nieznana |
| Ciężkie reakcje alergiczne (reakcje anafilaktyczne) | Częstość nieznana | Częstość nieznana |
| Obrzęk stawów | Częstość nieznana | Częstość nieznana |
Po zastosowaniu leku Spiriva Respimat natychmiastowe reakcje alergiczne, takie jak wysypka,
pokrzywka, obrzęk w obrębie jamy ustnej i twarzy lub nagłe trudności w oddychaniu (obrzęk
naczynioruchowy) lub inne reakcje nadwrażliwości (takie jak nagłe obniżenie ciśnienia krwi lub
zawroty głowy), mogą wystąpić samodzielnie lub jako część ciężkiej reakcji alergicznej (reakcji
anafilaktycznej).
Podobnie jak w przypadku innych leków stosowanych wziewnie, bezpośrednio po inhalacji leku
Spiriva Respimat u niektórych pacjentów może wystąpić nagły ucisk w klatce piersiowej, kaszel,
świszczący oddech lub duszność (skurcz oskrzeli).
W przypadku wystąpienia któregokolwiek z tych objawów, należy natychmiast skontaktować się
z lekarzem.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Działania niepożądane można zgłaszać
bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych
Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych,
Al. Jerozolimskie 181 C, 02-222 Warszawa, tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309, strona
internetowa: https://smz.ezdrowie.gov.pl.
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu. Dzięki zgłaszaniu
działań niepożądanych można będzie zgromadzić więcej informacji na temat bezpieczeństwa
stosowania leku.
5. Jak przechowywać lek Spiriva Respimat
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku oraz na etykiecie
wkładu z lekiem po: EXP. Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie zamrażać.
Okres ważności po pierwszym użyciu:
Należy wymienić wkład z lekiem nie później niż trzy miesiące po umieszczeniu go w inhalatorze.
Nie należy stosować inhalatora wielokrotnego użytku Respimat (re-usable) przez dłużej niż jeden rok.
Zalecane stosowanie: 6 wkładów z lekiem na inhalator.
Uwaga: Działanie inhalatora wielokrotnego użytku RESPIMAT (re-usable) wykazano w badaniach
dla 540 rozpyleń (odpowiada 9 wkładom z lekiem).
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Spiriva Respimat
Substancją czynną leku jest tiotropium. Dawka odmierzona zawiera 2,5 mikrograma tiotropium w
jednym rozpyleniu (na jedną dawkę leczniczą składają się dwa rozpylenia), co odpowiada 3,124
mikrogramom jednowodnego bromku tiotropiowego. Dawka odmierzona jest to dawka, która po
przejściu przez ustnik inhalatora jest dostępna dla pacjenta.
Pozostałe składniki to: benzalkoniowy chlorek, disodu edetynian, woda oczyszczona oraz kwas solny
3,6% do ustalenia pH.
Jak wygląda lek Spiriva Respimat i co zawiera opakowanie
Lek Spiriva Respimat 2,5 mikrograma/dawkę odmierzoną składa się z jednego wkładu z roztworem do
inhalacji oraz z jednego inhalatora Respimat. Wkład musi zostać umieszczony w inhalatorze przed
pierwszym użyciem.
Opakowanie pojedyncze: 1 inhalator wielokrotnego użytku Respimat (re-usable) oraz 1 wkład
z lekiem dostarczający 60 rozpyleń (30 dawek leczniczych).
Opakowanie potrójne: 1 inhalator wielokrotnego użytku Respimat (re-usable) i 3 wkłady z lekiem,
każdy dostarczający 60 rozpyleń (30 dawek leczniczych).
Pojedyncze opakowanie uzupełniające: 1 wkład z lekiem dostarczający 60 rozpyleń (30 dawek
leczniczych).
Potrójne opakowanie uzupełniające: 3 wkłady z lekiem, każdy dostarczający 60 rozpyleń (30 dawek
leczniczych).
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny:
Boehringer Ingelheim International GmbH
Binger Strasse 173
55216 Ingelheim am Rhein
Niemcy
Wytwórca:
Boehringer Ingelheim Pharma GmbH & Co. KG
Binger Strasse 173
55216 Ingelheim am Rhein
Niemcy
Boehringer Ingelheim España, SA
c/ Prat de la Riba, 50
08174 Sant Cugat del Vallès (Barcelona)
Hiszpania
Boehringer Ingelheim France
100-104 Avenue de France
75013 Paryż
Francja
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do przedstawiciela podmiotu
odpowiedzialnego:
Polska
Boehringer Ingelheim Sp. z o.o.
Tel: +48 22 699 0 699
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego oraz w Wielkiej Brytanii (Irlandia Północna) pod następującymi nazwami:
Austria, Liechtenstein, Belgia, Luksemburg, Cypr, Czechy, Dania, Estonia, Finlandia, Francja,
Niemcy, Grecja, Węgry, Islandia, Irlandia, Malta, Wielka Brytania (Irlandia Północna), Włochy,
Łotwa, Litwa, Holandia, Norwegia, Polska, Portugalia, Rumunia, Słowacja, Słowenia, Hiszpania,
Szwecja: Spiriva Respimat
Bułgaria : Спирива Респимат
Data ostatniej aktualizacji ulotki: 12/2024
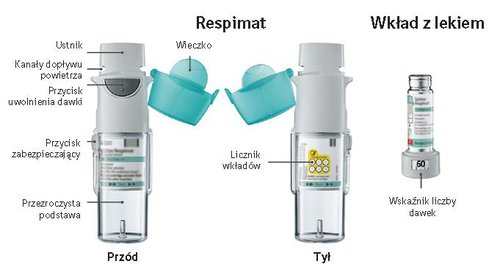
Instrukcja użycia inhalatora wielokrotnego użytku Respimat (re-usable)
Respimat jest inhalatorem wytwarzającym aerozol do inhalacji. Respimat przeznaczony jest tylko dla
jednego pacjenta. Jeden wkład z lekiem dostarcza wiele dawek. Inhalator wielokrotnego użytku
Respimat (re-usable) umożliwia wymianę wkładu z lekiem i może być używany z maksymalnie 6
wkładami
Należy zapoznać się z poniższymi instrukcjami przed rozpoczęciem stosowania leku Spiriva
Respimat.
Ten inhalator należy stosować tylko RAZ NA DOBĘ. Za każdym razem należy wdychać lek
uwolniony w czasie DWÓCH ROZPYLEŃ.
- Jeżeli Spiriva Respimat nie był używany przez dłużej niż 7 dni, należy wykonać jedno rozpylenie po skierowaniu inhalatora ku dołowi.
- Jeżeli Spiriva Respimat nie był używany przez dłużej niż 21 dni, należy powtarzać czynności opisane w punktach 4-6 w sekcji „Przygotowanie do użycia” do momentu, gdy widoczna będzie mgiełka. Następnie powtórzyć czynności opisane w punktach 4 do 6 jeszcze trzy razy.
Jak dbać o inhalator Respimat wielokrotnego użytku (re-usable)
Co najmniej raz na tydzień czyścić ustnik łącznie z jego metalową częścią umieszczoną w środku
jedynie wilgotną ściereczką bądź chusteczką.
Mała zmiana koloru ustnika nie wpływa na działanie inhalatora wielokrotnego użytku Respimat (re-
usable).
W razie potrzeby przetrzeć powierzchnię zewnętrzną inhalatora wielokrotnego użytku Respimat (re-
usable) wilgotną ściereczką.
Kiedy należy wymienić inhalator
Po użyciu inhalatora z 6 wkładami, należy zakupić nowe opakowanie Spiriva Respimat zawierające
inhalator. Inhalatora wielokrotnego użytku Respimat (re-usable) nie należy używać dłużej niż jeden
rok od włożenia pierwszego wkładu.


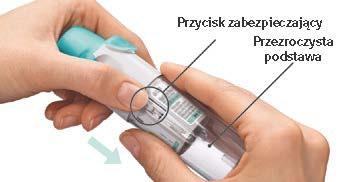
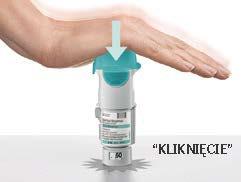
Przygotowanie do użycia
|  |
|   |
|  |
 | |
|  |
|  |
|  |
Codzienne używanie
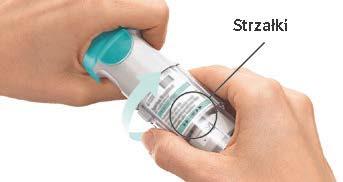
OBRÓĆ
| 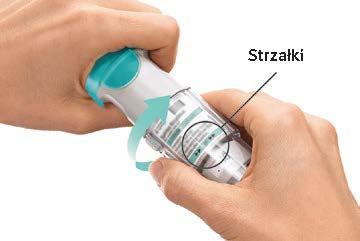 |
OTWÓRZ
|  |
NACIŚNIJ
| 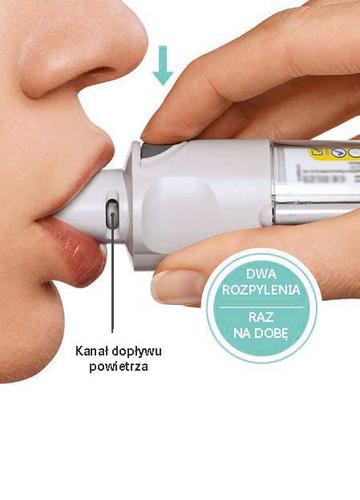 |
Kiedy należy wymienić wkład z lekiem Spiriva Respimat
Wskaźnik dawki pokazuje liczbę pozostałych rozpyleń we wkładzie z lekiem.

Pozostało 60 rozpyleń

Pozostało mniej niż 10 rozpyleń. Należy zakupić kolejny wkład z lekiem.

Wkład z lekiem został zużyty. Obróć przezroczystą podstawę w celu jego uwolnienia.
Inhalator jest teraz zablokowany. Wyjmij wkład z lekiem z inhalatora wielokrotnego użytku.
Włóż nowy wkład z lekiem do inhalatora do momentu usłyszenia kliknięcia (patrz punkt 2).
Nowo włożony wkład będzie bardziej wystawał niż wkład włożony jako pierwszy (kontynuuj
od punktu 3). Pamiętaj o włożeniu przezroczystej podstawy na miejsce w celu odblokowania
inhalatora.
Odpowiedzi na najczęściej zadawane pytania
Pojawiają się trudności z umieszczeniem wkładu z lekiem wystarczająco głęboko.
Czy przypadkowo obrócono przezroczystą podstawę przed umieszczeniem wkładu z lekiem?
Otwórz wieczko, naciśnij przycisk uwolnienia dawki i następnie umieść wkład z lekiem.
Czy wymieniasz wkład?
Kolejny, nowy wkład będzie wystawał w większym stopniu niż pierwszy wkład. Włóż go, aż
usłyszysz kliknięcie, a następnie nałóż przezroczystą podstawę.
Nie mogę nacisnąć przycisku uwolnienia dawki.
Czy włożono przezroczystą podstawę na miejsce?Jeśli nie, włóż przezroczystą podstawę na
miejsce. Inhalator wielokrotnego użytku Respimat (re-usable) działa tylko z przezroczystą podstawą
założoną w odpowiednim miejscu.
Czy obrócono przezroczystą podstawę?Jeżeli nie, obróć przezroczystą podstawę ciągłym ruchem
do momentu usłyszenia kliknięcia (pół obrotu).
Czy wskaźnik liczby dawek na wkładzie z lekiem wyświetla białą strzałkę na czerwonym tle?
Twój wkład z lekiem jest zużyty. Włóż nowy wkład i włóż przezroczystą podstawę na miejsce.
Po zużyciu trudno jest wyjąć wkład z lekiem.
Pociągnij i jednocześnie obróć wkład z lekiem.
Nie mogę obrócić lub nałożyć przezroczystej podstawy na miejsce .
Czy przezroczysta podstawa jest luźna i czy wskaźnik liczby dawek na wkładzie z lekiem
wyświetla białą strzałkę na czerwonym tle?Twój wkład z lekiem jest zużyty. Włóż nowy wkład.
Czy już obrócono przezroczystą podstawę?
Jeżeli przezroczysta podstawa została już obrócona, aby przyjąć lek należy wykonać czynności
opisane w punktach “OTWÓRZ” i “NACIŚNIJ” w sekcji „Codzienne używanie”.
Mój inhalator Spiriva Respimat zbyt szybko się wyczerpał.
Czy stosowano Spiriva Respimat zgodnie z zaleceniami (dwa rozpylenia raz na dobę)?Każdy
wkład z lekiem zawiera lek na 30 dni, gdy stosowane są dwa rozpylenia raz na dobę.
Czy często uruchamiano inhalator Spiriva Respimat w celu sprawdzenia prawidłowego
działania?Po przygotowaniu inhalatora Spiriva Respimat do użycia nie ma konieczności sprawdzania
jego działania, jeżeli jest stosowany codziennie.
Czy zdejmowano i wkładano przezroczystą podstawę wielokrotnie na miejsce?Nie należy
zdejmować przezroczystej podstawy przed zużyciem wkładu. Przy każdym zdejmowaniu
przezroczystej podstawy bez wymiany wkładu licznik dawek odnotowuje jedno rozpylenie i ilość
dawek pozostałych do użycia jest zmniejszona.
Mój inhalator Spiriva Respimat nie uruchamia się.
Czy włożono wkład z lekiem?Jeżeli nie, włóż wkład z lekiem. Po złożeniu zestawu Spiriva Respimat
nie zdejmuj przezroczystej podstawy ani nie wyjmuj wkładu z lekiem, dopóki wkład nie zostanie
zużyty.
Czy po włożeniu wkładu z lekiem powtórzono czynności z punktów Obróć, Otwórz, Naciśnij
mniej niż trzy razy?Powtórz czynności z punktów OBRÓĆ, OTWÓRZ, NACIŚNIJ trzy razy po
włożeniu wkładu z lekiem, tak jak pokazano w punktach 4-6 w sekcji „Przygotowanie do użycia”.
Czy wskaźnik liczby dawek na wkładzie z lekiem wyświetla białą strzałkę na czerwonym tle?
Twój wkład z lekiem jest zużyty. Włóż nowy wkład.
Mój inhalator Spiriva Respimat sam się uruchamia.
Czy wieczko było otwarte podczas obracania przezroczystej podstawy?Zamknij wieczko,
następnie obróć przezroczystą podstawę.
Czy naciśnięto przycisk uwolnienia dawki podczas obracania przezroczystej podstawy?Zamknij
wieczko, tak by przycisk uwolnienia dawki był zasłonięty i następnie obróć przezroczystą podstawę.
Czy zaprzestano obracania przezroczystej podstawy przed kliknięciem?Obróć przezroczystą
podstawę ciągłym ruchem do momentu usłyszenia kliknięcia (pół obrotu). Licznik dawek odnotowuje
każde niecałkowite obrócenie i ilość dawek pozostałych do użycia jest zmniejszona.
Czy wieczko było otwarte przy wymianie wkładu z lekiem?Zamknij wieczko, a następnie wymień
wkład.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterBoehringer Ingelheim Espana S.A. Boehringer Ingelheim France Boehringer Ingelheim Pharma GmbH & Co. KG
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Spiriva RespimatPostać farmaceutyczna: Proszek, 18 mcgSubstancja czynna: tiotropium bromideProducent: Ferrer Internacional, S.A.Wymaga receptyPostać farmaceutyczna: Proszek, 10 mcgSubstancja czynna: tiotropium bromideProducent: Actavis Ltd. Laboratorios Liconsa S.A. Teva Operations Poland Sp. z o.o. Teva Pharma B.V.Wymaga receptyPostać farmaceutyczna: Proszek, 18 μg/dawkę odmierzonąSubstancja czynna: tiotropium bromideWymaga recepty
Odpowiedniki Spiriva Respimat w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Spiriva Respimat – Ukraina
Odpowiednik Spiriva Respimat – Hiszpania
Lekarze online w sprawie Spiriva Respimat
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Spiriva Respimat – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














