
SMOFlipid

Zapytaj lekarza o receptę na SMOFlipid

Jak stosować SMOFlipid
Ulotka dołączona do opakowania: informacja dla użytkownika
SMOFlipid, 200 mg/ml, emulsja do infuzji
produkt złożony
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub pielęgniarki.
Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane
niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest SMOFlipid i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku SMOFlipid
- 3. Jak stosować SMOFlipid
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać SMOFlipid
- 6. Zawartość opakowania i inne informacje
1. Co to jest SMOFlipid i w jakim celu się go stosuje
SMOFlipid zawiera cztery różne tłuszcze (lipidy): olej sojowy, triglicerydy o średniej długości łańcucha, olej
z oliwek oraz olej rybny bogaty w kwasy tłuszczowe omega-3. Płyn jest mieszaniną tłuszczów i wody, czyli
tzw. „emulsją tłuszczową”.
- Działanie leku polega na dostarczaniu organizmowi energii oraz kwasów tłuszczowych.
- Lek podaje się do krwi za pomocą kroplówki lub pompy infuzyjnej. Fachowy personel medyczny podaje SMOFlipid pacjentom, u których inne sposoby żywienia są niewystarczające, niemożliwe lub przeciwwskazane.
2. Informacje ważne przed zastosowaniem leku SMOFlipid
Nie stosować leku SMOFlipid, jeśli u pacjenta występuje:
- uczulenie na olej sojowy, triglicerydy o średniej długości łańcucha, olej z oliwek, olej rybny lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6);
- uczulenie na produkty zawierające rybę, jaja, soję lub orzeszki ziemne;
- nadmiar tłuszczu we krwi (ciężka hiperlipidemia);
- ciężka niewydolność nerek lub wątroby;
- ciężkie zaburzenia krzepliwości krwi (zaburzenia krzepnięcia);
- ostry wstrząs;
- płyn w płucach (obrzęk płuc), nadmiar wody w organizmie (przewodnienie) lub niewydolność serca (spowodowana nadmiarem wody w organizmie);
- niestabilny stan ogólny, np. ciężki stan pourazowy, zawał serca, udar, skrzep krwi (zator), kwasica metaboliczna (zaburzenie metaboliczne powodujące duże stężenie kwasów we krwi) lub niewyrównana cukrzyca, ciężkie zakażenie (zespół ogólnoustrojowej reakcji zapalnej - posocznica) i odwodnienie.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku SMOFlipid należy poinformować lekarza lub pielęgniarkę,
jeśli u pacjenta występuje zbyt duże stężenie tłuszczów we krwi, spowodowane brakiem zdolności
organizmu do odpowiedniej eliminacji tłuszczu (zaburzony metabolizm tłuszczu).
Podczas stosowania u noworodków i dzieci w wieku poniżej 2 lat, roztwór (w worku i zestawie do
podawania) należy chronić przed światłem do momentu zakończenia podawania. Narażenie leku SMOFlipid
na działanie światła, szczególnie po dodaniu pierwiastków śladowych i (lub) witamin, prowadzi do
wytworzenia się nadtlenków i innych produktów rozpadu, co można ograniczyć zapewniając ochronę przed
światłem.
Reakcje alergiczne
Jeśli podczas stosowania leku SMOFlipid wystąpi reakcja alergiczna, należy natychmiast przerwać
stosowanie tego leku. Należy natychmiast poinformować lekarza lub pielęgniarkę o wystąpieniu podczas
infuzji następujących objawów:
- gorączka (wysoka temperatura);
- dreszcze;
- wysypka;
- trudności z oddychaniem.
Dzieci
Należy skonsultować się z lekarzem lub pielęgniarką, jeśli lek podawany jest noworodkowi, który ma:
- zbyt dużo substancji zwanej „bilirubiną” we krwi (hiperbilirubinemia);
- wysokie ciśnienie w płucach (nadciśnienie płucne). Podczas długotrwałego podawania leku SMOFlipid noworodkom lekarz zleci wykonanie badań krwi w celu kontroli stanu zdrowia pacjenta.
SMOFlipid a inne leki
Należy poinformować lekarza o wszystkich stosowanych przez pacjenta obecnie lub ostatnio lekach, a także
o lekach, które pacjent planuje stosować.
W szczególności, należy poinformować lekarza o stosowaniu obecnie lub ostatnio leków zmniejszających
krzepliwość krwi, takich jak warfaryna i heparyna.
- SMOFlipid zawiera witaminę K , która może mieć wpływ na warfarynę. Ilość witaminy K w leku SMOFlipid jest jednak tak mała, że tego typu problemy nie powinny występować.
- Heparyna podawana w dawkach klinicznych może krótkotrwale zwiększyć stężenie kwasów tłuszczowych we krwi, co jest spowodowane uwalnianiem kwasów tłuszczowych przez tkanki do krwiobiegu, po czym następuje zmniejszenie ilości wydzielanych kwasów tłuszczowych z krwi (zmniejszenie klirensu triglicerydów).
Ciąża i karmienie piersią
Brak danych dotyczących stosowania leku SMOFlipid u kobiet w okresie ciąży lub podczas karmienia
piersią. Dlatego SMOFlipid podaje się kobietom w okresie ciąży lub podczas karmienia piersią jedynie
wtedy, gdy lekarz uzna to za konieczne.
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie dotyczy, ponieważ lek jest stosowany w szpitalu.
SMOFlipid zawiera sód
Ten lek zawiera 5 mmol (115 mg) sodu w 1000 ml. Należy to uwzględnić u pacjentów kontrolujących
zawartość sodu w diecie.
3. Jak stosować SMOFlipid
SMOFlipid podaje się do krwi za pomocą kroplówki lub pompy infuzyjnej.
Lekarz ustala indywidualną dawkę w zależności od wieku, masy ciała oraz zdolności pacjenta do
wykorzystywania podawanego tłuszczu.
Podczas stosowania u noworodków i dzieci w wieku poniżej 2 lat, roztwór (w worku i zestawie do
podawania) należy chronić przed światłem do momentu zakończenia podawania (patrz punkt 2).
Szczegółowe informacje dotyczące dawkowania i podawania znajdują się na końcu ulotki w punkcie
„Informacje przeznaczone wyłącznie dla fachowego personelu medycznego”.
Zastosowanie większej niż zalecana dawki leku SMOFlipid
W przypadku zastosowania przez pacjenta większej niż zalecana dawki leku SMOFlipid, istnieje ryzyko
przyjęcia zbyt dużej ilości tłuszczu i problemów z metabolizmem tłuszczu. Jest to tzw. „zespół
przedawkowania tłuszczu”. Więcej informacji znajduje się w punkcie 4. Możliwe działania niepożądane.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Zespół przedawkowania tłuszczu
Zespół przedawkowania tłuszczu występuje, gdy organizm ma problem z metabolizmem tłuszczów
w związku z otrzymaniem nadmiernej ilości leku SMOFlipid. Może on także wystąpić z powodu nagłej
zmiany stanu zdrowia pacjenta (np. problemy z nerkami lub zakażenie). Możliwe objawy to zwiększona
ilość tłuszczu we krwi (hiperlipidemia) oraz w komórkach i tkankach, gorączka, zaburzenia
w funkcjonowaniu wielu narządów i śpiączka. Wszystkie te objawy na ogół ustępują po przerwaniu infuzji.
Często występujące działania niepożądane(mogą występować nie częściej niż u 1 na 10 pacjentów):
- nieznaczny wzrost temperatury ciała.
Niezbyt częstowystępujące działania niepożądane(mogą występować nie częściej niż u 1 na
100 pacjentów):
- dreszcze;
- utrata apetytu;
- nudności;
- wymioty.
Rzadkowystępujące działania niepożądane(mogą występować nie częściej niż u 1 na 1000 pacjentów):
- reakcje alergiczne (np. wysoka temperatura, obrzęk, obniżenie ciśnienia krwi, wysypka, zaczerwienienie, ból głowy);
- uczucie zimna lub gorąca;
- bladość;
- sine zabarwienie skóry i błon śluzowych (spowodowane obniżoną zawartością tlenu we krwi);
- bóle szyi, pleców, kości, klatki piersiowej i lędźwi;
- podwyższone lub obniżone ciśnienie krwi;
- duszność.
Bardzo rzadkowystępujące działania niepożądane(mogą występować nie częściej niż u 1 na
10 000 pacjentów):
- długotrwały i bolesny wzwód prącia.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane można
zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych
Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
tel.: +48 22 49 21 301
faks: +48 22 49 21 309
e-mail: [email protected]
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać SMOFlipid
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie przechowywać w temperaturze powyżej 25°C. Nie zamrażać.
Nie stosować leku po upływie terminu ważności zamieszczonego na opakowaniu. Termin ważności
oznacza ostatni dzień podanego miesiąca.
Nie stosować leku SMOFlipid, jeśli opakowanie jest uszkodzone. Stosować tylko jeśli emulsja jest biała
i jednorodna. Do jednorazowego użycia. Niezużytą pozostałość należy usunąć. Nie używać ponownie.
Podczas stosowania u noworodków i dzieci w wieku poniżej 2 lat, roztwór (w worku i zestawie do
podawania) należy chronić przed światłem do momentu zakończenia podawania (patrz punkt 2).
6. Zawartość opakowania i inne informacje
Co zawiera SMOFlipid
- Substancjami czynnymi leku są: olej sojowy, oczyszczony 60 mg/ml triglicerydy o średniej długości łańcucha 60 mg/ml olej z oliwek, oczyszczony 50 mg/ml olej rybny, bogaty w omega-3 kwasy 30 mg/ml
- Pozostałe składniki to: lecytyna z jaja kurzego, glicerol, sodu oleinian, all- rac-α-tokoferol, sodu wodorotlenek, woda do wstrzykiwań.
Jak wygląda SMOFlipid i co zawiera opakowanie
SMOFlipid jest to biała, jednorodna emulsja dostępna w butelkach szklanych lub workach typu Biofine.
Wielkości opakowań:
- butelka szklana: 1 x 100 ml, 10 x 100 ml, 1 x 250 ml, 10 x 250 ml, 1 x 500 ml i 10 x 500 ml;
- worek typu Biofine: 1 x 100 ml, 10 x 100 ml, 20 x 100 ml, 1 x 250 ml, 10 x 250 ml, 1 x 500 ml, 12 x 500 ml, 1 x 1000 ml i 6 x 1000 ml.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Fresenius Kabi AB
SE-75174 Uppsala
Szwecja
Wytwórca
Fresenius Kabi AB
Rapsgatan 7
SE-75174 Uppsala
Szwecja
Fresenius Kabi Austria GmbH
Hafnerstrasse 36
A-8055 Graz
Austria
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do przedstawiciela podmiotu
odpowiedzialnego:
Fresenius Kabi Polska Sp. z o.o.
Al. Jerozolimskie 134
02-305 Warszawa
tel.: +48 22 345 67 89
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego
Obszaru Gospodarczego pod następującymi nazwami:
Austria, Belgia, Finlandia, Francja, Niemcy, Islandia, Irlandia, Włochy, Holandia, Norwegia, Słowenia,
Szwecja, Wielka Brytania: SMOFlipid 200 mg/ml
Cypr, Czechy, Estonia, Grecja, Węgry, Łotwa, Litwa, Luksemburg, Hiszpania: SMOFlipid 20 %
Dania, Polska, Portugalia, Słowacja: SMOFlipid
Data ostatniej aktualizacji ulotki:06.03.2020 r.
-----------------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Ostrzeżenia i środki ostrożności
Podczas infuzji stężenie triglicerydów w surowicy nie powinno przekraczać 3 mmol/l.
Przedawkowanie może spowodować wystąpienie zespołu przedawkowania tłuszczu. Należy zachować
szczególną ostrożność u pacjentów z podwyższonym ryzykiem hiperlipidemii (np. u pacjentów
przyjmujących duże dawki tłuszczów, u pacjentów z ciężką posocznicą oraz u niemowląt z bardzo niską
masą urodzeniową).
Podawanie samych kwasów tłuszczowych o średniej długości łańcucha może wywołać kwasicę
metaboliczną. Jednoczesne podawanie długołańcuchowych kwasów tłuszczowych zawartych w leku
SMOFlipid znacznie zmniejsza to ryzyko. Jednoczesne podawanie węglowodanów może zmniejszyć to
ryzyko jeszcze bardziej. Dlatego zaleca się jednoczesne podawanie w infuzji roztworów węglowodanów lub
aminokwasów z węglowodanami. Należy regularnie wykonywać badania laboratoryjne związane
z kontrolowaniem żywienia pozajelitowego. Dotyczy to oznaczania stężenia glukozy we krwi, prób
czynnościowych wątroby, równowagi kwasowo-zasadowej, równowagi płynów, pełnej morfologii krwi
i stężenia elektrolitów.
Ten lek zawiera olej sojowy, olej rybny oraz fosfolipidy jaja, które rzadko mogą powodować reakcje
alergiczne. Obserwowano alergiczne reakcje krzyżowe między soją i orzeszkami ziemnymi.
W razie wystąpienia jakichkolwiek objawów przedmiotowych lub podmiotowych reakcji anafilaktycznej
(takich jak gorączka, dreszcze, wysypka czy duszności), należy natychmiast przerwać infuzję.
SMOFlipid należy podawać ostrożnie u noworodków i wcześniaków z hiperbilirubinemią oraz
w przypadkach nadciśnienia płucnego. U noworodków, a zwłaszcza wcześniaków w przypadkach
długotrwałego żywienia pozajelitowego, należy kontrolować liczbę płytek krwi, aktywność enzymów
wątrobowych oraz stężenie triglicerydów w surowicy krwi.
SMOFlipid zawiera do 5 mmol sodu na 1000 ml. Należy to wziąć pod uwagę u pacjentów kontrolujących
zawartość sodu w diecie.
Nie należy dodawać innych leków oraz dodatkowych substancji do leku SMOFlipid, chyba że ich zgodność
została ustalona.
Sposób podawania
Infuzja do żyły centralnej lub obwodowej.
Podczas stosowania u noworodków i dzieci w wieku poniżej 2 lat, roztwór (w worku i zestawie do
podawania) należy chronić przed światłem do momentu zakończenia podawania.
Instrukcja użycia i sposób postępowania Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Używać tylko, jeśli emulsja jest jednorodna.
Narażenie na działanie światła roztworów do dożylnego żywienia pozajelitowego, szczególnie po dodaniu
pierwiastków śladowych i (lub) witamin, może mieć niepożądane skutki dotyczące odpowiedzi klinicznej
u noworodków, ze względu na wytwarzanie się nadtlenków i innych produktów rozpadu. Podczas
stosowania u noworodków i dzieci w wieku poniżej 2 lat, lek SMOFlipid należy chronić przed światłem do
momentu zakończenia podawania.
Dotyczy worka typu Biofine: przed usunięciem ochronnego worka zewnętrznego należy sprawdzić wskaźnik
szczelności opakowania (Oxalert ). Jeśli wskaźnik ma barwę czarną, tlen przeniknął przez worek
zewnętrzny i lek należy usunąć.
Przed podaniem należy obejrzeć, czy emulsja jest jednorodna. Należy upewnić się, że emulsja gotowa
do infuzji nie wykazuje żadnych oznak rozwarstwienia faz.
Do jednorazowego użycia. Niezużytą pozostałość należy usunąć.
Po zmieszaniu z dodatkowymi substancjami
SMOFlipid można mieszać z zachowaniem aseptyki z roztworami aminokwasów, glukozy i elektrolitów,
w celu uzyskania mieszaniny do całkowitego żywienia pozajelitowego typu „wszystko w jednym”.
Na życzenie można uzyskać od podmiotu odpowiedzialnego informacje o zgodności leku z dodatkowymi
substancjami oraz na temat okresów przechowywania sporządzonych mieszanin. Wszelkie dodatkowe
substancje należy łączyć z lekiem w warunkach aseptycznych. Wszelkie niewykorzystane resztki leku lub
jego odpady należy usunąć zgodnie z lokalnymi przepisami.
Nie przechowywać w temperaturze powyżej 25°C. Nie zamrażać.
Przechowywanie po zmieszaniu
Jeśli SMOFlipid miesza się z dodatkowymi substancjami, z mikrobiologicznego punktu widzenia powstałą
mieszaninę należy użyć natychmiast. W przeciwnym razie, za okres przechowywania podczas użytkowania
i za warunki przechowywania przed zastosowaniem odpowiada użytkownik. Okres ten nie powinien
zasadniczo przekraczać 24 godzin w temperaturze 2-8 C, chyba że dodawanie miało miejsce
w kontrolowanych i zwalidowanych warunkach aseptycznych.
Specjalne środki ostrożności dotyczące usuwania i przygotowania produktu leczniczego do stosowania
Podczas stosowania u noworodków i dzieci w wieku poniżej 2 lat chronić przed światłem do momentu
zakończenia podawania. Narażenie leku SMOFlipid na działanie światła, szczególnie po dodaniu
pierwiastków śladowych i (lub) witamin, prowadzi do wytworzenia się nadtlenków i innych produktów
rozpadu, co można ograniczyć, zapewniając ochronę przed światłem.
SMOFlipid - Instrukcja przygotowania worka Biofine do użycia
- 1.
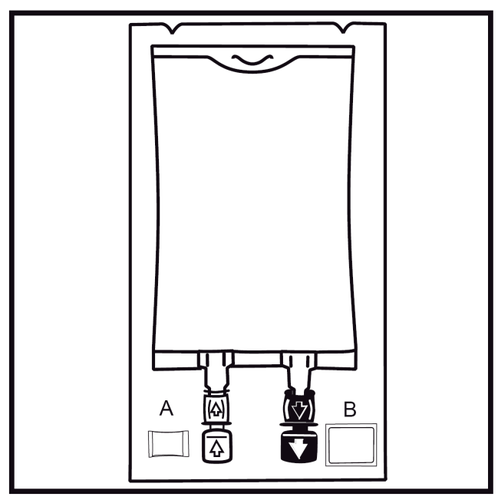
Należy sprawdzić wskaźnik szczelności opakowania (Oxalert ) Aprzed usunięciem worka zewnętrznego.
Jeżeli wskaźnik ma kolor czarny oznacza to, że worek zewnętrzny jest uszkodzony i lek należy usunąć.
- 2.
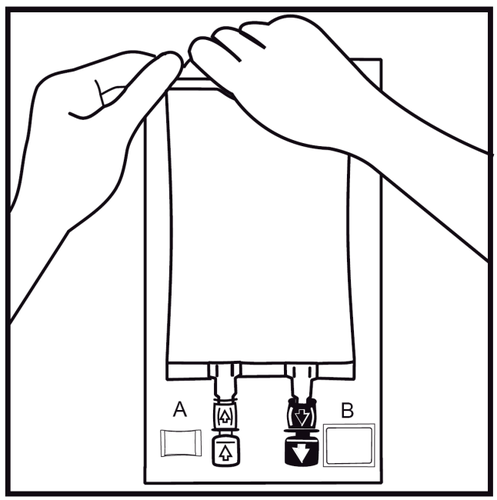
Usunąć worek zewnętrzny poprzez rozerwanie zgrzewu w górnej części i pociągnięcie wzdłuż opakowania.
Wskaźnik szczelności opakowania (Oxalert ) Ai pochłaniacz tlenu Bnależy usunąć.
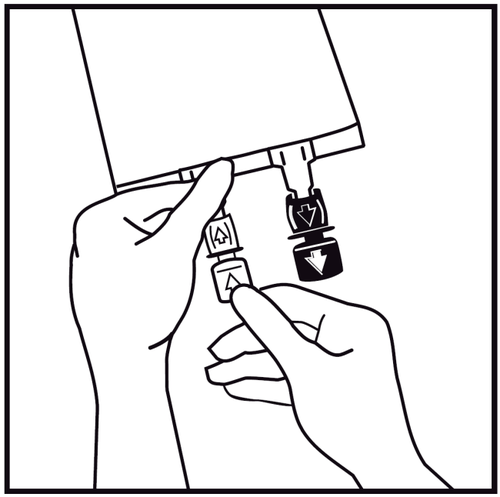
- 3.
W przypadku wprowadzania dodatkowych substancji, należy oderwać oznakowaną strzałką zatyczkę
jednorazowego użytku zabezpieczającą biały port do dodawania tych substancji.
Jeśli nie wprowadza się dodatkowych substancji – należy przejść do punktu 5.
- 4.
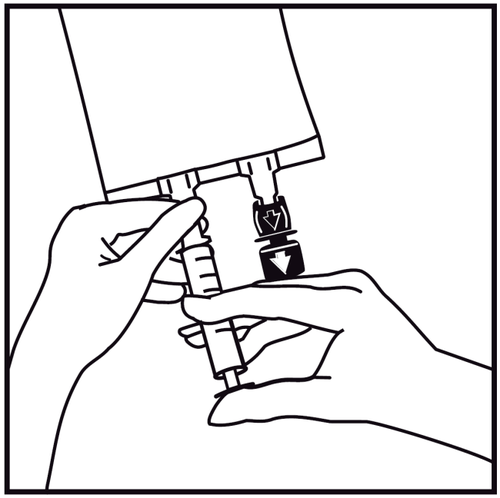
Wprowadzić igłę poziomo przez środek miejsca do wstrzykiwań i wstrzyknąć dodatkowe substancje
(o ustalonej zgodności). Stosować strzykawki z igłami o średnicy od 18 do 23 G i o maksymalnej długości
40 mm.
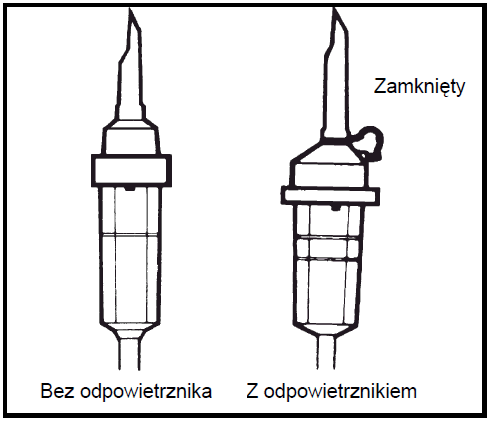
- 5.
Należy używać zestawu do infuzji bez odpowietrznika lub zamknąć wlot powietrza w przypadku zestawu
z odpowietrznikiem. Postępować zgodnie z instrukcją obsługi zestawu do infuzji. Stosować zestaw do infuzji
ze średnicą określoną w normie ISO 8536-4: 5,6 ± 0,1 mm.
- 6.
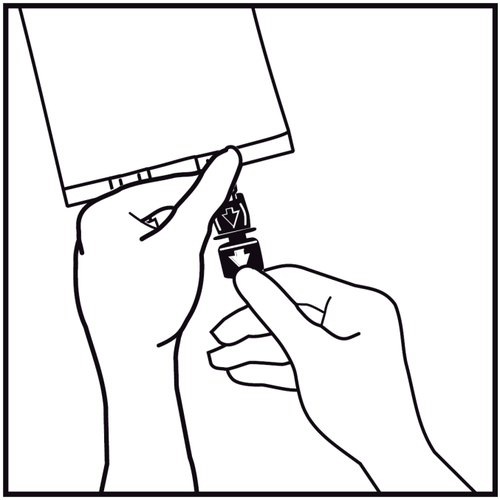
Oderwać zatyczkę jednorazowego użytku zabezpieczającą niebieski port infuzyjny.
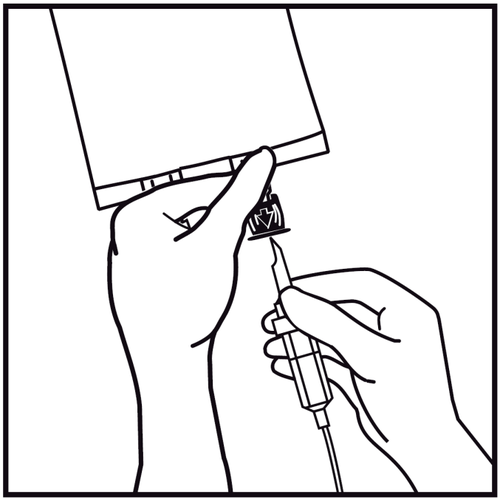
- 7.
Przytrzymać podstawę portu infuzyjnego. Wkłuć ostrze zestawu do infuzji do portu infuzyjnego i delikatnie
wkręcać, aż do wkłucia całej jego długości.
- 8.
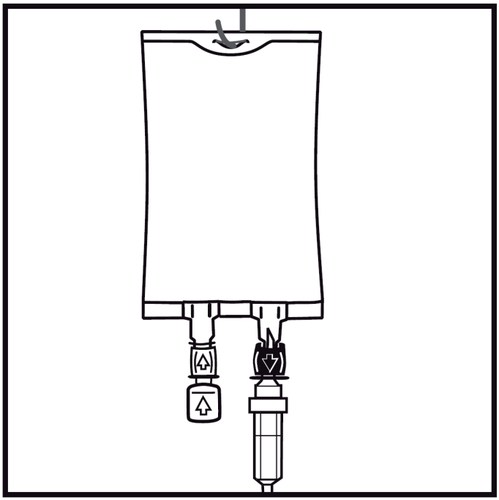
Zawiesić worek wykorzystując przygotowany do tego celu otwór i rozpocząć infuzję.
- Kraj rejestracji
- Wymaga receptyNie
- Producent
- ImporterFresenius Kabi AB Fresenius Kabi Austria GmbH
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki SMOFlipidPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez receptyPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez receptyPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez recepty
Odpowiedniki SMOFlipid w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik SMOFlipid – Hiszpania
Lekarze online w sprawie SMOFlipid
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na SMOFlipid – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














