
Gadovist 1,0

Zapytaj lekarza o receptę na Gadovist 1,0

Jak stosować Gadovist 1,0
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
Gadovist 1,0, 1,0 mmol/ml, roztwór do wstrzykiwań
Gadobutrolum
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza (radiologa) lub personelu pracowni rezonansu magnetycznego.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub personelowi pracowni rezonansu magnetycznego. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest lek Gadovist 1,0 i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Gadovist 1,0
- 3. Jak stosować lek Gadovist 1,0
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Gadovist 1,0
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Gadovist 1,0 i w jakim celu się go stosuje
Lek przeznaczony wyłącznie do diagnostyki.
Lek Gadovist 1,0 jest produktem (środkiem kontrastowym) do stosowania w czasie obrazowania
metodą rezonansu magnetycznego, służącym do badania różnych części ciała, takich jak: mózg,
kręgosłup, głowa, szyja, klatka piersiowa, piersi, brzuch (w tym trzustka, wątroba i śledziona),
miednica (w tym gruczoł krokowy, pęcherz moczowy, macica), przestrzeń nazywana zaotrzewnową
w tylnej części jamy brzusznej (w tym nerki), kończyny (górne i dolne) i układ mięśniowo-
szkieletowy (mięśnie, kości i stawy), naczynia krwionośne i serce. Można oceniać ukrwienie mięśnia
sercowego w warunkach obciążenia (spowodowanego na przykład lekami). Można diagnozować
żywotność mięśnia sercowego (na przykład można wykryć obecność blizny w tkance).
Badanie MRI jest rodzajem obrazowania diagnostycznego w medycynie, które wykorzystuje
odmienne zachowanie się cząsteczek wody w tkankach zdrowych i zmienionych chorobowo. Badanie
jest wykonywane przy pomocy złożonych układów magnesów i fal radiowych. Aktywność jest
rejestrowana przez komputery, które przekładają ją na obrazy.
Lek Gadovist 1,0 stosuje się u osób dorosłych oraz dzieci i młodzieży w każdym wieku (w tym u
nowonarodzonych niemowląt).
Lek Gadovist 1,0 podaje się w postaci iniekcji dożylnej. Lek powinien być podawany przez
fachowych pracowników służby zdrowia z doświadczeniem w wykonywaniu badań metodą rezonansu
magnetycznego (MRI).
2. Informacje ważne przed zastosowaniem leku Gadovist 1,0
Kiedy nie stosować leku Gadovist 1,0
jeśli pacjent ma uczulenie na substancję czynną lub którykolwiek z pozostałych składników tego leku
(wymienionych w punkcie 6). Nie ma innego bezwzględnego przeciwwskazania do zastosowania leku
Gadovist 1,0.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Gadovist 1,0 należy zwrócić się do lekarza, jeśli u pacjenta:
- stwierdzono uczulenie (nadwrażliwość) na gadobutrol lub którykolwiek z pozostałych składników leku Gadovist 1,0 (patrz „Co zawiera lek Gadovist 1,0”),
- występuje lub występowała alergia (np. katar sienny, pokrzywka) lub astma,
- wystąpiła wcześniej reakcja na środek kontrastowy,
- występują choroby mózgu z drgawkami lub inne choroby układu nerwowego. Lekarz zdecyduje, czy wykonanie zleconego badania będzie możliwe. Po zastosowaniu leku Gadovist 1,0 mogą występować reakcje typu alergicznego lub inne rodzaje reakcji, prowadzące do zaburzeń pracy serca, trudności w oddychaniu lub reakcji skórnych. Możliwe są reakcje o ciężkim przebiegu. Większość reakcji występuje w ciągu pół godziny od podania. Dlatego zaleca się obserwację pacjenta. Obserwowano występowanie reakcji opóźnionych (po wielu godzinach lub dniach) (patrz punkt 4 „Możliwe działania niepożądane”).
- Należy poinformować lekarza, jeśli pacjent ma wszczepiony rozrusznik serca lub jakiekolwiek implanty zawierające żelazo. Zaburzenia czynności nerek i (lub) wątroby Należy poinformować lekarza, jeżeli:
- nerki pacjenta nie działają prawidłowo,
- pacjent niedawno przebył lub w najbliższym czasie ma mieć przeszczepioną wątrobę.
Noworodki i niemowlęta
Ze względu na niedojrzałą funkcję nerek u noworodków (dzieci do 4 tygodnia życia) oraz u niemowląt
(dzieci do 1. roku życia), lek Gadovist 1,0 należy stosować u tych pacjentów tylko po starannym
rozważeniu przez lekarza.
Lekarz może podjąć decyzję o wykonaniu badania krwi w celu sprawdzenia czynności nerekprzed
podjęciem decyzji o zastosowaniu leku Gadovist 1,0, zwłaszcza u osób w wieku powyżej 65 lat.
Jeżeli nerki nie działają prawidłowo, lekarz upewni się, że lek Gadovist 1,0 został usunięty z
organizmu, zanim pacjent otrzyma kolejne wstrzyknięcie leku Gadovist 1,0.
Lek Gadovist 1,0 może być usunięty z organizmu poprzez zastosowanie dializy. Jeżeli nerki nie
działają prawidłowo, lekarz może podjąć decyzję o zastosowaniu dializy po otrzymaniu leku Gadovist
1,0.
Istnieją doniesienia o ciężkiej reakcji, głównie związanej z pogrubieniem skóry i tkanki łącznej
(nerkopochodne zwłóknienie układowe, ang. nephrogenic systemic fibrosis– NSF). NSF może
powodować znaczne osłabienie ruchomości stawów, osłabienie mięśni lub może mieć wpływ na
prawidłową czynność narządów wewnętrznych, co może stanowić zagrożenie życia. NSF jest
związane ze stosowaniem niektórych produktów zawierających gadolin (w tym Gadovist 1,0) u
pacjentów z ciężkim zaburzeniem czynności nerek. Jest również związane ze stosowaniem niektórych
produktów zawierających gadolin (w tym Gadovist 1,0) u pacjentów z ostrą niewydolnością nerek, ze
względu na zespół wątrobowo-nerkowy (niewydolność nerek u pacjentów z zaawansowaną
przewlekłą chorobą wątroby) lub u pacjentów z ostrą niewydolnością nerek, którzy niedawno przebyli
lub spodziewają się wkrótce przeszczepienia wątroby (patrz punkt „Możliwe działania niepożądane”).
Jeżeli u pacjenta występuje którekolwiek z powyższych zastrzeżeń, lekarz zdecyduje o podaniu leku
Gadovist 1,0 po starannym rozważeniu stosunku korzyści do ryzyka wynikających z podania leku.
Lek Gadovist 1,0 a inne leki
Należy powiedzieć lekarzowi o wszystkich lekach stosowanych przez pacjenta obecnie lub ostatnio, a
także o lekach, które pacjent planuje przyjmować.
Ciąża i karmienie piersią
Przed zastosowaniem jakiegokolwiek leku należy poradzić się lekarza.
Ciąża
Gadobutrol może przenikać przez łożysko. Nie wiadomo, czy ma to wpływ na dziecko. Kobiety, które
uważają, że są w ciąży lub mogą być w ciąży powinny powiedzieć o tym lekarzowi, gdyż leku
Gadovist 1,0 nie należy stosować podczas ciąży, o ile nie jest to bezwzględnie konieczne.
Karmienie piersią
Kobiety karmiące piersią lub zamierzające rozpocząć karmienie piersią powinny powiedzieć o tym
lekarzowi. Lekarz omówi z pacjentką, czy powinna ona kontynuować karmienie piersią, czy też
powinna przerwać karmienie piersią na okres 24 godzin po podaniu leku Gadovist 1,0.
Lek Gadovist 1,0 zawiera sód
Ten lek zawiera mniej niż 1 mmol sodu (23 mg) w jednej dawce (obliczonej na podstawie średniej
ilości podawanej osobie o masie ciała 70 kg), to znaczy, że uznaje się go za „wolny od sodu”.
3. Jak stosować lek Gadovist 1,0
Lek Gadovist 1,0 jest wstrzykiwany przez cienką igłę do żyły przez personel medyczny. Lek Gadovist
1,0 zostanie podany bezpośrednio przed badaniem metodą rezonansu magnetycznego.
Po wstrzyknięciu pacjent będzie obserwowany przez co najmniej 30 minut.
Rzeczywista dawka leku Gadovist 1,0 właściwa dla danego pacjenta będzie zależeć od masy ciała
i badanej okolicy ciała.
U osób dorosłych rekomendowane jest jednorazowe wstrzyknięcie dawki 0,1 mililitra leku Gadovist
1,0 na kg masy ciała (oznacza to, że osoba o masie ciała 70 kg otrzyma dawkę 7 mililitrów). W
badaniach obrazowych ośrodkowego układu nerwowego (OUN) oraz CE-MRA (ang. contrast
enhancement in magnetic resonance angiography- wzmocnienie kontrastowe w angiografii przy
użyciu rezonansu magnetycznego) łącznie można podać maksymalnie 0,3 mililitra leku Gadovist 1,0
na kg masy ciała (oznacza to, że osoba o masie ciała 70 kg otrzyma dawkę 21 mililitrów). W
badaniach obrazowych OUN najmniejsza dawka, którą można podawać to 0,075 mililitra leku
Gadovist 1,0 na kg masy ciała (oznacza to, że osoba o masie ciała 70 kg otrzyma dawkę 5,25
mililitra).
W celu obrazowania metodą rezonansu magnetycznego mózgu, kręgosłupa, wątroby i nerek
zasadniczo wystarczające jest pojedyncze wstrzyknięcie 0,1 mililitra leku Gadovist 1,0 na kilogram
masy ciała.
W celu obrazowania metodą rezonansu magnetycznego naczyń, w zależności od rodzaju badania,
zalecane jest pojedyncze wstrzyknięcie od 7,5 do 15 mililitrów (u pacjentów o masie ciała mniejszej
niż 75 kilogramów) lub 10 do 20 mililitrów (u pacjentów o masie ciała 75 kilogramów lub powyżej).
Dawkowanie w szczególnych grupach pacjentów
Nie zaleca się stosowania leku Gadovist 1,0 u pacjentów z poważnymi chorobami nerek, a także
u pacjentów, którzy niedawno przebyli lub w najbliższym czasie mają mieć przeszczepioną wątrobę.
Jeżeli jednak zastosowanie leku jest konieczne, pacjent powinien otrzymać tylko jedną dawkę leku
Gadovist 1,0 podczas badania i nie powinien otrzymywać drugiego wstrzyknięcia przez co najmniej
7 dni.
Stosowanie u dzieci i młodzieży
U dzieci w każdym wieku (w tym u nowonarodzonych niemowląt) zaleca się jednorazowe
wstrzyknięcie dawki 0,1 mililitra leku Gadovist 1,0 na kg masy ciała (patrz punkt 1: „Co to jest lek
Gadovist 1,0 i w jakim celu się go stosuje”). Ze względu na niedojrzałą funkcję nerek u noworodków
(dzieci do 4 tygodnia życia) oraz u niemowląt (dzieci do 1. roku życia), lek Gadovist 1,0 należy
stosować u tych pacjentów tylko po starannym rozważeniu przez lekarza. Noworodki i niemowlęta
powinny otrzymać pojedynczą dawkę podczas badania i nie powinny otrzymywać drugiego
wstrzyknięcia przez co najmniej 7 dni.
Osoby w podeszłym wieku
Nie ma konieczności korygowania dawek u pacjentów w wieku powyżej 65 lat, lecz należy wykonać
badanie krwi w celu sprawdzenia czynności nerek.
Więcej informacji na temat podawania i przygotowania do stosowania leku Gadovist 1,0 znajduje się
w końcowej części ulotki.
Zastosowanie większej niż zalecana dawki leku Gadovist 1,0:
Dotychczas nie zgłaszano przypadków przedawkowania. Gdyby to jednak nastąpiło, lekarz będzie
leczyć wszystkie występujące objawy i skontroluje, czy serce i nerki pacjenta działają prawidłowo.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem leku należy zwrócić się do
lekarza lub personelu pracowni rezonansu magnetycznego.
4. Możliwe działania niepożądane
Jak każdy lek, Gadovist 1,0 może powodować działania niepożądane, chociaż nie u każdego one
wystąpią. Większość tych reakcji występuje w ciągu pół godziny po podaniu leku Gadovist 1,0.
W rzadkich przypadkach obserwowano opóźnione reakcje alergiczne lub inne rodzaje reakcji
niepożądanych, występujące w ciągu kilku godzin do kilku dni po podaniu leku Gadovist 1,0. Jeśli tak
się stanie, natychmiast powiadom o tym lekarza lub radiologa.
Większość działań niepożądanych ma nasilenie od łagodnego do umiarkowanego. Najczęściej
obserwowanymi działaniami niepożądanymi u pacjentów otrzymujących lek Gadovist 1,0 (mogącymi
wystąpić u 5 lub więcej przypadków na 1 000 pacjentów) są: ból głowy, nudności (uczucie mdłości)
i zawroty głowy.
Najcięższymi działaniami niepożądanymi(w niektórych przypadkach zagrażającymi życiu lub
śmiertelnymi) są: zatrzymanie akcji serca (serce przestaje bić), ciężka choroba płuc (zespół ostrej
niewydolności oddechowej)/ płyn w płucach (obrzęk płuc)i ciężkie reakcje o typie alergii
(rzekomoanafilaktyczne) (w tym zatrzymanie oddechu i wstrząs rzekomoanafilaktyczny.
Ponadto, obserwowano działania niepożądane (w niektórych przypadkach zagrażające życiu lub
śmiertelne): duszność (spłycenie oddechu) i utratę przytomności (omdlenie).
Rzadko mogą wystąpić przypadki reakcji typu alergicznego, w tym ciężkie reakcje, które mogą
wymagać interwencji medycznej.
Pacjent powinien natychmiast poinformować personel pracowni rezonansu magnetycznego,jeśli
wystąpią:
- obrzęk twarzy, ust, języka lub gardła,
- kaszel i kichanie,
- trudności w oddychaniu,
- swędzenie,
- katar,
- pokrzywka (szczególny rodzaj wysypki).
Powyższe objawy mogą być pierwszymi sygnałami wystąpienia ciężkiej reakcji, co oznacza, że może
być konieczne przerwanie badania i zastosowanie odpowiedniego leczenia.
Najczęściej obserwowanymi działaniami niepożądanymi(mogą wystąpić u 5 lub więcej na 1000
osób) są: ból głowy, nudności, zawroty głowy.
Większość działań niepożądanych ma przebieg łagodny do umiarkowanego.
Poniżej wymieniono możliwe działania niepożądane, zaobserwowane w trakcie prowadzenia badań klinicznych, przed dopuszczeniem leku do obrotu, według częstości ich występowania.
Często(mogą wystąpić nie częściej niż u 1 na 10 osób):
- ból głowy
- nudności (uczucie mdłości) Niezbyt często(mogą wystąpić nie częściej niż u 1 na 100 osób):
- reakcje typu alergicznego (nadwrażliwość, reakcja rzekomoanafilaktyczna), np.:
- niedociśnienie (niskie ciśnienie krwi)
- pokrzywka
- obrzęk twarzy (opuchnięcie twarzy)
- obrzęk powiek (opuchnięcie powiek)
- zaczerwienienie Częstość występowania następujących reakcji o typie alergii jest nieznana:
- wstrząs rzekomoanafilaktyczny (ciężka reakcja typu alergicznego)
- załamanie krążenia (wstrząs)
- zatrzymanie czynności oddechowej (zatrzymanie oddechu)
- skurcz oskrzeli (trudności w oddychaniu)
- sinica (niebieskie zabarwienie ust)
- obrzęk jamy ustnej i gardła (opuchnięcie jamy ustnej i gardła)
- obrzęk krtani (opuchnięcie krtani)
- wzrost ciśnienia krwi
- ból w klatce piersiowej
- obrzęk naczynioruchowy (np. opuchnięcie twarzy, gardła, ust, warg i [lub] języka)
- zapalenie spojówek
- nadmierne pocenie się (zwiększona potliwość)
- kaszel
- kichanie
- uczucie palenia
- bladość (blada skóra)
- zawroty głowy, zaburzenia smaku (zakłócenia zmysłu smaku), parestezje (mrowienie i drętwienie)
- duszność (spłycenie oddechu)
- wymioty
- rumień (zaczerwienienie skóry)
- świąd (w tym świąd uogólniony) (swędzenie)
- wysypka (w tym wysypka uogólniona, wysypka plamkowa [małe, płaskie czerwone plamki], wysypka grudkowa [małe, wystające, ograniczone zmiany], rumień ze świądem [swędząca wysypka])
- różne rodzaje reakcji w miejscu wstrzyknięcia (np. wyciek przez otaczające tkanki, uczucie palenia, uczucie zimna, uczucie ciepła, zaczerwienienie, świąd, ból lub siniak)
- uczucie gorąca Rzadko(mogą wystąpić nie częściej niż u 1 na 1000 osób):
- utrata przytomności (zasłabnięcie)
- drgawki
- omamy węchowe (zaburzony zmysł powonienia)
- tachykardia (szybkie bicie serca)
- palpitacje (kołatanie serca)
- suchość w jamie ustnej
- złe samopoczucie
- uczucie zimna
Działania niepożądane zgłaszane po dopuszczeniu do obrotu leku Gadovist 1,0
Częstość nieznana(nie może być określona na podstawie dostępnych danych):
- zatrzymanie akcji serca (serce przestaje bić)
- ciężka choroba płuc (zespół ostrej niewydolności oddechowej)
- płyn w płucach (obrzęk płuc)
- zgłaszano przypadki nerkopochodnego zwłóknienia układowego (choroby związanej ze stwardnieniem skóry, która może także obejmować tkanki miękkie i narządy wewnętrzne), z których większość wystąpiła u pacjentów, którzy otrzymywali Gadovist 1,0 w połączeniu z innymi lekami zawierającymi gadolin. Po podaniu leku Gadovist 1,0 obserwowano zmiany w badaniach krwi w funkcji nerek (np. zwiększenie stężenia kreatyniny w surowicy).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce. Działania niepożądane można
zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów
Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów
Biobójczych, Al. Jerozolimskie 181C, 02-222 Warszawa, tel.: + 48 22 49 21 301, faks: + 48 22 49
21 309, strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Gadovist 1,0
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Przechowywać w temperaturze do 30ºC.
Stabilność chemiczną, fizyczną i mikrobiologiczną wykazano przez 24 godziny w temperaturze od 20
do 25ºC. Z mikrobiologicznego punktu widzenia lek powinien być użyty niezwłocznie po otwarciu.
Nie stosować leku Gadovist 1,0 po upływie terminu ważności zamieszczonego na oznakowaniu
opakowania po terminie ważności (EXP). Termin ważności oznacza ostatni dzień podanego miesiąca.
Numer serii na opakowaniu podany jest za napisem Lot.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Gadovist 1,0
- Substancją czynną leku jest gadobutrol. 1 mililitr roztworu do wstrzykiwań zawiera 604,72 mg gadobutrolu (równoważnik 1,0 mmol gadobutrolu zawierający 157,25 mg gadolinu ).
- Pozostałe składniki to: kalkobutrol sodowy, trometamol, kwas solny 3,6% i woda do wstrzykiwań. 1 fiolka zawiera 2 ml roztworu, co odpowiada 1209,44 mg gadobutrolu. 1 fiolka zawiera 7,5 ml roztworu, co odpowiada 4 535 mg gadobutrolu. 1 fiolka zawiera 10 ml roztworu, co odpowiada 6 047,20 mg gadobutrolu. 1 fiolka zawiera 15 ml roztworu, co odpowiada 9 070 mg gadobutrolu. 1 fiolka zawiera 30 ml roztworu, co odpowiada 18 141 mg gadobutrolu. 1 ampułkostrzykawka zawiera 5,0 ml roztworu, co odpowiada 3 023 mg gadobutrolu. 1 ampułkostrzykawka zawiera 7,5 ml roztworu, co odpowiada 4 535 mg gadobutrolu. 1 ampułkostrzykawka zawiera 10 ml roztworu, co odpowiada 6 047 mg gadobutrolu. 1 ampułkostrzykawka zawiera 15 ml roztworu, co odpowiada 9 070 mg gadobutrolu. 1 ampułkostrzykawka zawiera 20 ml roztworu, co odpowiada 12 094 mg gadobutrolu. 1 wkład do strzykawki automatycznej zawiera 15 ml roztworu, co odpowiada 9 070 mg gadobutrolu. 1 wkład do strzykawki automatycznej zawiera 20 ml roztworu, co odpowiada 12 094 mg gadobutrolu. 1 wkład do strzykawki automatycznej zawiera 30 ml roztworu, co odpowiada 18 140 mg gadobutrolu. 1 butelka z produktem do infuzji zawiera 65 ml roztworu, co odpowiada 39 307 mg gadobutrolu.
Jak wygląda lek Gadovist 1,0 i co zawiera opakowanie
Przed użyciem lek należy obejrzeć. Lek Gadovist 1,0 jest przezroczystym, bezbarwnym lub
jasnożółtym roztworem. Nie należy używać leku Gadovist 1,0 w przypadku istotnego przebarwienia,
obecności cząstek stałych lub uszkodzenia pojemnika.
Opakowania zawierają:
1 lub 3 fiolki, z których każda zawiera 2 ml roztworu do wstrzykiwań dożylnych.
1 lub 10 fiolek, z których każda zawiera 7,5; 15 lub 30 ml roztworu do wstrzykiwań dożylnych.
10 fiolek, z których każda zawiera 10 ml roztworu do wstrzykiwań dożylnych.
1 lub 5 ampułkostrzykawek, z których każda zawiera 5, 7,5 lub 10 ml roztworu do wstrzykiwań
dożylnych (w ampułkostrzykawce szklanej lub plastikowej o pojemności 10 ml).
1 lub 5 ampułkostrzykawek zawierających 15 ml roztworu do wstrzykiwań dożylnych
(w ampułkostrzykawce szklanej o pojemności 17 ml lub w ampułkostrzykawce plastikowej
o pojemności 20 ml).
1 lub 5 ampułkostrzykawek zawierających 20 ml roztworu do wstrzykiwań dożylnych
(w ampułkostrzykawce szklanej lub plastikowej o pojemności 20 ml).
1 lub 5 wkładów do strzykawek automatycznych zawierających 15, 20 lub 30 ml roztworu do
wstrzykiwań dożylnych (wkład o pojemności 65 ml).
1 lub 10 butelek zawierających 65 ml roztworu do wstrzykiwań (w butelce do infuzji o pojemności
100 ml).
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny:
Bayer AG
Kaiser-Wilhelm-Allee 1
51373 Leverkusen,
Niemcy
Wytwórca:
Bayer AG
Müllerstrasse 178
13353 Berlin
Niemcy
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do przedstawiciela podmiotu
odpowiedzialnego:
Bayer Sp. z o.o.
Al. Jerozolimskie 158
02-326 Warszawa
Polska
tel. (0-22) 572 35 00
Data ostatniej aktualizacji ulotki: Lipiec 2025
---------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego (patrz również punkty od 1
do 6):
Sposób podania
Lek jest przeznaczony tylko do wstrzykiwań dożylnych. Po podaniu leku należy obserwować pacjenta
przez co najmniej pół godziny, ponieważ doświadczenie wskazuje, że w tym okresie występuje
większość działań niepożądanych.
Wymaganą dawkę należy podawać w pojedynczym szybkim wstrzyknięciu dożylnym. Badanie MRI z
zastosowaniem środka kontrastowego można rozpocząć bezpośrednio po wstrzyknięciu (lub krótko po
wstrzyknięciu, w zależności od zastosowanych sekwencji impulsów i protokołu badania) ze względu
na szybkie wystąpienie efektu wzmocnienia pokontrastowego. Optymalne zakontrastowanie
występuje w trakcie pierwszego przejścia tętniczego w przypadku badania angiograficznego
(angiografia rezonansu magnetycznego ze wzmocnieniem kontrastowym, ang. contrast enhancement
in magnetic resonance angiography– CE-MRA) i w ciągu około 15 minut po wstrzyknięciu leku
Gadovist 1,0 w przypadku oceny ośrodkowego układu nerwowego (OUN) (czas zależy od rodzaju
zmiany chorobowej i tkanki).
Instrukcja użycia
- Przed wstrzyknięciem Przed użyciem lek należy obejrzeć. Nie należy używać leku Gadovist 1,0 w przypadku istotnego przebarwienia, obecności cząstek stałych lub uszkodzenia pojemnika.
- Sposób przygotowania Fiolki Lek Gadovist 1,0 należy pobierać do strzykawki bezpośrednio przed użyciem. Nie należy przekłuwać korka więcej niż 1 raz. Lek, który nie został zużyty w czasie jednego badania, należy wyrzucić. Ampułkostrzykawki Produkt Gadovist jest gotowy do użycia. Ampułkostrzykawkę należy przygotować do wstrzyknięcia bezpośrednio przed użyciem. Należy usunąć zatyczkę końcówki z ampułkostrzykawki bezpośrednio przed użyciem. Lek, który nie został zużyty w czasie jednego badania, należy wyrzucić. Ampułkostrzykawki szklane (tylko): WSTRZYKNIĘCIE RĘCZNE
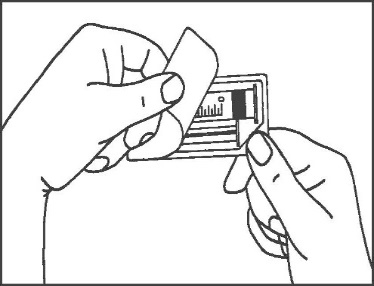
- 1. Otworzyć opakowania
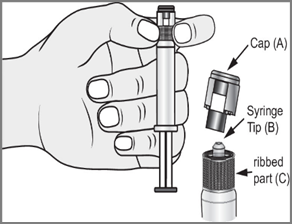
- 2.
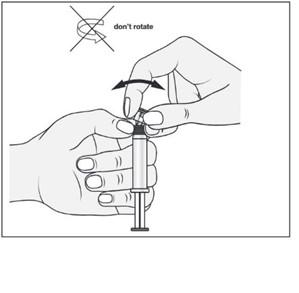
- 3. Drugą ręką chwycić za nasadkę (A) systemu zamykającego i ostrożnie przechylać ją do przodu i do tyłu, aż nasadka odłączy się i będzie można ją zdjąć (wszystkie plomby zostaną zerwane)
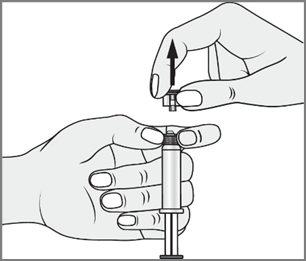
- 4. Zdjąć nasadkę (A) w kierunku prostym do góry. Nie dotykać końcówki strzykawki
- (B), aby zachować jej sterylność.
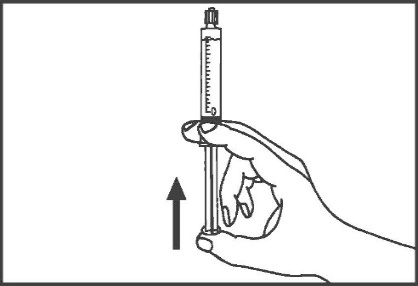
Ampułkostrzykawki plastikowe:
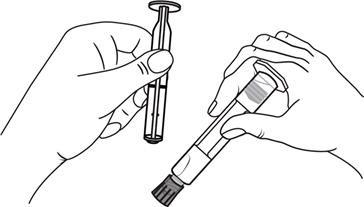
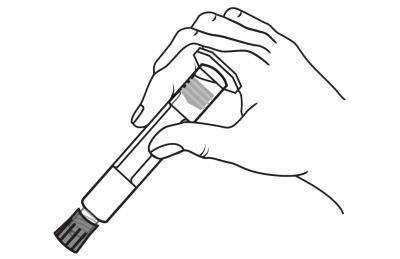
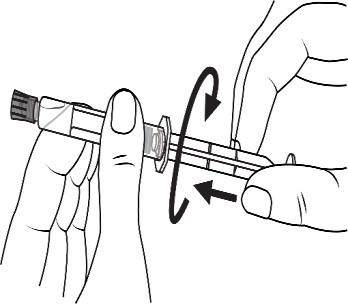
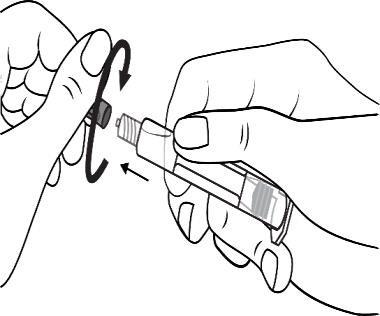
Otworzyć zatyczkę końcówki poprzez
przekręcenie
Wkręcić tłok w strzykawkę zgodnie
z kierunkiem ruchu wskazówek zegara
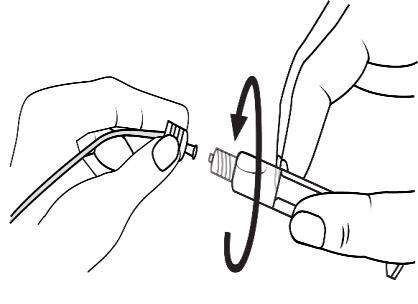
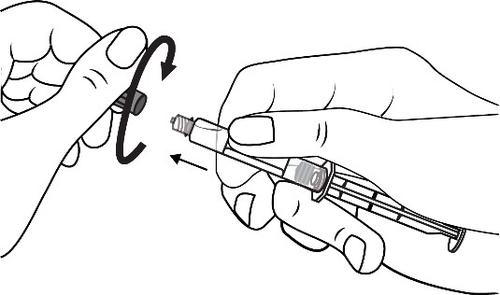
Połączyć końcówkę strzykawki z drenem
obracając ją zgodnie z kierunkiem ruchu
wskazówek zegara. Następnie postępować
zgodnie z instrukcją obsługi.
Otworzyć zatyczkę końcówki poprzez
przekręcenie
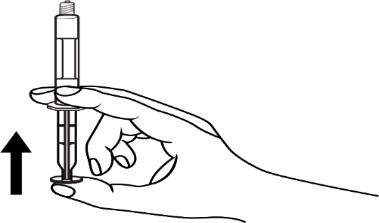
- 4. Usunąć powietrze ze strzykawki
Wkłady do strzykawek automatycznych
Lek powinien być podawany przez wyspecjalizowany personel medyczny z zastosowaniem
odpowiednich procedur i urządzeń.
Należy zachować jałowość podczas wszystkich wstrzyknięć leku.
Instrukcja obsługi urządzenia powinna zostać dostarczona przez producenta.
Lek, który nie został zużyty w czasie jednego badania, należy wyrzucić.
Butelki
Butelka zawiera 65 ml roztworu.
Lek może być podawany przy pomocy automatycznego dozownika.
Instrukcja obsługi urządzenia powinna zostać dostarczona przez producenta.
Pozostałe informacje patrz punkt: „Jak przechowywać lek Gadovist 1,0”.
Wszelkie resztki niewykorzystanego leku lub jego odpady należy usunąć w sposób zgodny
z lokalnymi przepisami.
Zerwaną z fiolki lub ampułkostrzykawki lub wkładu lub butelki etykietę należy przykleić w karcie
pacjenta w celu umożliwienia właściwej rejestracji zastosowanego leku zawierającego gadolin. Należy
również odnotować dawkę. Jeżeli stosowane są elektroniczne karty pacjenta należy wpisać w rejestr
pacjenta nazwę leku, numer serii oraz dawkę.
Niezgodności
Ponieważ nie wykonywano badań dotyczących zgodności, leku nie wolno mieszać z innymi
produktami leczniczymi.
Dawkowanie
Należy stosować najmniejszą dawkę zapewniającą wzmocnienie kontrastowe wystarczające dla celów
diagnostycznych. Dawkę należy obliczyć w oparciu o masę ciała pacjenta. Nie powinna ona
przekraczać zalecanej dawki na kilogram masy ciała określonej w tym punkcie.
Dorośli
Dawka zależy od wskazania. Pojedyncze wstrzyknięcie 0,1 mmol leku Gadovist 1,0 na kg masy ciała
(co odpowiada 0,1 ml/kg mc.) zasadniczo jest wystarczające. Całkowita, maksymalna dawka to 0,3
mmol leku Gadovist 1,0 na kg masy ciała (co odpowiada 0,3 ml/kg mc.).
Badanie OUN:
Zazwyczaj zalecana dawka, aby postawić diagnozę, wynosi 0,1 mmol na kg masy ciała.
Jeśli pomimo ujemnego wyniku badania MRI nadal istnieje istotne kliniczne podejrzenie obecności
zmiany chorobowej lub jeśli uzyskanie dokładniejszych informacji może wpłynąć na leczenie
chorego, można wykonać drugie wstrzyknięcie leku wyrównując dawkę do dawki maksymalnej
0,2 mmol/kg mc. w ciągu 30 minut od pierwszego podania. W badaniach obrazowych OUN
minimalna dawka, którą można podawać to 0,075 mmol gadobutrolu na kg masy ciała (co odpowiada
0,075 ml leku Gadovist 1,0 na kg masy ciała).
Badanie MRI całego ciała (z wyjątkiem CE-MRA):
W celu postawienia rozpoznania, zazwyczaj wystarczającą dawką jest 0,1 ml/kg mc. leku Gadovist
1,0.
Badanie angiograficzne:
Obrazowanie 1 pola widzenia (ang. field of view– FOV):
- 7,5 ml przy masie ciała poniżej 75 kg; 10 ml przy masie ciała 75 kg i powyżej (co odpowiada 0,1- 0,15 mmol/kg mc.)
- Obrazowanie więcej niż 1 pola widzenia (FOV):
- 15 ml przy masie ciała poniżej 75 kg; 20 ml przy masie ciała 75 kg i powyżej (co odpowiada 0,2- 0,3 mmol/kg mc.).
Specjalne grupy pacjentów
Dzieci i młodzież
U dzieci w każdym wieku (w tym u noworodków donoszonych) zalecana dawka wynosi 0,1 mmol
gadobutrolu na kg masy ciała (co odpowiada 0,1 ml leku Gadovist 1,0 na kg masy ciała) we
wszystkich wskazaniach (patrz punkt 1).
Ze względu na niedojrzałą funkcję nerek u noworodków do 4 tygodnia życia oraz u niemowląt do 1.
roku życia, lek Gadovist 1,0 należy stosować u tych pacjentów tylko po starannym rozważeniu, w
dawce nie większej niż 0,1 mmol/kg masy ciała. W trakcie badania nie wolno zastosować więcej niż
jednej dawki. Ze względu na brak danych dotyczących podań wielokrotnych, wstrzyknięć leku
Gadovist 1,0 nie należy powtarzać, chyba że przerwy pomiędzy wstrzyknięciami wynoszą co najmniej
7 dni.
Zaburzenia czynności nerek
Gadovist 1,0 można stosować u pacjentów z ciężkimi zaburzeniami czynności nerek (wskaźnik
filtracji kłębuszkowej, ang. glomerular filtration rate – GFR <30 ml min 1,73 m ) oraz u pacjentów
w okołooperacyjnym okresie przeszczepienia wątroby jedynie po starannej ocenie stosunku korzyści
do ryzyka oraz jeśli informacja diagnostyczna jest niezbędna i nie można jej uzyskać w badaniu
metodą MRI bez efektu wzmocnienia pokontrastowego (patrz punkt 4.4). Jeśli użycie leku Gadovist
1,0 jest konieczne, nie należy stosować dawki większej niż 0,1 mmol/kg masy ciała. Nie należy
stosować więcej niż jednej dawki podczas obrazowania. Ze względu na brak danych dotyczących
podań wielokrotnych, wstrzyknięć leku Gadovist 1,0 nie należy powtarzać, chyba że przerwy
pomiędzy wstrzyknięciami wynoszą co najmniej 7 dni.
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Nadwrażliwość
Tak jak w przypadku innych środków kontrastowych, stosowanie leku Gadovist 1,0 może być
związane z ryzykiem wystąpienia reakcji rzekomoanafilaktycznych, nadwrażliwości lub idiosynkrazji,
charakteryzujących się objawami ze strony układu krążenia, oddechowego lub objawami skórnymi, do
ciężkich reakcji, w tym wstrząsu. Ogólnie, pacjenci z chorobami układu krążenia są bardziej podatni
na wystąpienie poważnych objawów, nawet zgonu w wyniku ciężkich reakcji nadwrażliwości.
Ryzyko wystąpienia reakcji nadwrażliwości może zwiększyć się w przypadku:
- występujących w przeszłości reakcji na środki kontrastowe,
- astmy oskrzelowej w wywiadzie,
- chorób alergicznych w wywiadzie. U pacjentów ze skłonnością do alergii decyzja o zastosowaniu leku Gadovist 1,0 musi zostać podjęta po szczególnie uważnej ocenie stosunku korzyści do ryzyka. Większość reakcji występuje w ciągu pół godziny od podania leku. Dlatego zalecane jest obserwowanie pacjenta po wykonaniu badania. Należy zapewnić dostęp do produktów leczniczych stosowanych przy reakcjach nadwrażliwości i odpowiednią aparaturę. Rzadko obserwowano reakcje opóźnione (po upływie godzin do kilku dni). Zaburzenia czynności nerek
Przed podaniem leku Gadovist 1,0 zalecane jest objęcie wszystkich pacjentów badaniem w zakresie zaburzeń czynności nerek, obejmującym testy laboratoryjne.
Zgłaszano przypadki nerkopochodnego zwłóknienia układowego (ang. nephrogenic systemic fibrosis–
NSF) związanego ze stosowaniem niektórych produktów leczniczych zawierających gadolin
u pacjentów, u których występuje ostre lub przewlekłe ciężkie zaburzenie czynności nerek (wskaźnik
filtracji kłębuszkowej, ang. glomerular filtration rate– GFR<30 ml min 1,73 m ). pacjenci poddani
zabiegowi przeszczepienia wątroby są szczególnie narażeni, ponieważ ryzyko wystąpienia ostrej
niewydolności nerek w tej grupie pacjentów jest duże. Ze względu na możliwość wystąpienia NSF
podczas stosowania leku Gadovist 1,0, produkt ten można stosować u pacjentów z ciężkimi
zaburzeniami czynności nerek oraz u pacjentów w okołooperacyjnym okresie przeszczepienia wątroby
jedynie po starannej ocenie stosunku korzyści do ryzyka oraz jeśli informacja diagnostyczna jest
niezbędna i niedostępna dla badania MRI bez wzmocnienia środkiem kontrastowym. Jeśli użycie leku
Gadovist 1,0 jest konieczne, dawka nie powinna być większa niż 0,1 mmol/kg masy ciała. Nie należy
stosować więcej niż jednej dawki podczas obrazowania. Ze względu na brak danych dotyczących
wielokrotnego podawania, wstrzyknięć leku Gadovist 1,0 nie powinno się powtarzać, chyba że
przerwy pomiędzy wstrzyknięciami wynoszą co najmniej 7 dni.
Ponieważ klirens nerkowy gadobutrolu może ulec zmniejszeniu u pacjentów w podeszłym wieku,
szczególnie ważne jest obserwowanie pacjentów w wieku 65 lat i starszych pod względem zaburzeń
czynności nerek.
Hemodializa zaraz po podaniu leku Gadovist 1,0 może ułatwić jego usunięcie z organizmu. Brak
dowodów uzasadniających rozpoczęcie hemodializy w celu zapobiegania lub leczenia NSF
u pacjentów niepoddawanych jeszcze hemodializie.
Dlatego lek Gadovist 1,0 powinien być stosowany u tych pacjentów po starannym rozważeniu
stosunku korzyści do ryzyka (patrz punkt 4.8).
Ciąża i karmienie piersią
Leku Gadovist 1,0 nie należy stosować w okresie ciąży, jeśli stan kliniczny kobiety nie wskazuje na
konieczność stosowania gadobutrolu.
Lekarz wraz z karmiącą matką powinni podjąć decyzję o kontynuowaniu karmienia piersią lub o jego
przerwaniu na okres 24 godzin po podaniu leku Gadovist 1,0.
Działania niepożądane
Podsumowanie profilu bezpieczeństwa jest oparte o dane z badań klinicznych przeprowadzonych
z udziałem ponad 6300 pacjentów i z badań po wprowadzeniu produktu do obrotu.
Przedawkowanie
Pojedyncze dawki gadobutrolu do 1,5 mmol/kg masy ciała były dobrze tolerowane.
W przypadku przedawkowania, w ramach środków ostrożności zaleca się monitorowanie czynności
układu krążenia (w tym EKG) i kontrolę czynności nerek.
W przypadku przedawkowania lek Gadovist 1,0 można usunąć z organizmu dializą.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterBayer AG Bayer Schering Pharma AG
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Gadovist 1,0Postać farmaceutyczna: Roztwór, 279,3 mg/mlSubstancja czynna: gadobutrolProducent: BIPSO GmbH Bracco Imaging S.p.A.Bez receptyPostać farmaceutyczna: Roztwór, 0,5 mmol/mlSubstancja czynna: gadoteric acidProducent: GE Healthcare AS GE Healthcare IrelandWymaga receptyPostać farmaceutyczna: Roztwór, 0,5 mmol/mlSubstancja czynna: gadoteric acidProducent: GE Healthcare ASWymaga recepty
Odpowiedniki Gadovist 1,0 w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Gadovist 1,0 – Ucrania
Odpowiednik Gadovist 1,0 – España
Lekarze online w sprawie Gadovist 1,0
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Gadovist 1,0 – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














