
Cernevit

Zapytaj lekarza o receptę na Cernevit

Jak stosować Cernevit
Ulotka dołączona do opakowania: informacja dla użytkownika
CERNEVIT, proszek do sporządzania roztworu do wstrzykiwań i infuzji
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest lek CERNEVIT i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku CERNEVIT
- 3. Jak stosować lek CERNEVIT
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek CERNEVIT
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek CERNEVIT i w jakim celu się go stosuje
CERNEVIT jest proszkiem do sporządzania roztworu do wstrzykiwań i infuzji.
Zawiera 12 witamin:
| Substancje czynne | Co odpowiada | ||
| retynolu palmitynian | 3500 j.m. | witamina A | 3500 j.m. |
| cholekalcyferol | 220 j.m. | witamina D 3 | 220 j.m. |
| DL- α-tokoferol | 10,20 mg | witamina E | 11,20 j.m. |
| kwas askorbowy | 125 mg | witamina C | 125 mg |
| kokarboksylaza czterowodna | 5,80 mg | witamina B (tiamina) 1 | 3,51 mg |
| sól sodowa fosforanu ryboflawiny | 5,67 mg | witamina B (ryboflawina) 2 | 4,14 mg |
| pirydoksyny chlorowodorek | 5,50 mg | witamina B (pirydoksyna) 6 | 4,53 mg |
| cyjanokobalamina | 6 µg | witamina B 12 | 6 µg |
| kwas foliowy | 414 µg | kwas foliowy | 414 µg |
| dekspantenol | 16,15 mg | kwas pantotenowy | 17,25 mg |
| biotyna | 69 µg | biotyna | 69 µg |
| nikotynamid | 46 mg | witamina PP | 46 mg |
CERNEVIT dostarcza witamin pacjentom żywionym dożylnie (przez kroplówkę).
2. Informacje ważne przed zastosowaniem leku CERNEVIT
Kiedy nie należy stosować leku CERNEVIT
- jeśli pacjent ma uczulenie (nadwrażliwość) na substancje czynne lub którykolwiek z pozostałych składników tego leku, zwłaszcza witaminę B , białka soi lub orzeszków ziemnych (patrz punkt
- 6. Zawartość opakowania i inne informacje)
- u pacjentów poniżej 11 roku życia
- jeśli pacjent ma hiperwitaminozę którejkolwiek z witamin zawartych w preparacie CERNEVIT
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania CERNEVIT należy powiedzieć lekarzowi, farmaceucie lub
pielęgniarce:
- jeśli pacjent ma chorą wątrobę,
- jeśli pacjent ma chore nerki,
- jeśli pacjent ma padaczkę,
- jeśli pacjent ma chorobę Parkinsona.
Lek CERNEVIT a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować, również tych dostępnych bez
recepty.
Należy zachować szczególną ostrożność, jeżeli pacjent przyjmuje którykolwiek z poniższych
rodzajów leków:
- L-Dopa (stosowana w leczeniu choroby Parkinsona),
- fenobarbital, fenytoina i (lub) prymidon (stosowane w leczeniu padaczki) Lekarz może kontrolować stężenie tych leków we krwi pacjenta i odpowiednio dostosować ich dawki, gdy pacjent rozpoczyna lub kończy przyjmować lek CERNEVIT.
Zaburzenia testów laboratoryjnych
Cernevit zawiera 69 mikrogramów biotyny na 5 ml. Jeśli pacjent ma być poddany badaniom
laboratoryjnym, musi poinformować lekarza lub personel laboratoryjny o tym, że niedawno
przyjmował lek Cernevit, ponieważ biotyna może zaburzać wyniki takich badań. W zależności od
badania, wyniki mogą być fałszywie podwyższone lub fałszywie niskie ze względu na biotynę. Lekarz
może nakazać zaprzestania przyjmowania leku Cernevit przed przeprowadzeniem badań
laboratoryjnych. Należy również pamiętać, że inne ewentualnie przyjmowane produkty, takie jak
preparaty wielowitaminowe lub suplementy diety stosowane na poprawę włosów, skóry i paznokci
mogą również zawierać biotynę i wpływać na wyniki badań laboratoryjnych. Jeśli pacjent przyjmuje
takie produkty, powinien o tym powiedzieć lekarzowi lub personelowi laboratoryjnemu.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Ciąża
Jeżeli jest to konieczne, lek ten może być podany kobiecie w ciąży pod warunkiem ścisłego
przestrzegania wskazań i dawkowania, aby uniknąć przedawkowania witamin.
Karmienie piersią
Podawanie preparatu CERNEVIT podczas karmienia piersią jest niewskazane.
Jeżeli pacjentka karmi piersią i jednocześnie otrzymuje CERNEVIT, istnieje niebezpieczeństwo
przedawkowania witaminy A u dziecka.
Płodność
Brak dostępnych danych dotyczących wpływu leku CERNEVIT na płodność mężczyzn lub kobiet.
3. Jak stosować lek CERNEVIT
CERNEVIT będzie podawany przez fachowy personel medyczny. Zwykle jest podawany w postaci
wlewu do żyły.
Zalecana dawka to 1 fiolka na dobę.
Przyjęcie większej niż zalecana dawki leku CERNEVIT
W tym przypadku objawy przedawkowania leku CERNEVIT są głównie objawami związanymi z
przedawkowaniem witaminy A:
- objawy gwałtownego przedawkowania witaminy A to:
- zaburzenia przewodu pokarmowego (nudności, wymioty),
- zaburzenia układu nerwowego (ból głowy, obrzęk nerwu wzrokowego, drgawki) wywołane wzrostem ciśnienia w głowie pacjenta,
- zaburzenia psychiatryczne (drażliwość),
- zaburzenia skórne (opóźnione złuszczanie skóry).
- objawy długotrwałego przedawkowania witaminy A to:
- ból głowy wywołany wzrostem ciśnienia w głowie pacjenta,
- choroby kości (wrażliwość lub bolesne obrzęki na zakończeniach kończyn).
W przypadku zaobserwowania któregokolwiek z powyższych objawów przedawkowania, należy
poinformować lekarza. Lekarz może przerwać wlew leku CERNEVIT.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku, należy zwrócić
się do lekarza, farmaceuty lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Poniższe działania niepożądane są częste i występują u 1 do 10 na 100 pacjentów:
- ból w miejscu podania.
Poniższe działania niepożądane są rzadkie i występują u 1 do 10 na 1000 pacjentów:
- nudności (mdłości), wymioty.
Poniższe działania niepożądane występują z nieokreśloną częstością:
- reakcje alergiczne, z zaburzeniami oddychania, bólem w klatce piersiowej, obrzękiem gardła, pokrzywką, wysypką, zaczerwienieniem skóry, dyskomfortem w brzuchu, jak również z zatrzymaniem akcji serca,
- wzrost stężenia witaminy A i białek transportujących witaminę A we krwi,
- zaburzenia smaku (metaliczny posmak w ustach),
- przyspieszone bicie serca,
- przyspieszony oddech,
- biegunka,
- wzrost stężenia enzymów wątrobowych i kwasów żółciowych,
- świąd,
- gorączka, uogólniona bolesność, reakcje w miejscu podania wlewu, takie jak uczucie pieczenia, wysypka.
Należy niezwłocznie poinformować lekarza, jeżeli wystąpią objawy reakcji alergicznej, jak zaburzenia
oddychania, ból w klatce piersiowej, obrzęk gardła, pokrzywka, wysypka, zaczerwienienie skóry,
dyskomfort w brzuchu. Lekarz przerwie wlew i wprowadzi niezbędne działania zaradcze.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, należy zwrócić się do lekarza lub pielęgniarki.
Dotyczy to również wszelkich objawów niepożądanych niewymienionych w tej ulotce.
Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
PL 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
e-mail: [email protected]
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek CERNEVIT
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Przechowywać w temperaturze pokojowej, tj. od 15°C do 25°C. Chronić od światła.
Przechowywać w zewnętrznym opakowaniu tekturowym.
Po rozpuszczeniu preparat zachowuje stabilność chemiczną i fizyczną przez 24 godziny w
temperaturze 25°C.
Z mikrobiologicznego punktu widzenia, lek powinien zostać zużyty natychmiast po rozpuszczeniu.
W przeciwnym razie, za czas i warunki przechowywania do momentu użycia odpowiada osoba
podająca lek, a przechowywanie nie powinno trwać dłużej niż 24 godziny w temperaturze 2-8°C,
chyba że rozpuszczanie odbywało się w kontrolowanych i zwalidowanych warunkach aseptycznych.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na opakowaniu po „Termin
ważności”. Termin ważności oznacza ostatni dzień podanego miesiąca.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek CERNEVIT
- Substancjami czynnymi leku są:
1 fiolka 5 ml zawiera:
| Substancje czynne | Co odpowiada | ||
| retynolu palmitynian | 3500 j.m. | witamina A | 3500 j.m. |
| cholekalcyferol | 220 j.m. | witamina D 3 | 220 j.m. |
| DL- α-tokoferol | 10,20 mg | witamina E | 11,20 j.m. |
| kwas askorbowy | 125 mg | witamina C | 125 mg |
| kokarboksylaza czterowodna | 5,80 mg | witamina B (tiamina) 1 | 3,51 mg |
| sól sodowa fosforanu ryboflawiny | 5,67 mg | witamina B (ryboflawina) 2 | 4,14 mg |
| pirydoksyny chlorowodorek | 5,50 mg | witamina B (pirydoksyna) 6 | 4,53 mg |
| cyjanokobalamina | 6 µg | witamina B 12 | 6 µg |
| kwas foliowy | 414 µg | kwas foliowy | 414 µg |
| dekspantenol | 16,15 mg | kwas pantotenowy | 17,25 mg |
| biotyna | 69 µg | biotyna | 69 µg |
| nikotynamid | 46 mg | witamina PP | 46 mg |
j.m. = jednostki międzynarodowe
mg = miligramy
Pozostałe składniki to: glicyna, fosfolipidy sojowe, kwas glikocholowy, sodu wodorotlenek i kwas
solny.
CERNEVIT zawiera 24 mg sodu (1 mmol) na fiolkę. Należy to uwzględnić u pacjentów na diecie
kontrolującej ilość sodu.
Jak wygląda lek CERNEVIT i co zawiera opakowanie
CERNEVIT jest dostarczany w fiolkach z brązowego szkła. W celu przygotowania roztworu do
infuzji, fachowy personel medyczny może użyć zestawu BIO-SET, ułatwiającego rozpuszczenie leku
CERNEVIT.
CERNEVIT w opakowaniach zawierających 10 lub 20 fiolek z lub bez zestawu BIO-SET.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Baxter Polska Sp. z o.o.
ul. Kruczkowskiego 8
00-380 Warszawa
Wytwórca
Baxter SA
Boulevard René Branquart 80
7860 Lessines, Belgia
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do przedstawiciela podmiotu
odpowiedzialnego.
Baxter Polska Sp. z o.o.
ul. Kruczkowskiego 8
00-380 Warszawa
tel.: (22) 488 37 77
Data ostatniej aktualizacji ulotki: 26.03.2019
--------------------------------------------------------------------------------------------------------------
Poniższe informacje przeznaczone są wyłącznie dla lekarza lub fachowego personelu medycznego
Skład jakościowy i ilościowy
1 fiolka 5 ml zawiera:
| Substancje czynne | Co odpowiada | ||
| retynolu palmitynian | 3500 j.m. | witamina A | 3500 j.m. |
| cholekalcyferol | 220 j.m. | witamina D 3 | 220 j.m. |
| DL- α-tokoferol | 10,20 mg | witamina E | 11,20 j.m. |
| kwas askorbowy | 125 mg | witamina C | 125 mg |
| kokarboksylaza czterowodna | 5,80 mg | witamina B (tiamina) 1 | 3,51 mg |
| sól sodowa fosforanu ryboflawiny | 5,67 mg | witamina B (ryboflawina) 2 | 4,14 mg |
| pirydoksyny chlorowodorek | 5,50 mg | witamina B (pirydoksyna) 6 | 4,53 mg |
| cyjanokobalamina | 6 µg | witamina B 12 | 6 µg |
| kwas foliowy | 414 µg | kwas foliowy | 414 µg |
| dekspantenol | 16,15 mg | kwas pantotenowy | 17,25 mg |
| biotyna | 69 µg | biotyna | 69 µg |
| nikotynamid | 46 mg | witamina PP | 46 mg |
Substancje pomocnicze to: glicyna, fosfolipidy sojowe, kwas glikocholowy, sodu wodorotlenek i kwas
solny
Wygląd roztworu:
Po rozpuszczeniu, otrzymany roztwór ma kolor żółto-pomarańczowy.
Dawkowanie i sposób podawania
Tylko dla dorosłych i dzieci w wieku powyżej 11 lat
1 fiolka dziennie.
Podawać wstrzykując powoli domięśniowo lub dożylnie, lub dożylnie w postaci wlewów.
Sposób podawania
- podanie dożylneSposób rozpuszczania: patrz poniżej instrukcja dotycząca stosowania i przygotowania.
Po rozpuszczeniu: Wstrzykiwać powoli (co najmniej 10 min; patrz punkt Ostrzeżenia) dożylnie lub w
postaci wlewu dożylnego w roztworze soli fizjologicznej lub glukozy 5%.
Podawanie może być kontynuowane przez cały okres żywienia pozajelitowego. W celu spełnienia
potrzeb żywieniowych i zapobieganiu niedoborom oraz ewentualnym powikłaniom z nich
wynikających
CERNEVIT może być dodawany do mieszanin odżywczych zawierających
węglowodany, tłuszcze, aminokwasy i elektrolity, pod warunkiem wcześniejszego stwierdzenia
zgodności i stabilności w stosunku do każdego preparatu wchodzącego w skład mieszaniny
odżywczej.
- podanie domięśnioweSposób rozpuszczania: patrz poniżej instrukcja dotycząca stosowania i przygotowania.
Należy uwzględnić całkowitą ilość witamin pochodzących ze wszystkich źródeł, takich jak inne formy
żywienia, podawanie innych witamin lub leków zawierających witaminy jako składniki nieaktywne
(patrz punkt Interakcje).
Stan kliniczny pacjenta i stężenia witamin powinny być kontrolowane w celu utrzymania ich
odpowiedniego poziomu.
Należy wziąć pod uwagę, że niektóre witaminy, zwłaszcza A, B i B są wrażliwe na działanie światła
ultrafioletowego (np.: bezpośrednie i pośrednie światło słoneczne). Dodatkowo, duża zawartość tlenu
w roztworze może zwiększać utratę witamin A, B , C i E. Należy rozważyć te czynniki, jeżeli
właściwe stężenia witamin nie są osiągnięte.
Przeciwwskazania
Produktu CERNEVIT nie wolno stosować:
- w nadwrażliwości na którąkolwiek substancję czynną, zwłaszcza na witaminę B lub na którąkolwiek substancję pomocniczą, w tym na białko soi i produkty sojowe (lecytyna w mieszankach miceli pochodzi z soi), lub na białko orzeszków ziemnych i produkty je zawierające,
- u noworodków, niemowląt i dzieci poniżej 11 lat,
- w hiperwitaminozie którejkolwiek z witamin zawartych w tym produkcie.
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Ostrzeżenia
Reakcje nadwrażliwości
- Dla preparatu CERNEVIT, innych produktów wielowitaminowych oraz pojedynczych witamin (zwłaszcza B , B , B i kwasu foliowego) były zgłaszane ciężkie ogólnoustrojowe reakcje nadwrażliwości. Dla preparatu CERNEVIT i innych produktów witaminowych podawanych pozajelitowo zgłaszano reakcje zakończone zgonem.
- Obserwowano występowanie alergii krzyżowych pomiędzy białkami soi i orzeszków ziemnych,
- W niektórych przypadkach, wystąpienie reakcji nadwrażliwości po dożylnym podaniu produktów wielowitaminowych może być związane z szybkością podania. W przypadku podania we wlewie dożylnym, preparat CERNEVIT należy podawać powoli. W przypadku
podania we wstrzyknięciu dożylnym, należy podawać powoli (wstrzyknięcie powinno trwać
co najmniej 10 minut).
- Jeżeli wystąpią objawy przedmiotowe lub podmiotowe reakcji nadwrażliwości, wlew lub wstrzyknięcie musi być natychmiast przerwane.
Toksyczność witamin
- Stan kliniczny pacjenta i stężenie witamin we krwi powinny być monitorowane w celu uniknięcia przedawkowania i działania toksycznego, zwłaszcza witamin A, D i E, a w szczególności u pacjentów, którzy dodatkowo otrzymują witaminy z innych źródeł lub stosują inne czynniki zwiększające ryzyko toksycznego wpływu witamin.
- Monitorowanie jest szczególnie ważne u pacjentów długotrwale otrzymujących suplementację.
Hiperwitaminoza A
- Ryzyko hiperwitaminozy A i toksycznego wpływu witaminy A (np.: nieprawidłowości skóry i kości, podwójne widzenie, marskość wątroby) jest zwiększone, na przykład:
- u pacjentów z niedoborem białka
- u pacjentów z niewydolnością nerek (nawet w przypadku braku suplementacji witaminy A)
- u pacjentów z niewydolnością wątroby
- u pacjentów z małą masą ciała (np.: pacjenci pediatryczni)
- i u pacjentów leczonych przewlekle.
- Ostre schorzenia wątroby u pacjentów z dużymi zapasami witaminy A w wątrobie mogą prowadzić do wystąpienia objawów toksycznego wpływu witaminy A.
Zespół ponownego odżywiania u pacjentów otrzymujących żywienie pozajelitowe
Uzupełnianie substancji odżywczych u pacjentów ciężko niedożywionych może wywołać zespół
objawów z tym związanych, który charakteryzuje się przeniesieniem potasu, fosforu i magnezu do
przestrzeni wewnątrzkomórkowej, gdyż u pacjenta zaczynają przeważać przemiany anaboliczne.
Może także dojść do powstania niedoboru tiaminy i zatrzymania płynów w organizmie. Dokładna
kontrola i powolne zwiększanie podaży substancji odżywczych, unikając przekarmienia może
zapobiec tym powikłaniom. W razie wystąpienia niedoborów żywieniowych może być
uzasadniona odpowiednia suplementacja.
Osady u pacjentów otrzymujących żywienie pozajelitowe
U pacjentów żywionych pozajelitowo zgłaszano wytrącanie się osadu w naczyniach płucnych.
Niektóre przypadki zakończyły się zgonem. Nadmierny dodatek wapnia i fosforanu zwiększa
ryzyko powstawania osadu fosforanu wapnia. Wystąpienie osadów było zgłaszane nawet przy
nieobecności soli fosforanowych w roztworze. Zgłaszano również pojawienie się osadu
oddalonego od filtra umieszczonego na linii wlewu i podejrzenie formowania się osadu w
krwioobiegu.
Oprócz kontroli roztworu, należy również okresowo sprawdzać zestaw do infuzji i cewnik w
kierunku obecności osadów.
W przypadku wystąpienia objawów przedmiotowych zaburzenia funkcji płuc, należy przerwać
wlew i rozpocząć ocenę kliniczną pacjenta.
Sprawdzić, czy pojemnik nie jest uszkodzony.
Pracować w warunkach aseptycznych.
Nie należy przechowywać częściowo zużytych fiolek; nie używać, jeżeli barwa produktu po
rozpuszczeniu jest niewłaściwa.
Specjalne środki ostrożności przy stosowaniu
Wpływ na wątrobę
- U pacjentów otrzymujących CERNEVIT zaleca się monitorowanie parametrów czynności wątroby. Szczególna kontrola zalecana jest u pacjentów z żółtaczką pochodzenia wątrobowego lub innymi objawami cholestazy. U pacjentów otrzymujących CERNEVIT zgłaszano przypadki wzrostu aktywności enzymów wątrobowych, w tym izolowanego wzrostu aktywności aminotransferazy alaninowej (ALT) u osób z chorobami zapalnymi jelit. Dodatkowo, u pacjentów otrzymujących CERNEVIT obserwowano wzrost stężenia kwasów żółciowych (wszystkich jak i poszczególnych kwasów żółciowych, w tym kwasu glikocholowego).
- u niektórych pacjentów otrzymujących żywienie pozajelitowe (włączając żywienie pozajelitowe z suplementacją witaminami) dochodzi do wystąpienia zaburzeń wątroby i dróg żółciowych, w tym cholestazy, stłuszczenia, zwłóknienia i marskości wątroby, prowadzących prawdopodobnie do niewydolności wątroby, a także zapalenia woreczka żółciowego i kamicy żółciowej. Uważa się, że etiologia tych schorzeń jest wieloczynnikowa i może być różna u poszczególnych pacjentów. Pacjenci, u których wystąpią nieprawidłowości w wynikach badań laboratoryjnych lub inne oznaki zaburzeń wątroby i dróg żółciowych, powinni zostać jak najwcześniej poddani badaniu przez lekarza posiadającego wiedzę z zakresu chorób wątroby w celu identyfikacji możliwych czynników przyczynowych i sprzyjających oraz podjęcia możliwych środków terapeutycznych i profilaktycznych.
Stosowanie u pacjentów z zaburzeniami funkcji wątroby
Pacjenci z zaburzeniami funkcji wątroby mogą wymagać indywidualnego uzupełniania witamin.
Należy zwrócić szczególną uwagę, aby zapobiec toksyczności witaminy A, ponieważ występowanie
choroby wątroby wiąże się ze zwiększoną podatnością na toksyczne działanie witaminy A, w
szczególności w połączeniu z przewlekłym nadmiernym spożyciem alkoholu (patrz też powyżej
„Hiperwitaminoza A” i „Wpływ na wątrobę”).
Stosowanie u pacjentów z upośledzoną funkcją nerek
Pacjenci z zaburzoną funkcją nerek mogą wymagać indywidualnego uzupełniania witamin, w
zależności od stopnia uszkodzenia nerek i występowania chorób współistniejących. U pacjentów z
ciężką niewydolnością nerek, należy zwrócić szczególną uwagę na utrzymanie właściwego stężenia
witaminy D oraz na zapobieganie toksycznemu wpływowi witaminy A, który może się pojawić u
takich pacjentów nawet przy suplementacji małymi dawkami witaminy A lub nawet przy braku
suplementacji.
Hiperwitaminoza i toksyczność (obwodowa neuropatia, ruchy mimowolne) pirydoksyny (witaminy
B ) były zgłaszane u pacjentów przewlekle hemodializowanych, którzy otrzymywali dożylnie
produkty wielowitaminowe zawierające 4 mg pirydoksyny podawane trzy razy w tygodniu.
Ogólne monitorowanie
U pacjentów otrzymujących przez dłuższy czas dożylnie produkty wielowitaminowe jako jedyne
źródło witamin, należy monitorować stan kliniczny oraz stężenie witamin. Jest to szczególnie ważne,
w celu właściwej suplementacji, np.:
- witaminy A u pacjentów z odleżynami, ranami, oparzeniami, zespołem krótkiego jelita czy mukowiscydozą,
- witaminy B u pacjentów dializowanych,
- witaminy B u pacjentów z chorobą nowotworową,
- witaminy B u pacjentów z niewydolnością nerek,
- poszczególnych witamin, których wymaganie może być zwiększone z uwagi na interakcje z innymi produktami leczniczymi (patrz punkt Interakcje).
Niedobory jednej lub kilku witamin należy korygować poprzez specyficzną suplementację.
CERNEVIT nie zawiera witaminy K, którą w razie potrzeby należy podawać osobno.
Stosowanie u pacjentów z niedoborem witaminy B
Przed rozpoczęciem suplementacji produktem CERNEVIT u pacjentów z grupy ryzyka niedoboru
witaminy B i (lub) kiedy planuje się podawanie produktu CERNEVIT przez kilka tygodni, zaleca się
ocenę stanu witaminy B .
Po kilku dniach podawania, zarówno stężenie cyjanokobalaminy (witaminy B ) jak i kwasu
foliowego w produkcie CERNEVIT może być wystarczające, by spowodować wzrost ilości
czerwonych krwinek, retikulocytów oraz hemoglobiny u niektórych pacjentów z niedoborem
witaminy B z towarzyszącą anemią megaloblastyczną. Może to maskować niedobór witaminy B .
Skuteczne leczenie niedoboru witaminy B wymaga wyższych dawek cyjanokobalaminy niż jest
dostarczana w produkcie CERNEVIT.
Suplementacja kwasu foliowego u pacjentów z niedoborem witaminy B , którzy również nie
otrzymują witaminy B , nie zapobiega rozwojowi ani postępowi zmian neurologicznych związanych
z niedoborem witaminy B . Sugeruje się nawet możliwość pogorszenia stanu neurologicznego.
Podczas interpretacji poziomu witaminy B należy wziąć pod uwagę, że niedawne przyjmowanie
witaminy B może powodować prawidłowy poziom pomimo niedoboru w tkankach.
Zaburzenia testów laboratoryjnych
Biotyna może wpływać na badania laboratoryjne oparte na interakcji biotyny i streptawidyny,
prowadząc do fałszywie obniżonych lub fałszywie podwyższonych wyników badań, w zależności od
próby. Ryzyko interferencji jest większe u dzieci i pacjentów z zaburzeniami czynności nerek i
wzrasta w przypadku większych dawek. Interpretując wyniki badań laboratoryjnych należy wziąć pod
uwagę możliwą interferencję biotyny, zwłaszcza jeżeli obserwuje się brak zgodności z prezentacją
kliniczną (np. wyniki badania tarczycy imitujące wyniki wskazujące na chorobę Gravesa-Basedowa u
przyjmujących biotynę pacjentów bez objawów tej choroby lub fałszywie negatywne wyniki testów
troponinowych u pacjentów z zawałem mięśnia sercowego przyjmujących biotynę). W przypadkach,
w których podejrzewa się wystąpienie interferencji, należy wykonać alternatywne, niepodatne na
interferencję z biotyną, badania, jeżeli są one dostępne. Jeśli zleca się badania laboratoryjne u
pacjentów przyjmujących biotynę, należy skonsultować się z personelem laboratorium.
W zależności od stosowanych odczynników, obecność kwasu askorbinowego w surowicy krwi i
moczu może powodować fałszywie wysokie lub niskie odczyty stężenia glukozy w niektórych
systemach badania poziomu glukozy we krwi i moczu, w tym przenośnych paskach testowych i
przenośnych glukometrach. Należy zapoznać się z danymi technicznym dla każdego testu
laboratoryjnego w celu określenia potencjalnych zaburzeń wywołanych witaminami.
Równoczesne stosowanie z lekami przeciwpadaczkowymi:
Ze względu na obecność kwasu foliowego, łączne podawanie preparatu CERNEVIT z lekami
przeciwpadaczkowymi zawierającymi fenobarbital, fenytoinę lub prymidon wymaga zachowania
szczególnej ostrożności.
Równoczesne stosowanie z lewodopą:
Ze względu na obecność pirydoksyny w produkcie CERNEVIT, równoczesne stosowanie z lewodopą
wymaga zachowania środków ostrożności, gdyż może to zmniejszać skuteczność L-dopy.
Stosowanie u dzieci i młodzieży
CERNEVIT jest wskazany u dzieci i młodzieży w wieku powyżej 11 lat (patrz również punkt
„Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”).
Stosowanie u pacjentów w podeszłym wieku
Zazwyczaj, należy rozważyć dostosowanie dawkowania u pacjentów w podeszłym wieku
(zmniejszenie dawki i (lub) wydłużenie odstępów pomiędzy kolejnymi dawkami) uwzględniając
większą częstotliwość pogorszenia czynności wątroby, nerek lub serca oraz występowanie chorób
współistniejących lub terapii lekowej.
Zawartość sodu
CERNEVIT zawiera 24 mg sodu (1 mmol) na fiolkę. Należy wziąć to pod uwagę, jeżeli pacjenci są na
diecie kontrolującej ilość sodu.
Należy sprawdzić zgodność produktu przed zmieszaniem z innymi roztworami do wlewów,
zwłaszcza, gdy CERNEVIT jest dodawany do worków zawierających podwójne mieszaniny do
żywienia pozajelitowego, łączące glukozę, elektrolity i roztwór aminokwasów, jak również potrójne
mieszaniny łączące glukozę, elektrolity i roztwór aminokwasów oraz tłuszcze.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Należy odpowiednio uwzględnić interakcje pomiędzy poszczególnymi witaminami w produkcie
CERNEVIT i innymi czynnikami.
Interakcje te obejmują:
- czynniki mogące powodować wystąpienie pseudoguza mózgu (w tym pewne tetracykliny): ryzyko wystąpienia pseudoguza mózgu wzrasta przy jednoczesnym podawaniu witaminy A,
- alkohol (przewlekłe nadużywanie): podnosi ryzyko hepatotoksycznego wpływu witaminy A,
- leki przeciwdrgawkowe: kwas foliowy może zwiększyć metabolizm niektórych leków przeciwpadaczkowych, np.: fenobarbitalu, fenytoiny, fosfenytoiny i prymidonu, co zwiększa ryzyko wystąpienia napadu padaczkowego. Powinno się monitorować stężenie leków przeciwdrgawkowych w surowicy krwi przy równoczesnym stosowaniu folianów oraz po zakończeniu terapii nimi,
- leki przeciwpłytkowe (np.: aspiryna): witamina E może nasilać wpływ hamujący na czynność płytek,
- aspiryna (terapia dużymi dawkami): może redukować poziom kwasu foliowego przez zwiększenie wydalania moczu,
- niektóre leki przeciwdrgawkowe (np.: fenytoina, karbamazepina, fenobarbital, walproinian): mogą powodować niedobór folianów, pirydoksyny i witaminy D,
- niektóre leki antyretrowirusowe: obniżone poziomy witaminy D są związane np. z efavirenzem czy zydowudyną. Zmniejszone tworzenie aktywnych metabolitów witaminy D jest związane z inhibitorami proteaz,
- chloramfenikol: może hamować odpowiedź hematologiczną na leczenie witaminą B ,
- deferoksamina: zwiększa ryzyko niewydolności serca indukowanej żelazem z powodu zwiększonej mobilizacji żelaza przez większą niż fizjologiczna suplementację witaminy C. W celu zapoznania się ze specyficznymi środkami ostrożności, patrz informacja o produkcie deferoksaminy,
- etionamid: może powodować niedobór pirydoksyny,
- fluoropirymidyny (5-fluorouracyl, kapecytabina, tegafur): zwiększona cytotoksyczność w połączeniu z kwasem foliowym,
- antagoniści folianów, np.: metotreksat, sulfasalazyna, pirymetamina, triamteren, trimetoprim oraz wysokie stężenia katechin zawartych w herbacie: blokują przemianę folianów do ich aktywnych metabolitów i zmniejszają skuteczność suplementacji,
- antymetabolity folianów (metotreksat, raltitreksed): suplementacja kwasem foliowym może obniżyć skuteczność działania antymetabolicznego,
- lewodopa: witamina B może zmniejszać skuteczność lewodopy, ponieważ dekarboksylacja lewodopy wymaga enzymu zależnego od witaminy B . Aby zapobiec tej interakcji, można dodać inhibitor dopa-dekarboksylazy, np. karbidopę.
- antagoniści pirydoksyny, w tym cykloseryna, hydralazyna, izoniazyd, penicylamina, fenelzyna: mogą powodować niedobór pirydoksyny,
- retinoidy, w tym beksaroten: wzrasta ryzyko ich toksyczności, jeżeli są podawane wraz z witaminą A (patrz „Hiperwitaminoza A” w punkcie „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”),
- teofilina: może powodować niedobór pirydoksyny,
- roztwór doustny tipranawiru: zawiera 116 j.m/ml witaminy E, co przekracza zalecaną podaż dobową,
- antagoniści witaminy K (np.: warfaryna): nasilają przeciwkrzepliwe działanie witaminy E.
Produkty lecznicze łączące się z kwaśną alfa-1-glikoproteiną (AAG):
W badaniu in vitro z użyciem ludzkiej surowicy, około 4-krotnie wyższe stężenie kwasu
glikocholowego niż stężenie kwasu glikocholowego w surowicy, które mogło być rezultatem
wstrzyknięcia w bolusie osobie dorosłej produktu CERNEVIT, zwiększało o 50-80% frakcję
wybranych produktów leczniczych wiążących się z kwaśną alfa-1-glikoproteiną (AAG).
Nie wiadomo, czy efekt ten jest istotny klinicznie, jeżeli ilość kwasu glikocholowego zawarta w
standardowej dawce CERNEVIT (jako składnik zmieszanych miceli) jest podawana w powolnej
iniekcji dożylnej, powolnej iniekcji domięśniowej lub w infuzji przez dłuższy czas.
Pacjenci otrzymujący CERNEVIT oraz produkty lecznicze wiążące się z AAG powinni być ściśle
monitorowani pod kątem zwiększonego działania tych leków. Należą do nich propranolol, prazosyna i
wiele innych.
Interakcje związane z suplementacją innych witamin:
Niektóre produkty lecznicze mogą wchodzić w interakcje z niektórymi witaminami w dawkach
znacznie przekraczających dawki zawarte w produkcie CERNEVIT. Należy wziąć to pod uwagę u
pacjentów przyjmujących witaminy z wielu źródeł, a gdy ma to miejsce, należy monitorować
pacjentów pod kątem tych interakcji i odpowiednio postępować.
Przedawkowanie
Ostre lub przewlekłe przedawkowanie witamin (w szczególności A, B , D i E) może powodować
objawowe hiperwitaminozy.
Ryzyko przedawkowania jest szczególnie wysokie, jeżeli pacjent otrzymuje witaminy z wielu źródeł,
a ogólna suplementacja witaminy nie odpowiada indywidualnym potrzebom pacjenta oraz u
pacjentów ze zwiększoną podatnością na hiperwitaminozy (patrz punkt Specjalne środki ostrożności
przy stosowaniu).
Objawy przedawkowania preparatu CERNEVIT wynikają głównie z podania zbyt dużych dawek
witaminy A.
Objawy kliniczne ostrego przedawkowania witaminy A (dawki przekraczające 150000 j.m.)
- zaburzenia żołądkowo-jelitowe, ból głowy, wzrost ciśnienia wewnątrzczaszkowego, obrzęk tarczy nerwu wzrokowego, zaburzenia psychiczne, nadmierna pobudliwość a nawet drgawki. Jako późny objaw reakcji organizmu na przedawkowanie obserwowano uogólnione łuszczenie się skóry.
Objawy kliniczne toksyczności witaminy A przy przedawkowaniu przewlekłym (długotrwałe
podawanie wyższych niż fizjologiczne dawek witaminy A u pacjentów niewymagających
uzupełniania niedoboru)
- wzrost ciśnienia wewnątrzczaszkowego, nadmierny wzrost warstwy korowej kości długich oraz przedwczesne kostnienie części nasadowych kości. Rozpoznanie jest oparte na obecności tkliwych
uciskowo lub bolesnych podskórnych obrzęków w obrębie kończyn. W obrazie rentgenowskim
występują zgrubienia okostnej trzonu kości łokciowej, strzałkowej, obojczyków oraz żeber.
Leczenie przedawkowania witamin zazwyczaj polega na zaprzestaniu suplementacji witamin i innych
działaniach zgodnie ze wskazaniami klinicznymi (jak ograniczenie podaży wapnia, zwiększenie
diurezy i nawodnienie).
Dane farmaceutyczne
Okres ważności
2 lata
Specjalne środki ostrożności podczas przechowywania
Przechowywać w temperaturze pokojowej, tj. od 15°C do 25°C, chronić od światła.
Przechowywać w opakowaniu zewnętrznym.
Po rozpuszczeniu preparat zachowuje stabilność chemiczną i fizyczną przez 24 godziny w
temperaturze 25°C.
Z mikrobiologicznego punktu widzenia, produkt powinien zostać zużyty natychmiast po
rozpuszczeniu. W przeciwnym razie, za czas i warunki przechowywania do momentu użycia
odpowiada osoba podająca preparat, a przechowywanie nie powinno trwać dłużej niż 24 godziny w
temperaturze 2-8°C, chyba że rozpuszczanie odbywało się w kontrolowanych i zwalidowanych
warunkach aseptycznych.
Rodzaj i zawartość opakowania
Fiolki z oranżowego szkła zawierające po 750 mg proszku, w tekturowym pudełku. Opakowania 10 i
20 fiolek.
Fiolki z oranżowego szkła zawierające po 750 mg proszku, z systemem BIO-SET, w tekturowym
pudełku. Opakowania 10 i 20 fiolek.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Niezgodności, instrukcje dotyczące usuwania i przygotowania produktu leczniczego do stosowania
(jeśli dotyczy)
- Podczas przygotowywania roztworu i dodawania składnika do mieszaniny do żywienia pozajelitowego, należy przestrzegać warunków aseptycznych.
- Delikatnie wymieszać, aby rozpuścić liofilizowany proszek.
- CERNEVIT musi być całkowicie rozpuszczony zanim zostanie przeniesiony z fiolki.
- Nie używać produktu, jeżeli przygotowany roztwór nie jest klarowny a oryginalne zamknięcie jest naruszone.
- Po dodaniu CERNEVIT do roztworu do żywienia pozajelitowego, należy sprawdzić czy nie występuje nieprawidłowa zmiana koloru i (lub) czy nie są obecne osady nierozpuszczalnych kompleksów lub kryształów.
- Należy dokładnie wymieszać końcowy roztwór, jeżeli CERNEVIT jest stosowany jako składnik mieszaniny do żywienia pozajelitowego.
- Niewykorzystany rozpuszczony produkt CERNEVIT należy wyrzucić i nie należy przechowywać go do późniejszego użycia.
- Produkty lecznicze do podawania pozajelitowego przed podaniem należy ocenić wizualnie pod kątem obecności cząstek stałych i nieprawidłowej zmiany zabarwienia roztworu, gdy roztwór oraz opakowanie na to pozwala.
- Podczas podawania wszystkich rodzajów żywienia pozajelitowego zaleca się stosowanie filtra na końcu linii.
Jeśli potrzeba, należy odnieść się do odpowiednich referencji dotyczących zgodności oraz
wytycznych. Tego produktu leczniczego nie wolno mieszać z innymi produktami leczniczymi, chyba
że wykazano ich zgodność i stabilność. W celu uzyskania dalszych informacji należy skontaktować się
z podmiotem odpowiedzialnym.
Należy sprawdzić zgodność roztworów podawanych jednocześnie przez tą samą linię.
CERNEVIT (fiolki bez BIO-SET)
Podanie dożylne
Przy użyciu strzykawki wstrzyknąć 5 ml wody do wstrzykiwań lub roztworu glukozy 5% lub 0,9%
roztworu chlorku sodu do fiolki.
Delikatnie wymieszać, aż do rozpuszczenia proszku.
Otrzymany roztwór ma kolor żółto-pomarańczowy.
Podanie domięśniowe
Rozpuścić proszek w 2,5 ml wody do wstrzykiwań w sposób opisany powyżej.
CERNEVIT BIO-SET
CERNEVIT z systemem BIO-SET umożliwia bezpośrednie rozpuszczenie preparatu w workach
(jedno i wielokomorowych) z wejściem iniekcyjnym.
Worek jednokomorowy:
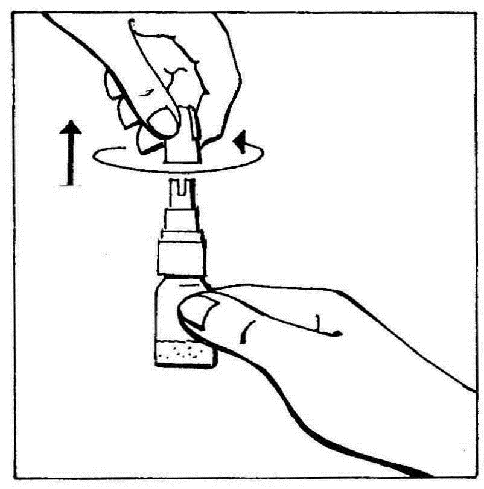
- 1. Zdjąć zatyczkę, przekręcając ją a następnie ciągnąć, aby przerwać pierścień zabezpieczający.
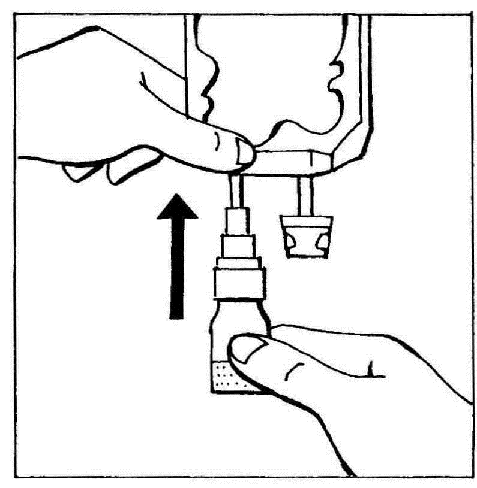
- 2. Połączyć BIO-SET bezpośrednio z wejściem iniekcyjnym worka.
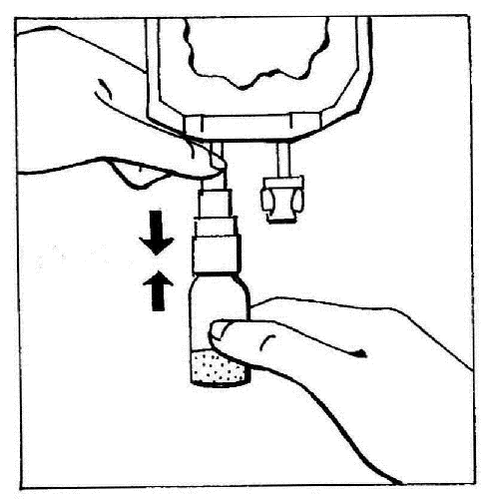
- 3. Aktywować BIO-SET dociskając przezroczystą, ruchomą część. Pozwala to przekłuć gumowy korek fiolki.
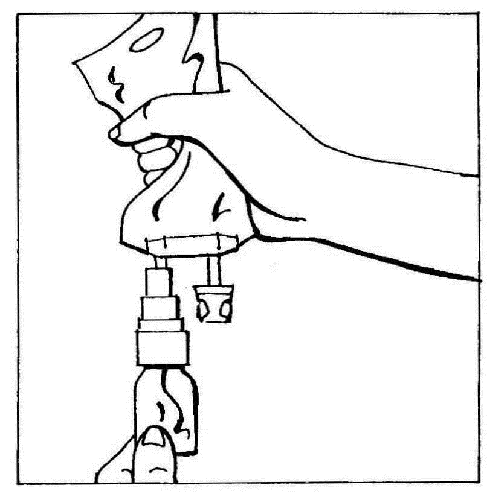
- 4. Ustawić w pozycji pionowej złączone elementy (CERNEVIT z BIO- SET i worek z płynem do wlewu), trzymając worek na górze. Delikatnie ścisnąć worek kilka razy, aby spowodować przepływ płynu do fiolki (ok. 5 ml). Wstrząsnąć fiolką w celu rozpuszczenia proszku.
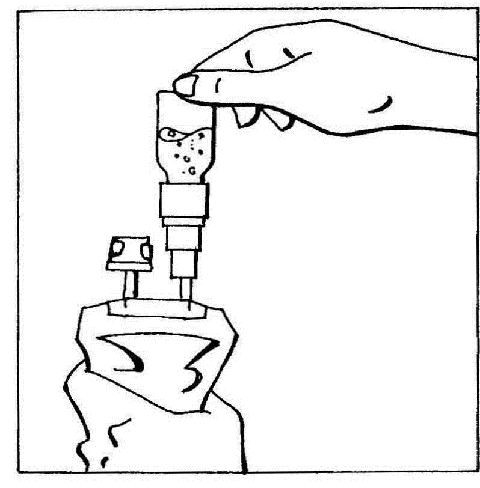
- 5. Odwrócić złączone elementy i przytrzymać je w pozycji pionowej z fiolką na górze. Delikatnie ścisnąć worek kilka razy, aby przemieścić powietrze z worka do fiolki. Spowoduje to zwrotny przepływ płynu do worka.
- 6. Powtórzyć kroki 4 i 5, aż do opróżnienia fiolki.
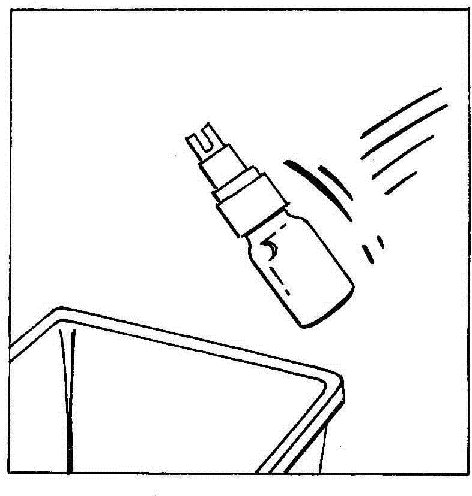
- 7. Odłączyć i wyrzucić fiolkę z BIO-SET.
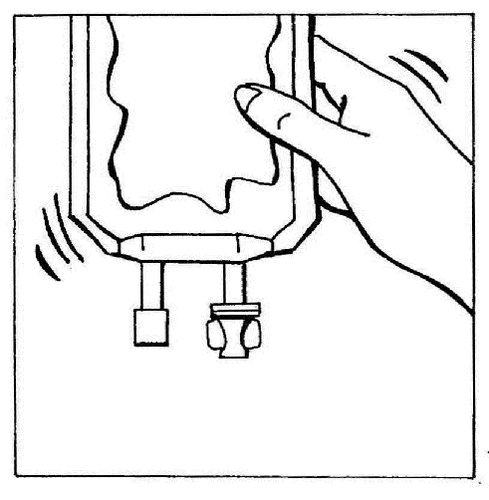
- 8. Zawartość worka delikatnie wymieszać.
Worek wielokomorowy:
Rozpuszczenie preparatu CERNEVIT z zestawem BIO-SET należy wykonać przed aktywacją worka
wielokomorowego (przed otwarciem rozrywalnych spawów i przed wymieszaniem wszystkich
komór).
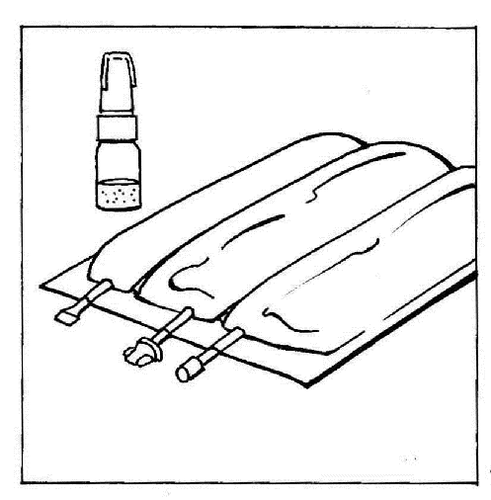
- 1. Umieścić worek wielokomorowy na stole.
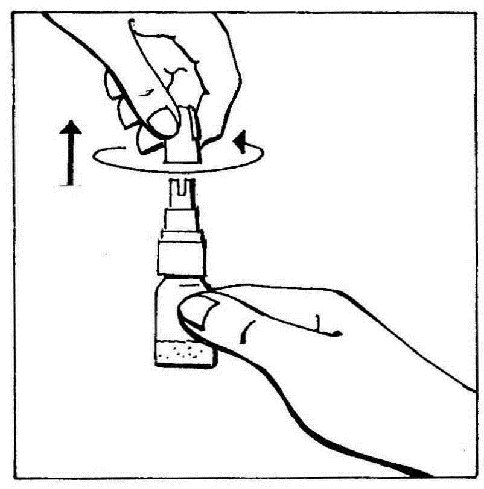
- 2. Zdjąć zatyczkę, przekręcając ją a następnie ciągnąć, aby przerwać pierścień zabezpieczający.
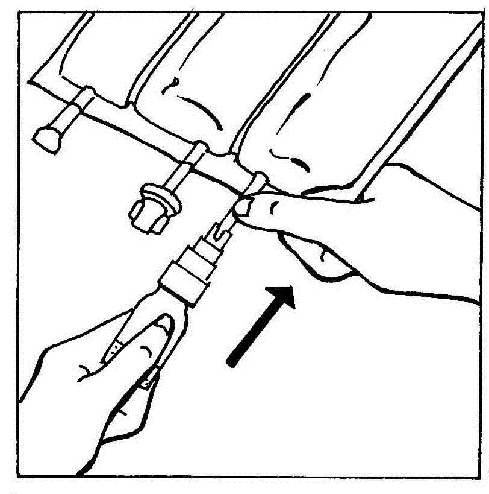
- 3. Połączyć BIO-SET bezpośrednio z wejściem iniekcyjnym worka.
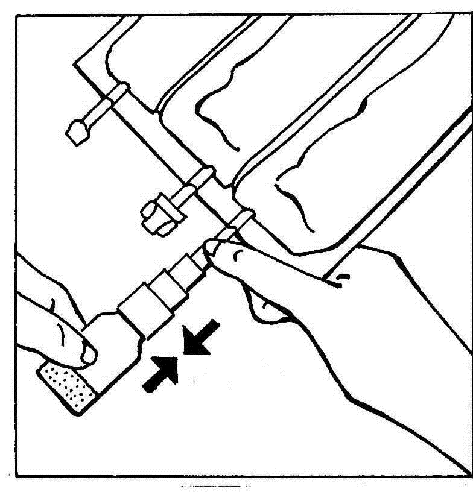
- 4. Aktywować BIO-SET dociskając przezroczystą, ruchomą część. Pozwala to przekłuć gumowy korek fiolki.
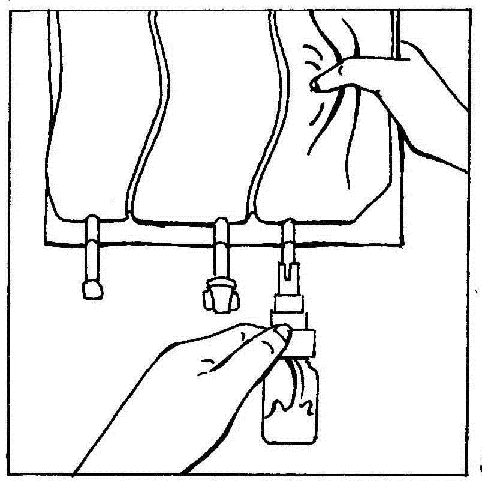
- 5. Przytrzymać fiolkę w pozycji pionowej. Delikatnie ścisnąć komorę worka kilka razy, aby spowodować przepływ płynu do fiolki (ok. 5 ml). Wstrząsnąć fiolką w celu rozpuszczenia proszku.
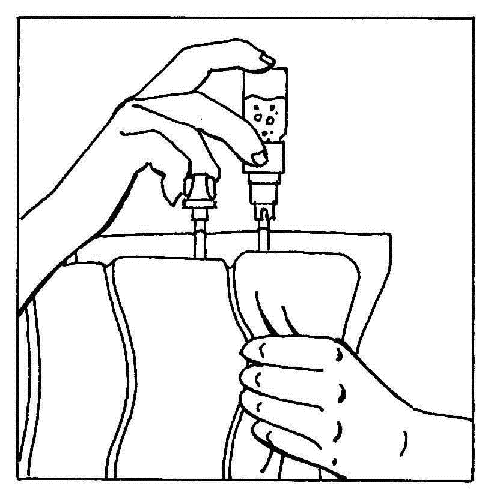
- 6. Odwrócić złączone elementy i przytrzymać je w pozycji pionowej fiolką na górze. Delikatnie ścisnąć komorę worka kilka razy, aby przemieścić powietrze z worka do fiolki. Spowoduje to zwrotny przepływ płynu do worka.
- 7. Powtórzyć kroki 5 i 6 aż do opróżnienia fiolki.
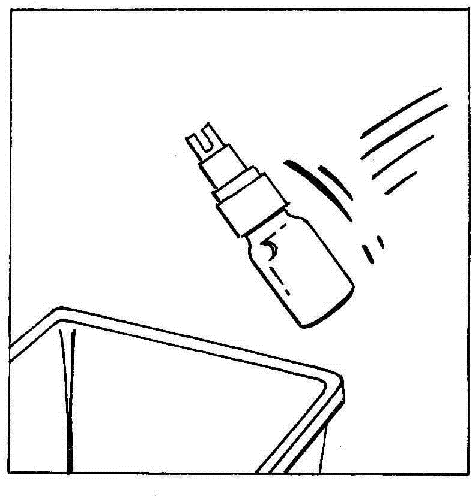
- 8. Odłączyć i wyrzucić fiolkę z CERNEVIT BIO-SET.
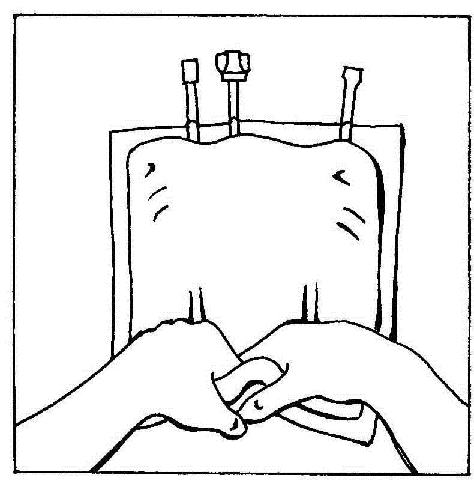
- 9. Przerwać spawy komór worka. Ostatecznie aktywować worek wielokomorowy.
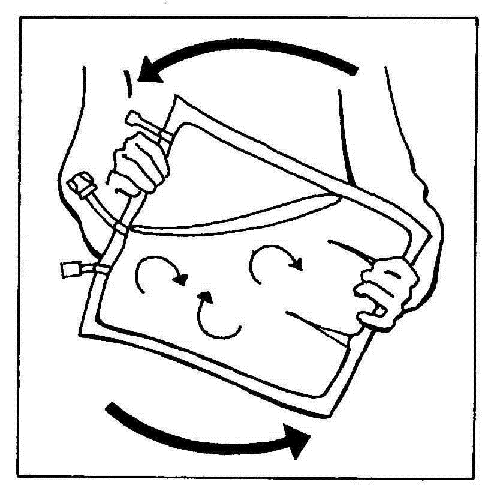
- 10. Zawartość worka delikatnie wymieszać, obracając go co najmniej 3 razy.
OSTRZEŻENIE:
Należy uważać, aby nie doszło do odłączenia zestawu BIO-SET od wejścia iniekcyjnego worka w
trakcie rozpuszczania preparatu.
- Kraj rejestracji
- Wymaga receptyNie
- Producent
- ImporterBaxter S.A.
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki CernevitPostać farmaceutyczna: Koncentrat, -Substancja czynna: electrolytes in combination with other drugsProducent: Fresenius Kabi Norge ASBez receptyPostać farmaceutyczna: Koncentrat, (170,1 mg + 133,5 mg + 14 mg)/mlSubstancja czynna: electrolytes in combination with other drugsBez receptyPostać farmaceutyczna: Roztwór, 1 g/10 mlSubstancja czynna: calcium chlorideProducent: Demo S.A.Wymaga recepty
Odpowiedniki Cernevit w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Cernevit – Ukraina
Odpowiednik Cernevit – Hiszpania
Lekarze online w sprawie Cernevit
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Cernevit – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














