
Octanate Lv

Consulta con un médico sobre la receta médica de Octanate Lv

Cómo usar Octanate Lv
Hoja de instrucciones del paquete: información para el usuario
Octanate LV, 100 UI/ml, polvo y disolvente para la preparación de una solución para inyección
Factor de coagulación sanguínea humano VIII Octanate LV, 200 UI/ml, polvo y disolvente para la preparación de una solución para inyección
Factor de coagulación sanguínea humano VIII
Es importante leer el folleto antes de usar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar este folleto para poder volver a leerlo si es necesario.
- Debe consultar a un médico, farmacéutico o enfermera si tiene alguna duda adicional.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si sus síntomas son los mismos que los suyos.
- Si alguno de los efectos secundarios se vuelve grave, o si nota algún efecto secundario no mencionado en este folleto, debe informar a su médico, farmacéutico o enfermera. Ver punto 4.
Índice del folleto:
- 1. Qué es Octanate LV y para qué se utiliza
- 2. Información importante antes de usar Octanate LV
- 3. Cómo usar Octanate LV
- 4. Posibles efectos secundarios
- 5. Cómo conservar Octanate LV
- 6. Contenido del paquete y otra información
1. Qué es Octanate LV y para qué se utiliza
Octanate LV pertenece a un grupo de medicamentos llamados factores de coagulación y contiene factor de coagulación sanguínea humano VIII. Es una proteína especial que aumenta la capacidad de la sangre para coagularse.
Octanate LV se utiliza para tratar y prevenir hemorragias en pacientes con hemofilia A. Es una condición en la que la sangre tarda más de lo normal en coagularse. Esto se debe a una deficiencia congénita de factor VIII en la sangre.
2. Información importante antes de usar Octanate LV
Se recomienda encarecidamente que cada vez que se administre una dosis de Octanate LV, se anote el nombre y el número de lote del producto para mantener un registro de la serie utilizada.
El médico puede recomendar considerar la vacunación contra la hepatitis viral A y B en caso de recibir regularmente o repetidamente productos de factor VIII de origen humano.
Cuándo no usar Octanate LV
si el paciente es alérgico al factor de coagulación sanguínea humano VIII o a alguno de los demás componentes de este medicamento (enumerados en el punto 6).
Precauciones y advertencias
Antes de comenzar a usar Octanate LV, debe consultar a un médico, farmacéutico o enfermera.
Octanate LV contiene cantidades residuales de otras proteínas humanas. Cualquier medicamento que contenga proteínas y se administre por vía intravenosa (inyección en una vena) puede causar reacciones alérgicas (ver punto 4. Posibles efectos secundarios).
La formación de inhibidores (anticuerpos) es una complicación conocida que puede ocurrir durante el tratamiento con todos los medicamentos que contienen factor VIII. Estos inhibidores, especialmente a concentraciones altas, interrumpen el tratamiento efectivo y el paciente será monitoreado de cerca para detectar la formación de estos inhibidores. Si la hemorragia en el paciente no se controla adecuadamente con Octanate LV, debe informar de inmediato a su médico.
Información sobre la sangre y el suero utilizados para producir Octanate LV
Durante la producción de medicamentos a partir de sangre o suero humano, se toman ciertas medidas para prevenir la transmisión de infecciones a los pacientes. Estas incluyen la selección cuidadosa de donantes de sangre y suero para garantizar la exclusión de donantes que puedan ser portadores de infecciones, así como pruebas de todas las muestras y pools de suero para detectar la presencia de virus/infecciones. Los fabricantes de estos productos han implementado etapas en el proceso de procesamiento de la sangre o el suero para inactivar o eliminar los virus. A pesar de estas medidas, no se puede excluir completamente la posibilidad de transmisión de una infección cuando se administran medicamentos preparados a partir de sangre o suero humano. Esto incluye infecciones desconocidas o que han aparecido recientemente, o otros tipos de infecciones.
Las medidas tomadas se consideran efectivas contra los virus con envoltura, como el virus de la inmunodeficiencia humana (VIH), el virus de la hepatitis B (VHB) y el virus de la hepatitis C (VHC), así como contra el virus de la hepatitis A (VHA) sin envoltura. Los métodos utilizados pueden tener una eficacia limitada contra los virus sin envoltura, como el parvovirus B19.
La infección por parvovirus B19 puede ser grave para las mujeres embarazadas (infección del feto) y para personas con sistemas inmunitarios debilitados o que padecen ciertos tipos de anemia (como anemia falciforme o destrucción anormal de glóbulos rojos).
Otros medicamentos y Octanate LV
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando actualmente o recientemente, así como sobre los medicamentos que planea tomar, incluyendo aquellos que se venden sin receta.
No se conocen interacciones entre el factor de coagulación sanguínea humano VIII y otros productos medicinales. Sin embargo, no debe mezclar Octanate LV con otros medicamentos durante la infusión.
Embarazo y lactancia
Antes de usar cualquier medicamento, debe consultar a un médico o farmacéutico.
Conducción de vehículos y uso de máquinas
No se ha observado ningún efecto en la capacidad para conducir vehículos o operar máquinas.
Octanate LV contiene
hasta 40 mg de sodio (principal componente de la sal común) por dosis. Esto equivale al 2% del consumo máximo recomendado de 2 g de sodio para un adulto.
3. Cómo usar Octanate LV
Octanate LV debe administrarse por vía intravenosa después de la reconstitución con el disolvente proporcionado.
El tratamiento debe iniciarse bajo supervisión médica.
Dosificación para la prevención de hemorragias:En la profilaxis a largo plazo de hemorragias en pacientes con hemofilia A grave, se debe administrar factor VIII en una dosis de 20 a 40 UI/kg de peso corporal cada 2 a 3 días. La dosis debe ajustarse según la respuesta clínica. En algunos casos, puede ser necesario administrar el medicamento en intervalos de tiempo más cortos o en dosis más altas.
Cálculo de la dosis:
Octanate LV siempre debe usarse según las instrucciones de un médico. En caso de duda, debe volver a consultar a su médico o farmacéutico.
La actividad del factor VIII en el suero sanguíneo es equivalente a la concentración de factor VIII en el suero. Se expresa como porcentaje (en relación con el suero sanguíneo humano normal) o en unidades internacionales (UI).
La dosis de factor VIII se expresa en UI.
Una unidad internacional (UI) de actividad del factor VIII es equivalente a la cantidad de factor VIII en 1 ml de suero sanguíneo humano normal. 1 UI de factor VIII por kilogramo de peso corporal aumenta la actividad del factor VIII en el suero sanguíneo en un 1,5% - 2% de la actividad normal. Para calcular la dosis necesaria, debe determinar la actividad del factor VIII en el suero sanguíneo del paciente. Esto permitirá determinar cuánto debe aumentar la actividad. Debe consultar a un médico en caso de duda sobre cuánto debe aumentar la actividad del factor VIII en el suero sanguíneo y cómo calcular la dosis necesaria.
La dosis necesaria se calcula utilizando la siguiente fórmula:
dosis necesaria = peso corporal (kg) x aumento necesario de la actividad del factor VIII (%)
(UI/ml) x 0,5
La cantidad que se debe administrar y la frecuencia de administración del producto deben ajustarse siempre según la eficacia clínica en cada paciente individual.
En los siguientes casos de hemorragia, la actividad del factor VIII no debe caer por debajo del nivel de actividad en el suero sanguíneo (% del valor normal) durante el período especificado.
| Gravedad de la hemorragia / Tipo de procedimiento quirúrgico | Nivel de factor VIII requerido (%) (UI/ml) | Frecuencia de administración (horas)/ Duración del tratamiento (días) |
| Hemorragia | ||
| Hemorragia leve en las articulaciones, músculos o boca | 20-40 | Repetir cada 12 a 24 horas. Al menos 1 día hasta que el dolor causado por la hemorragia cese o la herida se cure. |
| Hemorragia más grave en las articulaciones, músculos o hematoma | 30-60 | Repetir la infusión cada 12 a 24 horas durante 3-4 días o más hasta que el dolor cese y la función se restaure. |
| Hemorragias que ponen en peligro la vida | 60-100 | Repetir la infusión cada 8 a 24 horas hasta que el peligro cese. |
| Operaciones | ||
| Menores, incluyendo extracción de muelas | 30-60 | Cada 24 horas, durante al menos 1 día, hasta que la herida se cure. |
| Mayores | 80-100 (pre y postoperatorio) | Repetir la infusión cada 8 a 24 horas hasta que la herida se cure adecuadamente, luego continuar el tratamiento durante al menos 7 días más para mantener la actividad del factor VIII en un nivel del 30% al 60%. |
La dosis y la frecuencia de administración de Octanate LV deben determinarse por un médico.
La respuesta al factor VIII puede variar entre pacientes. Por lo tanto, se recomienda determinar los niveles de factor VIII durante el tratamiento para establecer la dosis y la frecuencia de administración adecuadas.
Uso en niños
No se han encontrado requisitos especiales de dosificación en niños en los estudios clínicos.
La dosificación es la misma en adultos y niños, tanto para el tratamiento como para la profilaxis.
Instrucciones para la administración en el hogar
- Debe leer todas las instrucciones y seguirlos cuidadosamente.
- No use el producto Octanate LV después de la fecha de caducidad impresa en la etiqueta.
- Debe mantener condiciones estériles durante el procedimiento descrito a continuación.
- Antes de la administración, debe verificar visualmente que la solución preparada del producto no contenga partículas sólidas o decoloración.
- La solución debe ser clara o ligeramente opalescente. No use soluciones que estén turbias o contengan partículas sólidas.
- Debe usar la solución preparada inmediatamente para evitar la contaminación microbiológica.
- Debe usar exclusivamente el conjunto de infusión proporcionado. El uso de otro equipo para inyecciones/infusiones puede causar riesgos adicionales y fracaso del tratamiento.
Instrucciones para la preparación de la solución:
- 1. No use el producto directamente después de sacarlo del refrigerador. Deje el disolvente y el polvo en los frascos cerrados hasta que alcancen la temperatura ambiente.
- 2. Retire las tapas de ambos frascos y limpie los tapones de goma con uno de los hisopos con alcohol proporcionados.
- 3. El conjunto de transferencia se muestra en la figura 1. Coloque el frasco con el disolvente en una superficie plana y sujételo firmemente. Tome el conjunto de transferencia y gírelo. Coloque la parte azul del conjunto de transferencia sobre el frasco con el disolvente y presione firmemente hasta que se bloquee (figura 2 + 3). No gire durante la conexión.
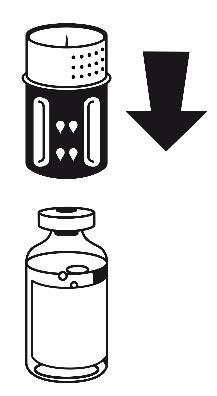
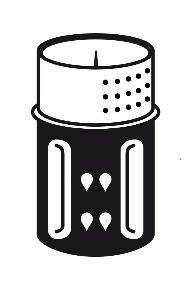
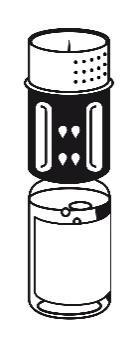
Figura 1
Figura 3
Figura 2
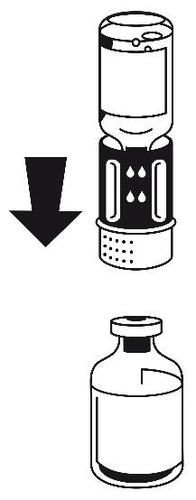
- 4. Coloque el frasco con el polvo en una superficie plana y sujételo firmemente. Tome el frasco con el disolvente con el conjunto de transferencia conectado y gírelo hacia abajo. Coloque la parte blanca del conjunto de transferencia sobre el frasco con el polvo y presione firmemente hasta que se bloquee (figura 4). No gire durante la conexión. El disolvente fluye automáticamente hacia el frasco con el polvo.
Figura 4
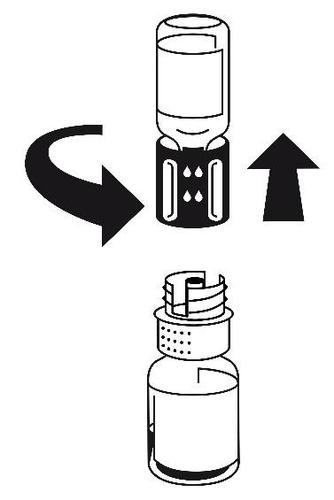
- 5. Con ambos frascos conectados, gire suavemente el frasco con el polvo hasta que el producto se disuelva. La disolución se completa en menos de 10 minutos a temperatura ambiente. Durante la preparación, puede formarse una ligera espuma. Desenrosque el conjunto de transferencia en dos partes (figura 5). La espuma desaparecerá.
Deseche el frasco vacío con el disolvente con la parte azul del conjunto de transferencia.
Figura 5
Instrucciones para la administración por inyección:
Como medida de precaución, debe verificar el pulso antes y durante la inyección. Si nota un aumento significativo en la frecuencia del pulso, debe reducir la velocidad de inyección o interrumpir la administración del medicamento durante un corto tiempo.
- 1. Conecte la jeringa al conjunto de transferencia. Gire el frasco hacia abajo y aspire la solución hacia la jeringa (figura 6). La solución debe ser clara o ligeramente opalescente. Después de transferir la solución, sujete firmemente el émbolo de la jeringa (manteniéndolo hacia abajo) y retire la jeringa del conjunto de transferencia (figura 7).
Deseche el frasco vacío con la parte blanca del conjunto de transferencia.
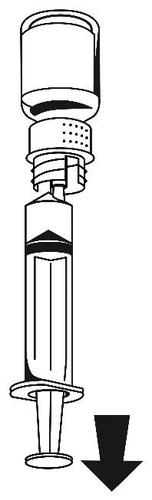
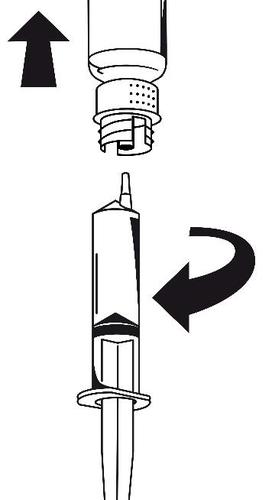
Figura 6
Figura 7
- 2. Limpie el lugar de inyección seleccionado con uno de los hisopos con alcohol proporcionados.
- 3. Conecte el conjunto de infusión proporcionado a la jeringa.
- 4. Introduzca la aguja en la vena seleccionada. Si usa una banda de compresión para visualizar la vena, debe aflojarla antes de comenzar la inyección del producto Octanate.
- 5. La sangre no debe entrar en la jeringa debido al riesgo de formación de coágulos de fibrina.
- 6. Administre la solución lentamente en la vena, no más rápido de 2-3 ml por minuto. Si se utilizan varias ampollas de polvo de Octanate durante una sola administración, es posible volver a usar el mismo conjunto de infusión y jeringa. El conjunto de transferencia está diseñado para un solo uso.
Debe eliminar cualquier residuo no utilizado del producto o sus desechos de acuerdo con las regulaciones locales.
Uso de una dosis mayor de la recomendada de Octanate LV
No se han observado síntomas de sobredosis de factor de coagulación sanguínea humano VIII. Sin embargo, se recomienda no exceder la dosis recomendada.
Omision de una dosis de Octanate LV
No debe administrar una dosis doble para compensar una dosis omitida. Debe continuar con la siguiente dosis según las instrucciones de su médico o farmacéutico.
Debe consultar a un médico o farmacéutico si tiene alguna otra pregunta sobre el uso de este producto.
4. Posibles efectos secundarios
Como cualquier medicamento, este medicamento puede causar efectos secundarios, aunque no todos los pacientes los experimentarán.
A pesar de que son poco frecuentes(ocurren en 1 de cada 10.000 pacientes), se han observado reacciones de hipersensibilidad o alérgicas en pacientes tratados con productos que contienen factor VIII.
Debe consultar a un médico si experimenta alguno de los siguientes síntomas:
vómitos, sensación de ardor y dolor punzante en el lugar de la infusión, sensación de opresión en el pecho, escalofríos, taquicardia, náuseas, sensación de hormigueo, enrojecimiento, dolor de cabeza, urticaria, caída de la presión arterial, erupción, ansiedad, hinchazón de la cara, los labios, la boca, la lengua o la garganta, que puede provocar dificultad para tragar o respirar (edema angioneurótico), fatiga (letargo), respiración silbante.
Muy raramente(ocurren en menos de 1 de cada 10.000 pacientes) la hipersensibilidad puede provocar una reacción alérgica grave y potencialmente mortal llamada anafilaxia, que puede incluir shock, así como alguno o todos los síntomas mencionados anteriormente. En tal caso, debe consultar a un médico o llamar a los servicios de emergencia de inmediato.
Otros efectos secundarios raros (ocurren en 1 de cada 10.000 pacientes)
Fiebre.
En niños no tratados previamente con medicamentos que contienen factor VIII, los anticuerpos bloqueadores (ver punto 2) pueden ocurrir muy frecuentemente (más de 1 de cada 10 pacientes). Sin embargo, en pacientes que han sido tratados previamente con factor VIII (más de 150 días de tratamiento), el riesgo es poco frecuente (menos de 1 de cada 100 pacientes). Si esto sucede, los medicamentos del paciente pueden dejar de funcionar adecuadamente y el paciente puede experimentar una hemorragia persistente. Si esto sucede, debe consultar a un médico de inmediato.
Información relacionada con la seguridad viral, ver punto 2. (Debe tener especial cuidado al usar Octanate LV).
Notificación de efectos secundarios
Si experimenta alguno de los efectos secundarios mencionados anteriormente o cualquier otro efecto secundario no mencionado en este folleto, debe informar a su médico, farmacéutico o enfermera. Los efectos secundarios pueden notificarse directamente al Departamento de Vigilancia de Efectos Secundarios de los Productos Farmacéuticos de la Agencia de Registro de Productos Farmacéuticos, Dispositivos Médicos y Productos Biocidas
Al. Jerozolimskie 181C
PL-02 222 Varsovia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
correo electrónico: [email protected]
Al notificar los efectos secundarios, se pueden recopilar más información sobre la seguridad del uso del medicamento.
5. Cómo conservar Octanate LV
Debe conservar el medicamento en un lugar donde no pueda ser visto ni alcanzado por los niños.
No use este medicamento después de la fecha de caducidad impresa en la etiqueta. La fecha de caducidad se refiere al último día del mes indicado.
Conservar en el refrigerador (2˚C – 8˚C).
No congelar.
Conservar en el paquete exterior para protegerlo de la luz.
La solución reconstituida debe usarse de inmediato y solo durante una administración.
No use este medicamento si nota que la solución está turbia o no se ha disuelto completamente.
No debe tirar los medicamentos por el desagüe o los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Octanate LV?
La sustancia activadel medicamento es el factor de coagulación sanguínea humano VIII.
Volumen y concentraciones
| Tamaño del frasco con polvo de Octanate LV (UI de factor VIII) | Tamaño del frasco con disolvente (ml) | Concentración nominal de la solución después de la reconstitución (UI de factor VIII/ml) |
| 500 UI | 5 | 100 |
| 1.000 UI | 5 | 200 |
Los demás componentes son:
Para el polvo: citrato de sodio, cloruro de sodio, cloruro de calcio, glicina
Para el disolvente: agua para inyección
Cómo se presenta Octanate LV y qué contiene el paquete?
Octanate LV se presenta en forma de polvo y disolvente para la preparación de una solución para inyección.
El polvo es blanco o ligeramente amarillento y puede estar en forma de grumos.
El disolvente es un líquido transparente e incoloro.
2 potencias del producto están disponibles y difieren en la cantidad de factor VIII y disolvente:
100 UI/ml polvo y disolvente
- Polvo, 500 UI, en un frasco con tapón y tapa de tipo flip-off
- 5 ml de disolvente en un frasco con tapón y tapa de tipo flip-off
- 1 paquete con equipo para inyección intravenosa (1 conjunto de transferencia, 1 conjunto de infusión, 1 jeringa de un solo uso)
- 2 hisopos con alcohol.
200 UI/ml polvo y disolvente
- Polvo, 1.000 UI, en un frasco con tapón y tapa de tipo flip-off
- 5 ml de disolvente en un frasco con tapón y tapa de tipo flip-off
- 1 paquete con equipo para inyección intravenosa (1 conjunto de transferencia, 1 conjunto de infusión, 1 jeringa de un solo uso)
- 2 hisopos con alcohol.
No todas las tallas de paquete pueden estar disponibles en el mercado.
Titular de la autorización de comercialización
Octapharma (IP) SPRL
Allée de la Recherche 65
1070 Anderlecht
Bélgica
Fabricante
Octapharma Pharmazeutika Produktionsges.m.b.H
Oberlaaer Str. 235
1100 Viena
Austria
Octapharma S.A.S
72 rue du Maréchal Foch
67380 Lingolsheim
Francia
Octapharma AB
Lars Forssells gata 23
112 75 Estocolmo
Suecia
Este producto está autorizado en los estados miembros de la Comunidad Europea bajo los siguientes nombres:
Octanate LV: Austria, Chipre, Dinamarca, Francia, Holanda, Malta, Polonia, Rumania, España, Suecia, Reino Unido
Octafil LV: Finlandia
Octanate: Bélgica, República Checa, Alemania, Irlanda, Italia, Letonia, Lituania, Luxemburgo, Portugal
Octanate Kons: República de Eslovenia
Fecha de la última actualización del folleto:26.03.2021
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorOctapharma AB Octapharma Pharmazeutika Produktions.ges.m.b.H. Octapharma S.A.S.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a Octanate LvForma farmacéutica: Polvo, 1000 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere recetaForma farmacéutica: Polvo, 2000 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere recetaForma farmacéutica: Polvo, 250 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere receta
Alternativas a Octanate Lv en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Octanate Lv en España
Alternativa a Octanate Lv en Ucrania
Médicos online para Octanate Lv
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Octanate Lv – sujeta a valoración médica y normativa local.














