Cómo usar Metiofill
Hoja de instrucciones del paquete: información para el usuario
Methofill, 50 mg/ml, solución para inyección en jeringa precargada
Metotrexato
Es importante leer atentamente el contenido de esta hoja de instrucciones antes de usar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- Debe consultar a su médico, farmacéutico o enfermera si tiene alguna duda.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si aparecen efectos adversos, incluidos todos los posibles efectos adversos no enumerados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera (ver sección 4).
Índice de la hoja de instrucciones
- 1. Qué es Methofill y para qué se utiliza
- 2. Información importante antes de usar Methofill
- 3. Cómo usar Methofill
- 4. Posibles efectos adversos
- 5. Cómo conservar Methofill
- 6. Contenido del paquete y otra información
1. Qué es Methofill y para qué se utiliza
El principio activo de Methofill es metotrexato.
El metotrexato tiene las siguientes propiedades:
- Inhibe el crecimiento de algunas células que se dividen rápidamente
- Reduce la actividad del sistema inmunológico (mecanismos de defensa del organismo)
- Tiene un efecto antiinflamatorio
Indicaciones para el uso de Methofill:
- artritis reumatoide activa en pacientes adultos,
- formas poliarticulares de artritis idiopática juvenil severa, si la respuesta a los medicamentos antiinflamatorios no esteroideos es insuficiente,
- psoriasis severa resistente al tratamiento, si no se ha obtenido una respuesta satisfactoria con la fototerapia, la terapia PUVA y los retinoides, y artritis psoriásica severa en pacientes adultos,
- enfermedad de Crohn de curso leve a moderado en pacientes adultos, cuando el tratamiento con otros medicamentos no es posible.
La artritis reumatoide (AR) es una enfermedad crónica que se clasifica como una colagenosis, que se caracteriza por la inflamación de las membranas sinoviales que recubren las articulaciones. Las membranas sinoviales producen un líquido que actúa como lubricante para muchas articulaciones. El estado inflamatorio provoca el engrosamiento de las membranas y la hinchazón de las articulaciones.
La artritis juvenil ocurre en niños y adolescentes menores de 16 años. La forma poliarticular se indica por el hecho de que 5 o más articulaciones se ven afectadas por la enfermedad en los primeros 6 meses de la enfermedad.
La artritis psoriásica se refiere a la inflamación de las articulaciones, especialmente de los dedos de las manos y los pies, con lesiones psoriásicas en la piel y las uñas.
La psoriasis es una enfermedad crónica de la piel que se caracteriza por placas rojas cubiertas con una escama gruesa, seca y plateada que se adhiere firmemente.
Methofill modifica y ralentiza el progreso de la enfermedad.
La enfermedad de Crohn es un tipo de enfermedad inflamatoria intestinal que puede afectar cualquier parte del tracto gastrointestinal, causando síntomas como dolor abdominal, diarrea, vómitos o pérdida de peso.
2. Información importante antes de usar Methofill
Cuándo no usar Methofill
- si el paciente es alérgico al metotrexato o a alguno de los demás componentes de este medicamento (enumerados en la sección 6);
- si el paciente tiene una enfermedad hepática o renal grave o una enfermedad sanguínea;
- si el paciente consume regularmente grandes cantidades de alcohol;
- si el paciente tiene una infección grave, como la tuberculosis, la infección por VIH u otros trastornos de la inmunidad;
- si el paciente tiene úlceras en la boca, el estómago o los intestinos;
- si el paciente está recibiendo una vacuna que contiene microorganismos vivos;
- si el paciente es mujer y está embarazada o en período de lactancia (ver sección "Embarazo, lactancia y fertilidad").
Advertencias y precauciones
Antes de comenzar a usar Methofill, debe discutir con su médico o farmacéutico:
- si el paciente es anciano, está debilitado o en mal estado general;
- si el paciente tiene trastornos de la función hepática;
- si el paciente tiene deshidratación (falta de agua en el organismo);
- si el paciente tiene diabetes y está siendo tratado con insulina.
Durante el tratamiento con metotrexato, se han notificado casos de hemorragia pulmonar aguda en pacientes con enfermedad reumatológica subyacente. Si el paciente presenta tos con sangre, debe consultar inmediatamente a su médico.
Precauciones especiales para el uso de Methofill
El metotrexato puede alterar temporalmente la producción de espermatozoides y óvulos; en la mayoría de los casos, este efecto desaparece. El metotrexato puede causar abortos y malformaciones congénitas. La paciente debe evitar quedar embarazada durante el tratamiento con metotrexato y durante al menos 6 meses después de finalizar el tratamiento. Los pacientes deben evitar la procreación durante el tratamiento con metotrexato y durante al menos 3 meses después de finalizar el tratamiento. Ver también la sección "Embarazo, lactancia y fertilidad".
Exámenes de control y precauciones recomendadas:
Incluso cuando se usa metotrexato en dosis bajas, pueden ocurrir efectos adversos graves. Para detectarlos lo antes posible, el médico debe realizar exámenes de control y análisis de laboratorio.
Antes de comenzar el tratamiento:
Antes de comenzar el tratamiento, se realizarán análisis de sangre para comprobar que el paciente tenga suficientes células sanguíneas. La sangre también se analizará para comprobar la función hepática, para determinar si el paciente tiene hepatitis. Además, se comprobarán los niveles de albúmina en suero (proteína en la sangre), la presencia de hepatitis (infección hepática) y la función renal. El médico también puede decidir realizar otros análisis de función hepática. Algunos de ellos pueden ser análisis de imagen, otros pueden requerir la extracción de una pequeña muestra de tejido hepático para su examen más detallado. El médico también puede comprobar si el paciente tiene tuberculosis, ordenar una radiografía de tórax o un análisis de función pulmonar.
Durante el tratamiento:
El médico puede realizar los siguientes exámenes:
- examen de la boca y la garganta para detectar cambios en la mucosa, como inflamación o úlceras;
- análisis de sangre/morfología con evaluación del número de células sanguíneas y medición de la concentración de metotrexato en suero;
- análisis de sangre para controlar la función hepática;
- análisis de imagen para controlar el estado del hígado;
- extracción de una pequeña muestra de tejido hepático para su examen más detallado;
- análisis de sangre para controlar la función renal;
- monitoreo de las vías respiratorias y, si es necesario, análisis de función pulmonar.
Es muy importante que el paciente acuda a los exámenes programados.
Si los resultados de alguno de estos exámenes son anormales, el médico ajustará el tratamiento según sea necesario.
Pacientes ancianos
Los pacientes ancianos tratados con metotrexato deben ser monitoreados estrechamente por su médico para detectar cualquier efecto adverso lo antes posible. Los trastornos hepáticos y renales relacionados con la edad, así como las reservas bajas de ácido fólico en la vejez, requieren dosis relativamente bajas de metotrexato.
El metotrexato puede afectar el sistema inmunológico, los resultados de las vacunas y los resultados de las pruebas inmunológicas. Puede haber una reactivación de enfermedades crónicas latentes (como el herpes zóster, la tuberculosis, la hepatitis viral tipo B o C). No se deben usar vacunas que contengan microorganismos vivos mientras se está tomando Methofill.
El metotrexato puede aumentar la sensibilidad de la piel a la luz solar. Se debe evitar la exposición intensa al sol y no se debe usar una cama de bronceado o una lámpara de bronceado sin consultar a un médico.
Para proteger la piel del sol intenso, se debe usar ropa adecuada o aplicar un filtro solar con un alto factor de protección.
Durante el tratamiento con metotrexato, puede ocurrir una recaída de la dermatitis por radioterapia y las quemaduras solares (llamada "reacción de recuerdo"). Las lesiones cutáneas psoriásicas pueden empeorar durante la exposición a la luz UV y la administración concomitante de metotrexato.
Puede ocurrir un aumento de los ganglios linfáticos (linfoma). En tal caso, se debe interrumpir el tratamiento.
La diarrea puede ser un signo de toxicidad de Methofill y requiere la interrupción del tratamiento.
Si el paciente presenta diarrea, debe informar a su médico.
Se han notificado casos de encefalopatía (trastorno cerebral)/leucoencefalopatía (trastorno del área blanca del cerebro) en pacientes oncológicos que reciben metotrexato; no se puede descartar que esto ocurra en pacientes que reciben metotrexato para otras indicaciones. Los síntomas de este tipo de trastorno cerebral pueden incluir: alteraciones del estado mental, trastornos del movimiento, trastornos de la visión o trastornos de la memoria[frecuencia desconocida]
Los siguientes son otros efectos adversos que pueden ocurrir:
Muy frecuentes:puede ocurrir en más de 1 de cada 10 personas
- inflamación de la mucosa oral, náuseas, vómitos, pérdida de apetito, dolor abdominal
- resultados anormales de las pruebas de función hepática (aumento de la actividad de la AspAT, AlAT, fosfatasa alcalina y aumento de la bilirrubina)
Frecuentes:puede ocurrir en hasta 1 de cada 10 personas
- úlceras de la mucosa oral, diarrea
- erupciones cutáneas, enrojecimiento de la piel, picazón
- dolor de cabeza, fatiga, somnolencia
- disminución de la producción de glóbulos, lo que puede llevar a una disminución del número de glóbulos blancos y/o rojos y/o plaquetas
Poco frecuentes:puede ocurrir en hasta 1 de cada 100 personas
- inflamación de la garganta
- inflamación del intestino, vómitos, inflamación del páncreas, heces negras o con sangre, úlcera del tracto gastrointestinal y sangrado
- reacciones que recuerdan a quemaduras solares debido a una mayor sensibilidad de la piel a la luz solar, pérdida de cabello, aumento del número de nódulos reumatoideos, úlcera cutánea, herpes zóster, inflamación de los vasos sanguíneos, erupción cutánea similar al herpes, urticaria
- aparición de la diabetes
- mareos, confusión, depresión
- disminución de la albúmina en suero
- disminución del número de glóbulos blancos, glóbulos rojos y/o plaquetas
- inflamación y úlcera de la vejiga o la vagina, trastornos de la función renal, trastornos de la micción
- dolor en las articulaciones, dolor muscular, disminución de la densidad ósea
Raros:puede ocurrir en hasta 1 de cada 1000 personas
- inflamación de las encías
- pigmentación cutánea intensa, acné, manchas azules en la piel debido a sangrado de los vasos sanguíneos (equimosis, petequias)
- inflamación alérgica de los vasos sanguíneos
- disminución de los niveles de anticuerpos en la sangre
- infecciones (incluyendo la reactivación de infecciones crónicas latentes), inflamación de la conjuntiva
- cambios de humor
- trastornos de la visión
- inflamación del saco que rodea el corazón, acumulación de líquido en el saco que rodea el corazón, trastornos de la función cardíaca debido a la acumulación de líquido en el saco que rodea el corazón
- presión arterial baja
- formación de tejido cicatricial en los pulmones (fibrosis pulmonar), dificultad para respirar y asma, acumulación de líquido en la pleura
- fracturas por estrés
- trastornos electrolíticos
- fiebre
- trastornos de la cicatrización de heridas
Muy raros:puede ocurrir en hasta 1 de cada 10 000 personas
- sangrado grave, inflamación tóxica aguda del intestino grueso (megacolon tóxico)
- intensificación de la pigmentación de las uñas, inflamación de la uña (paroniquia aguda), infección grave de los folículos pilosos (furónculo), vasos sanguíneos visibles
- daño local (formación de un absceso estéril, cambios en el tejido adiposo) en el lugar de la inyección
- dolor, pérdida de fuerza muscular o sensación de entumecimiento o hormigueo o disminución de la reacción a los estímulos, cambios en el gusto (sabor metálico), convulsiones, parálisis, reacción de las meninges
- disminución de la visión, enfermedad no inflamatoria del ojo (retinopatía)
- disminución de la libido, impotencia, aumento del tamaño de los senos en los hombres, trastornos de la producción de espermatozoides (oligospermia), trastornos del ciclo menstrual, flujo vaginal
- aumento del tamaño de los ganglios linfáticos (linfoma)
- trastornos de la proliferación de linfocitos (producción excesiva de glóbulos blancos)
Frecuencia desconocida:no puede ser determinada a partir de los datos disponibles
- aumento del número de glóbulos blancos
- sangrado nasal
- proteinuria
- sensación de debilidad
- hemorragia pulmonar
- daño a los huesos de la mandíbula (debido a la producción excesiva de glóbulos blancos)
- destrucción del tejido en el lugar de la inyección
- enrojecimiento y descamación de la piel
- edema
Las inyecciones subcutáneas de metotrexato son generalmente bien toleradas. Solo se han observado reacciones cutáneas locales leves (como ardor, enrojecimiento, hinchazón, decoloración, picazón, picazón intensa, dolor) que disminuyen con el tratamiento.
Notificación de efectos adversos
Si ocurren efectos adversos, incluidos todos los posibles efectos adversos no enumerados en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad
Al. Jerozolimskie 181C
02-222 Varsovia
tel.: + 48 22 49 21 301
fax: + 48 22 49 21 309
sitio web: https://smz.ezdrowie.gov.pl
Los efectos adversos también pueden notificarse al titular de la autorización de comercialización.
Al notificar los efectos adversos, se pueden recopilar más información sobre la seguridad del medicamento.
5. Cómo conservar Methofill
El medicamento debe conservarse en un lugar donde no pueda ser visto ni alcanzado por los niños.
Conservar a una temperatura inferior a 30°C.
Conservar las jeringas precargadas en el paquete exterior para protegerlas de la luz.
No use este medicamento después de la fecha de caducidad que aparece en el etiquetado/paquete después de EXP.
La fecha de caducidad es el último día del mes indicado.
No deseche los medicamentos por el desagüe ni en los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo desechar los medicamentos que ya no necesita. Este comportamiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Methofill?
- El principio activo es metotrexato. 1 ml de solución contiene metotrexato disódico en una cantidad equivalente a 50 mg de metotrexato.
- Los demás componentes son cloruro de sodio, hidróxido de sodio (para ajustar el pH) y agua para inyección.
Cómo se presenta Methofill y qué contiene el paquete?
El medicamento en jeringas precargadas es una solución transparente, amarilla a marrón.
La jeringa precargada tiene una cubierta de seguridad adicional para la aguja. Los paquetes contienen jeringas precargadas que están disponibles en blister con almohadillas empapadas en alcohol. Los blister están diseñados para jeringas precargadas individuales con cubierta de seguridad para la aguja.
Están disponibles las siguientes tallas de paquete:
Las jeringas precargadas que contienen 0,15 ml, 0,20 ml, 0,30 ml y 0,40 ml de solución están disponibles en paquetes que contienen 1, 2, 4, 5, 6, 8, 10, 12 o 24 jeringas precargadas con agujas con cubierta de seguridad. La jeringa precargada tiene una cubierta de seguridad adicional para la aguja.
Las jeringas precargadas que contienen 0,25 ml, 0,35 ml, 0,45 ml, 0,55 ml y 0,60 ml de solución están disponibles en paquetes que contienen 1, 4, 5, 6, 8 o 12 jeringas precargadas con agujas con cubierta de seguridad. La jeringa precargada tiene una cubierta de seguridad adicional para la aguja.
Las jeringas precargadas que contienen 0,50 ml de solución están disponibles en paquetes que contienen 1, 2, 4, 5, 6, 8, 10 o 12 jeringas precargadas con agujas con cubierta de seguridad. La jeringa precargada tiene una cubierta de seguridad adicional para la aguja.
No todos los tamaños de paquete deben estar disponibles en el mercado.
Título del responsable
Accord Healthcare Polska Sp. z o.o.
ul. Taśmowa 7
02-677 Varsovia
Tel: + 48 22 577 28 00
Fabricante
Accord Healthcare Polska Sp. z o.o.
ul. Lutomierska 50
95-200 Pabianice
Este medicamento está autorizado para su comercialización en los estados miembros del Espacio Económico Europeo y en el Reino Unido (Irlanda del Norte) bajo los siguientes nombres:
| País miembro | Nombre del producto |
| Austria | Injexate 50 mg/mL solución inyectable en jeringa precargada |
| Bélgica | Methofill 50 mg/ml solución para inyección en jeringa precargada |
| Bulgaria | Injexate 50 mg/mL solución para inyección en jeringa precargada |
| República Checa | INJEXATE 50 MG/ML solución inyectable en jeringa precargada |
| Chipre | Injexate 50 mg/mL solución para inyección en jeringa precargada |
| Dinamarca | Injexate |
| Finlandia | Injexate 50 mg/mL solución inyectable en jeringa precargada |
| Francia | INJEXATE 50 mg/mL solución inyectable en jeringa precargada |
| Alemania | Methofill 50 mg/ml solución para inyección en jeringa precargada |
| Grecia | Injexate 50mg/ml ενέσιμο διάλυμα σε προγεμισμένη σύριγγα |
| Hungría | METHOFILL 50 mg/ml oldatos injekció előretöltött fecskendőben |
| Islandia | Injexate |
| Irlanda | Methofill 50 mg/mL solución para inyección en jeringa precargada |
| Italia | Metother |
| Letonia | Injexate 50mg/ml injekcijas šķīstums iepriekš pildītā špricē |
| Lituania | Metother 50 mg/mL injekcinis tirpalas užpildytame švirkšte |
| Luxemburgo | Methofill 50mg/ml solution pour injection en seringue préremplie |
| Malta | Injexate |
| Países Bajos | Injexate 7.5 mg = 0.15 ml/10 mg = 0.20 ml/ 12.5 mg = 0.25 ml/15 mg = 0.30 ml/17.5 mg = 0.35 ml/20 mg = 0.40 ml/22.5 mg = 0.45 ml/25 mg = 0.50 ml/27.5 mg = 0.55 ml/30 mg = 0.60 ml solución para inyección en jeringa precargada |
| Polonia | Methofill |
| Portugal | Methofill 50mg/ml solução para injeção em seringa pré-cheia |
| Reino Unido | Methofill 50 mg/mL solución para inyección en jeringa precargada |
| Rumania | Injexate 50 mg/mL soluţie injectabilă în seringă preumplută |
| Eslovaquia | Injexate 50 mg/ml injekčný roztok v přednaplnenej injekčnej striekačke |
| Eslovenia | Methofill 50 mg/ml raztopina za injiciranje v napolnjeni injekcijski brizgi |
| España | Methofill 50 mg/ml solución para inyección en jeringa precargada |
| Suecia | Injexate 50 mg/mL injektionsvätska, lösning i förfylld spruta |
| Reino Unido | Methofill 7.5 mg/10 mg/12.5 mg/15 mg/17.5 mg/20 mg/22.5 mg/25 mg/27.5 mg/30 mg solución para inyección en jeringa precargada |
Fecha de la última revisión de la hoja de instrucciones: diciembre 2024
Instrucciones de uso
Antes de comenzar la inyección, lea atentamente las instrucciones a continuación y siempre siga la técnica de inyección recomendada por su médico, farmacéutico o enfermera.
Si tiene algún problema o pregunta, consulte a su médico, farmacéutico o enfermera.
Preparación
Elige una superficie de trabajo bien iluminada, limpia y plana.
Antes de comenzar, prepare los objetos necesarios:
- 1 jeringa precargada de Methofill con cubierta de seguridad para la aguja.
Lávese las manos. Antes de usar, inspeccione la jeringa de Methofill en busca de daños visibles (o grietas).
Los mejores lugares para la inyección incluyen:
- la parte superior del muslo,
- el abdomen, excepto la zona alrededor del ombligo.
- Si otra persona ayuda al paciente a realizar la inyección, también puede realizarla en la parte posterior del brazo, justo debajo del hombro.
- Cada vez que se administre una inyección, elige un lugar diferente. Este procedimiento ayuda a limitar el riesgo de irritación en el lugar de la inyección.
- Nunca inyecte el medicamento en un lugar doloroso, enrojecido, endurecido, con cicatrices o con estrías. En caso de psoriasis, no inyecte el medicamento directamente en áreas de piel elevadas, engrosadas, enrojecidas o con escamas.
- 1. Inyección de la solución
Saque la jeringa precargada de Methofill con cubierta de seguridad para la aguja que contiene metotrexato y lea atentamente la hoja de instrucciones.
Saque la jeringa precargada de la caja en temperatura ambiente.
- 2. Desinfección
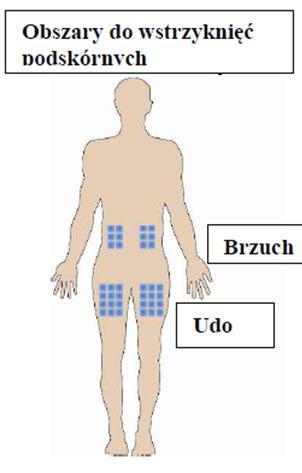

Elige el lugar de la inyección y desinfecte con una almohadilla empapada en alcohol.
Esperar al menos 60 segundos para que el desinfectante se seque.
- 3. Asegúrese de que el mecanismo de la jeringa precargada no esté dañado
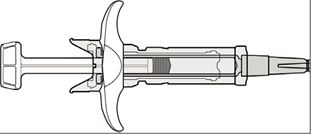
No use el producto:
- si hay daños visibles (la jeringa o la cubierta de seguridad para la aguja están rotas) o si faltan algunos componentes.
- si la cubierta de seguridad para la aguja está en la posición de seguridad antes de usar, como se muestra en la fig. 7, lo que indica que ya se ha usado. El producto no debe usarse si el aspecto de la jeringa precargada no coincide con la fig. 3. Si es así, el producto debe desecharse en un contenedor para objetos punzocortantes
- 4. Retire la cubierta de plástico protectora
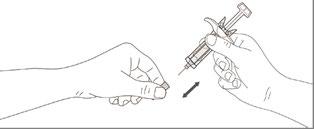
Sostenga la jeringa precargada por la cubierta de seguridad para la aguja con la aguja apuntando hacia afuera, sin tocar el émbolo.
Con la otra mano, retire la cubierta de la aguja y deseche en un contenedor para objetos punzocortantes.
- 5. Introducción de la aguja
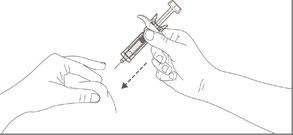
Sostenga suavemente la piel en el lugar de la inyección con una mano, con la otra mano, sin tocar el émbolo de la jeringa, introduzca la aguja en la piel (en un ángulo de 90 grados)
- 6. Inyección
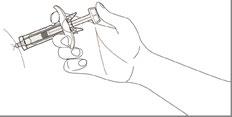
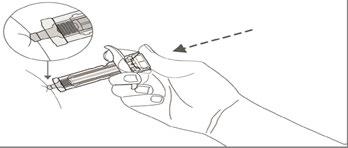
Con el pulgar, presione el émbolo y inyecte el contenido de la jeringa con un movimiento firme.
Mantenga la piel plegada hasta que termine la inyección.
- 7. Sistema de seguridad de la aguja
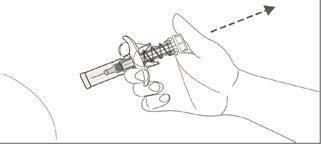
El sistema de seguridad se activa cuando el émbolo está completamente presionado.
Sostenga la jeringa firmemente y retire la presión del émbolo levantando suavemente el pulgar.
El émbolo se moverá hacia arriba con el pulgar y la aguja se cubrirá automáticamente con la cubierta de seguridad.
- 8. Retirar la cubierta de seguridad
Después de usar la jeringa, deseche la cubierta de seguridad de la aguja en un contenedor para objetos punzocortantes.
No la deseche en la basura común.
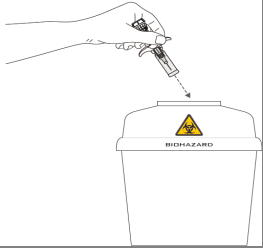
El metotrexato no debe entrar en contacto con la piel o las membranas mucosas.
En caso de contacto, el área afectada debe lavarse inmediatamente con abundante agua.
Eliminación y procedimiento
El procedimiento de eliminación y el manejo de la jeringa deben cumplir con los requisitos locales. El personal médico que esté embarazado no debe preparar ni administrar Methofill.
- País de registro
- Principio activo
- Requiere recetaSí
- ImportadorAccord Healthcare Polska Sp. z o.o.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a MetiofillForma farmacéutica: Solución, 20 mg/mlPrincipio activo: MetotrexatoRequiere recetaForma farmacéutica: Solución, 7.5 mgPrincipio activo: MetotrexatoRequiere recetaForma farmacéutica: Solución, 12.5 mgPrincipio activo: MetotrexatoRequiere receta
Alternativas a Metiofill en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Metiofill en Spain
Alternativa a Metiofill en Ukraine
Médicos online para Metiofill
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Metiofill – sujeta a valoración médica y normativa local.