
Immunate 1000 Iu Fviii/750 Iu Vvf

Consulta con un médico sobre la receta médica de Immunate 1000 Iu Fviii/750 Iu Vvf

Cómo usar Immunate 1000 Iu Fviii/750 Iu Vvf
Hoja de instrucciones para el paciente
Immunate 1000 UI de FVIII/ 750 UI de VWF polvo y disolvente para preparar una solución inyectable
Para inyección
Factor de coagulación humana VIII / factor de von Willebrand humano
Es importante leer detenidamente el folleto antes de tomar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar este folleto para poder volver a leerlo si es necesario.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento ha sido prescrito específicamente para usted. No lo debe dar a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos los efectos adversos no mencionados en este folleto, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice del folleto
- 1. Qué es Immunate 1000 UI de FVIII/ 750 UI de VWF y para qué se utiliza
- 2. Información importante antes de tomar Immunate 1000 UI de FVIII/ 750 UI de VWF
- 3. Cómo tomar Immunate 1000 UI de FVIII/ 750 UI de VWF
- 4. Posibles efectos adversos
- 5. Cómo conservar Immunate 1000 UI de FVIII/ 750 UI de VWF
- 6. Contenido del envase y otra información
1. Qué es Immunate 1000 UI de FVIII/ 750 UI de VWF y para qué se utiliza
Qué es Immunate 1000 UI de FVIII/ 750 UI de VWF
Immunate es un complejo de factor de coagulación VIII/factor de von Willebrand, producido a partir de plasma humano. El factor de coagulación VIII contenido en Immunate reemplaza el factor VIII que falta o no funciona correctamente en la hemofilia A. La hemofilia A es un trastorno hereditario de la coagulación de la sangre, causado por una disminución del nivel de factor VIII. Esto conduce a hemorragias graves en las articulaciones, músculos y órganos internos, que pueden ocurrir espontáneamente o como resultado de lesiones o cirugías. La administración de Immunate proporciona temporalmente el factor VIII que falta y reduce la tendencia a las hemorragias. Además de su acción como proteína protectora del factor VIII, el factor de von Willebrand (VWF) media en el proceso de adhesión de las plaquetas en el sitio de lesión del vaso y juega un papel en la agregación de las plaquetas.
Para qué se utiliza Immunate 1000 UI de FVIII/ 750 UI de VWF
Immunate se utiliza para el tratamiento y la prevención de hemorragias en la deficiencia congénita (hemofilia A) o adquirida del factor VIII. Immunate también se utiliza para el tratamiento de hemorragias en pacientes con enfermedad de von Willebrand con deficiencia de factor VIII, si no hay disponible ningún producto específico efectivo para la enfermedad de von Willebrand y cuando el tratamiento con desmopresina (DDAVP) es ineficaz o está contraindicado.
2. Información importante antes de tomar Immunate 1000 UI de FVIII/ 750 UI de VWF
Cuándo no debe tomarse el medicamento Immunate 1000 UI de FVIII/ 750 UI de VWF
- Si el paciente es alérgico al factor de coagulación humana VIII o a cualquiera de los demás componentes de este medicamento (enumerados en el punto 6). En caso de duda, consulte a su médico.
Advertencias y precauciones
En caso de reacciones alérgicas:
- Existe una pequeña probabilidad de que se produzca una reacción anafiláctica (reacción alérgica grave) con el medicamento Immunate. El paciente debe estar familiarizado con los primeros síntomas de las reacciones alérgicas, como enrojecimiento facial repentino, erupción, urticaria, ampollas, picazón generalizada, hinchazón de los labios, párpados y lengua, dificultad para respirar, respiración silbante, dolor en el pecho, sensación de opresión en el pecho, malestar general, mareos, taquicardia y presión arterial baja. Estos síntomas pueden ser los primeros signos de un shock anafiláctico, que también puede incluir mareos severos, pérdida de conciencia y dificultad para respirar severa.
- Si se producen alguno de estos síntomas, debe interrumpir inmediatamente la inyección/infusión y consultar a su médico. Los síntomas graves, incluida la dificultad para respirar y el casi desmayo, requieren tratamiento inmediato como en caso de emergencia.
Cuando se requiere monitoreo del tratamiento:
- Su médico puede ordenar pruebas para asegurarse de que la dosis actual es suficiente para lograr y mantener los niveles adecuados de factor VIII y factor de von Willebrand.
Si la hemorragia persiste:
- La formación de inhibidores (anticuerpos) es una complicación conocida que puede ocurrir durante el tratamiento con todos los medicamentos que contienen factor VIII. Estos inhibidores, especialmente a altas concentraciones, interrumpen el tratamiento efectivo y el paciente será monitoreado cuidadosamente para detectar la formación de estos inhibidores. Si la hemorragia del paciente no se controla adecuadamente con el medicamento Immunate, debe informar inmediatamente a su médico. Los pacientes con enfermedad de von Willebrand, especialmente los pacientes de tipo 3, pueden producir anticuerpos neutralizantes (inhibidores) contra el factor de von Willebrand. Su médico puede ordenar pruebas para confirmar su presencia. Los inhibidores contra el factor de von Willebrand son anticuerpos en la sangre que bloquean el factor de von Willebrand utilizado. Por lo tanto, el factor de von Willebrand es menos efectivo para controlar la hemorragia. En el caso de los medicamentos producidos a partir de sangre o plasma humano, se toman medidas preventivas para evitar la transmisión de infecciones a los pacientes. Estas medidas incluyen la selección cuidadosa de los donantes de sangre y plasma para asegurarse de que se excluyan las personas con riesgo de ser portadoras de infecciones, la prueba de cada lote de sangre donada y plasma para detectar virus/infecciones y la inclusión en el proceso de elaboración de la sangre o plasma de procedimientos que inactivan o eliminan los virus. A pesar de la implementación de estas medidas, no se puede excluir completamente la posibilidad de transmisión de infecciones con los medicamentos derivados de la sangre o plasma humano. Esto también se aplica a los virus desconocidos o recientemente descubiertos y otros tipos de infecciones.
Las medidas utilizadas se consideran efectivas contra los virus con envoltura, como el virus de la inmunodeficiencia humana (VIH), el virus de la hepatitis B y C, y el virus de la hepatitis A sin envoltura. Las medidas utilizadas pueden tener una eficacia limitada contra los virus sin envoltura, como el parvovirus B19. La infección por parvovirus B19 puede tener consecuencias graves para las mujeres embarazadas (infección del feto) y los pacientes con deficiencias del sistema inmunológico o con ciertos tipos de anemia (por ejemplo, esferocitosis congénita o anemia hemolítica). En el caso de la administración regular o repetida de productos que contienen factor VIII derivados del plasma humano, su médico puede recomendar la vacunación contra la hepatitis A y B. Es especialmente recomendable que, en cada administración de una dosis de Immunate, se anote el nombre y el número de lote del producto en el registro del paciente. Immunate contiene isoaglutininas de grupos sanguíneos (anti-A y anti-B). En los pacientes con grupo sanguíneo A, B o AB, puede ocurrir hemólisis debido a la administración repetida en un corto período de tiempo o a la administración de dosis muy altas.
Niños
El producto debe utilizarse con precaución en niños menores de 6 años que han estado expuestos de manera limitada a productos que contienen factor VIII, ya que los datos clínicos sobre este grupo de pacientes son limitados.
Immunate 1000 UI de FVIII/ 750 UI de VWF y otros medicamentos
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando actualmente o recientemente, así como sobre los medicamentos que planea tomar. No se han reportado interacciones del medicamento Immunate con otros medicamentos. No debe mezclar el medicamento Immunate con otros medicamentos o disolventes antes de la administración, excepto con el agua para inyección suministrada, ya que podrían afectar negativamente la eficacia y seguridad del producto. Se recomienda enjuagar el acceso venoso con una solución adecuada, como una solución salina, antes y después de la inyección de Immunate.
Immunate 1000 UI de FVIII/ 750 UI de VWF con alimentos y bebidas
No hay recomendaciones especiales sobre la administración de Immunate en relación con las comidas.
Embarazo, lactancia y fertilidad
Como la hemofilia A es rara en mujeres, no hay experiencia sobre el uso de Immunate durante el embarazo, la lactancia y la fertilidad. Immunate debe utilizarse durante el embarazo y la lactancia solo si es absolutamente necesario. Si la paciente está embarazada o en período de lactancia, cree que puede estar embarazada o planea tener un hijo, debe consultar a su médico o farmacéutico antes de tomar este medicamento.
Conducción de vehículos y uso de maquinaria
No hay información sobre el efecto de Immunate en la capacidad para conducir vehículos o operar maquinaria.
Immunate 1000 UI de FVIII/ 750 UI de VWF contiene sodio
El medicamento contiene 19,6 mg de sodio (principal componente de la sal común) en cada vial. Esto corresponde al 1% de la dosis máxima recomendada de sodio en la dieta para adultos.
3. Cómo tomar Immunate 1000 UI de FVIII/ 750 UI de VWF
El tratamiento debe realizarse bajo la supervisión de un médico con experiencia en el tratamiento de trastornos de la hemostasia.
Este medicamento siempre debe tomarse según las indicaciones de su médico. En caso de duda, consulte a su médico.
Dosis para la prevención de hemorragias
Si el medicamento Immunate se utiliza para prevenir hemorragias, la dosis será calculada por su médico. Esto se hará teniendo en cuenta las necesidades individuales del paciente. La dosis habitual es de 20 a 40 UI de factor VIII por kilogramo de peso corporal, administrada en intervalos de 2 a 3 días. Sin embargo, en algunos casos, especialmente en pacientes más jóvenes, pueden ser necesarios intervalos más cortos entre dosis o dosis más altas. Si el paciente siente que el efecto del medicamento Immunate es demasiado débil, debe consultar a su médico.
Dosis para el tratamiento de hemorragias
Si el medicamento Immunate se utiliza para tratar hemorragias, la dosis será calculada por su médico. Esto se hará teniendo en cuenta las necesidades individuales del paciente. Si el paciente siente que el efecto del medicamento Immunate es demasiado débil, debe consultar a su médico.
Monitoreo del tratamiento por el médico
Para asegurarse de que los niveles de factor VIII sean suficientes, su médico realizará las pruebas de laboratorio adecuadas. Esto es especialmente importante en caso de cirugías importantes.
Dosis en la enfermedad de von Willebrand
Su médico controlará las hemorragias de acuerdo con las pautas para la hemofilia A.
Vía y/o método de administración
El medicamento Immunate se administra por vía intravenosa después de preparar la solución con el disolvente suministrado. Debe seguir estrictamente las indicaciones de su médico. Para reconstituir el producto, solo debe utilizarse el kit de administración suministrado con el envase, ya que la adsorción del factor de coagulación humano VIII en las superficies internas de algunos kits de infusión puede provocar el fracaso del tratamiento. El medicamento Immunate debe reconstituirse justo antes de la administración. La solución debe utilizarse de inmediato, ya que no contiene conservantes.
Reconstitución del polvo para preparar la solución inyectable Utilice técnica aséptica
- 1. Caliente el frasco cerrado que contiene el disolvente (agua para inyección) a temperatura ambiente (hasta 37°C).
- 2. Retire las tapas protectoras de los frascos que contienen el polvo y el disolvente (figura A) y limpie los tapones de goma de ambos frascos.
- 3. Coloque el extremo ondulado del kit de transferencia en el frasco del disolvente y presione (figura B).
- 4. Retire la cubierta protectora del otro extremo del kit de transferencia, teniendo cuidado de no tocar el extremo expuesto.
- 5. Invierta el kit de transferencia con el frasco del disolvente conectado sobre el frasco que contiene el polvo y inserte la aguja libre a través del tapón de goma del frasco que contiene el polvo (figura C). El disolvente será succionado por el vacío en el frasco que contiene el polvo.
- 6. Después de aproximadamente un minuto, separe los frascos retirando el kit de transferencia con el frasco del disolvente del frasco que contiene el polvo (figura D). Como la reconstitución es fácil, no agite enérgicamente el frasco que contiene el concentrado. NO AGITE EL CONTENIDO DEL FRASCO. NO INVIERTA EL FRASCO QUE CONTIENE EL POLVO HASTA QUE ESTÉ LISTO PARA TRANSFERIR EL CONTENIDO.
- 7. Después de la reconstitución, antes de la administración, verifique la solución preparada para detectar la presencia de partículas no disueltas y cambios de color. La solución debe ser clara o ligeramente opalescente. Sin embargo, incluso si se sigue el procedimiento de reconstitución, a veces se puede observar una pequeña cantidad de partículas finas. El kit de filtración suministrado eliminará las partículas, y la potencia del medicamento indicada en el envase no se reducirá. La solución que es turbia o contiene sedimento debe ser descartada. No vuelva a colocar en el refrigerador la solución preparada para su uso.
Administración Utilice técnica aséptica
Utilice el kit de filtración suministrado para evitar la administración de partículas de goma procedentes del tapón (riesgo de microembolia). Para extraer el producto reconstituido, coloque el kit de filtración en la jeringa de un solo uso y introdúzcala a través del tapón de goma (figura E). Desconecte la jeringa del kit de filtración durante un momento. El aire entrará en el frasco que contiene el polvo, y cualquier espuma que se encuentre dentro se asentará. A través del kit de filtración (figura F), extraiga la solución en la jeringa. Desconecte la jeringa del kit de filtración y administre lentamente la solución por vía intravenosa (velocidad máxima de inyección: 2 ml por minuto) utilizando el kit de infusión suministrado - aguja alada (o la aguja de un solo uso suministrada).
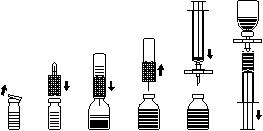
Figura A
Figura B
Figura C
Figura D
Figura E
Figura F
Cualquier residuo no utilizado del producto o sus desechos debe eliminarse de acuerdo con las regulaciones locales. La administración de Immunate debe documentarse, y el número de lote debe registrarse. Con cada frasco se suministra una etiqueta adhesiva que se adjunta a la documentación.
Frecuencia de administración
Su médico le informará con qué frecuencia y en qué intervalos de tiempo debe tomar el medicamento Immunate. Esto se determinará según la eficacia del tratamiento en cada paciente individual.
Duración del tratamiento
Por lo general, el tratamiento sustitutivo con el medicamento Immunate se utiliza durante toda la vida.
Uso de una dosis mayor que la recomendada de Immunate 1000 UI de FVIII/ 750 UI de VWF
- No se han reportado síntomas de sobredosis de factor de coagulación VIII. En caso de duda, consulte a su médico.
- Pueden ocurrir incidentes tromboembólicos.
- Puede ocurrir hemólisis en pacientes con grupo sanguíneo A, B o AB.
Omision de la administración de Immunate 1000 UI de FVIII/ 750 UI de VWF:
- No debe tomar una dosis doble para compensar una dosis omitida.
- Debe tomar la siguiente dosis habitual y continuar el tratamiento en los intervalos de tiempo recomendados por su médico.
Interrupción del tratamiento con Immunate 1000 UI de FVIII/ 750 UI de VWF:
No debe decidir interrumpir el tratamiento con Immunate sin consultar a su médico. En caso de cualquier otra pregunta relacionada con el uso de este medicamento, consulte a su médico.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Efectos adversos graves que pueden ocurrir con los productos que contienen factor VIII derivados del plasma humano
Factor VIII
Raramente se han observado reacciones alérgicas, que en algunos casos han llevado a reacciones graves y potencialmente mortales (anafilaxia). Por lo tanto, es importante familiarizarse con los primeros síntomas de las reacciones alérgicas, como enrojecimiento facial repentino, erupción, urticaria, ampollas, picazón generalizada, hinchazón de los labios y la lengua, dificultad para respirar, respiración silbante, dolor en el pecho, sensación de opresión en el pecho, malestar general, mareos, taquicardia y presión arterial baja. Estos síntomas pueden ser los primeros signos de un shock anafiláctico. En caso de cualquier reacción alérgica o anafiláctica, debe interrumpir inmediatamente la inyección/infusión y notificar a su médico. Los síntomas graves requieren tratamiento inmediato como en caso de emergencia. En niños no tratados previamente con medicamentos que contienen factor VIII, los anticuerpos bloqueantes (ver punto 2) pueden producirse con mucha frecuencia (más de 1 de cada 10 pacientes). Sin embargo, en pacientes que han sido tratados previamente con factor VIII (tratamiento durante más de 150 días), el riesgo es poco frecuente (menos de 1 de cada 100 pacientes). Si esto ocurre, los medicamentos del paciente pueden dejar de funcionar correctamente y el paciente puede experimentar hemorragias persistentes. Si esto ocurre, debe contactar inmediatamente a su médico. La formación de anticuerpos neutralizantes contra el factor de von Willebrand es una complicación conocida del tratamiento de pacientes con enfermedad de von Willebrand. Si se producen anticuerpos neutralizantes (inhibidores), puede manifestarse como un resultado clínico insuficiente del tratamiento (la hemorragia no se controla con la dosis adecuada) o como una reacción alérgica. En estos casos, se recomienda contactar a un centro especializado en el tratamiento de la hemofilia. Después de la administración de dosis altas, puede ocurrir hemólisis en pacientes con grupo sanguíneo A, B o AB.
Efectos adversos reportados con el uso de Immunate Muy frecuentes (pueden ocurrir en más de 1 de cada 10 pacientes)
- inhibición del factor VIII (en niños que no han sido tratados previamente con medicamentos que contienen factor VIII). Poco frecuentes (pueden ocurrir en menos de 1 de cada 100 pacientes)
- hipersensibilidad;
- inhibición del factor VIII [en pacientes que han sido tratados previamente con factor VIII (tratamiento durante más de 150 días)]. Frecuencia desconocida (la frecuencia no puede determinarse a partir de los datos disponibles)
- trastornos de la coagulación (incapacidad para formar coágulos);
- ansiedad;
- parestesia (sensación de hormigueo o picazón);
- mareos;
- dolor de cabeza;
- conjuntivitis;
- taquicardia (frecuencia cardíaca acelerada);
- palpitaciones;
- hipotensión (presión arterial baja);
- enrojecimiento facial repentino;
- palidez (apariencia pálida);
- dificultad para respirar;
- tos;
- vómitos;
- náuseas;
- urticaria (erupción urticaria en todo el cuerpo);
- erupción;
- picazón (sensación de picazón);
- rubor (enrojecimiento de la piel);
- transpiración excesiva;
- dermatitis atópica (piel sensible o áspera);
- dolor muscular;
- dolor en el pecho;
- sensación de malestar en el pecho;
- edema (retención de líquidos);
- fiebre;
- escalofríos;
- picazón y hormigueo en el lugar de la inyección (reacciones en el lugar de la inyección);
- dolor.
Notificación de efectos adversos
Si ocurren cualquier efecto adverso, incluidos los efectos adversos no mencionados en este folleto, debe informar a su médico o farmacéutico. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Efectos Adversos de Medicamentos del Ministerio de Sanidad. Los efectos adversos también pueden notificarse al titular de la autorización de comercialización. Al notificar los efectos adversos, se puede recopilar más información sobre la seguridad del medicamento.
5. Cómo conservar Immunate 1000 UI de FVIII/ 750 UI de VWF
Conservar en un lugar fuera del alcance de los niños. Conservar y transportar en condiciones refrigeradas (2°C – 8°C). No congelar. Conservar en el envase original para proteger del luz. No utilizar este medicamento después de la fecha de caducidad indicada en el envase y el embalaje después de EXP. La fecha de caducidad es el último día del mes indicado. Durante el período de validez, el producto puede conservarse a temperatura ambiente (hasta 25°C) durante un período no superior a 6 meses. Debe anotar en el envase del producto el momento en que comienza a conservarlo a temperatura ambiente. Después de la conservación a temperatura ambiente, no debe volver a colocar el medicamento Immunate en el refrigerador, sino que debe usarlo o desecharlo de inmediato. No utilice este medicamento si, después de la reconstitución, la solución es turbia o contiene sedimento. Los medicamentos no deben desecharse por el desagüe ni en los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del envase y otra información
Qué contiene Immunate 1000 UI de FVIII/ 750 UI de VWF
Polvo:
- Los principios activos del medicamento son el factor de coagulación humana VIII y el factor de von Willebrand humano. Cada frasco contiene nominalmente 1000 UI de factor VIII y 750 UI de factor de von Willebrand obtenidos a partir de plasma humano. Después de la reconstitución en el disolvente suministrado, el producto contiene aproximadamente 100 UI/ml de factor VIII de plasma humano y 75 UI/ml de factor de von Willebrand de plasma humano.
- Los demás componentes son albúmina humana, glicina, cloruro de sodio, citrato de sodio, clorhidrato de lisina y cloruro de calcio.
Disolvente:
- Agua para inyección
Cómo se presenta Immunate 1000 UI de FVIII/ 750 UI de VWF y qué contiene el envase
Polvo y disolvente para preparar una solución inyectable. Polvo blanco o amarillento claro o masa cristalina seca. El polvo y el disolvente están disponibles en frascos de un solo uso de vidrio, Ph. Eur. (polvo: vidrio tipo II; disolvente: vidrio tipo I), cerrados con tapones de goma de butilo, Ph. Eur. Cada envase contiene: 1 frasco de Immunate 1000 UI de FVIII/ 750 UI de VWF, 1 frasco con agua para inyección (10 ml), 1 kit de transferencia o filtración, 1 jeringa de un solo uso (10 ml), 1 aguja de un solo uso, 1 kit de infusión (aguya alada). Tamaño del envase: 1 x 1000 UI de FVIII/ 750 UI de VWF
Título del responsable y fabricante
Responsable
Takeda Pharma Sp. z o.o. ul. Prosta 68, 00-838 Varsovia
Fabricante
Takeda Manufacturing Austria AG, Industriestrasse 67, 1221 Viena, Austria
Este medicamento está autorizado para su comercialización en los países miembros del Espacio Económico Europeo bajo los siguientes nombres:
Immunate:
Austria, Bulgaria, Chipre, Estonia, Finlandia, Alemania, Letonia, Lituania, Malta, Polonia, Portugal, Rumania, Eslovaquia, Eslovenia, Suecia. Immunate Stim Plus: República Checa. Immunate S/D: Hungría. Talate: Italia. Fecha de la última actualización del folleto:12/2021
Otras fuentes de información
Información destinada exclusivamente al personal médico especializado: Dosis en hemofilia ALa dosis y la duración del tratamiento sustitutivo dependen del grado de deficiencia del factor VIII, la ubicación y la gravedad de la hemorragia, así como del estado clínico del paciente. La dosis de factor VIII administrada se expresa en unidades internacionales (UI), referidas al estándar actual de la OMS para los productos que contienen factor VIII. La actividad del factor VIII en el suero se expresa como porcentaje (en relación con el suero humano normal) o en UI (en relación con el Estándar Internacional para el factor VIII en suero). Una unidad internacional (UI) de actividad del factor VIII es la cantidad de factor VIII en un mililitro de suero humano normal. El cálculo de la dosis necesaria de factor VIII se basa en la observación empírica de que 1 UI de factor VIII por kilogramo de peso corporal aumenta la actividad del factor VIII en suero en aproximadamente un 2% de la actividad normal. La dosis necesaria se calcula según la siguiente fórmula:
Dosis necesaria = peso corporal (kg) x aumento deseado del factor VIII (%) x 0,5
La cantidad administrada, así como la frecuencia de administración, deben basarse siempre en la eficacia clínica en cada caso individual. Hemorragias y cirugíasEn el caso de los siguientes tipos de hemorragias, la actividad del factor VIII en el momento adecuado no debe caer por debajo del nivel de actividad en suero indicado (en % de la normal o UI/dl). Al determinar la dosis en función del tipo de hemorragia y la cirugía, se puede utilizar la siguiente tabla:
| Gravedad de la hemorragia / tipo de cirugía | Nivel de factor VIII requerido (en % de la normalidad) (UI/dl) | Frecuencia de dosificación (horas) / duración del tratamiento (días) |
| Hemorragia leve Hemorragia temprana en las articulaciones, músculos o hemorragia oral Hemorragia más grave en las articulaciones, músculos o hematoma Hemorragias que ponen en peligro la vida | 20–40 30–60 60–100 | Repetir cada 12–24 horas. Al menos 1 día, hasta que la hemorragia se resuelva según la evaluación del dolor o hasta que la herida se cierre. Repetir las infusiones cada 12–24 horas durante 3–4 días o más, hasta que el dolor se resuelva y se restaure la función. Repetir las infusiones cada 8–24 horas, hasta que el peligro haya pasado. |
| Cirugías menores, incluida la extracción de dientes Cirugías mayores | 30–60 80–100 (pre y postoperatorio) | Cada 24 horas, al menos durante 1 día, hasta que la herida se cierre. Repetir las infusiones cada 8–24 horas, hasta lograr una cicatrización adecuada de la herida, luego continuar el tratamiento durante al menos 7 días más para mantener la actividad del factor VIII en un nivel de 30–60% (UI/dl). |
En ciertas circunstancias (por ejemplo, en presencia de un título bajo de inhibidor), pueden ser necesarias dosis más altas que las calculadas con la fórmula. Profílaxis a largo plazoEn la profilaxis a largo plazo de hemorragias en pacientes con hemofilia A grave, las dosis habituales de factor VIII son de 20 a 40 UI por kilogramo de peso corporal, administradas en intervalos de 2 a 3 días. En algunos casos, especialmente en pacientes más jóvenes, pueden ser necesarios intervalos más cortos entre dosis o dosis más altas. Dosis en la enfermedad de von WillebrandEl tratamiento sustitutivo con Immunate para controlar las hemorragias se basa en las pautas para la hemofilia A. Immunate contiene una cantidad relativamente alta de factor VIII en relación con el contenido de factor de von Willebrand, por lo que el médico que lo administra debe ser consciente de que la continuación del tratamiento puede provocar un aumento excesivo de FVIII:C, lo que puede aumentar el riesgo de incidentes tromboembólicos. Niños y adolescentesEl producto debe utilizarse con precaución en niños menores de 6 años que han estado expuestos de manera limitada a productos que contienen factor VIII, ya que los datos sobre este grupo de pacientes son limitados. La dosis en la hemofilia A en niños y adolescentes menores de 18 años se determina según el peso corporal y, por lo tanto, generalmente se basa en las mismas pautas que para los pacientes adultos. La dosis y la frecuencia de administración deben basarse siempre en la eficacia clínica en cada caso individual (ver punto 4.4). En algunos casos, especialmente en pacientes más jóvenes, pueden ser necesarios intervalos más cortos entre dosis o dosis más altas.
- País de registro
- Principio activo
- Requiere recetaNo
- Fabricante
- ImportadorTakeda Manufacturing Austria AG
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a Immunate 1000 Iu Fviii/750 Iu VvfForma farmacéutica: Polvo, 1000 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere recetaForma farmacéutica: Polvo, 2000 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere recetaForma farmacéutica: Polvo, 250 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere receta
Alternativas a Immunate 1000 Iu Fviii/750 Iu Vvf en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Immunate 1000 Iu Fviii/750 Iu Vvf en Spain
Alternativa a Immunate 1000 Iu Fviii/750 Iu Vvf en Ukraine
Médicos online para Immunate 1000 Iu Fviii/750 Iu Vvf
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Immunate 1000 Iu Fviii/750 Iu Vvf – sujeta a valoración médica y normativa local.














