
Iaemoctin 500

Consulta con un médico sobre la receta médica de Iaemoctin 500

Cómo usar Iaemoctin 500
Hoja de instrucciones del paquete: información para el usuario
Haemoctin 250
Haemoctin 500
Haemoctin 1000
Polvo y disolvente para la preparación de una solución para inyección
Factor de coagulación sanguínea VIII humano
Es importante leer atentamente el contenido de esta hoja de instrucciones antes de usar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a su médico, farmacéutico o enfermera.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si sus síntomas son los mismos que los suyos.
- Si el paciente experimenta algún efecto adverso, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es Haemoctin y para qué se utiliza
- 2. Información importante antes de usar Haemoctin
- 3. Cómo usar Haemoctin
- 4. Posibles efectos adversos
- 5. Cómo conservar Haemoctin
- 6. Contenido del paquete y otra información
1. Qué es Haemoctin y para qué se utiliza
Haemoctin es un medicamento producido a partir de plasma humano. Contiene factor de coagulación VIII necesario para el proceso de coagulación sanguínea normal. Después de disolver el polvo en agua para inyección, la solución está lista para ser inyectada en una vena.
Haemoctin se utiliza para el tratamiento y la prevención de hemorragias en pacientes con hemofilia A (deficiencia congénita de factor VIII).
Haemoctin no contiene factor de von Willebrand en cantidades farmacológicamente efectivas, por lo que no está indicado para el tratamiento de la enfermedad de von Willebrand.
2. Información importante antes de usar Haemoctin
Cuándo no usar Haemoctin
- si el paciente es alérgico al principio activo o a alguno de los demás componentes de este medicamento (enumerados en el punto 6). La reacción alérgica puede incluir erupción, picazón, dificultad para respirar o hinchazón de la cara, los labios, la garganta o la lengua.
Precauciones y advertencias
La formación de inhibidores (anticuerpos) es una complicación conocida que puede ocurrir durante el tratamiento con todos los medicamentos que contienen factor VIII. Estos inhibidores, especialmente a altas concentraciones, interrumpen el tratamiento efectivo y el paciente será monitoreado de cerca para detectar la formación de estos inhibidores. Si la hemorragia en el paciente no se controla adecuadamente con Haemoctin, debe informar a su médico de inmediato.
Si el paciente tiene factores de riesgo preexistentes para enfermedades cardiovasculares, el tratamiento con Haemoctin puede aumentar el riesgo cardiovascular. En caso de duda, debe discutirlo con su médico.
Complicaciones relacionadas con la inserción de un catéter venoso: si se requiere un dispositivo de acceso venoso central (CVAD), debe considerar el riesgo de complicaciones relacionadas con el CVAD, incluyendo infecciones locales, bacteriemia y trombosis en el sitio de inserción del catéter.
Seguridad virológica
Cuando los productos medicinales se producen a partir de sangre o plasma humano, se toman medidas para prevenir la transmisión de infecciones a los pacientes. Estas medidas incluyen:
- selección cuidadosa de donantes de sangre y plasma para garantizar la exclusión de donantes que puedan ser portadores de infecciones,
- pruebas de todas las muestras y pools de plasma para detectar la presencia de virus/infecciones,
- incorporación de etapas de inactivación o eliminación de virus en el proceso de tratamiento de la sangre o el plasma. A pesar de estas medidas, en el caso de la administración de medicamentos preparados a partir de sangre o plasma humano, no se puede excluir completamente la posibilidad de transmisión de infección. Esto también se aplica a virus desconocidos o recientemente descubiertos u otros tipos de infecciones.
Las medidas tomadas se consideran efectivas contra los virus con envoltura, como el virus de la inmunodeficiencia humana (VIH), el virus de la hepatitis B y el virus de la hepatitis C, así como contra el virus de la hepatitis A sin envoltura. Las medidas tomadas pueden tener una eficacia limitada contra los virus sin envoltura, como el parvovirus B19. La infección por parvovirus B19 puede ser grave para las mujeres embarazadas (infección fetal) y para personas con sistemas inmunitarios debilitados o con ciertos tipos de anemia (por ejemplo, anemia falciforme o hemolítica).
Su médico puede recomendar que el paciente considere la vacunación contra el virus de la hepatitis A y B, si el paciente recibe regularmente productos que contienen factor VIII producido a partir de plasma humano.
Se recomienda encarecidamente que en cada caso de administración de una dosis de Haemoctin se registre el nombre y el número de lote del medicamento, para poder determinar las series de medicamento utilizadas en el futuro.
Niños y adolescentes
Las precauciones y advertencias para el uso en adultos también deben ser consideradas para los niños y adolescentes.
Haemoctin y otros medicamentos
Debe informar a su médico sobre todos los medicamentos que esté tomando actualmente o recientemente, así como sobre los medicamentos que planea tomar.
No se han notificado interacciones entre Haemoctin y otros productos medicinales.
Embarazo, lactancia y fertilidad
Si la paciente está embarazada o en período de lactancia, o si sospecha que puede estar embarazada o planea tener un hijo, debe consultar a su médico antes de usar este medicamento.
Debido a la rareza de la hemofilia A en mujeres, no hay experiencia disponible sobre el uso de factor VIII durante el embarazo o la lactancia. No se han realizado estudios en animales durante el embarazo y la lactancia.
Conducción de vehículos y uso de máquinas
Haemoctin no tiene efecto o tiene un efecto insignificante en la capacidad para conducir vehículos o usar máquinas.
Haemoctin contiene sodio
Haemoctin 250 contiene como máximo 16,1 mg (0,70 mmol) de sodio (principal componente de la sal común) en cada vial. Esto equivale al 0,81% de la ingesta diaria máxima recomendada de sodio en la dieta para adultos.
Haemoctin 500/1000 contiene como máximo 32,2 mg (1,40 mmol) de sodio (principal componente de la sal común) en cada vial. Esto equivale al 1,61% de la ingesta diaria máxima recomendada de sodio en la dieta para adultos.
3. Cómo usar Haemoctin
Haemoctin está indicado para administración intravenosa (inyección en una vena). El tratamiento debe estar bajo la supervisión de un médico con experiencia en el tratamiento de la hemofilia A. Haemoctin siempre debe usarse según las indicaciones de su médico. En caso de duda, debe volver a consultar a su médico.
La dosis y la duración del tratamiento dependen del grado de deficiencia de factor VIII, de la ubicación y la extensión de la hemorragia, así como del estado clínico del paciente. Su médico determinará la dosis adecuada para usted.
Debe garantizar condiciones estériles durante todos los pasos del procedimiento.
Fig. 1a
Fig. 1b
Fig. 1c
Fig. 2
Fig. 3
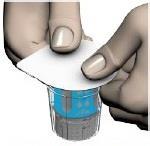

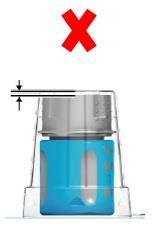


Fig. 4
Fig. 5
Fig. 6
Fig. 7
Fig. 8





Reconstitución del concentrado:
- Llevar el disolvente (agua para inyección) y el producto a temperatura ambiente en los viales no abiertos. Si se utiliza un baño de agua para calentar, tenga mucho cuidado de no permitir que el agua entre en contacto con las tapas o los tapones de los viales. De lo contrario, puede ocurrir contaminación del medicamento.
- Muy importantepara el uso correcto del sistema de transferencia: antes de abrir, asegúrese de que la parte inferior blanca del sistema de transferencia esté colocada directamente en la base de la caja de blister (fig. 1a: bien / fig. 1b: mal). Si está mal: presione el sistema de transferencia hacia abajo en la caja de blister hasta que la parte inferior blanca del sistema de transferencia esté colocada directamente en la base de la caja de blister (fig. 1c).
- Retire las tapas de los viales del disolvente y del producto, para exponer las partes centrales de los tapones de goma (fig. 2). Limpie los tapones de goma de los viales del producto y del disolvente con un desinfectante.
- Retire la parte superior de la cubierta del sistema de transferencia (fig. 3).
- Coloque el vial del disolvente en una superficie plana. Coloque la parte azul del sistema de transferencia en la caja de blister directamente sobre el vial del disolvente en posición vertical (fig. 4). No gire el sistema de transferencia.
- Retire el resto de la cubierta del sistema de transferencia. No apriete la cubierta. Ahora se expone la parte blanca del sistema de transferencia (fig. 5).
- Coloque el vial del producto en una superficie plana.
- Gire el sistema de transferencia unido y el vial del disolvente hacia abajo. Inserte la aguja de la parte blanca del adaptador hacia abajo a través del tapón del vial del producto (fig. 6). El vacío en el vial del producto hace que el disolvente entre en el vial del producto.
- Un movimiento de balanceo suave del vial del producto ayuda a disolver el polvo. No agite enérgicamente, evite la formación de espuma. La solución es transparente o ligeramente opalescente.
- Luego, gire la parte azul del sistema de transferencia junto con el vial del disolvente en el sentido contrario a las agujas del reloj (fig. 7). Deseche el vial del disolvente con la parte azul del sistema de transferencia unida. Ahora se ve la conexión de bloqueo de luer.
La solución reconstituida debe usarse inmediatamente después de la reconstitución. No use soluciones que estén turbias o contengan partículas sólidas.
Administración:
- Después de reconstituir el polvo como se describe anteriormente, conecte la jeringa proporcionada a la conexión de bloqueo de luer del vial del producto con la parte blanca del sistema de transferencia (fig. 8). Esto permitirá una fácil aspiración de la solución reconstituida a la jeringa. No se requiere un filtro separado, ya que el sistema de transferencia está equipado con un filtro integrado.
- Con cuidado, separe el vial con la parte blanca del sistema de transferencia de la jeringa. Inyecte lentamente el producto por vía intravenosa utilizando la aguja de ala de mariposa proporcionada. Se recomienda no administrar más de 2-3 ml/minuto.
- Después de usar la aguja de ala de mariposa, puede cubrirla con una cubierta de protección.
Uso de una dosis mayor de la recomendada de Haemoctin
Si el paciente cree que ha recibido una dosis demasiado grande de Haemoctin, debe consultar a su médico, quien tomará la decisión sobre el tratamiento posterior.
Omisión de la administración de Haemoctin
En tal caso, el médico decidirá si es necesario continuar con el tratamiento.
Interrupción del tratamiento con Haemoctin
No debe interrumpir el tratamiento con Haemoctin sin consultar a su médico.
En caso de dudas adicionales sobre el uso de este medicamento, debe consultar a su médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
En caso de observar alguno de los siguientes síntomas, debe informar a su médico de inmediato:
- enrojecimiento de la piel,
- sensación de ardor y picazón en el lugar de la inyección,
- escalofríos,
- enrojecimiento repentino de la cara,
- dolor de cabeza,
- urticaria,
- hipotensión,
- letargo,
- náuseas,
- inquietud motora,
- taquicardia,
- opresión en el pecho,
- entumecimiento,
- vómitos,
- respiración sibilante. Esto puede ser una reacción alérgica o una reacción alérgica grave (anafilaxia) o una reacción de hipersensibilidad.
Los siguientes efectos adversos se han observado con el uso de Haemoctin
Frecuencia desconocida: no puede establecerse a partir de los datos disponibles
- anafilaxia (choque), reacción alérgica
- enrojecimiento de la piel, picazón, urticaria
En niños no tratados previamente con medicamentos que contienen factor VIII, los anticuerpos bloqueantes (ver punto 2) pueden ocurrir muy frecuentemente (más de 1 de cada 10 pacientes). Sin embargo, en pacientes que han sido tratados previamente con factor VIII (más de 150 días de tratamiento), el riesgo es poco frecuente (menos de 1 de cada 100 pacientes). Si esto ocurre, los medicamentos del paciente pueden dejar de funcionar correctamente y el paciente puede experimentar una hemorragia persistente. Si esto ocurre, debe informar a su médico de inmediato.
Efectos adversos en niños y adolescentes
Con la excepción de la formación de inhibidores (anticuerpos), se prevé que los efectos adversos en niños sean los mismos que en adultos.
Notificación de efectos adversos
Si ocurren algún efecto adverso, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad y Consumo
Calle de Alcalá, 56
28071 Madrid
Teléfono: +34 91 596 34 00
Fax: +34 91 596 34 01
Sitio web: https://www.aemps.gob.es/
Los efectos adversos también pueden notificarse al titular de la autorización de comercialización.
La notificación de efectos adversos permite recopilar más información sobre la seguridad del medicamento.
5. Cómo conservar Haemoctin
Debe conservar el medicamento en un lugar donde no pueda ser visto o alcanzado por los niños.
Debe conservar los viales en el paquete exterior para protegerlos de la luz.
No debe conservar a una temperatura superior a 25°C. No congelar.
No debe usar este medicamento después de la fecha de caducidad que figura en el etiquetado del vial y el paquete exterior después de: Fecha de caducidad.
Debe eliminar cualquier resto de producto no utilizado o sus residuos de acuerdo con las regulaciones locales. No debe tirar los medicamentos por el desagüe ni por los contenedores de basura domésticos.
Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Haemoctin?
- El principio activo del medicamento es: factor de coagulación sanguínea VIII humano.
- Los demás componentes son: glicina, cloruro de sodio, citrato de sodio y cloruro de calcio.
- El vial del disolvente contiene agua para inyección.
Cómo se presenta Haemoctin y qué contiene el paquete?
Haemoctin se presenta en forma de polvo liofilizado (liofilizado). El agua para inyección se utiliza como disolvente. La solución reconstituida es transparente o ligeramente opalescente.
Haemoctin 250 contiene 1 vial con 250 UI y 1 vial con 5 ml de agua para inyección (50 UI/ml)
Haemoctin 500 contiene 1 vial con 500 UI y 1 vial con 5 ml de agua para inyección (100 UI/ml)
Haemoctin 1000 contiene 1 vial con 1000 UI y 1 vial con 5 ml de agua para inyección (200 UI/ml)
Cada paquete contiene
- 1 jeringa de un solo uso
- 1 sistema de transferencia con filtro integrado
- 1 aguja de ala de mariposa
Titular de la autorización de comercialización y fabricante:
Biotest Pharma GmbH
Landsteinerstrasse 5
63303 Dreieich
Alemania
Teléfono: +49 6103 801-0
Fax: +49 6103 801-150
Correo electrónico: [email protected]
Fecha de la última actualización de la hoja de instrucciones: 12/2022.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorBiotest Pharma GmbH
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a Iaemoctin 500Forma farmacéutica: Polvo, 1000 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere recetaForma farmacéutica: Polvo, 2000 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere recetaForma farmacéutica: Polvo, 250 UIPrincipio activo: factor de coagulación VIIIFabricante: CSL Behring GmbHRequiere receta
Alternativas a Iaemoctin 500 en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Iaemoctin 500 en Испания
Alternativa a Iaemoctin 500 en Украина
Médicos online para Iaemoctin 500
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Iaemoctin 500 – sujeta a valoración médica y normativa local.














