
Disport

Consulta con un médico sobre la receta médica de Disport

Cómo usar Disport
HOJA DE INSTRUCCIONES PARA EL PACIENTE: INFORMACIÓN PARA EL USUARIO
Dysport
300 u.; 500 u. de complejo de neurotoxina Clostridium botulinumtipo A,
polvo para preparar solución para inyección
Es importante leer detenidamente el contenido de esta hoja de instrucciones antes de usar el medicamento, ya que contiene información importante para el paciente.
Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, consulte a su médico o farmacéutico.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es Dysport y para qué se utiliza
- 2. Información importante antes de usar Dysport
- 3. Cómo usar Dysport
- 4. Posibles efectos adversos
- 5. Cómo conservar Dysport
- 6. Contenido del envase y otra información
1. Qué es Dysport y para qué se utiliza
Dysport contiene complejo de neurotoxina Clostridium botulinumtipo A (comúnmente conocida como toxina botulínica) producida por la bacteria Clostridium botulinum(bacilo de la toxina botulínica). Su acción consiste en inhibir la contracción muscular al evitar la liberación de una sustancia química que causa la contracción muscular fisiológica. Esto ayuda a reducir la tensión muscular anormal llamada espasticidad.
Indicaciones
- Tratamiento sintomático de la espasticidad focal de las extremidades inferiores en niños con parálisis cerebral infantil de 2 años o más
- Tratamiento sintomático de la espasticidad focal de las extremidades superiores en niños con parálisis cerebral infantil de 2 años o más
- Incontinencia urinaria (incontinencia de orina) debido a problemas con la vejiga urinaria relacionados con daño en la médula espinal o esclerosis múltiple en pacientes que realizan cateterización intermitente limpia de forma regular
- Tortícolis en adultos
- Blefarospasmo en adultos
- Hemifacial en adultos
- Espasticidad de las extremidades superiores en adultos
- Espasticidad de las extremidades inferiores en adultos
- Hiperhidrosis axilar
2. Información importante antes de usar Dysport
Cuándo no usar Dysport
- si el paciente es alérgico (hipersensible) a la toxina botulínica o a cualquier otro componente de Dysport (enumerados en el punto 6)
- si el paciente tiene una infección del tracto urinario durante el tratamiento de la incontinencia de orina.
Advertencias y precauciones
Antes de comenzar a usar Dysport, debe discutirlo con su médico:
- si hay problemas o enfermedades musculares, como miastenia (enfermedad crónica caracterizada por un cansancio y debilidad muscular rápida)
- si los músculos en el sitio de inyección propuesto muestran signos de atrofia
- si se han detectado problemas de deglución o respiración
- si hay una debilidad muscular significativa
- si hay problemas respiratorios crónicos
- si hay tendencia a sangrado
- si hay inflamación o infección en el sitio de inyección propuesto
Interacción con otros medicamentos
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando actualmente o recientemente, así como sobre los medicamentos que planea tomar.
Algunos medicamentos que afectan la función neuromuscular pueden potenciar el efecto de Dysport.
Embarazo y lactancia
Si la paciente está embarazada o en período de lactancia, o si cree que puede estar embarazada o planea tener un hijo, debe consultar a su médico o farmacéutico antes de usar este medicamento.
Dysport no se recomienda durante el embarazo, a menos que sea estrictamente necesario.
Dysport no se recomienda durante la lactancia.
Niños y adolescentes
En el tratamiento de la espasticidad asociada con la parálisis cerebral infantil, Dysport debe usarse en niños de 2 años o más.
Conducción de vehículos y uso de máquinas
Después de la inyección de Dysport, puede ocurrir una debilidad muscular transitoria y una alteración de la visión.
En tales casos, no debe conducir vehículos ni operar máquinas.
Este medicamento contiene albúmina (un tipo de proteína) derivada de sangre humana.
La posibilidad de transmisión de agentes infecciosos es muy poco probable, pero no puede ser completamente excluida.
3. Cómo usar Dysport
La inyección la realizará un médico, quien decidirá con qué frecuencia debe administrarse el medicamento. Esto dependerá del tipo de afección detectada en el paciente.
Dysport debe usarse solo para un paciente y solo durante una sesión terapéutica.
En el tratamiento de la espasticidad focal de las extremidades inferiores en niños:Dosificación
La dosis se determinará según la edad y el peso del niño. Dysport se inyectará en los músculos de las extremidades inferiores afectados por la espasticidad.
La dosis total de Dysport por sesión terapéutica no debe exceder las 1000 unidades o 30 unidades/kg, según la dosis más baja. Las inyecciones se realizarán aproximadamente cada 16 a 22 semanas o según sea necesario, pero no con más frecuencia que cada 12 semanas.
En el tratamiento de la espasticidad focal de las extremidades superiores en niños:Dosificación
La dosis se determinará según la edad y el peso del niño. Dysport se inyectará en los músculos de las extremidades superiores afectados por la espasticidad. En el caso de la inyección en una extremidad superior, la dosis por sesión terapéutica no debe exceder las 640 unidades o 16 unidades/kg, según la dosis más baja. En el caso de la inyección en ambas extremidades superiores durante una sesión terapéutica, la dosis no debe exceder las 840 unidades o 21 unidades/kg, según la dosis más baja. Por lo general, dentro de unas semanas después del final del tratamiento, los espasmos musculares deben disminuir, y el efecto del tratamiento debe durar hasta 34 semanas. El médico repetirá los procedimientos aproximadamente cada 16 a 28 semanas o según sea necesario, pero no con más frecuencia que cada 16 semanas.
En el tratamiento simultáneo de la espasticidad focal de las extremidades superiores e inferiores en niños:Si durante la misma sesión terapéutica es necesario tratar tanto las extremidades superiores como las inferiores, el médico determinará la dosis de Dysport que se inyectará en cada extremidad, sin exceder la dosis total por sesión terapéutica de 1000 unidades o 30 unidades/kg, según la dosis más baja. El tratamiento simultáneo de las extremidades superiores e inferiores debe considerarse no antes de 12 a 16 semanas después de la sesión terapéutica anterior. El momento óptimo para repetir el procedimiento debe determinarse según la progresión de la enfermedad y la respuesta al tratamiento.
Tratamiento de la incontinencia urinaria
Dosificación
La primera dosis administrada en el músculo de la vejiga urinaria es de 600 unidades. Sin embargo, en la siguiente inyección, el médico puede decidir aumentar la dosis a 800 unidades.
Dysport se administrará durante una cistoscopia. Se insertará un cystoscopio, equipado con una fuente de luz en el extremo, en la vejiga urinaria a través de la abertura por la que se elimina la orina (llamada meato urinario). De esta manera, el médico que realiza el procedimiento tendrá una visión del interior de la vejiga urinaria, lo que permitirá la inyección de Dysport en la pared de la vejiga urinaria. Dysport se administrará solo a pacientes que realicen cateterización intermitente limpia (CIC) de forma regular. La CIC es un procedimiento en el que se inserta un catéter (un tubo suave y hueco) en la vejiga urinaria a través del meato urinario para facilitar la eliminación de la orina de la vejiga urinaria, y luego se retira después de vaciar la vejiga urinaria. Para obtener más información sobre el procedimiento, consulte a su médico.
Para prevenir infecciones del tracto urinario, es necesario tomar antibióticos. Si está tomando un medicamento que diluye la sangre, el médico ajustará el tratamiento antes y después de la inyección con Dysport. Antes de la inyección, el paciente puede recibir anestesia local o general, o un medicamento sedante. El paciente será observado durante al menos 30 minutos después de la inyección. Por lo general, los síntomas deben disminuir dentro de las 2 semanas, y la mejora puede durar hasta 48 semanas. El médico decidirá si es necesario repetir el tratamiento, pero no con más frecuencia que cada 12 semanas.
Tratamiento del tortícolis
Dosificación
Por lo general, la primera dosis de Dysport es de 500 unidades. El médico puede dividir esta dosis e inyectarla en varios sitios del cuello, probablemente en 2 o 3 músculos más activos.
Se puede administrar una dosis más baja a pacientes con bajo peso o de edad avanzada.
La mejora de los espasmos musculares debe ocurrir dentro de la 1 semana. Dependiendo de la duración del efecto del tratamiento, se pueden administrar dosis adicionales (250-1000 unidades) aproximadamente cada 12 a 16 semanas.
Tratamiento del blefarospasmo y del hemifacial
Dosificación
El médico inyectará Dysport en el área de la cara afectada por la enfermedad. La primera dosis es de 40 unidades por ojo. Dependiendo de la duración del efecto del tratamiento, se pueden realizar inyecciones aproximadamente cada 12 semanas. Si es necesario un efecto de tratamiento más prolongado, la dosis de Dysport se puede aumentar a 80 unidades por ojo.
La dosis máxima administrada no debe exceder la dosis total de 120 unidades por ojo.
Tratamiento de la espasticidad de las extremidades superiores en adultos
Dosificación
Según la decisión del médico, Dysport se inyectará en una dosis que oscila entre 500 y 1000 unidades. El médico puede dividir esta dosis e inyectarla en los músculos individuales del brazo y el hombro. La mejora de los espasmos musculares debe ocurrir dentro de la 1 semana. Las inyecciones se realizarán aproximadamente cada 12 a 16 semanas.
Tratamiento de la espasticidad de las extremidades inferiores en adultos
Dosificación
Dysport se administra generalmente en una dosis de 1500 unidades. El médico puede dividir esta dosis e inyectarla en los músculos individuales de la extremidad inferior. Las inyecciones se realizarán aproximadamente cada 12 a 16 semanas.
Tratamiento de la espasticidad de las extremidades superiores e inferiores en adultos
Si durante la misma sesión de tratamiento es necesario administrar el medicamento en ambos músculos de la extremidad superior e inferior, el médico puede dividir la dosis de Dysport entre los músculos de estas dos partes del cuerpo. En este caso, la dosis total del medicamento no debe exceder las 1500 unidades.
Tratamiento de la hiperhidrosis axilar
Dosificación
Dysport se administra generalmente en una dosis de 100 unidades por axila. El médico dividirá esta dosis e inyectará en 10 sitios de la axila. El efecto máximo debe ser visible alrededor de la 2 semana después de la administración. La dosis máxima administrada no debe exceder las 200 unidades por axila.
Uso de una dosis mayor de la recomendada de Dysport
En caso de administrar una dosis mayor de la recomendada de Dysport, el paciente puede experimentar debilidad muscular en músculos distintos de aquellos en los que se inyectó el medicamento. Los síntomas de sobredosis pueden no ocurrir inmediatamente después de la inyección. Si ocurren, debe comunicarse de inmediato con el médico. Si ocurren dificultades para respirar, tragar o hablar, debe acudir al centro médico más cercano.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Debe informar a su médico de inmediato si:
- el paciente experimenta problemas para tragar, respirar o hablar
- el paciente experimenta dificultades para respirar con o sin hinchazón de la cara, los labios, la lengua y/o la garganta, enrojecimiento de la piel o erupción cutánea con picazón (urticaria). La aparición de estos síntomas puede indicar que el paciente es alérgico a Dysport. La probabilidad de que ocurran efectos adversos se ha clasificado de la siguiente manera:
| Frecuencia de ocurrencia | |
| Muy frecuente | pueden ocurrir en más de 1 de cada 10 personas |
| Frecuente | pueden ocurrir en como máximo 1 de cada 10 personas |
| Poco frecuente | pueden ocurrir en como máximo 1 de cada 100 personas |
| Raro | pueden ocurrir en como máximo 1 de cada 1000 personas |
| Frecuencia desconocida | la frecuencia no puede determinarse a partir de los datos disponibles |
Algunos efectos adversos pueden ocurrir en todos los pacientes tratados con Dysport, mientras que la ocurrencia de otros efectos adversos puede depender del tipo de afección por la que se administra el medicamento.
Debe leer la información relacionada con la afección específica.
Se han notificado los siguientes efectos adversos (independientemente de la indicación):
Frecuente:
- moretones y/o dolor en el sitio de inyección
- debilidad general
- fatiga
- síntomas similares a los de la gripe
Poco frecuente:
- picazón
Raro:
- erupción cutánea, neuralgia con atrofia muscular
Frecuencia desconocida (la frecuencia no puede determinarse a partir de los datos disponibles):
- entumecimiento
- atrofia muscular
También se han notificado otros efectos adversos relacionados con la propagación del medicamento más allá del sitio de inyección (aumento de la debilidad muscular, dificultades para tragar o aspiración con resultado mortal en casos muy raros).
Tratamiento sintomático de la espasticidad focal de las extremidades inferiores en niños con parálisis cerebral infantil
Se han notificado los siguientes efectos adversos:
- dolor muscular
- debilidad de la fuerza muscular de la extremidad inferior
- síntomas similares a los de la gripe
- dolor, enrojecimiento, moretones en el sitio de inyección
- alteración de la marcha
- fatiga
- caídas
Poco frecuente:
- disminución de la fuerza y la debilidad
Tratamiento sintomático de la espasticidad focal de las extremidades superiores en niños con parálisis cerebral infantil
Se han notificado los siguientes efectos adversos:
- debilidad muscular
- dolor muscular
- síntomas similares a los de la gripe
- fatiga
- picazón de la piel, moretones, dolor, hinchazón y erupción cutánea en el sitio de inyección
- erupción cutánea
Poco frecuente:
- disminución de la fuerza y la debilidad
Tratamiento simultáneo de la espasticidad focal de las extremidades superiores e inferiores en niños con parálisis cerebral infantil
No se han notificado efectos adversos adicionales durante el tratamiento simultáneo de la extremidad superior e inferior en comparación con la administración del medicamento en la extremidad superior o inferior por separado.
Tratamiento de la incontinencia urinaria debido a la hiperactividad del detrusor
Se han notificado los siguientes efectos adversos:
- hematuria*
- estreñimiento
- bacteriuria*
- disfunción eréctil, a veces llamada impotencia
- infección del tracto urinario*
- dolor de cabeza
- fiebre
Poco frecuente:
- entumecimiento
- debilidad muscular
- dolor de la vejiga urinaria*
- reacción refleja autónoma (dysreflexia autónoma)*
- incapacidad para vaciar la vejiga urinaria (retención urinaria)
- sangrado de la vejiga urinaria o del conducto que lleva la orina desde la vejiga urinaria hacia el exterior del cuerpo (uretra) * Este efecto adverso puede estar relacionado con el procedimiento
Tratamiento del tortícolis
Se han notificado los siguientes efectos adversos:
- dificultades para tragar (disfagia)
- sequedad de boca
- debilidad muscular
Frecuente:
- dolor de cabeza
- debilidad facial
- mareo
- visión borrosa
- deterioro de la agudeza visual
- dificultades para respirar
- dolor de cuello
- dolor musculoesquelético
- dolor muscular
- dolor en las manos y los dedos
- rigidez muscular
- alteración de la voz (disfonía)
Poco frecuente:
- visión doble
- caída de los párpados
- atrofia muscular
- debilidad de los músculos de la mandíbula
- náuseas
Raro:
- aspiración (ahogamiento)
Tratamiento del blefarospasmo y del hemifacial
Se han notificado los siguientes efectos adversos:
- caída de los párpados
Frecuente:
- sequedad de ojos
- visión doble
- aumento de la lágrima
- hinchazón del párpado
- debilidad facial
Poco frecuente:
- parálisis del nervio facial
Raro:
- parálisis del músculo ocular (limitación de la capacidad de mover el globo ocular)
- entrecerramiento del párpado
Tratamiento de la espasticidad de las extremidades superiores en adultos
Se han notificado los siguientes efectos adversos:
- debilidad muscular
- dolor musculoesquelético
- dolor en la mano y los dedos
- dolor, enrojecimiento, hinchazón en el sitio de inyección
- fatiga, debilidad
- síntomas similares a los de la gripe
Poco frecuente:
- dificultades para tragar
Tratamiento de la espasticidad de las extremidades inferiores en adultos
Se han notificado los siguientes efectos adversos:
- caídas
- debilidad muscular
- dolor muscular
- dificultades para tragar (disfagia)
- debilidad
- fatiga
- síntomas similares a los de la gripe
- moretones, dolor, erupción cutánea, picazón de la piel en el sitio de inyección
Tratamiento de la hiperhidrosis axilar
Se han notificado los siguientes efectos adversos:
- dificultades para respirar
- sudoración compensatoria (aumento de la sudoración en otras áreas distintas de las axilas)
- dolor de espalda, hombros y cuello
- dolor muscular en la espalda y los tobillos
Poco frecuente:
- mareo
- dolor de cabeza
- entumecimiento o hormigueo en las manos o los pies
- espasmo involuntario de los músculos de los párpados
- enrojecimiento de la cara
- sangrado nasal
Si alguno de los efectos adversos empeora o si ocurren efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico o farmacéutico.
Notificación de efectos adversos
Si ocurren efectos adversos, incluidos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad, Consumo y Bienestar Social.
Dirección:
Ministerio de Sanidad, Consumo y Bienestar Social
Calle de Alcalá, 56
28071 Madrid
Teléfono: 913 954 400
Fax: 913 954 411
Correo electrónico: [[email protected]](mailto:[email protected])
Los efectos adversos también pueden notificarse al titular de la autorización de comercialización o a su representante.
5. Cómo conservar Dysport
Debe conservar este medicamento en un lugar que esté fuera del alcance de los niños.
No use este medicamento después de la fecha de caducidad que se indica en el envase.
Dysport debe conservarse en la nevera (2°C - 8°C). No congelar.
La solución debe usarse inmediatamente después de la reconstitución. Después de la reconstitución, la solución puede conservarse durante 24 horas en la nevera (2°C - 8°C).
Caducidad (EXP)
Número de lote (Lote)
6. Contenido del envase y otra información
Qué contiene Dysport
- El principio activo es toxina botulínica tipo A, 300 o 500 unidades por vial
- Los demás componentes son albúmina humana y lactosa monohidratada.
Cómo se presenta Dysport y contenido del envase
Dysport es un polvo blanco para preparar solución para inyección. Está disponible en envases que contienen 1 o 2 viales.
Título de la autorización de comercialización
Ipsen Pharma, 65 Quai Georges Gorse, 92100 Boulogne-Billancourt, Francia
Importador
Ipsen Manufacturing Ireland Limited, Blanchardstown Industrial Park
Blanchardstown, Dublín 15, Irlanda
Fecha de la última revisión de la hoja de instrucciones:junio de 2022
Información adicional o la hoja de instrucciones en un formato adecuado para personas ciegas o con discapacidad visual puede obtenerse contactando a:
Ipsen España, S.A.
Calle de María de Molina, 40
28006 Madrid
Teléfono: 913 816 400
Fax: 913 816 401
Logo del titular de la autorización de comercialización
--------------------------------------------------------------------------------------------------------------
Información destinada exclusivamente al personal médico especializado:
Para mejorar la identificabilidad de los productos biológicos, debe anotar claramente el nombre y el número de lote del producto administrado.
Las unidades del producto Dysport son específicas de este producto y no son idénticas a las unidades de otros productos que contienen toxina botulínica.
Dysport debe administrarse por médicos adecuadamente capacitados.
No cubra el tapón de goma del vial con el dedo para evitar la contaminación.
Utilice agujas estériles de calibre 23 o 25.
La siguiente instrucción describe la preparación del producto Dysport para la inyección. Los volúmenes de diluyente especificados permiten obtener concentraciones destinadas a usarse en la indicación específica, con la excepción de la indicación de la incontinencia urinaria, para la que existen instrucciones específicas (véase a continuación).
Para obtener más información, consulte a su médico o farmacéutico.
Obstrucción bilateral del párpado y contracción facial hemifacial
Dosificación
Se debe inyectar 10 unidades (0,05 ml) del producto medicinal hacia la médula y 10 unidades (0,05 ml) hacia el lado, en relación con la unión de la parte del párpado y la órbita, tanto en la parte superior (3 y 4) como en la parte inferior del músculo orbicular (5 y 6) de cada ojo.
Para limitar el riesgo de ptosis, se debe evitar la inyección cerca del elevador del párpado superior.
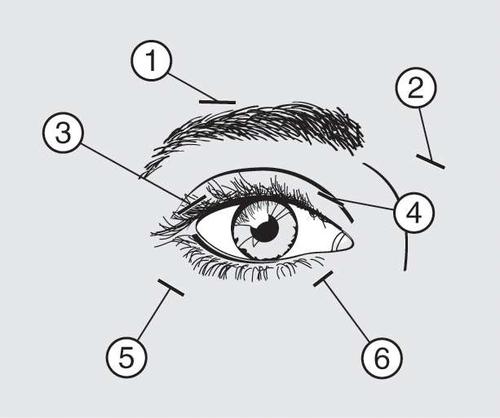
En el caso de la inyección del producto en el párpado superior, la aguja debe alejarse del centro del párpado para evitar la administración del producto en el músculo elevador del párpado superior. El esquema anterior está diseñado para ayudar en la distribución adecuada de la administración del producto. Se puede esperar el comienzo de la remisión de los síntomas de la enfermedad dentro de dos a cuatro días después de la inyección del producto, pero el efecto máximo se produce generalmente después de dos semanas.
Las inyecciones deben repetirse cada aproximadamente 12 semanas o con la frecuencia que sea necesaria para prevenir la recurrencia de los síntomas, pero no más frecuentemente que cada 12 semanas.
Si la respuesta al tratamiento inicial se considera insuficiente, durante las visitas posteriores puede ser necesario aumentar la dosis a 60 unidades de la siguiente manera: 10 unidades (0,05 ml) hacia la médula y 20 unidades (0,1 ml) hacia el lado, 80 unidades: 20 unidades (0,1 ml) hacia la médula y 20 unidades (0,1 ml) hacia el lado, o hasta 120 unidades: 20 unidades (0,1 ml) hacia la médula y 40 unidades (0,2 ml) hacia el lado, por encima y por debajo de cada ojo, utilizando la técnica de inyección descrita anteriormente. También se puede inyectar adicionalmente Dysport en el músculo frontal por encima de la ceja (1 y 2), si la contracción en esta zona causa trastornos de la visión.
En casos de contracción unilateral del párpado, las inyecciones deben limitarse al ojo afectado. Los pacientes con contracción hemifacial del músculo facial deben ser tratados de la misma manera que en el caso de contracción unilateral del párpado. Las dosis recomendadas se aplican en personas adultas de cualquier edad, incluyendo la edad avanzada.
Niños: No se ha demostrado la eficacia y seguridad del uso de este producto medicinal en el tratamiento de la contracción del párpado y la contracción hemifacial del músculo facial en niños.
Forma de administración
En el tratamiento de la contracción del párpado y la contracción hemifacial del músculo facial, se utiliza una solución que contiene 200 unidades en 1 ml, que se obtiene después de la reconstitución del producto medicinal Dysport 300 UI en 1,5 ml o del producto medicinal Dysport 500 UI en 2,5 ml de solución de cloruro de sodio al 0,9% (p/v) para inyección. Dysport se administra en inyecciones subcutáneas hacia la médula y hacia el lado, en relación con la unión de la parte del párpado y la órbita, tanto en la parte superior como en la parte inferior del músculo orbicular de cada ojo.
Espasticidad focal de las extremidades superiores e inferiores en adultos
Extremidad superior
Dosificación
En los estudios clínicos, las dosis de 500 y 1000 unidades se dividieron entre los músculos seleccionados, en sesiones de tratamiento según el esquema presentado a continuación.
No se debe inyectar más de 1 ml de solución en un solo lugar.
Extremidad inferior
Dosificación
La dosis total del producto medicinal no debe exceder las 1500 unidades. No se debe inyectar más de 1 ml de solución en un solo lugar.
| Músculos en los que se realizaron las inyecciones | Dosis recomendada de Dysport (UI) |
| Músculo flexor radial del carpo (FCR) Músculo flexor cubital del carpo (FCU) | 100-200 UI 100-200 UI |
| Músculo flexor profundo de los dedos (FDP) Músculo flexor superficial de los dedos (FDS) Músculo flexor largo del pulgar Músculo aductor del pulgar | 100-200 UI 100-200 UI 100-200 UI 25-50 UI |
| Músculo braquial Músculo braquiorradial Músculo bíceps braquial (BB) Músculo supinador | 200-400 UI 100-200 UI 200-400 UI 100-200 UI |
| Músculo tríceps braquial (cabeza larga) Músculo pectoral mayor Músculo subescapular Músculo dorsal ancho | 150-300 UI 150-300 UI 150-300 UI 150-300 UI |
| Músculos en los que se realizaron las inyecciones | Dosis recomendada de Dysport (UI) | Número de inyecciones por músculo |
| Distal | ||
| Músculo extensor común de los dedos | 300-550 UI | 2-4 |
| Músculo gastrocnemio | ||
| cabeza medial | 100-450 UI | 1-3 |
| cabeza lateral | 100-450 UI | 1-3 |
| Músculo tibial posterior | 100-250 UI | 1-3 |
| Músculo flexor largo de los dedos | 50-200 UI | 1-2 |
| Músculo flexor corto de los dedos | 50-200 UI | 1-2 |
| Músculo flexor largo del pulgar | 50-200 UI | 1-2 |
| Músculo flexor corto del pulgar | 50-100 UI | 1-2 |
| Proximal | ||
| Músculo recto femoral | 100-400 UI | 1-3 |
| Músculos isquiotibiales | 100-400 UI | 1-3 |
| Músculo aductor mayor | 100-300 UI | 1-3 |
| Músculo aductor largo | 50-150 UI | 1-2 |
| Músculo aductor corto | 50-150 UI | 1-2 |
| Músculo grácil | 100-200 UI | 1-3 |
| Músculo glúteo mayor | 100-400 UI | 1-2 |
El grado y la forma de la espasticidad muscular en el momento de la inyección pueden requerir un cambio en la dosis de Dysport y el lugar de la inyección.
Extremidad superior e inferior
Si durante una sesión terapéutica es necesario administrar el producto en ambos músculos de la extremidad superior e inferior, la dosis de Dysport debe adaptarse a las necesidades del paciente, teniendo en cuenta que la dosis total no debe exceder las 1500 unidades.
Forma de administración
En el tratamiento de la espasticidad focal de las extremidades superiores e inferiores, se utiliza una solución que contiene 100, 200 o 500 unidades en 1 ml, que se obtiene después de la reconstitución del producto medicinal Dysport en solución de cloruro de sodio al 0,9% (p/v) para inyección. Dysport se administra en inyecciones intramusculares en los músculos especificados anteriormente.
Hiperhidrosis axilar
Dosificación
La dosis inicial recomendada para el tratamiento de la hiperhidrosis axilar es de 100 unidades por axila. Si el efecto deseado no se logra, la dosis puede aumentarse a 200 unidades por axila en la siguiente administración. La dosis máxima administrada no debe exceder las 200 unidades por axila.
El área en la que se realizarán las inyecciones debe ser examinada previamente con la prueba de yodo-almidón. Ambas axilas deben ser limpiadas y desinfectadas cuidadosamente. Se deben realizar inyecciones intradérmicas en diez lugares. En cada lugar, se deben administrar 10 unidades, es decir, 100 unidades por axila. El efecto máximo debe ser visible alrededor de dos semanas después de la inyección.
Forma de administración
En el tratamiento de la hiperhidrosis axilar, se utiliza una solución que contiene 200 unidades en 1 ml, que se obtiene después de la reconstitución del producto medicinal Dysport 300 UI en 1,5 ml o del producto medicinal Dysport 500 UI en 2,5 ml de solución de cloruro de sodio al 0,9% (p/v) para inyección. Dysport se administra en inyecciones intradérmicas de la manera descrita anteriormente.
La información detallada sobre la dosificación y la forma de administración se encuentra en la Característica del Producto Medicinal.
- País de registro
- Principio activo
- Requiere recetaSí
- ImportadorIpsen Manufacturing Ireland Limited
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a DisportForma farmacéutica: Solución, 200 U Speywood/mlPrincipio activo: Botulinum toxinRequiere recetaForma farmacéutica: Polvo, 125 unidades SpeywoodPrincipio activo: Botulinum toxinRequiere recetaForma farmacéutica: Polvo, 125 unidades SpeywoodPrincipio activo: Botulinum toxinRequiere receta
Alternativas a Disport en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Disport en Ucrania
Alternativa a Disport en España
Médicos online para Disport
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Disport – sujeta a valoración médica y normativa local.














