
Curosurf

Consulta con un médico sobre la receta médica de Curosurf

Cómo usar Curosurf
Hoja de instrucciones del paquete: información para padres y cuidadores
Curosurf, 80 mg/ml, suspensión para administración intratraqueal y endobronquial
(Poractant alfa)
Fracción de fosfolípidos de pulmón de cerdo
Es importante leer atentamente el contenido de la hoja de instrucciones antes de administrar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a un médico.
- Si el paciente presenta algún efecto adverso, incluidos aquellos no mencionados en esta hoja de instrucciones, debe informar a su médico o enfermera. Véase el punto 3.
Índice de la hoja de instrucciones:
- 1. Qué es Curosurf y para qué se utiliza
- 2. Cómo se administra Curosurf
- 3. Posibles efectos adversos
- 4. Cómo conservar Curosurf
- 5. Contenido del paquete y otra información
1. QUÉ ES CUROSURF Y PARA QUÉ SE UTILIZA
Curosurf se utiliza para tratar y prevenir el síndrome de dificultad respiratoria (SDR) en recién nacidos. En la mayoría de los recién nacidos, hay una sustancia en los pulmones llamada surfactante (factor de superficie). Esta sustancia cubre los alvéolos pulmonares, evita que se peguen y permite una respiración normal. Sin embargo, algunos recién nacidos, especialmente los prematuros, nacen con una deficiencia de surfactante, lo que lleva al desarrollo del SDR. Curosurf es un surfactante natural que actúa de la misma manera que el surfactante producido por los recién nacidos y, por lo tanto, ayuda a los recién nacidos a respirar normalmente hasta que comiencen a producir su propio surfactante natural.
En el recién nacido pueden ocurrir otras afecciones que pueden requerir un tratamiento diferente.
2. CÓMO SE ADMINISTRA CUROSURF
Dosificación:
El médico determina la dosis adecuada del medicamento según el peso del niño. Si se administra Curosurf para prevenir el SDR, el medicamento debe administrarse dentro de los 15 minutos después del nacimiento. Si se administra Curosurf para tratar el SDR, el medicamento debe administrarse lo antes posible después del diagnóstico. Si el niño necesita una dosis adicional de Curosurf, se administra 12 horas después de la primera dosis. Si es necesario, se puede administrar una tercera dosis después de otras 12 horas.
No se ha estudiado el uso de Curosurf en prematuros con insuficiencia hepática o renal.
1
Forma de administración del medicamento:
Curosurf se administra al niño en una incubadora por un médico o enfermera. El medicamento se calentará a temperatura ambiente y luego se administrará mediante una jeringa a través de un tubo endotraqueal en la tráquea del niño. Para ello, puede ser necesario desconectar al niño del respirador durante unos minutos.
También se puede utilizar un método de administración de surfactante menos invasivo a través de un catéter delgado (LISA, administración de surfactante menos invasiva).
Curosurf contiene sodio
El medicamento contiene menos de 1 mmol (23 mg) de sodio por vial, es decir, el medicamento se considera "libre de sodio".
3. POSIBLES EFECTOS ADVERSOS
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán. Los posibles efectos adversos se enumeran a continuación según su frecuencia de aparición:
En caso de duda sobre los efectos adversos, debe consultar a un médico.
No muy frecuentes(ocurren en menos de 1 de cada 100 pacientes):
Raros(ocurren en menos de 1 de cada 1000 pacientes):
- infección
- hemorragia cerebral
- neumotórax
- bradicardia
- hipotensión
- enfermedad pulmonar crónica
- hipoxemia
Además, se han notificado los siguientes efectos adversos:
- hiperóxemia
- citosis
- apnea
- complicaciones relacionadas con la intubación
- depresión del sistema nervioso central
Durante la administración de Curosurf a través de un catéter delgado, se han informado algunos efectos adversos leves y transitorios: bradicardia, apnea, disminución de la saturación de oxígeno, espuma en la boca, tos, ahogamiento y estornudos.
Notificación de efectos adversos
Si ocurren algún efecto adverso, incluidos aquellos no mencionados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera.
Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad, Consumo y Bienestar Social, o a la autoridad sanitaria correspondiente.
La notificación de efectos adversos permite recopilar más información sobre la seguridad del medicamento.
daño pulmonar
2
4. CÓMO CONSERVAR CUROSURF
- El medicamento debe conservarse en un lugar inaccesible para los niños.
- Conservar en nevera a una temperatura entre 2°C y 8°C, conservar en el embalaje original para protegerlo de la luz. Antes de administrar al niño, debe calentarse a temperatura ambiente.
- Los viales de Curosurf que no se han abierto y no se han utilizado, y que se han calentado a temperatura ambiente, se pueden volver a colocar en la nevera dentro de las 24 horas para su uso posterior. No debe calentarse a temperatura ambiente y volver a colocarse en la nevera más de una vez.
- No debe utilizarse después de la fecha de caducidad indicada en el paquete y el vial. La fecha de caducidad es el último día del mes indicado.
- Un contenedor solo debe utilizarse una vez, y los restos deben desecharse. El hospital debe asegurarse de que se eliminen de manera segura los restos no utilizados de Curosurf.
- No debe tirar los medicamentos por el desagüe. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se necesitan. Este comportamiento ayudará a proteger el medio ambiente.
5. CONTENIDO DEL PAQUETE Y OTRA INFORMACIÓN
Qué contiene Curosurf?
- -El principio activo es una mezcla de lípidos y proteínas obtenidas de los alvéolos pulmonares de cerdo.
- Los demás componentes son: cloruro de sodio, agua para inyección, bicarbonato de sodio (para ajustar el pH).
Cómo se presenta Curosurf y qué contiene el paquete?
Curosurf es una suspensión estéril. Está disponible en viales de vidrio de un solo uso con una capacidad de 5 ml, que contienen 1,5 ml (120 mg) o 3 ml (240 mg) de fracción de fosfolípidos de alvéolos pulmonares de cerdo. Cada mililitro de suspensión estéril contiene 80 mg de fracción de fosfolípidos de alvéolos pulmonares de cerdo. En un paquete hay 2 viales de 1,5 ml de suspensión o 1 vial de 3 ml de suspensión de Curosurf.
No todos los tamaños de paquete pueden estar disponibles en el mercado.
Titular de la autorización de comercialización:
Chiesi Farmaceutici S.p.A, Via Palermo 26/A, 43 122 Parma, Italia.
Fabricante:
Chiesi Farmaceutici S.p.A, Via San Leonardo 96 - Via Palermo 26/A, 43 122 Parma, Italia.
Chiesi Pharmaceuticals GmbH, Gonzagagasse 16/16, A-1010 Viena, Austria.
Para obtener más información, debe ponerse en contacto con el representante del titular de la autorización de comercialización en España:
Chiesi España S.A., Calle de María de Molina, 41, 28006 Madrid
Tel.: 91 456 33 00, Fax: 91 456 33 01, Correo electrónico: [email protected]
Fecha de la última revisión de la hoja de instrucciones:
Por favor, lea la información en el dorso de la hoja de instrucciones
-------------------------------------------------------------------------------------------------------------------------
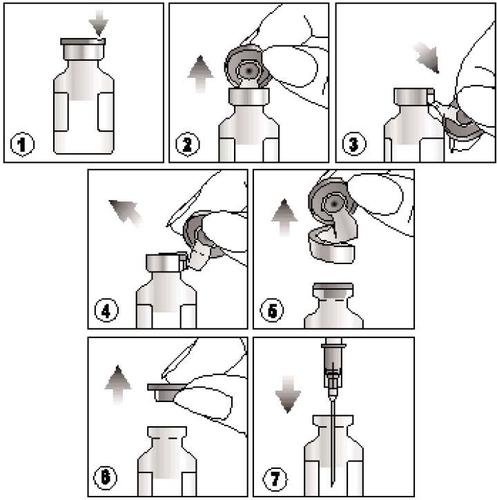
Cómo abrir el producto?

3
- 1) Encontrar la ranura en la tapa de plástico de color,
- 2) Levantar la tapa en la ranura y tirar de ella hacia arriba,
- 3) Tirar hacia abajo de la parte de plástico de la tapa junto con la parte de aluminio,
- 4) y 5) Quitar toda la tapa tirando del anillo de aluminio
- 6) y 7) Quitar el tapón de goma antes de extraer el contenido del vial.
Para un solo uso. El contenido no utilizado del vial debe desecharse.
No debe conservarse el contenido no utilizado para un uso posterior.
Los restos del producto no utilizado o sus desechos deben eliminarse de acuerdo con las regulaciones.
4
- País de registro
- Principio activo
- Requiere recetaNo
- Fabricante
- ImportadorChiesi Farmaceutici S.p.A. Chiesi Pharmaceuticals GmbH
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a CurosurfForma farmacéutica: Suspensión, 80 mg/mlPrincipio activo: natural phospholipidsNo requiere recetaForma farmacéutica: Suspensión, 80 mg/mlPrincipio activo: natural phospholipidsNo requiere recetaForma farmacéutica: Pastillas, 1500 mg + 125 mgPrincipio activo: NiketamidaFabricante: Przedsiębiorstwo Produkcyjno-Handlowe EWA S.A.No requiere receta
Alternativas a Curosurf en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Curosurf en Украина
Alternativa a Curosurf en Испания
Médicos online para Curosurf
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Curosurf – sujeta a valoración médica y normativa local.














