Cómo usar Betadine Vag
Hoja de instrucciones del paquete: información para el usuario
Es importante leer atentamente el contenido de la hoja de instrucciones antes de usar el medicamento, ya que contiene
información importante para el paciente.
Este medicamento debe usarse siempre exactamente como se describe en esta hoja de instrucciones para el paciente o según las indicaciones del médico o farmacéutico.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- Si necesita consejo o información adicional, debe consultar a un farmacéutico.
- Si el paciente experimenta algún efecto adverso, incluidos todos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
- Si después de 7 días no se produce una mejora o el paciente se siente peor, debe ponerse en contacto con su médico.
Índice de la hoja de instrucciones
- 1. Qué es Betadine VAG y para qué se utiliza
- 2. Información importante antes de usar Betadine VAG
- 3. Cómo usar Betadine VAG
- 4. Posibles efectos adversos
- 5. Cómo conservar Betadine VAG
- 6. Contenido del paquete y otra información
1. Qué es Betadine VAG y para qué se utiliza
Betadine VAG está indicado exclusivamente para uso intravaginal. Betadine VAG contiene como principio activo povidona yodada. La povidona yodada es un complejo de yodo con povidona - después de la aplicación intravaginal, libera yodo. El yodo actúa sobre bacterias Gram-positivas y Gram-negativas, virus, hongos y algunos protozoos.
Indicaciones para el uso
Betadine VAG está indicado para el tratamiento de infecciones vaginales.
Betadine VAG se usa en mujeres adultas y en chicas después de la pubertad.
Si después de 7 días no se produce una mejora o el paciente se siente peor, debe ponerse en contacto con su médico.
2. Información importante antes de usar Betadine VAG
Cuándo no usar Betadine VAG
- si el paciente es alérgico a la povidona yodada o a alguno de los demás componentes de este medicamento (enumerados en el punto 6),
- si la glándula tiroides del paciente no funciona correctamente (el paciente tiene una tiroides hiperactiva o otras alteraciones funcionales de la tiroides - véase el punto "Advertencias y precauciones")
- antes, durante y después del tratamiento con yodo radioactivo y escintigrafía,
- en casos de erupción cutánea similar al herpes (llamada erupción cutánea de Duhring),
- en chicas antes de la pubertad (antes de la primera menstruación),
- en mujeres embarazadas y en período de lactancia,
- si el paciente está usando productos que contienen mercurio, porque el uso concomitante de Betadine VAG con productos que contienen mercurio puede causar daño a la piel.
El uso de Betadine VAG debe discutirse con un médico o farmacéutico si ocurre alguno de los siguientes síntomas:
- Hemorragias vaginales irregulares
- Hemorragia vaginal anormal o sangrado
- Úlceras, ampollas o ulceraciones vaginales o vulvares
- Dolor o dificultad para orinar
Si alguno de los siguientes síntomas ocurre en caso de infecciones vaginales, antes de usar Betadine VAG, debe ponerse en contacto con un médico:
- Fiebre o escalofríos
Advertencias y precauciones
Antes de comenzar a usar Betadine VAG, debe discutirlo con un médico o farmacéutico.
- Las pacientes con insuficiencia renal preexistente deben consultar a un médico antes de usar Betadine VAG.
- Debe evitarse el uso regular de óvulos de Betadine VAG en caso de uso concomitante de medicamentos que contienen sales de litio.
- El uso prolongado de medicamentos que contienen povidona yodada puede causar irritación de la piel, y en casos raros, reacciones cutáneas graves. Si ocurre irritación o sensibilidad, debe dejar de usar el medicamento y ponerse en contacto con un médico de inmediato (véase el punto 4. Posibles efectos adversos).
- El uso de povidona yodada (Betadine VAG) puede causar un cambio temporal de color de la piel en el lugar de aplicación, lo que se debe al color propio del medicamento.
- El medicamento puede causar resultados falsos positivos en algunas pruebas de laboratorio, como la detección de sangre oculta en heces o orina y la detección de glucosa en orina.
- Si después de 7 días no se produce una mejora, debe ponerse en contacto con un médico.
- Si dentro de 6 meses ocurren más de 2 infecciones vaginales, el paciente debe ponerse en contacto con un médico.
Niños y jóvenes
Betadine VAG está contraindicado para el uso en chicas antes de la pubertad.
Betadine VAG y otros medicamentos
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté usando actualmente o recientemente (incluidos los que se venden sin receta), así como sobre los medicamentos que planea usar.
Los productos que contienen mercurio (véase el punto "Cuándo no usar Betadine VAG"), plata, peróxido de hidrógeno y taurolidina pueden interactuar con la povidona yodada y no deben usarse al mismo tiempo.
El uso concomitante de Betadine VAG con medicamentos para el tratamiento de heridas que contienen componentes enzimáticos conduce a una disminución de la eficacia de ambos medicamentos, por lo que no deben usarse al mismo tiempo.
No debe usarse Betadine VAG al mismo tiempo que agentes reductores o sales de metales alcalinos.
Los medicamentos que contienen povidona yodada (Betadine VAG) usados antes o después de la aplicación de agentes antisépticos que contienen octenidina pueden causar decoloración oscura transitoria en los lugares afectados, por lo que no deben usarse al mismo tiempo.
Durante el uso de povidona yodada, puede ocurrir una disminución de la absorción de yodo por la tiroides, lo que puede alterar los resultados de algunas pruebas diagnósticas de la función tiroides [(por ejemplo, escintigrafía de la tiroides, determinación de PBI (yodo unido a proteínas), diagnóstico de yodo radioactivo] y puede impedir el tratamiento planificado de la tiroides con yodo (terapia con yodo radioactivo). Para obtener resultados objetivos de la escintigrafía de la tiroides, se recomienda asegurar un período lo suficientemente largo (al menos 4 semanas) después de terminar el tratamiento con Betadine VAG.
Betadine VAG puede causar resultados falsos positivos en algunas pruebas diagnósticas (como la detección de sangre en heces o glucosa en orina). Debe informar a su médico sobre el uso de Betadine VAG antes de las pruebas de laboratorio.
Embarazo, lactancia y fertilidad
Embarazo
El uso de óvulos que contienen povidona yodada en mujeres embarazadas está contraindicado, porque el yodo absorbido puede pasar a través de la barrera placentaria.
Lactancia
El uso de Betadine VAG está contraindicado en mujeres en período de lactancia, porque el yodo absorbido puede pasar a la leche materna (véase el punto 5.2).
Fertilidad
Existen datos limitados sobre el efecto de la povidona yodada en la fertilidad humana. Los óvulos de Betadine VAG tienen propiedades espermicidas. En este sentido, no se recomienda su uso en mujeres que planean quedar embarazadas.
Si el paciente sospecha que puede estar embarazada o planea tener un hijo, debe consultar a un médico o farmacéutico antes de usar este medicamento.
Conducción de vehículos y uso de máquinas
El medicamento no afecta la capacidad de conducir vehículos o usar máquinas.
3. Cómo usar Betadine VAG
Betadine VAG debe usarse siempre exactamente como se describe en la hoja de instrucciones para el paciente, o según las indicaciones del médico o farmacéutico. En caso de duda, debe consultar a un médico o farmacéutico.
Uso intravaginal.
No debe calentarse antes de la aplicación.
Betadine VAG está indicado para el uso en mujeres adultas y en chicas después de la pubertad.
Adultos
Se recomienda usar 1 óvulo intravaginalmente una vez al día durante 7 días. En caso de falta de mejora, debe consultar a un médico.
Se recomienda humedecer el óvulo antes de usarlo y luego introducirlo profundamente en la vagina por la noche antes de acostarse.
Aplicación del óvulo:
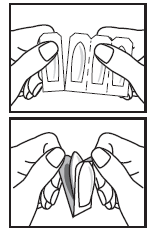
- Debe separar un óvulo de la tira, rompiendo a lo largo de la perforación en el lugar del corte "V".
- Debe agarrar las pestañas de plástico con ambas manos y tirar para sacar el óvulo del paquete.
También se recomienda el uso de toallas sanitarias durante el tratamiento.
Es importante humedecer el óvulo antes de su aplicación para asegurar la máxima disolución del principio activo y evitar la irritación local. No es necesario interrumpir el tratamiento incluso después de la aparición de sangrado menstrual.
Uso en niños y jóvenes
Betadine VAG está contraindicado para el uso en chicas antes de la pubertad.
Uso de una dosis mayor de la recomendada de Betadine VAG
Betadine VAG está indicado exclusivamente para uso intravaginal.
Al usar según las instrucciones, no hay riesgo de sobredosis.
En caso de sobredosis local, se recomienda retirar el óvulo aplicado.
En caso de uso de una dosis mayor de la recomendada de Betadine VAG o ingesta accidental del óvulo, debe ponerse en contacto con un médico de inmediato.
El exceso de yodo en el organismo puede causar la aparición de bocio, alteraciones de la función tiroides.
Los síntomas de intoxicación aguda por yodo son:
- insuficiencia renal y falta de producción de orina (anuria),
- insuficiencia circulatoria (colapso),
- dificultad para respirar (edema pulmonar),
- alteraciones metabólicas
En caso de aparición de los siguientes síntomas de toxicidad sistémica, debe buscar ayuda médica de inmediato:
- alteraciones de la función renal (incluida la anuria),
- latido cardíaco rápido (taquicardia),
- presión arterial baja (hipotensión),
- colapso circulatorio,
- dificultad para respirar (edema de glotis que conduce a asfixia o edema pulmonar),
- convulsiones,
- fiebre,
- acidosis metabólica,
- también puede desarrollarse hipertiroidismo o hipotiroidismo (véase el punto 4. - "Posibles efectos adversos", frecuencia "muy rara" y "frecuencia desconocida").
Omisión de la dosis de Betadine VAG
Debe continuar el tratamiento como antes y usar el medicamento lo antes posible.
No debe usar una dosis doble para compensar la dosis omitida.
Interrupción del uso de Betadine VAG
Para prevenir la recurrencia de la enfermedad y asegurar la curación completa de la infección, no debe interrumpir el tratamiento antes de 7 días.
En caso de dudas adicionales relacionadas con el uso de este medicamento, debe consultar a un médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
En caso de aparición de los siguientes efectos adversos, debe dejar de usar
Betadine VAG y ponerse en contacto con un médico de inmediato.
Reacciones adversas poco frecuentes (que ocurren con una frecuencia inferior a 1 de cada 1000 pacientes):
- Reacciones de hipersensibilidad.
Reacciones adversas muy raras (que ocurren con una frecuencia inferior a 1 de cada 10 000 pacientes):
- Reacción anafiláctica (reacción alérgica grave que causa dificultad para respirar, mareos, caída de la presión arterial).
- Edema angioneurótico (reacción alérgica grave que causa edema de la cara o la garganta).
Además, pueden ocurrir:
Poco frecuentes (que ocurren con una frecuencia inferior a 1 de cada 1000 pacientes):
dermatitis de contacto (con síntomas como enrojecimiento, pequeñas ampollas y picazón).
Muy raras (que ocurren con una frecuencia inferior a 1 de cada 10 000 pacientes):
hipertiroidismo (actividad excesiva de la glándula tiroides que causa aumento del apetito, pérdida de peso, sudoración, latido cardíaco rápido o inquietud) en pacientes con enfermedad tiroides en la historia clínica.
Reacciones adversas con frecuencia desconocida(en base a los datos disponibles, no se puede determinar la frecuencia de su aparición):
- Después de un uso más prolongado o intenso de povidona yodada, puede ocurrir hipotiroidismo (actividad insuficiente de la glándula tiroides que causa fatiga, aumento de peso, latido cardíaco lento).
- Alteraciones de la función renal, insuficiencia renal aguda;
- Alteraciones electrolíticas (falta de equilibrio de líquidos y sales en la sangre),
- Acidosis metabólica (estado de aumento de la acidez de la sangre que puede causar respiración acelerada, desorientación o letargo),
- Alteraciones de la osmolalidad de la sangre (que se refiere al grado de concentración de la sangre) pueden ocurrir después de la ingesta de grandes cantidades de povidona yodada.
- Decoloración transitoria de la piel en el lugar de aplicación.
Notificación de reacciones adversas
Si ocurren algún efecto adverso, incluidos todos los efectos adversos no mencionados en la hoja de instrucciones, debe informar a su médico o farmacéutico. Las reacciones adversas pueden notificarse directamente al Departamento de Vigilancia de Reacciones Adversas de Medicamentos del Instituto de Salud Pública.
Las reacciones adversas también pueden notificarse al titular de la autorización de comercialización.
Gracias a la notificación de reacciones adversas, podrá recopilarse más información sobre la seguridad del medicamento.
5. Cómo conservar Betadine VAG
Conservar en el refrigerador (2-8°C).
El medicamento debe conservarse en un lugar donde no pueda ser visto ni alcanzado por los niños. No use este medicamento después de la fecha de caducidad indicada en el paquete: Fecha de caducidad (EXP). La fecha de caducidad indica el último día del mes indicado.
No debe tirar los medicamentos por el desagüe ni por los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este comportamiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Betadine VAG?
El principio activo del medicamento es povidona yodada.
Cada óvulo contiene 200 mg de povidona yodada.
El otro componente del medicamento es macrogol 1000.
Cómo se presenta Betadine VAG y qué contiene el paquete?
El medicamento tiene la forma de óvulos. Cada óvulo es uniforme, de color marrón-rojizo, con forma de torpedo, de aproximadamente 33 mm de largo y 12 mm de diámetro. El paquete del medicamento contiene 7 óvulos (1 blister de PVC/PE), colocados en una caja de cartón.
Título del responsable
Egis Pharmaceuticals PLC.
1106 Budapest, Keresztúri út 30-38.
Hungría
Fabricante
Egis Pharmaceuticals PLC Fábrica de Lacta
Mátyás király u. 65
9900 Körmend
Hungría
Para obtener información más detallada sobre este medicamento, debe ponerse en contacto con el representante local del titular de la autorización de comercialización:
EGIS Polska Sp. z o.o.
ul. Komitetu Obrony Robotników 45D
02-146 Varsovia
Teléfono: +48 22 417 92 00
Fecha de la última actualización de la hoja de instrucciones:
- País de registro
- Principio activo
- Requiere recetaNo
- Fabricante
- ImportadorEgis Pharmaceuticals Ltd.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a Betadine VagForma farmacéutica: Supositorios, 200 mgPrincipio activo: Povidona iodadaNo requiere recetaForma farmacéutica: Supositorios, 90 mgPrincipio activo: policresulenFabricante: Takeda GmbHNo requiere recetaForma farmacéutica: Crema, 10 mg/gPrincipio activo: ciclopiroxFabricante: Doppel Farmaceutici S.r.l.No requiere receta
Alternativas a Betadine Vag en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Betadine Vag en Ukraine
Alternativa a Betadine Vag en Spain
Médicos online para Betadine Vag
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Betadine Vag – sujeta a valoración médica y normativa local.