CLARELUX 500 micrograms/g CUTANEOUS FOAM IN A PRESSURIZED CONTAINER


How to use CLARELUX 500 micrograms/g CUTANEOUS FOAM IN A PRESSURIZED CONTAINER
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show translationContents of the leaflet
Introducción
Prospecto: información para el usuario
CLARELUX 500 microgramos/g espuma cutánea en envase a presión
Propionato de clobetasol
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es CLARELUX y para qué se utiliza
- Qué necesita saber antes de empezar a usar CLARELUX
- Cómo usar CLARELUX
- Posibles efectos adversos
- Conservación de CLARELUX
- Contenido del envase e información adicional
1. Qué es CLARELUX y para qué se utiliza
CLARELUX contiene propionato de clobetasol como principio activo y pertenece a un grupo de medicamentos conocidos como corticoesteroides tópicos. Propionato de clobetasol es un corticoesteroide tópico muy potente.
CLARELUX 500 microgramos/g espuma cutánea en envase a presión es una espuma que se aplica en la piel.
CLARELUX 500 microgramos/g espuma cutánea en envase a presión se utiliza, en pacientes adultos y adolescentes a partir de los 12 años, como un tratamiento a corto plazo de las dermatosis del cuero cabelludo con respuesta a esteroides, como: la psoriasis, que no responde de forma satisfactoria a esteroides menos potentes.
2. Qué necesita saber antes de empezar a usar CLARELUX
No useCLARELUX:
- Si es alérgico al propionato de clobetasol, a otros corticosteroides o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
- Si tiene lesiones cutáneas infectadas, ya sea víricas (p. ej. Herpes simple, herpes zoster, varicela…), bacterianas (p. ej. impétigo), fúngicas (causadas por hongos microscópicos) o parasitarias.
- Si tiene quemaduras, lesiones ulcerativas u otros trastornos de la piel como rosácea, acné, dermatitis alrededor de la boca.
- Si tiene picor cerca del ano o en los genitales.
- En otra zona del cuerpo o cara (incluyendo los párpados) que no sea el cuero cabelludo.
- En aplicación en los párpados (riesgo de daño al nervio del ojo (glaucoma) y opacidad del cristalino (cataratas)).
- En niños menores de 2 años.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar CLARELUX.
Informe a su médico si anteriormente ha tenido alergia a los corticosteroides y/o a algún componente de este medicamento.
Debe consultar con su médico e interrumpir immediatamente el tratamiento si su condición empeora durante el uso, es posible que esté experimentando una reacción alérgica, si presenta signos como erupción de la piel, picor o hinchazón del tejido sin dolor (edema), si tiene una infección o si su afección requiere un tratamiento diferente.
Debe evitar el tratamiento a largo plazo.
Si experimenta una reaparición de su afección poco después (dentro de las 2 semanas) de suspender el tratamiento, no reinicie el uso de CLARELUX sin consultar a su médico, a menos que su médico le haya aconsejado previamente. Si su afección se ha resuelto y, en caso de recurrencia, el enrojecimiento se extiende más allá del área de tratamiento inicial y experimenta una sensación de ardor, consulte con un médico antes de reiniciar el tratamiento, ya que podría sospecharse de un efecto rebote. (ver sección 4).
Debido al deterioro de la barrera cutánea, existe el riesgo de aparición repentina de pústulas dolorosas llenas de líquido no infeccioso que pueden ir acompañadas de fiebre (psoriasis pustulosa generalizada) o de aparición de toxicidad local o sistémica.
Evitar el contacto con los ojos o las mucosas (nariz, boca).
No aplique CLARELUX en los párpados ni en el rostro debido al riesgo de opacidad del cristalino (cataratas) y aumento de la presión ocular (glaucoma), que pueden causar daños irreversibles en los ojos. Consulte a su médico si experimenta visión borrosa u otras alteraciones visuales.
Se debe lavar las manos cuidadosamente después de cada aplicación. No se toque los ojos hasta que te hayas lavado las manos.
En caso de contacto accidental con la cara o los ojos, debe lavarse con abundante agua.
A menos que lo supervise un médico, se debe evitar la aplicación de CLARELUX sobre una superficie extensa o en zonas vendadas o cubiertas, debido al riesgo de que parte del principio activo pase a al torrente sanguineo. Puede producirse una infección bacteriana, facilitada por el calor y la humedad de la piel en vendajes oclusivos. No utilice un vendaje oclusivo a menos que se lo indique su médico. En este caso, debe limpiarse la piel antes de cada cambio de vendaje.
Informe a su médico sobre cualquier irritación o infección, ya que se deberá administrar el tratamiento adecuado si se produce una infección. Si la infección se propaga, se debe suspender el tratamiento con CLARELUX y tratarse.
Al igual que con todos los corticorsteroides, CLARELUX puede ser absorbido a través de la piel con riesgo de que el principio activo pase la sangre causando efectos adversos como la disminución de la producción de hormonas de las glándulas suprarrenales (supresión del sistema pituitario suprarrenal) y el síndrome de Cushing ver sección 4. para todos los posibles efectos adversos. El riesgo de que este corticosteroide pase al torrente sanguineo aumenta en las siguientes situaciones:
- Tratamiento prolongado.
- Aplicación en áreas muy extensas.
- Aplicación en zonas vendadas o cubiertas, como apósitos oclusivos.
- Aplicación sobre piel dañada o lesionada, como heridas o llagas abiertas (ulceraciones).
- Aplicación en zonas de piel fina como el rostro.
- Mayor hidratación de la piel.
Informe a su médico si:
- Experimenta dolor óseo de reciente aparición o un empeoramiento de los síntomas óseos previos durante el tratamiento con CLARELUX, especialmente si ha estado usando CLARELUX durante un periodo prolongado de tiempo o repetidamente.
- Está usando otro medicamento oral o tópico que contiene corticosteroides o medicamentos para el control de su sistema inmune (por ejemplo, enfermedad autoinmune o después de un trasplante). La combinación de CLARELUX con estos medicamentos puede resultar en infecciones graves.
- Su afección no mejora después de 2 semanas de tratamiento.
- Desarrolla una infección, ya que debe ser retirado el tratamiento con CLARELUX y administración de terapia antimicrobiana adecuada.
Uso en niños y adolescentes
No se recomienda su uso en niños menores de 12 años.
Otros medicamentos y CLARELUX
Informe a su médico o farmacéutico si está utilizando o ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento.
Uso de CLARELUX con alimentos, bebidas y alcohol
No aplicable
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
Embarazo
CLARELUX no debe utilizarse durante el embarazo a menos que lo indique su médico.
Lactancia
CLARELUX no debe utilizarse durante la lactancia a menos que lo indique su médico.
Conducción y uso de máquinas
CLARELUX no debería afectar la capacidad para conducir y utilizar máquinas.
Información importante sobre algunos de los componentes de CLARELUX
Este medicamento contiene:
- 2145 mg de alcohol (etanol) en cada aplicación, puede causar sensación de ardor en piel lesionada,
- 74 mg de propilenglicol (E 1520) en cada aplicación,
- alcohol cetílico y alcohol estearílico, que pueden producir reacciones locales en la piel (como dermatitis de contacto),
- polisorbato 60 (E 435) pueden causar reacciones alérgicas.
3. Cómo usar CLARELUX
ATENCIÓN:
El envase contiene un líquidopresurizado inflamable.
No lo utilice o almacene cerca de una llama, de una fuente de ignición, de cualquier material que genere calor o productos eléctricos en funcionamiento.
No fumar mientras está utilizando o agarrando el envase.
Siga exactamente las instrucciones de administración de CLARELUX indicadas por su médico. Consulte a su médico o farmacéutico si tiene dudas.
Use esta medicación únicamente para la condición para la cual se le prescribió. CLARELUX debe aplicarse únicamente en el cuero cabelludo y no debe tragarse.
No se recomienda, dispensar la espuma directamente en las manos, ya que la espuma empezará a deshacerse inmediatamente al entrar en contacto con la piel caliente.
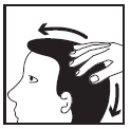
Aplique CLARELUX sobre la zona afectada del cuero cabelludo dos veces al día, una por la mañana y otra por la noche, como se indica a continuación:
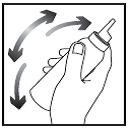
Atención: ¡para una adecuada dispensación de la espuma, es importante mantener el envase boca abajo!
|
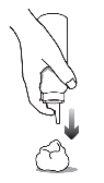
|
CLARELUX se debe aplicar en una capa fina, por lo que debe usar la mínima cantidad cuando lo aplica a la zona afectada. La cantidad exacta que necesita depende del tamaño de la zona afectada. No dispense la espuma en las manos, ya que empezará a deshacerse inmediatamente al entrar en contacto con la piel caliente. |
|
|
|
Después de haberse aplicado CLARELUX, lávese las manos y elimine cualquier cantidad del medicamento sin utilizar.
No utilice CLARELUX en la cara o a los párpados. Si accidentalmente le entra espuma en los ojos, nariz o en la boca, lávese inmediatamente con agua fría. Tendrá una sensación de escozor. Contacte con su médico si el dolor continúa.
Las zonas tratadas no deberán vendarse ni cubrirse a menos que así se lo indique su médico.
No se lave ni se aclare las zonas tratadas del cuero cabelludo inmediatamente después de la aplicación de CLARELUX.
Duración del tratamiento
No utilice más de 50 g de CLARELUX por semana.
El tratamiento no debe continuar más de 2 semanas. Después de este uso CLARELUX puede utilizarse ocasionalmente si es necesario. Alternativamente su médico puede prescribirle un esteroide más débil para controlar su afección.
Si usa másCLARELUXdel que debe
Consulte a su médico inmediatamente si usted se ha aplicado CLARELUX:
en cantidades mayores de las prescritas o durante un período más largo de lo prescrito. En estos casos, existe el riesgo de que el principio activo pase la sangre, causando efectos adversos como síntomas de hipercorticoidismo (aumento de peso, acumulación de grasa facial, hipertensión arterial). El uso de CLARELUX debe suspenderse gradualmente y bajo supervisión médica, reduciendo la frecuencia de aplicación o sustituyéndolo por un corticosteroide menos potente.
En caso de sobredosis o ingestión accidental, consulte inmediatamente a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono 91 562 04 20 indicando el medicamento y la cantidad utilizada.
Si olvidó usarCLARELUX
Se debe utilizar tan pronto como sea posible, después continuar como antes.
Si se acuerda al aplicar la siguiente dosis, utilice una única dosis y continúe el tratamiento como ha descrito el médico (no aplique una dosis doble para compensar las dosis olvidadas). Si ha olvidado varias dosis, informe a su médico.
Si interrumpe el tratamiento conCLARELUX
No interrumpa el tratamiento de repente ya que puede producirle algún daño. Su médico deberá discontinuar el tratamiento gradualmente y deberá hacerse revisiones regulares.
Si tiene cualquier otra duda sobre el uso de este producto, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Deje de usar CLARELUX 500 microgramos/g espuma cutánea en envase a presión y póngase en contacto con su médico inmediatamente si se producen reacciones alergicas ( hipersensibilidad), tales como irritación local.
Los efectos adversos incluyen:
Frecuentes (puede afectar a menos de 1 de cada 10, pero en más de 1 de cada 100 personas):
- Sensación de escozor de piel donde se aplica CLARELUX
- Otras reacciones cutáneas donde se aplica CLARELUX
Raras (puede afectarhasta 1 de cada 1.000 personas):
- Psoriasis pustulosa (inflamación crónica de la piel acompañada de pústulas)
Muy raras (puede afectar hasta 1 de cada 10.000 personas):
- Disminución de la producción de hormonas de las glándulas suprarrenales (supresión del sistema hipotálamo-hipofisario-suprarrenal)
- Sensación como entumecimiento, hormigueo o pinchazo (parestesia)
- Irritación ocular
- Hinchazón vasos sanguíneos (vasodilatación)
- Irritación de la piel, dolor en la piel (sensibilidad), tirantez de la piel
- Erupción de la piel que produce picor (dermatitis de contacto), inflamación de la piel (dermatitis)
- Empeoramiento de la psoriasis
- Enrojecimiento (eritema) en el lugar de aplicación
- Picor (purito) en el lugar de aplicación
- Dolor
- Presencia de sangre, proteínas y nitrógeno en orina
- Alteraciones en el análisis de sangre que indican que los glóbulos rojos son más grandes que el promedio (volumen celular medio aumentado)
Pueden incluirse los siguientes efectos adversos adicionales con frecuencia no conocida (no puede estimarse a partir de los datos disponibles):
- Puede producirse una infección secundaria, sobre todo si el tratamiento se cubre con un vendaje oclusivo o se aplica en pliegues cutáneos (axilas, región anal y genital). Los signos de infección incluyen enrojecimiento de la piel, posiblemente acompañado de dolor o picazón
- vello excesivo (hipertricosis)
- Cambios en el color de la piel
- Inflamación de los folículos capilares (foliculitis)
- Erupción en la boca (dermatitis perioral)
- Enrojecimiento y erupciones en la cara (dermatitis similar a la rosácea)
- Retraso en la cicatrización de heridas
- Opacidad del cristalino del ojo (cataratas), aumento de la presión en el ojo (glaucoma)
- Visión borrosa
Efectos adversos debido al uso prolongado con frecuencia no conocida (no puede estimarse a partir de los datos disponibles):
- Al igual que con otros corticosteroides tópicos, cuando CLARELUX se usa en grandes cantidades y durante un periodo largo de tiempo, esto puede conducir al llamado síndrome de Cushing que incluyen signos como aumento de peso, acumulación de grasa en la cara y hematomas causados ??por un exceso de hormona corticosteroide
- Reacción de retirada de corticoesteroides tópicos (efecto rebote): enrojecimiento de la piel que puede extenderse más allá del área tratada inicialmente, sensación de ardor o escozor, picazón intensa, descamación de la piel, llagas abiertas supurantes
- Cambios locales en la piel como adelgazamiento (atrofia cutánea) y fragilidad, hematomas coloridos (equimosis), pequeños vasos sanguíneos visibles (telangiectasias) especialmente en la cara, estrías que afectan particularmente las extremidades proximales
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de CLARLEUX
- El envase contiene unlíquido presurizado inflamable.
- No lo almacene cerca de una llama, de una fuente de ignición, de material que genere calor o productos eléctricos en funcionamiento.
- No lo exponga a temperaturas superiores a50ºCni a la luz solar directa.
- No perforar ni quemar el envase, incluso si está vacío.
- Cuando finalice el tratamiento,elimine el envase de forma segura.
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice CLARELUX después de la fecha de caducidad que aparece en el envase después de CAD. La fecha de caducidad es el último día del mes que se indica.
No conservar a temperatura superior a 25°C. No refrigerar. Conservar en posición vertical.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia.En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición deCLARELUX
El principio activo es propionato de clobetasol y 1 g de espuma cutánea contiene 500 microgramos de propionato de clobetasol.
Los demás componentes son: etanol anhidro, agua purificada, propilenglicol (E 1520), alcohol cetílico, alcohol estearílico, polisorbato 60 (E 435), ácido cítrico anhidro, citrato potásico y una mezcla propelente de propano/n-butano/isobutano.
Aspecto del producto y contenido del envase
CLARELUX 500 microgramos/g espuma cutánea es una espuma cutánea blanca en envase a presión. Cada envase contiene 50 ó 100 gramos.
No todos los envases pueden estar comercializados.
Titular de la autorización de comercialización
PIERRE FABRE IBÉRICA, S.A.
C/ Ramón Trias Fargas, 7-11
08005 Barcelona - España
Responsable de la fabricación
Recipharm Uppsala AB
Björkgatan 30
751 82 Uppsala
Suecia
o
Farmol Health Care S.r.L.
Via del Maglio, 6
23868 Valmadrera (LC)
Italia
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeoy en el Reino Unido (Irlanda del Norte)con los siguientes nombres:
Alemania y Austria:CLARELUX 500 Mikrogramm/g Schaum zur Anwendung auf der Haut im Druckbehältnis
Bélgica y Luxemburgo:CLARELUX 500 microgrammes/g mousse pour application cutanée en flacon pressurisé
República Eslovaca:CLARELUX 500 mikrogramov/g dermalna pena, v tlakovom obale
República Checa:CLARELUX 500 mikrogramu/g kožní pena
Francia: CLARELUX 500 microgrammes/g mousse pour application cutanée en flacon pressurisé
Grecia:CLARELUX 500 μικρογραμμ?ρια/g δερματικ?ς αφρ?ς σε περι?κτη υπ? π?εση
Reino Unido (Irlanda del Norte):CLARELUX 500 microgram/g cutaneous foam in pressurised container
Países Bajos:CLARELUX 500 microgram/g schuim voor cutaan gebruik in spuitbus
Polonia:Clarelux 500 mikrogramów/g, piana na skóre
Portugal:CLARELUX 500 microgramas/g espuma cutânea num recipiente pressurizado
Italia:OLUX 500 microgrammi/g schiuma cutanea
Fecha de la última revisión de este prospecto: Mayo 2025
“La información detallada y actualizada de este medicamento está disponible en la página Web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) https://www.aemps.gob.es/”
- Country of registration
- Dosage formTOPICAL SOLUTION, 0.05%
- ATC codeD07AD01
- Average pharmacy price8.7 EUR
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to CLARELUX 500 micrograms/g CUTANEOUS FOAM IN A PRESSURIZED CONTAINERDosage form: SHAMPOO, 500 mcg clobetasol propionate/gActive substance: clobetasolManufacturer: Laboratorios Galderma S.A.Prescription requiredDosage form: TOPICAL SOLUTION, 500 micrograms/gActive substance: clobetasolManufacturer: Isdin S.A.Prescription requiredDosage form: SHAMPOO, 500 µg/gActive substance: clobetasolManufacturer: Industrial Farmaceutica Cantabria S.A.Prescription required
Online doctors for CLARELUX 500 micrograms/g CUTANEOUS FOAM IN A PRESSURIZED CONTAINER
Discuss questions about CLARELUX 500 micrograms/g CUTANEOUS FOAM IN A PRESSURIZED CONTAINER, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions