
Пгармавате
Спросите врача о рецепте на Пгармавате

Инструкция по применению Пгармавате
Инструкция, прилагаемая к упаковке: информация для пользователя
Фармават, 50 МЕ/мл, порошок и растворитель для приготовления раствора для инъекций
Человеческий фактор VIII свертывания крови Фармават, 100 МЕ/мл, порошок и растворитель для приготовления раствора для инъекций
Человеческий фактор VIII свертывания крови
Прежде чем использовать лекарство, необходимо ознакомиться с содержанием инструкции, поскольку она содержит важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы иметь возможность повторно прочитать ее при необходимости.
- В случае любых дальнейших сомнений необходимо обратиться к врачу, фармацевту или медсестре.
- Это лекарство назначено конкретному человеку. Не следует передавать его другим. Лекарство может навредить другому человеку, даже если симптомы его заболевания такие же.
- Если любой из нежелательных эффектов ухудшится или появятся какие-либо нежелательные эффекты, включая те, которые не указаны в этой инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре.
Содержание инструкции:
- 1. Что такое лекарство Фармават и для чего оно используется
- 2. Важные сведения перед использованием лекарства Фармават
- 3. Как использовать лекарство Фармават
- 4. Возможные нежелательные эффекты
- 5. Как хранить лекарство Фармават
- 6. Содержание упаковки и другие сведения
1. Что такое лекарство Фармават и для чего оно используется
Фармават относится к группе лекарств, называемых факторами свертывания, и содержит человеческий фактор VIII свертывания крови. Это специальное белок, которое увеличивает способность крови свертываться.
Фармават используется для лечения и профилактики кровотечений у пациентов с гемофилией А. Это состояние, при котором наблюдается длительное кровотечение по сравнению с ожидаемым. Оно возникает из-за врожденного дефицита фактора VIII свертывания крови в крови.
2. Важные сведения перед использованием лекарства Фармават
Рекомендуется, чтобы при каждом введении пациенту дозы Фармавата записать название и номер серии продукта для сохранения информации о использованной серии.
Врач может рекомендовать рассмотреть возможность вакцинации против вирусного гепатита А и Б в случае регулярного или повторного получения продуктов фактора VIII человеческого происхождения.
Когда не использовать лекарство Фармават
- если пациент имеет аллергическую реакцию на человеческий фактор VIII свертывания крови или любой другой компонент этого лекарства (указанный в пункте 6).
Предостережения и меры предосторожности
Прежде чем начать принимать Фармават, необходимо обратиться к врачу, фармацевту или медсестре.
Фармават содержит следовые количества других человеческих белков. Любое лекарство, содержащее белки и вводимое в вену (внутривенно), может вызывать аллергические реакции (см. пункт 4. Возможные нежелательные эффекты).
Формирование ингибиторов (антител) является известным осложнением, которое может возникать во время лечения всеми лекарствами, содержащими фактор VIII. Эти ингибиторы, особенно при высоких концентрациях, нарушают правильное лечение, и пациент будет тщательно отслеживаться на предмет образования этих ингибиторов. Если кровотечение у пациента не контролируется должным образом с помощью лекарства Фармават, необходимо немедленно сообщить об этом врачу.
Сведения о крови и плазме, использованных для производства Фармавата
Во время производства лекарств из человеческой крови или плазмы принимаются определенные меры для предотвращения передачи инфекций пациентам. Они включают тщательный отбор доноров крови и плазмы для обеспечения исключения доноров, которые могут быть носителями инфекций, а также тестирование всех полученных проб и пула плазмы для обнаружения вирусов/инфекций. Производители этих продуктов ввели в процесс обработки крови или плазмы этапы, направленные на инактивацию или удаление вирусов. Несмотря на эти меры, при введении лекарств, приготовленных из человеческой крови или плазмы, нельзя полностью исключить возможность передачи инфекции. Это относится также к неизвестным или недавно появившимся вирусам или другим типам инфекций.
Принимаемые меры считаются эффективными против вирусов с оболочкой, таких как вирус иммунодефицита человека (ВИЧ), вирус гепатита Б (ВГБ) и вирус гепатита С (ВГС), а также против безоболочечного вируса гепатита А (ВГА). Применяемые методы могут иметь ограниченную эффективность против безоболочечных вирусов, таких как парвовирус В19.
Инфекция парвовирусом В19 может быть опасна для беременных женщин (инфекция плода) и для людей, у которых иммунная система подавлена или которые страдают от определенных видов анемии (например, серповидно-клеточной анемии или неправильного распада красных кровяных клеток).
Другие лекарства и Фармават
Необходимо сообщить врачу или фармацевту о всех лекарствах, принимаемых в настоящее время или недавно, а также о лекарствах, которые пациент планирует принимать, включая те, которые отпускаются без рецепта.
Не известны взаимодействия человеческого фактора VIII свертывания крови с другими лекарственными продуктами.
Однако не следует смешивать Фармават с другими лекарствами во время инфузии.
Беременность и грудное вскармливание
Во время беременности и в период грудного вскармливания или если существует подозрение, что женщина беременна, или если она планирует беременность, перед использованием этого лекарства необходимо проконсультироваться с врачом или фармацевтом.
Вождение транспортных средств и эксплуатация машин
Не наблюдалось влияния на способность управлять транспортными средствами и эксплуатировать машины.
Лекарство Фармават содержит:
В случае флакона 250 МЕ продукт содержит менее 1 ммоль натрия (23 мг) на дозу, то есть лекарство считается «безнатриевым».
В случае флакона 500 МЕ и 1000 МЕ продукт содержит максимум 1,75 ммоль натрия (40 мг) на дозу. Это соответствует 2% максимальной рекомендуемой суточной дозы натрия для взрослых. Необходимо учитывать это у пациентов, следующих диете с контролируемым содержанием натрия.
3. Как использовать лекарство Фармават
Фармават должен быть введен внутривенно после реconstitution в прилагаемом растворителе.
Лечение должно быть начато под медицинским наблюдением.
Дозирование для профилактики кровотечений:
При длительной профилактике кровотечений у пациентов с тяжелой формой гемофилии А следует вводить фактор VIII в дозе 20 до 40 МЕ на килограмм массы тела с интервалом 2 до 3 дней.
Дозу необходимо корректировать в зависимости от клинической реакции. В некоторых случаях может быть необходимо введение лекарства в более короткие интервалы или в более высоких дозах.
Расчет дозы:
Фармават всегда должен использоваться в соответствии с рекомендациями врача. В случае сомнений необходимо повторно обратиться к врачу или фармацевту.
Активность фактора VIII в плазме соответствует содержанию фактора VIII в плазме. Она выражается либо в процентах (относительно нормальной человеческой плазмы) либо в международных единицах (МЕ).
Доза фактора VIII выражается в МЕ.
Одна международная единица (МЕ) активности фактора VIII равна количеству фактора VIII в 1 мл нормальной человеческой плазмы. 1 МЕ фактора VIII на килограмм массы тела увеличивает активность плазменного фактора VIII на 1,5% - 2% нормальной активности. Для расчета необходимой дозы необходимо определить активность фактора VIII в плазме пациента. Это позволит определить, насколько необходимо увеличить активность.
Необходимо проконсультироваться с врачом в случае неопределенности, насколько необходимо увеличить активность фактора VIII в плазме и как рассчитать необходимую дозу.
Требуемая доза рассчитывается по следующей формуле:
требуемое количество единиц = масса тела (кг) x необходимый рост активности фактора VIII
(%) (МЕ/мл) x 0,5
Количество, которое должно быть введено, и частота введения продукта всегда должны корректироваться в зависимости от клинической эффективности у отдельного пациента.
В следующих случаях кровотечения активность фактора VIII не должна снижаться ниже указанного уровня активности плазмы (в % от нормальных значений) в течение указанного периода.
Следующая таблица может быть полезна для определения доз при кровотечениях или хирургических процедурах:
| Степень кровотечения / Тип хирургической процедуры | Необходимый уровень фактора VIII (%) (МЕ/мл) | Частота введения (часы)/ Продолжительность терапии (дни) |
| Кровотечение | ||
| Раннее кровотечение в суставах, мышцах или из полости рта | 20-40 | Повторять каждые 12 до 24 часов. Не менее 1 дня до тех пор, пока боль, вызванная кровотечением, не уменьшится или рана не заживет. |
| Более сильное кровотечение в суставах, мышцах или гематома | 30-60 | Повторять инфузию каждые 12 до 24 часов в течение 3-4 дней или более до тех пор, пока боль и функция не восстановятся. |
| Кровотечения, угрожающие жизни | 60-100 | Повторять инфузию каждые 8 до 24 часов до тех пор, пока угроза не минует. |
| Операции | ||
| Меньшие, включая удаление зуба | 30-60 | Каждые 24 часа, не менее 1 дня, до заживления. |
| Более крупные | 80-100 (до и после операции) | Повторять инфузию каждые 8 до 24 часов до тех пор, пока рана не заживет, затем продолжать терапию не менее 7 последующих дней для поддержания активности фактора VIII на уровне 30% до 60%. |
Доза и частота введения Фармавата будут определены врачом.
Ответ на фактор VIII может различаться у отдельных пациентов. Поэтому во время лечения рекомендуется определять уровни фактора VIII для определения подходящей дозы и частоты введения инфузии.
Использование у детей
В клинических исследованиях не было выявлено особых требований к дозированию у детей. Дозирование такое же, как у взрослых и детей, как в лечении, так и в профилактике.
Инструкция по использованию в домашних условиях
- Необходимо прочитать все инструкции и тщательно их соблюдать!
- Не использовать продукт Фармават после истечения срока годности, указанного на этикетке.
- Во время описанной ниже процедуры необходимо соблюдать стерильные условия!
- Раствор в шприце должен быть прозрачным или слегка перламутровым, блестящим. Не вводить растворы, которые являются мутными или содержат твердые частицы.
- Приготовленный раствор необходимо использовать немедленно для предотвращения микробиологического загрязнения.
- Использовать только прилагаемый набор для инъекций. Использование другого оборудования для инъекций/инфузии может привести к дополнительным рискам и неудачам в лечении.
Инструкция по приготовлению раствора с использованием системы Mix2Vial:
- 1. Не использовать продукт непосредственно после извлечения из холодильника. Оставить растворитель и порошок в закрытых флаконах до достижения комнатной температуры.
- 2. Удалить крышки с обоих флаконов и очистить резиновые пробки одним из прилагаемых ватных шариков, смоченных в спирте.
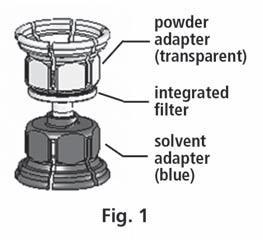
- 3. Система Mix2Vial представлена на рис. 1. Поместить флакон с растворителем на плоскую поверхность и крепко удерживать. Взять систему Mix2Vial и повернуть. Поместить синюю часть Mix2Vial на верх флакона с растворителем и крепко нажать до щелчка (рис. 2 + 3).
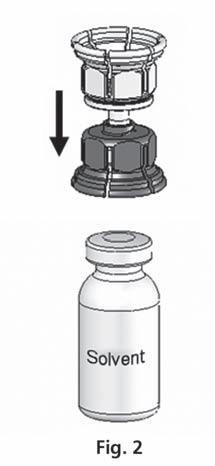
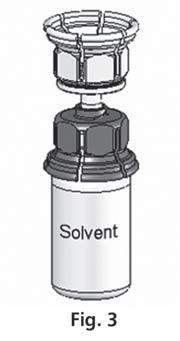
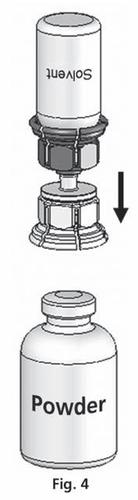
- 4. Поместить флакон с порошком на плоскую поверхность и крепко удерживать. Взять флакон с растворителем с подключенной системой Mix2Vial и повернуть его вверх дном. Поместить прозрачную часть набора на верх флакона с порошком и крепко нажать до щелчка (рис. 4). Растворитель автоматически переходит в флакон с порошком.
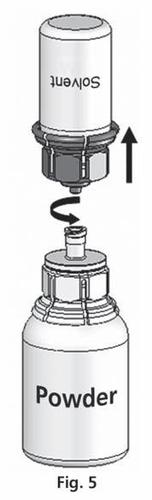
- 5. С одновременно подключенными обоими флаконами осторожно вращать флакон с порошком до тех пор, пока продукт не растворится. Фармават растворяется быстро при комнатной температуре до прозрачного раствора (рис. 5). Во время приготовления может образоваться незначительная пена. Отвернуть Mix2Vial на две части (рис. 6). Пена исчезнет.
Утилизировать пустой флакон с растворителем с синей частью Mix2Vial.
Инструкция по выполнению инъекции:
В качестве меры предосторожности необходимо перед инъекцией и во время инъекции проверить пульс.
В случае значительного увеличения частоты пульса необходимо уменьшить скорость введения или прервать введение лекарства.
- 1. Подключить шприц к прозрачной части Mix2Vial. Перевернуть флакон вверх дном и набрать раствор в шприц (рис. 6). Раствор в шприце должен быть прозрачным или слегка перламутровым, блестящим. После переноса раствора крепко удерживать поршень шприца (держа его направленным вниз) и удалить шприц из Mix2Vial (рис. 7). Утилизировать Mix2Vial и пустой флакон.
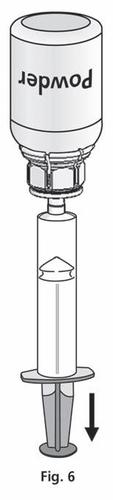
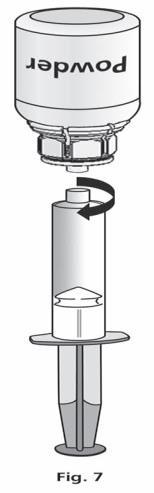
- 2. Очистить выбранное место инъекции одним из прилагаемых ватных шариков, смоченных в спирте.
- 3. Подключить прилагаемую иглу для инъекций к шприцу.
- 4. Ввести иглу в выбранную вену. В случае использования жгута для выявления вены необходимо ослабить жгут перед началом введения продукта Фармават. Кровь не должна попасть в шприц из-за риска образования фибриновых сгустков.
- 5. Раствор вводить медленно в вену, не быстрее 2-3 мл в минуту.
В случае использования более одного флакона с порошком Фармават во время одного введения возможно повторное использование той же иглы и шприца. Набор Mix2Vial предназначен только для одноразового использования.
Инструкция по приготовлению раствора с использованием передаточного набора (1 двусторонняя игла и 1 фильтрующая игла):
- 1. Не использовать продукт непосредственно после извлечения из холодильника. Необходимо согреть порошок и растворитель в закрытых флаконах до достижения комнатной температуры. Такую температуру необходимо поддерживать во время приготовления. Если для нагревания используется ванна, необходимо следить, чтобы вода не соприкасалась с резиновыми пробками (без латекса) или с колпачками флаконов. Температура водяной ванны не должна превышать +37°C.
- 2. Удалить крышки с флакона с порошком и флакона с растворителем (рис. 1) и очистить резиновые пробки одним из прилагаемых ватных шариков, смоченных в спирте (рис. 2).
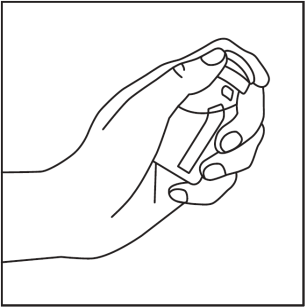
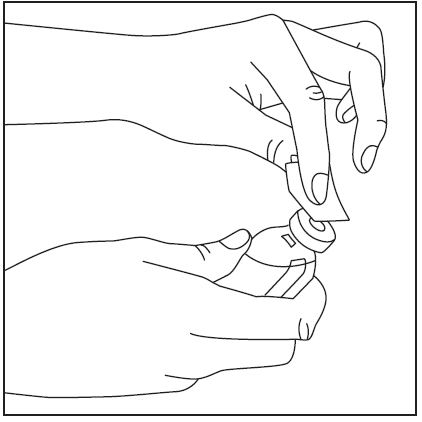
рис.1
рис.2
рис.1
рис.2
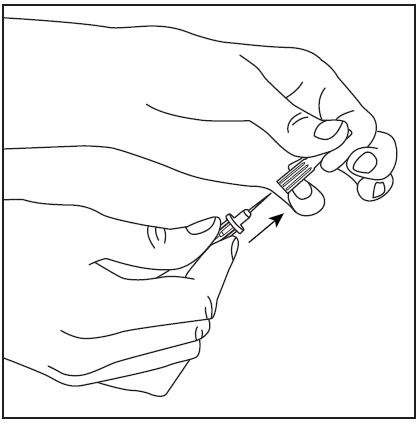
- 3. Снять защитный чехол с короткого конца двусторонней иглы (рис. 3), убедившись, что не коснулись открытого конца иглы. Затем проколоть центр резиновой пробки флакона с растворителем иглой вертикально (рис. 4). Для полного удаления жидкости из флакона с растворителем иглу необходимо ввести в пробку так, чтобы она входила в пробку и была видна в флаконе.
рис. 4
рис.3
рис.4
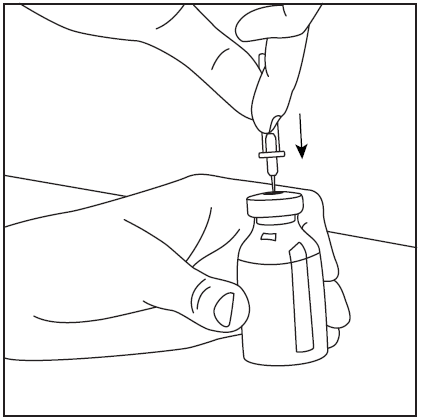
- 4. Снять защитный чехол с другого, длинного конца двусторонней иглы, убедившись, что не коснулись открытого конца иглы (рис. 5). Взять флакон с растворителем и введенную иглу вверх дном над флаконом с порошком и быстро проколоть иглой центр резиновой пробки флакона с порошком (рис. 6). Вакуум внутри флакона вызывает переход растворителя в флакон с порошком.
рис.6
рис.5
рис.6
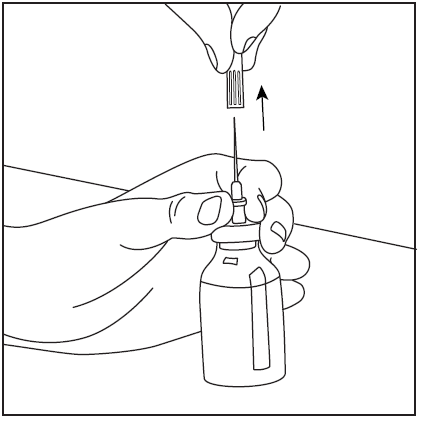
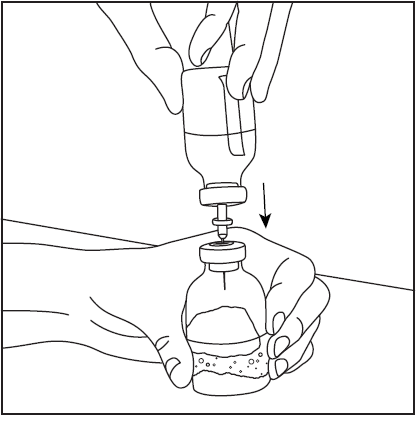
- 5. Удалить двустороннюю иглу вместе с пустым флаконом после растворителя (рис. 7), затем медленно вращать флакон с порошком и растворителем до тех пор, пока продукт не растворится. Фармават быстро растворяется при комнатной температуре до прозрачного раствора (рис. 8).
рис.8
рис.7
рис.8
Инструкция по выполнению инъекции:
В качестве меры предосторожности необходимо перед инъекцией и во время инъекции проверить пульс.
В случае значительного увеличения частоты пульса необходимо уменьшить скорость введения или прервать введение лекарства.
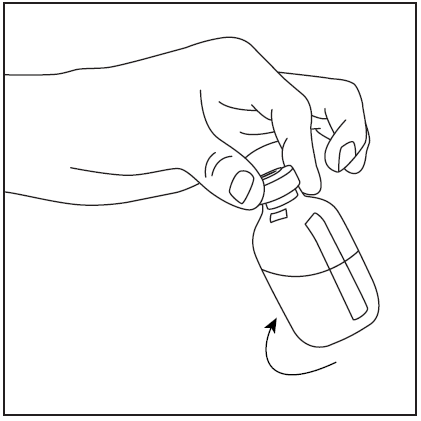
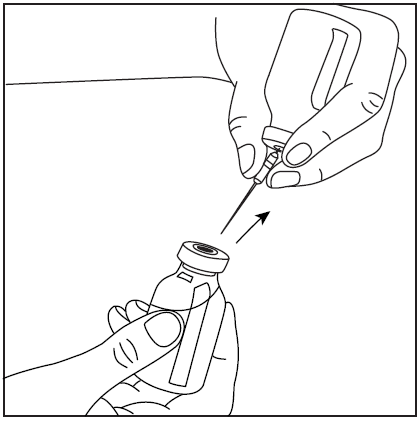
- 1. После приготовления порошка в соответствии с вышеуказанными инструкциями снять защитный чехол с фильтрующей иглы и проколоть резиновую пробку флакона с приготовленным концентратом.
- 2. Снять насадку фильтрующей иглы и подключить шприц.
- 3. Перевернуть флакон с подключенным шприцем вверх дном и набрать раствор в шприц.
- 4. Очистить выбранное место инъекции одним из прилагаемых ватных шариков, смоченных в спирте.
- 5. Снять фильтрующую иглу из шприца и подключить иглу для инфузии к шприцу.
- 6. Ввести раствор в вену, не быстрее 2-3 мл в минуту.
Любые неиспользованные остатки лекарственного продукта или его отходы необходимо утилизировать в соответствии с местными правилами.
Пациенты, использующие более одного флакона концентрата Фармават, могут использовать для инъекции одну и ту же иглу для инфузии и шприц, но фильтрующая игла предназначена только для одноразового использования.
При наборе раствора в шприц всегда необходимо использовать фильтрующую иглу.
Использование большей, чем рекомендуемая, дозы лекарства Фармават
Не наблюдалось симптомов передозировки человеческого фактора VIII свертывания крови. Однако рекомендуется не превышать рекомендуемую дозу.
Пропуск приема лекарства Фармават
Не следует использовать двойную дозу для компенсации пропущенной дозы. Необходимо немедленно перейти к следующей дозе и продолжать дозирование в соответствии с рекомендацией врача или фармацевта.
Необходимо обратиться к врачу или фармацевту в случае других вопросов, связанных с использованием этого продукта.
4. Возможные нежелательные эффекты
Как и любой лекарственный продукт, это лекарство может вызывать нежелательные эффекты, хотя они не возникают у каждого.
Несмотря на то, что они возникают редко(могут возникать у 1 человека из 1000), были отмечены случаи реакций повышенной чувствительности или аллергических реакций у пациентов, леченных продуктами, содержащими фактор VIII.
Необходимо обратиться к врачу, если возникают следующие симптомы:
рвота, ощущение жжения и парения в месте инъекции, ощущение сжатия в грудной клетке, озноб, тахикардия, тошнота, ощущение онемения, покраснение, головная боль, крапивница, снижение артериального давления, сыпь, беспокойство, отек лица, губ, полости рта, языка или горла, который может привести к затруднению глотания или дыхания (ангиоэдем), усталость (летаргия), свистящее дыхание.
Очень редко(могут возникать у 1 человека из 10 000) повышенная чувствительность может привести к возникновению угрожающей жизни аллергической реакции, называемой анафилаксией, которая может включать шок, а также часть или все вышеуказанные симптомы. В таком случае необходимо немедленно обратиться к врачу или вызвать скорую помощь.
Другие редкие нежелательные эффекты (могут возникать у 1 человека из 1000)
Лихорадка
В случае детей, не леченных ранее лекарствами, содержащими фактор VIII, могут образовываться блокирующие антитела (см. пункт 2) очень часто (более 1 из 10 пациентов). Однако у пациентов, ранее леченных фактором VIII (более 150 дней лечения), риск не очень часто встречается (менее 1 из 100 пациентов). Если это произойдет, лекарства пациента могут перестать действовать правильно, и у пациента может возникнуть продолжающееся кровотечение. Если это произойдет, необходимо немедленно обратиться к врачу.
Сведения, связанные с вирусной безопасностью, см. пункт 2. (Необходимо проявлять особую осторожность при использовании Фармавата).
Сообщение о нежелательных эффектах
Если возникают какие-либо нежелательные эффекты, включая те, которые не указаны в инструкции, необходимо сообщить об этом врачу или фармацевту.
Нежелательные эффекты можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных средств Управления по регистрации лекарственных средств, медицинских изделий и биоцидных продуктов
ул. Аллея Ерозолимских 181С
PL - 02-222 Варшава
тел.: +48 22 49 21 301
факс: +48 22 49 21 309
веб-сайт: https://smz.ezdrowie.gov.pl
Нежелательные эффекты можно сообщать также ответственному лицу.
Благодаря сообщению о нежелательных эффектах можно будет собрать больше информации о безопасности использования лекарства.
5. Как хранить лекарство Фармават
Лекарство должно храниться в месте, недоступном для детей.
Не использовать это лекарство после истечения срока годности, указанного на этикетке. Срок годности относится к последнему дню указанного месяца.
Хранить при температуре ниже 25°C.
Не замораживать.
Хранить в наружной упаковке для защиты от света.
Раствор после реconstitution необходимо использовать немедленно и только во время одного введения.
Не использовать это лекарство, если заметно, что раствор мутный или не полностью растворен.
Лекарства не следует выбрасывать в канализацию или домашние контейнеры для отходов. Необходимо спросить фармацевта, как утилизировать лекарства, которые больше не используются. Такое поведение поможет защитить окружающую среду.
6. Содержание упаковки и другие сведения
Что содержит лекарство Фармават
Активным веществомлекарства является человеческий фактор VIII свертывания крови.
Объем и концентрации
| Размер флакона с порошком Фармават (МЕ фактора VIII) | Размер флакона с растворителем (мл) для добавления к флакону с порошком Фармават | Номинальная концентрация раствора после реconstitution (МЕ фактора VIII/мл) |
| 250 МЕ | 5 | 50 |
| 500 МЕ | 10 | 50 |
| 1000 МЕ | 10 | 100 |
Другие компоненты: для порошка: цитрат натрия, хлорид натрия, хлорид кальция, глицерин; для растворителя: вода для инъекций
Как выглядит лекарство Фармават и что содержит упаковка
Фармават выпускается в виде порошка и растворителя для приготовления раствора для инъекций.
Белый или светло-желтый порошок или хрупкая масса.
Растворитель является чистой, бесцветной жидкостью.
3 доступных размера упаковки различаются содержанием фактора VIII и растворителем:
- 250 МЕ/флакон: после реconstitution в 5 мл концентрация составляет 50 МЕ/мл
- 500 МЕ/флакон: после реconstitution в 10 мл концентрация составляет 50 МЕ/мл
- 1000 МЕ/флакон: после реconstitution в 10 мл концентрация составляет 100 МЕ/мл
Все размеры упаковки содержат:
1 систему для передачи Mix2Vial, 1 шприц для одноразового использования, 1 иглу для инъекций и 2 ватных шарика, смоченных в спирте
или
1 передаточный набор (1 двусторонняя игла и 1 фильтрующая игла), 1 шприц для одноразового использования, 1 игла для инъекций и 2 ватных шарика, смоченных в спирте.
Не все размеры упаковки могут находиться в обращении.
Ответственное лицо
Octapharma (IP) SPRL
Route de Lennik 451
1070 Андерлехт
Бельгия
Производитель
Octapharma Pharmazeutika Produktionsges.m.b.H
Оberlaaer Str. 235
1100 Вена
Австрия
Octapharma S.A.S
72 Rue du Maréchal Foch
67380 Лингольсхайм
Франция
Octapharma AB
112 75 Стокгольм
Швеция
Дата последнего обновления инструкции: 01.01.2025
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- Производитель
- ИмпортерOctapharma AB Octapharma Pharmazeutika Produktionsges.m.g.H. Octapharma S.A.S.
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги ПгармаватеФорма выпуска: Порошок, 1000 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: CSL Behring GmbHТребуется рецептФорма выпуска: Порошок, 2000 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: CSL Behring GmbHТребуется рецептФорма выпуска: Порошок, 250 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: CSL Behring GmbHТребуется рецепт
Аналоги Пгармавате в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Пгармавате в Испания
Аналог Пгармавате в Украина
Врачи онлайн по Пгармавате
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Пгармавате – по решению врача и с учетом местных правил.














