
Емоцлот

Спросите врача о рецепте на Емоцлот

Инструкция по применению Емоцлот
Инструкция, прилагаемая к упаковке: информация для пользователя
ЭМОКЛОТ, 500 МЕ, порошок и растворитель для приготовления раствора
для инъекций и инфузий
ЭМОКЛОТ, 1000 МЕ, порошок и растворитель для приготовления раствора
для инъекций и инфузий
Человеческий фактор VIII свертывания крови
Прежде чем использовать лекарство, необходимо внимательно ознакомиться с содержанием инструкции, поскольку она содержит
важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу.
- Это лекарство назначено строго определённому человеку. Не следует его передавать другим. Лекарство может навредить другому человеку, даже если симптомы его болезни такие же.
- Если у пациента появляются любые нежелательные реакции, включая все нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу. См. пункт 4.
Содержание инструкции:
- 1. Что такое ЭМОКЛОТ и для чего он используется
- 2. Важная информация перед использованием лекарства ЭМОКЛОТ
- 3. Как использовать ЭМОКЛОТ
- 4. Возможные нежелательные реакции
- 5. Как хранить ЭМОКЛОТ
- 6. Содержание упаковки и другие сведения
1. Что такое ЭМОКЛОТ и для чего он используется
ЭМОКЛОТ является высокоочищенным концентратом фактора VIII свертывания крови, полученным из человеческой плазмы. Фактор VIII является белком с антигеморрагическим действием.
ЭМОКЛОТ используется:
- для лечения и профилактики кровотечений у пациентов с врожденным дефицитом фактора VIII (гемофилия А);
- для лечения кровотечений у пациентов с приобретенным дефицитом фактора VIII;
- для лечения пациентов с гемофилией и ингибиторами фактора VIII.
Это лекарство не содержит фармакологически эффективного количества фактора фон Виллебранда, поэтому не показано для лечения болезни фон Виллебранда.
2. Важная информация перед использованием лекарства ЭМОКЛОТ
Когда не использовать лекарство ЭМОКЛОТ
если пациент имеет аллергию на человеческий фактор VIII или любой другой компонент этого лекарства (указанный в пункте 6).
Предостережения и меры предосторожности
Прежде чем начать использовать лекарство ЭМОКЛОТ, необходимо обсудить это с врачом.
Гиперчувствительность
Возможно возникновение реакций гиперчувствительности типа аллергии, связанных с лекарством ЭМОКЛОТ.
ЭМОКЛОТ содержит следовые количества человеческих белков, кроме фактора VIII. Пациенты должны быть проинформированы о ранних симптомах реакций гиперчувствительности. Введение лекарства должно быть немедленно прекращено, если у пациента出现ят следующие симптомы, которые могут указывать на аллергию: сыпь, общая крапивница, чувство сдавления в груди, свистящее дыхание, низкое кровяное давление и острая аллергическая реакция.
В случае возникновения шока необходимо немедленно прекратить введение и действовать согласно рекомендациям по лечению шока.
Ингибиторы
Формирование ингибиторов (антител) является известным осложнением, которое может возникать во время лечения всеми лекарствами, содержащими фактор VIII. Эти ингибиторы, особенно при высоких концентрациях, нарушают правильное лечение, и пациент будет внимательно отслеживаться на предмет образования этих ингибиторов. Если кровотечение у пациента не контролируется должным образом после использования лекарства ЭМОКЛОТ, необходимо немедленно сообщить об этом врачу.
Сердечно-сосудистые события
У пациентов с существующими факторами риска сердечно-сосудистых заболеваний заместительная терапия фактором VIII может увеличивать риск сердечно-сосудистых осложнений.
Осложнения, связанные с введением через катетер
В случае необходимости использования устройства для введения в центральную вену необходимо учитывать риск осложнений, связанных с его применением, включая местную инфекцию, бактериемию и тромбоз в месте введения катетера.
Вирусная безопасность
В случае лекарств, производимых из человеческой крови или плазмы, принимаются соответствующие меры предосторожности для предотвращения передачи инфекции пациентам. Они включают:
- тщательный отбор доноров крови и плазмы, чтобы гарантировать, что исключены лица, подверженные риску носительства инфекции;
- исследование каждой донорской крови и пула плазмы (коллекции донорской крови) на вирусы и инфекцию.
- включение в процесс обработки крови или плазмы процедур, которые инактивируют или удаляют вирусы. Несмотря на эти меры предосторожности, нельзя полностью исключить возможность передачи инфекционных агентов через лекарство, приготовленное из человеческой крови или плазмы. Это относится также к неизвестным или недавно открытых вирусам и другим патогенам. Считается, что принимаемые меры предосторожности эффективны против вирусов с оболочкой, таких как вирус приобретенного иммунодефицита (ВИЧ), вирус гепатита Б (ВГБ) и вирус гепатита С (ВГС) и вирусов без оболочки, таких как вирус гепатита А (ВГА). Эти меры могут иметь ограниченную эффективность против вирусов без оболочки, таких как парвовирус В19. Инфекция парвовирусом В19 может быть вредной для беременных женщин (инфекция плода) и для пациентов с иммунодефицитом или некоторыми типами анемии (например, серповидно-клеточной анемии или гемолитической анемии).
Рекомендуется, чтобы каждый раз, когда вводится пациенту ЭМОКЛОТ, записывать название и номер серии продукта для определения в будущем, какую серию продукта получил пациент.
У пациентов, получающих регулярно или повторно фактор VIII из плазмы, необходимо учитывать соответствующие вакцинации (против вирусного гепатита А и В).
Дети и подростки
Указанные предостережения и меры предосторожности относятся как к взрослым, так и к детям.
Более подробную информацию см. в конце инструкции в разделе, предназначенном для медицинских специалистов.
Лекарство ЭМОКЛОТ и другие лекарства
Необходимо сообщить врачу или фармацевту о всех лекарствах, которые пациент принимает в настоящее время или принимал ранее, а также о лекарствах, которые пациент планирует принимать.
Не было зарегистрировано никаких взаимодействий фактора VIII с другими лекарствами.
Нет специальных данных о применении у детей.
Беременность и грудное вскармливание
- Если пациентка беременна или кормит грудью, предполагает, что может быть беременной или планирует иметь ребенка, она должна проконсультироваться с врачом перед использованием этого лекарства.
- Не проводились исследования влияния фактора VIII на репродукцию животных. Из-за редкого возникновения гемофилии А у женщин нет опыта применения фактора VIII у беременных и кормящих женщин. Поэтому фактор VIII может быть использован во время беременности и лактации только по строгим показаниям.
Вождение транспортных средств и эксплуатация машин
ЭМОКЛОТ не влияет на способность вождения транспортных средств и эксплуатации машин.
ЭМОКЛОТ содержит натрий
Лекарство содержит до 41 мг натрия (основного компонента поваренной соли) на флакон 10 мл. Это соответствует 2,05% максимальной рекомендуемой суточной дозы натрия в диете для взрослых.
3. Как использовать ЭМОКЛОТ
Это лекарство должно всегда использоваться в соответствии с рекомендациями врача. Лечение должно быть начато под контролем врача, имеющего опыт в лечении гемофилии.
Рекомендуемая доза
Дозирование и продолжительность заместительной терапии зависят от степени дефицита фактора VIII, от места и объема кровотечения и от клинического состояния пациента.
Лечение по требованию
При определении необходимой дозы и частоты введения необходимо руководствоваться клинической эффективностью в индивидуальном случае.
Профилактика
При длительной профилактике кровотечений у пациентов с тяжелой формой гемофилии А обычно используются дозы от 20 до 40 МЕ фактора VIII на кг массы тела, вводимые с интервалом 2-3 дня.
В некоторых случаях, особенно у молодых пациентов, может быть необходимо введение лекарства в более короткие интервалы или в более высоких дозах.
Пациенты, леченные фактором VIII, должны быть внимательно отслеживаемы и подвергаться исследованиям на образование ингибиторов.
Во время лечения необходимо оценить правильный уровень фактора VIII для коррекции дозирования и частоты повторных инфузий. Особенно при серьезных хирургических операциях необходимо точное мониторинг заместительной терапии с помощью исследований свертывания (активность фактора VIII в плазме).
Дети и подростки
ЭМОКЛОТ не рекомендуется для использования у детей младше 12 лет из-за недостаточного количества данных о безопасности и эффективности.
Более подробную информацию о дозировании и продолжительности лечения см. в конце этой инструкции в разделе, предназначенном для врачей и медицинских специалистов.
Способ введения
Лекарство вводится внутривенно в инъекции или медленной инфузии.
При внутривенной инъекции рекомендуется соблюдать время введения от 3 до 5 минут, проверяя частоту сердечных сокращений пациента и прекращая введение или уменьшая скорость инфузии, если частота сердечных сокращений увеличивается.
Скорость инфузии должна быть определена индивидуально для каждого пациента.
Необходимо использовать только прилагаемые наборы для инъекций или инфузий, поскольку адсорбция человеческого фактора VIII на внутренних поверхностях некоторых наборов для инъекций или инфузий может быть причиной терапевтической неудачи.
Несовместимости: из-за отсутствия исследований совместимости этого лекарства не следует смешивать его с другими лекарственными продуктами.
Реконструкция порошка с растворителем:
- 1. Довести флакон с порошком и флакон с растворителем до комнатной температуры;
- 2. Необходимо поддерживать комнатную температуру во время всего процесса реконструкции (максимум 10 минут);
- 3. Снять защитные колпачки с флакона с порошком и флакона с растворителем;
- 4. Очистить поверхность пробки на обоих флаконах спиртом;
- 5. Открыть упаковку медицинского материала для реконструкции, удалив крышку осторожно, чтобы не касаться устройства внутри упаковки (рис. А);
- 6. Не вынимать устройство из упаковки;
- 7. Перевернуть упаковку с устройством вверх дном и вставить пластиковый наконечник через пробку в флакон с растворителем для соединения синей части устройства с флаконом растворителя (рис. Б);
- 8. Держа за край упаковки, снять ее с устройства без его касания (рис. В);
- 9. Убедиться, что флакон с порошком находится на безопасной поверхности, перевернуть соединенное устройство и флакон с растворителем так, чтобы флакон оказался сверху; нажать на прозрачный адаптер на пробке флакона с порошком, чтобы пластиковый наконечник устройства прошел через пробку флакона; растворитель автоматически стечет в флакон с порошком (рис. Г);
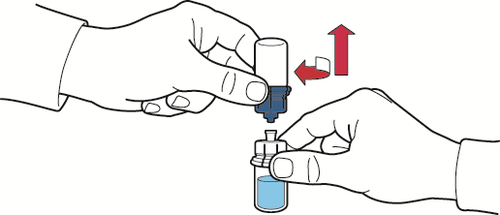
- 10. После стока растворителя, открутить синюю часть устройства для реконструкции с закрепленным флаконом с растворителем и удалить ее (рис. Д);
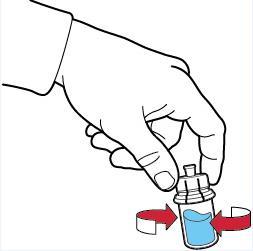
- 11. Взболтать осторожно до полного растворения порошка (рис. Е);
- 12. Не встряхивать энергично, необходимо избегать пенообразования раствора.
Рис. А
Рис. Б
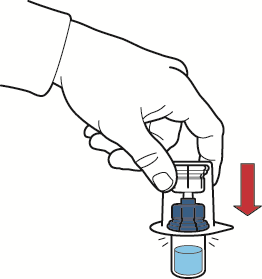
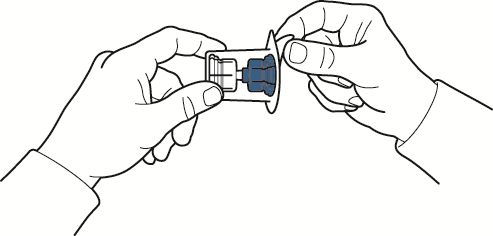
Рис. В
Рис. Г
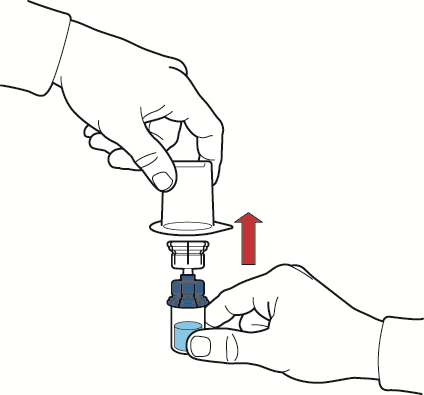
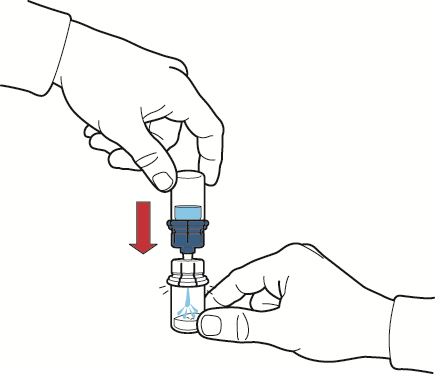
Рис. Д
Рис. Е
Введение раствора
После реконструкции раствор может содержать несколько небольших хлопьев или частиц.
Перед введением необходимо визуально проверить раствор на наличие частиц или изменение цвета.
Раствор должен быть прозрачным или слегка опалесцирующим. Не следует использовать мутные или содержащие осадок растворы.
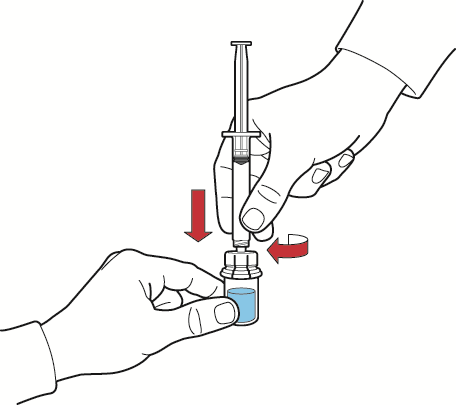
- 1. Заполнить шприц воздухом, оттянув поршень шприца, соединить шприц с устройством и, нажимая на поршень шприца, ввести воздух в флакон с растворенным раствором (рис. Ж);
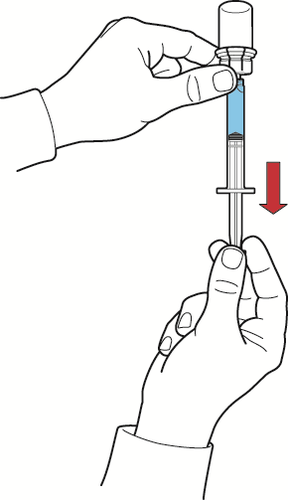
- 2. Держа поршень шприца неподвижно, перевернуть флакон и шприц так, чтобы флакон с раствором после реконструкции был сверху, медленно оттягивая поршень, ввести раствор в шприц (рис. З);
- 3. Отключить шприц, повернув его в противоположную сторону от движения часовой стрелки;
- 4. Проверить раствор в шприце, который должен быть прозрачным или слегка опалесцирующим, без частиц;
- 5. Соединить иглу-бабочку с шприцем и ввести в инфузии или медленной внутривенной инъекции.
Рис. Ж
Рис. З
Использование большей, чем рекомендуемая, дозы лекарства ЭМОКЛОТ
Не известны симптомы передозировки человеческого фактора VIII свертывания крови.
В случае случайного проглатывания или передозировки лекарства ЭМОКЛОТ необходимо немедленно обратиться в ближайшую больницу.
В случае любых дальнейших сомнений, связанных с использованием этого лекарства, необходимо обратиться к врачу.
4. Возможные нежелательные реакции
Как и любой лекарственный препарат, это лекарство может вызывать нежелательные реакции, хотя они не возникнут у каждого.
В случае возникновения любого из указанных нежелательных реакций необходимо немедленно сообщить об этом врачу или в ближайшую больницу:
- Тяжелые аллергические реакции (гиперчувствительность): быстро прогрессирующий отек кожи и слизистых оболочек вокруг рта и лица (ангиоотек). Эта реакция наблюдается редко, но в некоторых случаях может усиливаться до возникновения острой аллергической реакции, включая анафилаксию.
- У пациентов с гемофилией А могут образовываться нейтрализующие антитела (ингибиторы) против фактора VIII, что проявляется слабой клинической реакцией на лечение. В этих случаях рекомендуется консультация со специалистическим центром лечения гемофилии.
Другие возможные нежелательные реакции:
- Остальные аллергические реакции (гиперчувствительность) могут включать:
- жжение и боль в месте введения;
- озноб, внезапное покраснение лица, общая крапивница (возникающая на коже всего тела), сыпь;
- головная боль
- понижение кровяного давления (гипотония), беспокойство, учащенное сердцебиение (тахикардия), чувство сдавления в груди, свистящее дыхание;
- сонливость (летаргия);
- тошнота, рвота;
- чувство онемения. Эти нежелательные реакции наблюдались в редких случаях после введения лекарств, содержащих фактор VIII, но в некоторых случаях могут усиливаться до возникновения острого аллергического шока.
Частота возникновения нежелательных реакций после введения лекарства ЭМОКЛОТ на рынок неизвестна, что означает, что она не может быть определена на основе имеющихся данных.
Также было отмечено возникновение лихорадки.
У детей, не леченных ранее лекарствами, содержащими фактор VIII, антитела-блокаторы (см. пункт 2) могут образовываться очень часто (более 1 из 10 пациентов). Однако у пациентов, ранее леченных фактором VIII (более 150 дней лечения), риск не очень частый (менее 1 из 100 пациентов). Если это произойдет, лекарства у пациента могут перестать действовать правильно, и может возникнуть продолжающееся кровотечение. Если это произойдет, необходимо немедленно обратиться к врачу.
Дополнительные нежелательные реакции у детей
Хотя нет специальных данных о педиатрической популяции, несколько опубликованных данных о исследованиях эффективности и безопасности не показали значительных различий между взрослыми и детьми, страдающими одним и тем же заболеванием.
Сообщение о нежелательных реакциях
Если возникают любые нежелательные реакции, включая все нежелательные реакции, не указанные в инструкции, необходимо сообщить об этом врачу или медсестре. Нежелательные реакции можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных средств Управления по регистрации лекарственных средств, медицинских изделий и биоцидных продуктов:
ул. Аллея Ерозолимских, 181С,
02-222 Варшава,
тел: 22 4921301,
факс: 22 4921309,
Сайт: https://smz.ezdrowie.gov.pl
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности использования лекарства.
Нежелательные реакции можно сообщать также ответственному лицу.
Информация о безопасности, связанная с передачей инфекционных агентов, см. в пункте 2.
5. Как хранить ЭМОКЛОТ
Лекарство хранить в месте, недоступном для детей. Не использовать лекарство после истечения срока годности, указанного на упаковке после EXP. Срок годности указывает последний день указанного месяца.
Хранить в холодильнике (2°C - 8°C). Не замораживать. Хранить в наружной упаковке для защиты от света.
До использования и в течение срока годности лекарства флакон с порошком может храниться при комнатной температуре, не превышающей 25°C, не более 6 месяцев. После этого срока лекарство необходимо уничтожить. В любом случае нельзя лекарство повторно помещать в холодильник, если оно хранилось при комнатной температуре.
На наружной упаковке (коробке) необходимо записать начальную дату хранения при комнатной температуре.
После открытия флакона его содержимое необходимо использовать немедленно. Содержимое флакона должно быть использовано для одного введения лекарства.
Лекарства не следует выбрасывать в канализацию или домашние мусорные контейнеры. Необходимо спросить у фармацевта, как уничтожить лекарства, которые больше не используются. Такое поведение поможет защитить окружающую среду.
6. Содержание упаковки и другие сведения
Что содержит ЭМОКЛОТ
Активным веществом лекарства является человеческий фактор VIII свертывания крови.
| ЭМОКЛОТ 500 МЕ | ЭМОКЛОТ 1000 МЕ | |
| Человеческий фактор VIII свертывания крови | 500 МЕ/флакон | 1000 МЕ/флакон |
| Человеческий фактор VIII свертывания крови после реконструкции в воде для инъекций | 50 МЕ/мл (500 МЕ/10 мл) | 100 МЕ/мл (1000 МЕ/10 мл) |
| Растворитель (вода для инъекций) | 10 мл | 10 мл |
Сила продукта (МЕ) была определена хромогенным методом в соответствии с Европейской фармакопеей.
Специфическая активность лекарства составляет примерно 80 МЕ/мг белка.
Лекарство произведено из человеческой плазмы, полученной от доноров.
Лекарство содержит: человеческий фактор фон Виллебранда: активность кофактора ристоцетина (RCO) не менее 10 МЕ/мл для дозы 500 МЕ/10 мл и не менее 20 МЕ/мл для дозы 1000 МЕ/10 мл.
Другие компоненты лекарства: цитрат натрия, хлорид натрия, глицерин, хлорид кальция.
Растворитель: вода для инъекций.
Как выглядит ЭМОКЛОТ и что содержит упаковка
Порошок и растворитель для приготовления раствора для инъекций и инфузий.
После реконструкции раствор может содержать несколько небольших хлопьев или частиц.
Раствор после реконструкции необходимо визуально проверить на наличие частиц или изменение цвета.
Раствор должен быть прозрачным или слегка опалесцирующим. Не следует использовать мутные или содержащие осадок растворы.
Упаковка лекарства ЭМОКЛОТ содержит один флакон с порошком, один флакон с растворителем для приготовления раствора для введения, а также стерильный набор для приготовления раствора и введения, состоящий из устройства для реконструкции, шприца одноразового использования и иглы-бабочки с трубкой ПЦВ.
ЭМОКЛОТ, 500 МЕ/10 мл
1 флакон с порошком + 1 флакон с растворителем + набор для приготовления раствора и введения.
ЭМОКЛОТ, 1000 МЕ/10 мл,
1 флакон с порошком + 1 флакон с растворителем + набор для приготовления раствора и введения.
Ответственное лицо и производитель Ответственное лицо
Kedrion S.p.A. - Loc. Ai Conti, 55051 Castelvecchio Pascoli, Barga (Lucca), Италия
Производитель
Kedrion S.p.A. - 55027 Bolognana, Gallicano (Lucca), Италия
Для получения более подробной информации необходимо обратиться к представителю ответственного лица
MB&S, ул. Челмская, 30/34, Варшава
Тел/факс: 22 8515210
Дата последней актуализации инструкции:
Информация, предназначенная только для медицинских специалистов:
Мониторинг лечения
Во время лечения необходимо оценить правильный уровень фактора VIII для коррекции дозирования и частоты повторных инфузий. Ответ на фактор VIII у отдельных пациентов может различаться по периоду полувыведения и уровням восстановления. Дозировка, основанная на массе тела, может потребовать коррекции у пациентов с недостаточным или избыточным весом.
Особенно при серьезных хирургических операциях необходимо точное мониторинг заместительной терапии с помощью исследований свертывания (активность фактора VIII в плазме) для определения точной дозировки и частоты инфузий.
При использовании одноступенчатого теста свертывания in vitro, основанного на времени частичной тромбопластиной после активации (аПТТ), используемого для определения активности фактора VIII в пробах крови пациентов, как тип реагента аПТТ, так и эталонный образец, используемые в тесте, могут существенно влиять на результаты определения уровня активности фактора VIII в плазме.
Могут также возникать значительные различия между результатами одноступенчатого теста свертывания, основанного на аПТТ, и результатами хромогенного теста, выполненного в соответствии с Европейской фармакопеей. Это особенно важно при изменении лаборатории и (или) реагентов, используемых в тесте.
Дозирование
Дозирование и продолжительность заместительной терапии зависят от степени дефицита фактора VIII, от места и объема кровотечения и от клинического состояния пациента.
Количество вводимых единиц фактора VIII выражается в международных единицах (МЕ), соответствующих текущим стандартам ВОЗ для продуктов фактора VIII. Активность фактора VIII в плазме выражается либо в процентах (относительно нормальной человеческой плазмы), либо в международных единицах (относительно международных стандартов фактора VIII в плазме).
Одна международная единица (МЕ) активности фактора VIII равна количеству фактора VIII, присутствующего в 1 мл плазмы здорового человека.
Лечение по требованию
Расчет необходимой дозировки фактора VIII основан на эмпирических данных, подтверждающих, что 1 МЕ фактора VIII на кг массы тела увеличивает активность фактора VIII в плазме на 1,5% до 2%.
Необходимая дозировка определяется по следующей формуле:
Необходимое количество единиц = масса тела [кг] x желаемый рост активности фактора VIII [%]
[МЕ/дл] x 0,4
При определении необходимой дозы и частоты введения необходимо всегда руководствоваться клинической эффективностью в индивидуальном случае.
В следующих случаях кровотечений активность фактора VIII в плазме в соответствующее время не должна падать ниже указанного значения (в % от нормы или МЕ/дл).
Ниже приведенная таблица может служить основой для дозирования при эпизодах кровотечения и хирургических операциях:
Степень кровотечения / Тип хирургической операции
Частота дозирования (часы)/
Продолжительность лечения (дни)
Кровотечения:
Ранний кровоизлияние в сустав,
кровотечение в мышцы или из полости рта
Необходимый уровень фактора VIII (%) (МЕ/дл)
- 20 - 40 Повторять инфузии каждые 12-24 часа в течение как минимум 1 дня, до исчезновения кровотечения, оцениваемого по исчезновению боли или заживлению раны. Более тяжелое кровоизлияние в сустав, кровотечение в мышцы или гематома
- 30 - 60 Повторять каждые 12-24 часа в течение 3-4 дней или дольше, до исчезновения боли или острой инвалидности. Кровотечения, угрожающие жизни
- 60 - 100 Повторять каждые 8-24 часа до момента исчезновения угрозы Хирургические операции: Минимальные хирургические операции, включая удаление зуба
- 30 – 60 Повторять инфузии каждые 24 часа в течение как минимум 1 дня, до заживления. Серьезные хирургические операции
- 80 – 100 (до и после операции) Повторять каждые 8-24 часа до заживления ран, затем в течение как минимум 7 дней для поддержания активности фактора VIII на уровне 30% до 60% (30 МЕ/дл - 60 МЕ/дл).
Профилактика
При длительной профилактике кровотечений у пациентов с тяжелой формой гемофилии А обычно используются дозы от 20 до 40 МЕ фактора VIII на кг массы тела, вводимые с интервалом 2-3 дня.
В некоторых случаях, особенно у молодых пациентов, может быть необходимо введение лекарства в более короткие интервалы или в более высоких дозах.
Дети и подростки
ЭМОКЛОТ не рекомендуется для использования у детей младше 12 лет из-за недостаточного количества данных о безопасности и эффективности. Дозировка у подростков (12-18 лет) в каждом показании рассчитывается на основе массы тела.
Способ введения
Вводить внутривенно в инъекции или медленной инфузии.
При внутривенной инъекции рекомендуется соблюдать время введения от 3 до 5 минут, проверяя частоту сердечных сокращений пациента и прекращая введение или уменьшая скорость инфузии, если частота сердечных сокращений увеличивается.
Скорость инфузии должна быть определена индивидуально для каждого пациента.
Инструкция по реконструкции лекарственного препарата перед введением см. в пункте 3. Как использовать ЭМОКЛОТ.
Ингибиторы
Клиническое значение образовавшегося ингибитора будет зависеть от титра ингибитора, при этом ингибиторы с низким титром представляют меньший риск недостаточной клинической реакции, чем ингибиторы с высоким титром.
В целом, все пациенты, леченные продуктами фактора VIII, должны быть внимательно отслеживаемы на предмет образования ингибиторов путем наблюдения за клиническим состоянием и оценки лабораторных исследований. Если несмотря на введение достаточной дозы не удается достичь ожидаемого уровня активности фактора VIII в плазме или не удается контролировать кровотечение, необходимо выполнить исследование на предмет наличия ингибиторов фактора VIII. У пациентов с значительной активностью ингибитора лечение фактором VIII может быть неэффективным, и необходимо рассмотреть другие варианты терапии. Лечение таких пациентов должно проводиться под руководством врачей, имеющих опыт в лечении гемофилии и ингибиторов фактора VIII.
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- Производитель
- ИмпортерKedrion S.p.A.
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги ЕмоцлотФорма выпуска: Порошок, 1000 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: CSL Behring GmbHТребуется рецептФорма выпуска: Порошок, 2000 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: CSL Behring GmbHТребуется рецептФорма выпуска: Порошок, 250 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: CSL Behring GmbHТребуется рецепт
Аналоги Емоцлот в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Емоцлот в Испания
Аналог Емоцлот в Украина
Врачи онлайн по Емоцлот
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Емоцлот – по решению врача и с учетом местных правил.














