
VERASEAL Soluções Adesivas para Tecidos

Pergunte a um médico sobre a prescrição de VERASEAL Soluções Adesivas para Tecidos

Como usar VERASEAL Soluções Adesivas para Tecidos
Introdução
Prospecto: informação para o utilizador
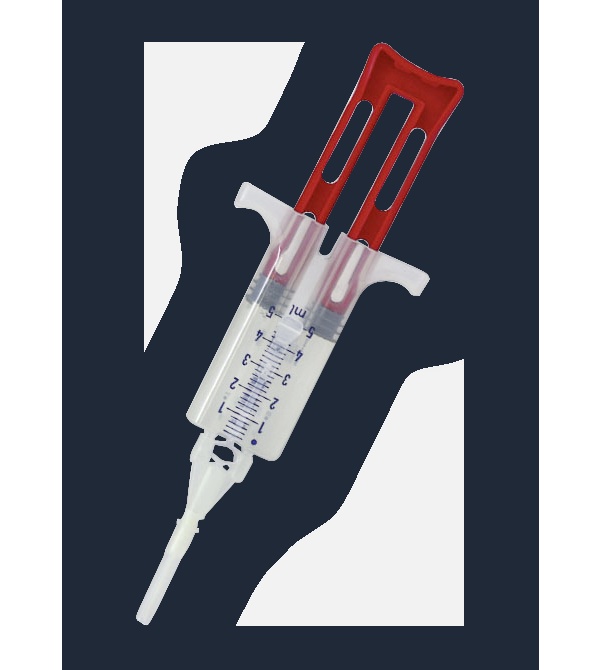
VeraSeal soluções para adesivo tecidual
fibrinogénio humano/trombina humana
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico.
- Se experimentar efeitos adversos, consulte o seu médico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é VeraSeal e para que é utilizado
- O que necessita saber antes de começar a usar VeraSeal
- Como usar VeraSeal
- Possíveis efeitos adversos
- Conservação de VeraSeal
- Conteúdo do envase e informação adicional
1. O que é VeraSeal e para que é utilizado
VeraSeal contém fibrinogénio humano e trombina humana, duas proteínas extraídas do sangue que, quando misturadas, formam um coágulo.
VeraSeal é utilizado como adesivo tecidual em operações cirúrgicas em pacientes. É aplicado na superfície do tecido sangrante para reduzir o sangramento durante e após a operação, quando as técnicas cirúrgicas padrão não são suficientes.
VeraSeal está indicado em todos os grupos etários.
2. O que necessita saber antes de começar a usar VeraSeal
Seu cirurgião não deve administrar-lhe VeraSeal
- se é alérgico ao fibrinogénio humano ou à trombina humana ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
VeraSeal não deve ser administrado directamente no interior dos vasos sanguíneos.
VeraSeal não deve ser utilizado para tratar o sangramento intenso ou rápido de uma artéria.
Advertências e precauções
Podem ocorrer reacções alérgicas. Os sintomas dessas reacções alérgicas são urticária generalizada, opressão torácica, sibilância, hipotensão (por exemplo, tontura, desmaio, visão turva) e anafilaxia (uma reacção grave de aparecimento rápido). Se ocorrerem estes sintomas durante a cirurgia, a administração do medicamento será suspensa imediatamente.
VeraSeal deve ser aplicado por pulverização apenas quando for possível calcular com precisão a distância de pulverização. Essa distância de pulverização deve estar dentro do intervalo recomendado.
Precauções especiais de segurança
Quando os medicamentos são elaborados a partir de sangue ou plasma humanos, devem ser adoptadas uma série de medidas para prevenir uma possível transmissão de infecções aos pacientes. Essas medidas incluem uma selecção cuidadosa dos doadores de sangue e plasma para garantir a exclusão de doadores com risco de padecer infecções, e a análise de cada doação e mistura de plasmas para detectar possíveis vírus ou infecções. Os fabricantes desses medicamentos incluem, além disso, uma série de etapas no processamento do sangue ou do plasma que podem inactivar ou eliminar os vírus. Apesar dessas medidas, quando se administram medicamentos preparados a partir de sangue ou plasma humanos, não se pode excluir totalmente a possibilidade de transmissão de infecções. Isso também é aplicável a vírus desconhecidos ou emergentes e a outros tipos de infecções.
As medidas tomadas são consideradas eficazes para os vírus envoltos, como o vírus da imunodeficiência humana (VIH), o vírus da hepatite B e o vírus da hepatite C, e para o vírus não envolto da hepatite A. As medidas podem ser ineficazes contra vírus não envoltos, como o parvovirus B19. A infecção por parvovirus B19 pode ser grave em mulheres grávidas (infecção fetal) e em pessoas com imunodeficiência ou com aumento da eritropoyese (p. ex., anemia hemolítica).
É altamente recomendável que cada vez que se administre VeraSeal a um paciente, se deixe constância do nome do medicamento e do número do lote administrado, a fim de manter uma relação entre o paciente e o lote do medicamento.
Crianças e adolescentes
Recomenda-se o uso de VeraSeal em crianças e adolescentes com menos de 18 anos de idade.
Uso de VeraSeal com outros medicamentos
O medicamento pode ser afectado se entrar em contacto com soluções que contenham álcool, iodo ou metais pesados (p. ex., soluções antisépticas).
Informa ao seu médico ou farmacêutico se está a tomar, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento. O seu médico decidirá se deve receber tratamento com VeraSeal.
3. Como usar VeraSeal
O uso de VeraSeal está limitado a cirurgiões experientes que tenham sido devidamente formados no uso de VeraSeal.
O cirurgião lhe administrará VeraSeal na superfície dos vasos sanguíneos ou na superfície do tecido dos órgãos internos, utilizando o aplicador durante a cirurgia. Este aplicador permite administrar a mesma quantidade dos dois componentes de VeraSeal que se devem administrar ao mesmo tempo e garante que se misturem de forma uniforme, o que é importante para que o adesivo tecidual logre o seu efeito óptimo.
A quantidade de VeraSeal que se deve aplicar depende de variáveis como o tipo de cirurgia, o tamanho da zona a tratar durante a operação e a forma como se aplica VeraSeal. O cirurgião decidirá a quantidade apropriada e aplicará a quantidade suficiente para formar uma camada fina e uniforme. Se não parecer suficiente, pode ser aplicada uma segunda camada.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
VeraSeal é um adesivo tecidual de fibrina. Os adesivos teciduais de fibrina, em geral, podem produzir uma reacção alérgica em casos raros (até 1 paciente de cada 1000 pessoas). Se experimentar uma reacção alérgica, pode apresentar um ou mais dos seguintes sintomas: inchaço debaixo da pele (angioedema), erupção cutânea, urticária ou bexigas, opressão torácica, arrepios, rubor, dor de cabeça, redução da pressão arterial, letargia, náuseas, inquietude, aumento da frequência cardíaca, formigamento, vómitos ou sibilância. Em casos isolados, essas reacções podem progredir até uma reacção alérgica grave. As reacções alérgicas podem ser observadas especialmente se a preparação for aplicada repetidamente ou for administrada a pacientes que se sabe que são alérgicos aos componentes do medicamento. Se experimentar algum desses sintomas após a cirurgia, deve consultar imediatamente o seu médico ou cirurgião.
Também existe a possibilidade de que o seu sistema imunológico faça com que as proteínas ataquem VeraSeal e que as mesmas possam interferir na coagulação do sangue. Desconhece-se a frequência deste tipo de ocorrência.
Se este medicamento for colocado acidentalmente dentro de um vaso sanguíneo, podem formar-se coágulos sanguíneos, incluindo coagulação intravascular disseminada (CID) (quando se formam coágulos nos vasos sanguíneos do corpo). Existe, além disso, risco de que se produza uma reacção alérgica grave.
Os efeitos adversos observados durante os ensaios clínicos com VeraSeal incluíram:
Efeitos adversos mais graves
Pouco frequentes (podem afectar até 1 pessoa de cada 100):
- Abscesso abdominal (abdomen) (área inflamada no abdômen devido a uma infecção)
- Deiscência da ferida abdominal (abdomen) (ruptura da ferida por cura incompleta)
- Fuga biliar (líquido que produz o fígado) após o procedimento
- Celulite (infecção da pele)
- Trombose venosa profunda (coágulos de sangue nos vasos sanguíneos)
- Abscesso hepático (área inflamada no fígado devido a uma infecção)
- Peritonite (inflamação da parede abdominal)
- Teste positivo para o parvovirus B19 (resultado de laboratório que mostra infecção pelo vírus)
- Infecção pós-operatória da ferida
- Embolia pulmonar (coágulos de sangue nos vasos sanguíneos dos pulmões)
- Infecção da ferida
Outros efeitos adversos
Frequentes (podem afectar até 1 pessoa de cada 10):
- Náuseas
- Dor causada pela cirurgia
- Prurido (picazão)
Pouco frequentes (podem afectar até 1 pessoa de cada 100):
- Anemia (falta de glóbulos vermelhos)
- Ansiedade
- Fibrilação atrial (batimento cardíaco irregular)
- Dor de costas
- Espasmos na bexiga
- Arrepios
- Irritação conjuntival (irritação ocular)
- Prisão de ventre
- Contusão (hematoma)
- Redução na produção de urina
- Dispnéia (dificuldade para respirar)
- Disúria (dor ou dificuldade para urinar)
- Equimose (cardenais)
- Eritema (avermelhamento da pele)
- Flatulências
- Dor de cabeça
- Temperatura corporal alta
- Pressão sanguínea alta ou baixa
- Níveis altos ou baixos de glóbulos brancos no sangue
- Níveis altos de potássio no sangue
- Íleus (obstrução intestinal)
- Alteração da coagulação do sangue
- Eritema do local da incisão (avermelhamento da pele no local da incisão)
- Infecção no local da incisão
- Aumento da bilirrubina no sangue
- Aumento dos níveis de enzimas hepáticas
- Aumento ou diminuição dos níveis de glicose no sangue
- Insónia
- Pressão arterial baixa devido ao procedimento
- Níveis baixos de cálcio no sangue
- Níveis baixos de magnésio no sangue
- Nível baixo de oxigénio no sangue
- Níveis baixos de potássio no sangue
- Níveis baixos de proteínas no sangue
- Níveis baixos de glóbulos vermelhos causados por uma perda de sangue
- Níveis baixos de sódio no sangue
- Edema periférico (acumulação de fluidos)
- Dor, sem especificar
- Dor no local da incisão
- Dor nas extremidades
- Mieloma de células plasmáticas (câncer de células sanguíneas)
- Pleuresia (quantidade anormal de fluido ao redor do pulmão)
- Efusão pleural (inflamação da parede do pulmão)
- Hemorragia pós-procedimento (sangramento após o procedimento)
- Infecção pós-procedimental (infecção após o procedimento)
- Edema pulmonar (excesso de fluido aquoso nos pulmões)
- Hematoma retroperitoneal (acumulação de sangue no abdômen)
- Roncos
- Sonolência
- Retenção urinária
- Complicação do enxerto vascular (complicação do bypass vascular)
- Trombose do enxerto vascular (coágulos sanguíneos no bypass dos vasos sanguíneos)
- Taquicardia ventricular (batimento rápido)
- Hematoma na zona de punção do vaso
- Vómitos
- Sibilância
- Secreção da ferida
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de VeraSeal
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e na caixa após CAD.
Conservar e transportar congelado a -18 ºC ou inferior. A cadeia de frio não deve ser interrompida até ao seu uso. Conservar o blister esterilizado no embalagem exterior para protegê-lo da luz. Descongelar completamente antes da sua utilização. Uma vez descongelado, não voltar a congelar. Após a descongelação, pode ser mantido por não mais de 7 dias a 2 ºC - 8 ºC ou 24 horas a temperatura não superior a 25 ºC antes da sua utilização.
Uma vez aberto o blister, VeraSeal deve ser utilizado imediatamente.
Não utilize este medicamento se a solução estiver turva ou tiver sedimentos.
Elimine se o envase estiver danificado.
6. Conteúdo do envase e informação adicional
Composição de VeraSeal
Os princípios ativos são:
- Componente 1: Fibrinógeno humano
- Componente 2: Trombina humana
Os outros componentes são:
- Componente 1: Citrato de sódio dihidratado, cloreto de sódio, arginina, isoleucina, ácido glutâmico monossódio, água para preparações injetáveis.
- Componente 2: Cloreto cálcio, albumina humana, cloreto de sódio, glicina, água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
VeraSeal apresenta-se como soluções para adesivo tecidual em um kit de um só uso com duas seringas precarregadas ensambladas em um suporte. Soluções congeladas. Após a descongelação, as soluções são transparentes ou ligeiramente opalescentes, incolores ou de cor amarela pálida.
Inclui-se com o medicamento um Aplicador Duplo com duas bicos de pulverização sem ar adicionais, para uma aplicação mediante pulverização ou gota a gota. Os bicos de pulverização sem ar são radiopacos. Ver esquema mais abaixo.
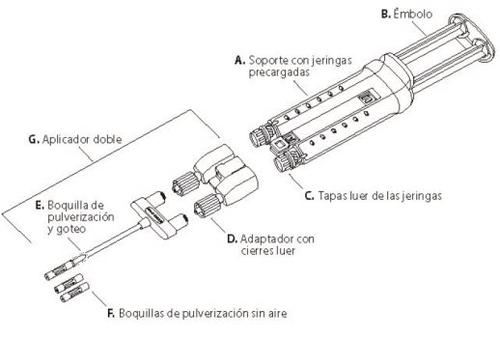
VeraSeal está disponível nas seguintes apresentações:
- VeraSeal 2 ml (contém 1 ml de fibrinógeno humano e 1 ml de trombina humana)
- VeraSeal 4 ml (contém 2 ml de fibrinógeno humano e 2 ml de trombina humana)
- VeraSeal 6 ml (contém 3 ml de fibrinógeno humano e 3 ml de trombina humana)
- VeraSeal 10 ml (contém 5 ml de fibrinógeno humano e 5 ml de trombina humana)
Pode ser que apenas alguns tamanhos de envases estejam comercializados.
Título da autorização de comercialização e responsável pela fabricação
Instituto Grifols, S.A.
Can Guasc, 2 - Parets del Vallès
E-08150 Barcelona - Espanha
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização:
AT/BE/BG/CY/EE/EL/ES/HR/HU/IE/LV/ LT/LU/MT/NL/RO/SI/SK/UK(NI) Instituto Grifols, S.A. Tel: +34 93 571 01 00 | CZ Grifols S.R.O. Tel: +4202 2223 1415 |
DE Grifols Deutschland GmbH Tel: +49 69 660 593 100 | DK/FI/IS/NO/SE Grifols Nordic AB Tel: +46 8 441 89 50 |
FR Johnson & Johnson Medical S.A.S. Tél: +33 (0)1 55 00 22 33 | |
IT Grifols Italia S.p.A. Tel: +39 050 8755 113 | PL Grifols Polska Sp. z o. o. Tel: +48 22 378 85 60 |
PT Grifols Portugal, Lda. Tel: +351 219 255 200 | |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada deste medicamento está disponível na página web da Agência Europeia de Medicamentos: http://www.ema.europa.eu
-------------------------------------------------------------------------------------------------------------------
Esta informação está destinada apenas a profissionais de saúde:
Posologia e forma de administração
O uso de VeraSeal está limitado a cirurgiões experientes que tenham sido treinados no uso deste medicamento.
A quantidade de VeraSeal que deve ser aplicada e a frequência da aplicação devem estar sempre orientadas às necessidades clínicas subjacentes do paciente.
A dose que deve ser aplicada dependerá de variáveis como o tipo de intervenção cirúrgica, o tamanho da superfície de sangramento, a gravidade do sangramento, o método de aplicação escolhido pelo cirurgião e o número de aplicações, entre outras.
O cirurgião responsável deve aplicar o medicamento de forma individualizada. Em ensaios clínicos, as doses individuais que foram administradas oscilaram entre 0,3 e 12 ml. Para outros procedimentos, podem ser necessários volumes maiores.
A quantidade inicial do medicamento que será aplicada em uma zona anatômica concreta ou em uma superfície concreta deve ser suficiente para cobrir totalmente a área de aplicação prevista. Se necessário, pode-se repetir a aplicação.
Incompatibilidades
Na ausência de estudos de compatibilidade, este medicamento não deve ser misturado com outros.
Precauções especiais
Uso epilesional apenas. Não administrar por via intravascular.
Podem ocorrer complicações tromboembólicas potencialmente mortais se o preparado for administrado involuntariamente por via intravascular.
Quando se utilizarem os acessórios, devem-se seguir as instruções de uso destes.
Antes de aplicar VeraSeal, devem-se proteger (cobrir) bem as partes do corpo que não estejam dentro da zona de aplicação desejada para evitar a adesão tecidual em zonas não desejadas.
Deve-se aplicar uma camada fina de VeraSeal. Se o espessura do coágulo for excessiva, pode interferir de forma negativa com a eficácia do medicamento e com o processo de cicatrização da ferida.
Instruções de uso
Leia este prospecto antes de abrir o envase. Por favor, consulte os pictogramas no final deste prospecto.
Instruções de manipulação e eliminação de VeraSeal
VeraSeal apresenta-se em envases esterilizados e deve ser utilizado mediante técnicas estéreis em condições assépticas. Descarte os envases danificados, pois não é possível reesterilizá-los.
Na Tabela 1, mostra-se um resumo dos métodos de descongelação e de armazenamento após a descongelação.
Tabela 1. Descongelação e armazenamento após a descongelação
Método de descongelação | Tempo de descongelação por apresentação | Armazenamento após a descongelação | |
Apresentações de 2 ml e 4 ml | Apresentações de 6 ml e 10 ml | ||
Geladeira (2 - 8 °C) | Mínimo de 7 horas | Mínimo de 10 horas | 7 dias a 2 - 8 °C (geladeira) em seu envase original Ou 24 horas a temperatura não superior a 25 °C em seu envase original |
Descongelação a 20 - 25 °C | Mínimo de 70 minutos | Mínimo de 90 minutos | |
Banho termostático de água estéril (37 °C) em zona estéril | Mínimo de 5 minutos. Não exceder os 10 minutos. | Mínimo de 5 minutos. Não exceder os 10 minutos. | Utilizar imediatamente durante a cirurgia |
- Métodos de descongelação preferidos
Descongelação em geladeira
- Saia a caixa do congelador e coloque-a na geladeira para sua descongelação a 2 - 8 °C
durante um mínimo de 7 horas para as apresentações de 2 ml e de 4 ml
durante um mínimo de 10 horas para as apresentações de 6 ml e de 10 ml
Após a descongelação, não é necessário aquecer o medicamento para seu uso.
Após a descongelação, as soluções são transparentes ou ligeiramente opalescentes, incolores ou de cor amarela pálida. As soluções que estiverem turvas ou apresentarem sedimentos não devem ser utilizadas.
Descongelação a 20 °C - 25 °C
Saia a caixa do congelador, abra-a e retire os dois blisteres.
Coloque o bliste que contém o Aplicador Duplo em uma superfície a 20 °C - 25 °C até que o adesivo tecidual de fibrina esteja pronto para seu uso.
Descongele as seringas precarregadas VeraSeal a 20 °C - 25 °C seguindo os passos descritos a seguir:
- Coloque o bliste que contém o suporte de seringas com seringas precarregadas em uma superfície a 20 °C – 25 °C
durante um mínimo de 70 minutos para as apresentações de 2 ml e 4 ml
durante um mínimo de 90 minutos para as apresentações de 6 ml e 10 ml
Após a descongelação, não é necessário aquecer o medicamento para seu uso.
Após a descongelação, as soluções são transparentes ou ligeiramente opalescentes, incolores ou de cor amarela pálida. As soluções que estiverem turvas ou apresentarem sedimentos não devem ser utilizadas.
Conservação após a descongelação
Após a descongelação, o kit que contém o suporte de seringas de VeraSeal com seringas precarregadas e o Aplicador Duplo pode ser conservado por não mais de 7 dias no refrigerador a 2 °C - 8 °C ou 24 horas a temperatura não superior a 25 °C antes de seu uso, se permanecer selado no envase original. Uma vez abertos os blisteres, utilize VeraSeal imediatamente e descarte o conteúdo não utilizado.
Uma vez descongelado, não volte a congelar.
Instruções de transferência
- Após a descongelação, retire o bliste da superfície a 20 °C - 25 °C ou do refrigerador a 2 °C – 8 °C.
- Abrir o bliste e verifique que as seringas precarregadas de VeraSeal estejam completamente descongeladas. Entregue o suporte de seringas de VeraSeal com seringas precarregadas a uma segunda pessoa para que o transfira para a zona estéril. O exterior do bliste não deve entrar em contato com a zona estéril. Ver a Figura 1.
- Banho termostático de água estéril (Descongelação rápida)
Saia a caixa do congelador, abra-a e retire os dois blisteres.
Coloque o bliste que contém o Aplicador Duplo em uma superfície a 20 °C - 25 °C até que o adesivo tecidual de fibrina esteja pronto para seu uso.
Descongele as seringas precarregadas VeraSeal dentro da zona estéril em um banho termostático de água estéril a uma temperatura de 37±2 °C seguindo os passos descritos a seguir:
NOTA: Uma vez abertos os blisteres de VeraSeal, utilize o produto imediatamente. Para evitar a possibilidade de contaminação por manipulação incorreta, utilize uma técnica estéril e siga exatamente os passos indicados mais abaixo. Não retire a tampa luer da seringa até que a descongelação seja completa e o Aplicador Duplo esteja pronto para ser montado.
- Abrir o bliste e entregue o suporte de seringas de VeraSeal com seringas precarregadas a uma segunda pessoa para que o transfira para a zona estéril. O exterior do bliste não deve entrar em contato com a zona estéril. Ver a Figura 1.
- Coloque o suporte de seringas com seringas precarregadas diretamente no banho, certificando-se de que permaneça completamente submerso na água estéril. Ver a Figura 2.
- A 37 °C, o tempo necessário é de 5 minutos aproximadamente para as apresentações de 2 ml, 4 ml, 6 ml e 10 ml, mas não devem ser deixados a esta temperatura por mais de 10 minutos. A temperatura do banho não deve superar os 39 °C.
- Após a descongelação, seque o suporte de seringas com seringas precarregadas utilizando uma gaze cirúrgica estéril.
Confirme que as seringas precarregadas de VeraSeal estejam completamente descongeladas. Após a descongelação, as soluções são transparentes ou ligeiramente opalescentes, incolores ou de cor amarela pálida. Não utilize as soluções que estiverem turvas ou apresentarem sedimentos.
Utilize VeraSeal imediatamente e descarte o conteúdo não utilizado.
- Instruções de montagem
- Abrir o bliste e entregue o Aplicador Duplo VeraSeal e as duas bicos de pulverização sem ar adicionais a uma segunda pessoa para que o transfira para a zona estéril. O exterior do bliste não deve entrar em contato com a zona estéril.
- Sustente o suporte de seringas de VeraSeal com as tampas luer das seringas apontando para cima. Ver a Figura 3.
- Desrosqueie e retire as tampas luer das seringas de fibrinógeno e de trombina. Ver a Figura 3.
- Sustente o suporte de seringas com os conectores luer apontando para cima. Para eliminar as bolhas das seringas, golpeie suavemente o bordo do suporte de seringas uma ou duas vezes enquanto o mantém na vertical e pressione ligeiramente o êmbolo para sacar o ar. Ver a Figura 4.
- Monte o Aplicador Duplo. Ver a Figura 5.
NOTA: não pressione o êmbolo durante o montagem ou antes da utilização, pois os dois componentes biológicos se misturariam previamente nas bicos de pulverização sem ar, formando um coágulo de fibrina que impediria a aplicação do produto. Ver a Figura 6.
- Ajuste os fechaduras luer e certifique-se de que o Aplicador Duplo esteja montado corretamente. O dispositivo está agora pronto para seu uso.
- Administração
Aplique VeraSeal utilizando o suporte de seringas e o êmbolo que são incluídos.
Aplique VeraSeal utilizando o Aplicador Duplo que é fornecido com o medicamento. Também podem ser utilizadas outras bicos de aplicação (incluindo dispositivos para cirurgia aberta e laparoscópica) destinadas a um uso específico com VeraSeal e que disponham de marca CE.
Quando utilizar o Aplicador Duplo fornecido, siga as instruções de conexão descritas anteriormente. Quando utilizar outras bicos de aplicação, siga as instruções de uso fornecidas com as bicos de aplicação.
Aplicação por pulverização
- Pegue o Aplicador Duplo e incline-o para a posição desejada. A bico conservará sua forma.
- Coloque as bicos de pulverização sem ar a uma distância de pelo menos 2 cm do tecido a tratar. Aplique uma pressão firme e regular sobre o êmbolo para pulverizar o adesivo tecidual. Aumente a distância conforme necessário para lograr a cobertura desejada da zona a tratar.
- Se a pulverização parar por qualquer motivo, troque a bico de pulverização sem ar antes de reiniciar a aplicação, pois pode ter se formado um coágulo na bico de pulverização sem ar. Para trocar a bico de pulverização sem ar, retire o dispositivo do paciente e desrosqueie a bico utilizada. Ver a Figura 7. Coloque a bico de pulverização sem ar utilizada longe das bicos de pulverização sem ar de recambio. Limpe a ponta do aplicador utilizando uma gaze cirúrgica estéril seca ou umedecida. Em seguida, conecte uma nova bico de pulverização sem ar fornecida no embalagem e certifique-se de que esteja firmemente conectada antes de seu uso.
NOTA: O indicador vermelho não será visível se a bico de pulverização sem ar estiver conectada corretamente. Ver a Figura 8.
NOTA: Não continue pressionando o êmbolo para tentar eliminar o coágulo de fibrina da bico de pulverização sem ar, pois o aplicador poderia ficar inutilizável.
NOTA: Não corte o Aplicador Duplo para evitar a exposição do fio interno.
Aplicação gota a gota
- Retire a bico de pulverização sem ar da bico de goteo desenroscando-a. Ver a Figura 7.
- Pegue e incline a bico de goteo para a posição desejada. A bico conservará sua forma.
- Durante a aplicação gota a gota, mantenha o extremo da bico o mais próximo possível da superfície tecidual sem tocar o tecido durante a aplicação.
- Aplique gotas individuais na superfície do área a tratar. Para evitar uma coagulação descontrolada, permita que as gotas se separem entre si e do extremo da bico de goteo.
NOTA: Não reconecte uma bico de goteo utilizada após que seja removida do adaptador, pois pode se formar um coágulo na bico e o aplicador poderia ficar inutilizável.
- Eliminação
A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele será realizada de acordo com a normativa local.
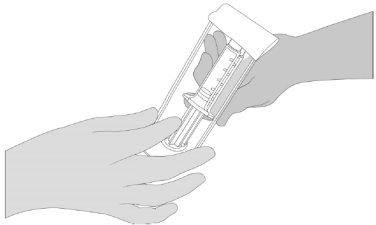
Figura 1
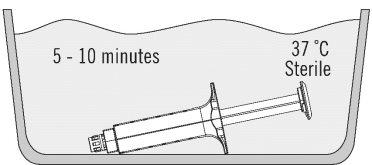
Figura 2
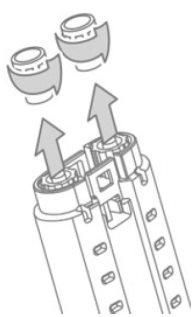
Figura 3
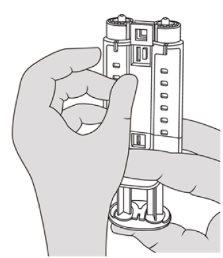
Figura 4
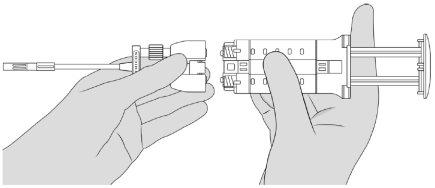
Figura 5
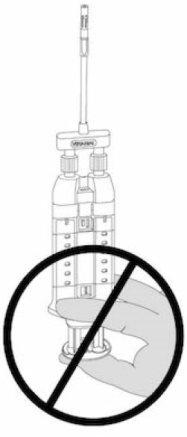
Figura 6
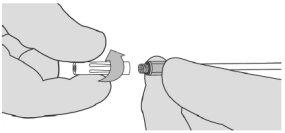
Figura 7
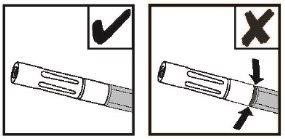
Figura 8
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a VERASEAL Soluções Adesivas para TecidosForma farmacêutica: ADESIVO TECIDUAL, conforme as necessidades clínicas do pacienteSubstância ativa: combinationsFabricante: Baxter S.L.Requer receita médicaForma farmacêutica: ADESIVO TECIDUAL, 50-90 mg/ml 800-1200 UISubstância ativa: combinationsFabricante: Omrix BiopharmaceuticalsRequer receita médicaForma farmacêutica: ADESIVO TECIDUAL, -Substância ativa: combinationsFabricante: Corza Medical GmbhRequer receita médica
Alternativas a VERASEAL Soluções Adesivas para Tecidos noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a VERASEAL Soluções Adesivas para Tecidos em Ukraine
Médicos online para VERASEAL Soluções Adesivas para Tecidos
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de VERASEAL Soluções Adesivas para Tecidos – sujeita a avaliação médica e regras locais.














