SYNFLORIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA

Pergunte a um médico sobre a prescrição de SYNFLORIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA

Como usar SYNFLORIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA
Introdução
Prospecto: informação para o utilizador
Synflorix suspensão injetável em seringa pré-carregada
vacina conjugada antineumocócica de polisacáridos (adsorvida)
Leia todo o prospecto atentamente antes de o seu filho receber esta vacina, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Esta vacina foi prescrita apenas para o seu filho e não deve ser dada a outras pessoas.
- Se o seu filho experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Synflorix e para que é utilizado
- O que precisa saber antes de o seu filho receber Synflorix
- Como é administrado Synflorix
- Posíveis efeitos adversos
- Conservação de Synflorix
- Conteúdo do envase e informação adicional
1. O que é Synflorix e para que é utilizado
Synflorix é uma vacina conjugada antineumocócica. O seu médico ou enfermeira injetará esta vacina no seu filho.
É utilizado para ajudar a proteger o seu filho a partir das 6 semanas até aos 5 anos de idade contra:
uma bactéria chamada “Streptococcus pneumoniae”. Esta bactéria pode causar doenças graves, incluindo meningite, sepsis e bacteriemia (bactérias no fluxo sanguíneo), bem como infecção de ouvido ou pneumonia.
Como funciona Synflorix
Synflorix ajuda o organismo a gerar os seus próprios anticorpos. Os anticorpos formam uma parte do sistema imunológico que protegerá o seu filho dessas doenças.
2. O que precisa saber antes de o seu filho receber Synflorix
Não deve ser administrado Synflorix se
- o seu filho é alérgico ao princípio ativo, ou a algum dos outros componentes desta vacina (incluídos na secção 6).
Os sinais de uma reação alérgica podem incluir erupção cutânea com picazón, dificuldade para respirar e inchação do rosto ou da língua.
- o seu filho tem uma infecção grave com febre alta (superior a 38 °C). Se isto acontecer ao seu filho, deve adiar a vacinação até que se sinta melhor. Uma infecção de pouca importância, como um resfriado, não deve ser um problema para a vacinação. No entanto, consulte antes com o seu médico.
Não deve ser administrado Synflorix se o seu filho se encontrar em alguma das circunstâncias anteriores. Se não tiver certeza, consulte o seu médico ou farmacêutico antes de o seu filho receber Synflorix.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar esta vacina se:
- o seu filho tem algum problema de coagulação ou faz equimoses com facilidade.
Em crianças a partir de 2 anos de idade, antes ou depois de qualquer injeção, pode ocorrer um desmaio, por isso deve informar o seu médico ou enfermeira se o seu filho desmaiou em ocasiões anteriores após a administração de uma injeção.
Assim como todas as vacinas, Synflorix pode não proteger completamente todas as crianças vacinadas.
Synflorix apenas protegerá contra as infecções causadas pelas bactérias para as quais a vacina foi desenvolvida.
As crianças com um sistema imunológico debilitado (por exemplo, devido a uma infecção pelo vírus da imunodeficiência humana (VIH) ou a um tratamento imunossupressor) podem não se beneficiar completamente de Synflorix.
Se não tiver certeza, fale com o seu médico ou farmacêutico antes de usar Synflorix.
Crianças maiores de 5 anos
Não foi estabelecida a segurança nem a eficácia da vacina em crianças maiores de 5 anos, por isso não se recomenda a vacinação dessas crianças.
Outros medicamentos e Synflorix
Informa o seu médico ou farmacêutico se o seu filho está a utilizar, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento, ou se lhe foi administrada recentemente qualquer outra vacina. Pode ser que Synflorix não funcione tão bem se o seu filho estiver a tomar medicamentos que afetem o sistema imunológico para combater uma infecção.
Synflorix pode ser administrado ao mesmo tempo que outras vacinas infantis, como vacinas contra a difteria, tétano, pertussis (tosse ferina), Haemophilus influenzaetipo b, polio oral ou inativada, hepatite B, tríplice vírica (sarampo, rubéola e caxumba), varicela, vacinas orais anti-rotavírus e vacinas conjugadas contra o meningococo do serogrupo C e dos serogrupos A, C, W-135 e Y. Será utilizado um local de injeção diferente para cada uma das vacinas.
O seu médico pode recomendar que dê ao seu filho um medicamento que baixe a febre (como paracetamol) antes ou imediatamente após receber Synflorix, especialmente em crianças que foram vacinadas ao mesmo tempo com Synflorix e outras vacinas que contêm células enteras de pertussis. Também se recomenda administrar um medicamento que reduza a febre em crianças com distúrbios convulsivos ou com antecedentes de convulsões febris.
No entanto, se o seu filho recebeu paracetamol antes ou imediatamente após receber Synflorix, os níveis de anticorpos obtidos podem ser ligeiramente reduzidos. Desconhece-se se a redução dos níveis de anticorpos tem impacto na proteção contra as doenças neumocócicas.
Synflorix contém sódio
Este medicamento contém menos de 1 mmol de sódio (23 mg) por dose, isto é, é essencialmente “isento de sódio”.
3. Como é administrado Synflorix
Como usar a vacina
Synflorix é injetado sempre num músculo. Geralmente no músculo da coxa ou na parte superior do braço.
Quantidade a usar
Geralmente o seu filho (desde as 6 semanas aos 6 meses de idade) receberá um ciclo de 4 injeções de acordo com as recomendações oficiais, mas o profissional de saúde pode empregar um esquema de vacinação diferente. É importante seguir as instruções do médico ou da enfermeira para completar o ciclo de injeções.
- Cada injeção será administrada com pelo menos um mês de diferença, exceto a última injeção (de recorde), que será administrada pelo menos seis meses após a terceira injeção.
- A primeira injeção pode ser administrada a partir das 6 semanas de idade. A última injeção (de recorde) pode ser administrada a partir dos 9 meses de idade.
- Será informado de quando o seu filho deve voltar para as próximas injeções.
Recém-nascidos prematuros (nascidos após a semana 27 e antes da semana 37 de gravidez):
O seu filho (desde os 2 meses aos 6 meses de idade) receberá 3 injeções com um intervalo de pelo menos um mês de diferença entre cada dose. O seu filho receberá uma injeção adicional (de recorde) pelo menos seis meses após a última injeção.
As crianças de 7 a 11 meses de idade receberão 2 injeções. Cada injeção será administrada com pelo menos um mês de diferença. Será administrada uma terceira injeção (de recorde) durante o segundo ano de vida com pelo menos dois meses de diferença.
As crianças de 12 meses a 5 anos receberão 2 injeções. Cada injeção será administrada com pelo menos dois meses de diferença.
Populações especiais:
As crianças desde as 6 semanas até aos 5 anos de idade com um maior risco de sofrer uma infecção neumocócica (como aquelas com infecção por VIH, com anemia falciforme, com o baço danificado ou em mau funcionamento) podem receber Synflorix. Por favor, consulte o seu médico para obter informações sobre o número e o momento das injeções para o seu filho.
Se o seu filho perder uma injeção
Se o seu filho não receber uma das injeções, é importante que peça outra consulta. Dessa forma, você e o seu médico poderão falar sobre os passos a serem dados para proteger o seu filho.
Se tiver alguma outra dúvida sobre o uso desta vacina, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Posíveis efeitos adversos
Assim como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram. Os seguintes efeitos adversos podem ocorrer com este medicamento:
Podem ocorrer de forma muito rara reações alérgicas graves (até com 1 de 10.000 doses da vacina). Estas reações podem ser reconhecidas por:
- erupções abultadas que picam (habões)
- inchação, às vezes do rosto ou da boca (angioedema), que causa dificuldade para respirar
- desmaio.
Em geral, estas reações ocorrerão antes de sair da consulta do médico. Em qualquer caso, se o seu filho tiver algum desses sintomas, contacte urgentemente um médico.
Muito frequentes(podem ocorrer com mais de 1 de cada 10 doses da vacina): dor, vermelhidão e inchação do local onde é administrada a injeção, temperatura alta, de 38 °C ou superior (febre), sonolência, irritabilidade, perda de apetite.
Frequentes(podem ocorrer até com 1 de cada 10 doses da vacina): endurecimento do local onde é administrada a injeção.
Pouco frequentes(podem ocorrer até com 1 de cada 100 doses da vacina): picazón, aparecimento de coágulos sanguíneos, sangramento ou pequenos nódulos onde é administrada a injeção, náuseas, diarreia ou malestar (vómitos), choro não habitual, paradas temporárias da respiração (apneia) se o seu filho nasceu prematuro (às 28 semanas de gravidez ou antes), dor de cabeça, erupção cutânea, inflamação difusa no membro injetado, afetando às vezes a articulação adjacente, urticária.
Raros(podem ocorrer até com 1 de cada 1.000 doses da vacina): convulsões sem temperatura elevada ou devidas a temperatura elevada (febre), reações alérgicas, tais como alergias na pele, colapso (flacidez muscular repentina), períodos de inconsciência ou perda de conhecimento e palidez ou mudança de cor da pele para um tom azulado.
Muito raros(podem ocorrer até com 1 de cada 10.000 doses da vacina): doença de Kawasaki (alguns dos sinais graves da doença são: febre, erupção cutânea, inchação dos gânglios linfáticos, inflamação e erupção das membranas mucosas da boca e da garganta).
As doses de recorde de Synflorix podem aumentar o risco de efeitos adversos.
Para crianças maiores de 12 meses, o risco de dor no local da injeção pode aumentar com a idade.
Em crianças muito prematuras (nascidas às 28 semanas de gestação ou antes) durante os 2-3 dias posteriores à vacinação, os períodos entre respirações podem ser mais longos do que o normal.
Comunicação de efeitos adversos
Se o seu filho experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Synflorix
Mantenha este medicamento fora da vista e do alcance das crianças.
- Não utilize este medicamento após a data de validade que aparece no envase. A data de validade é o último dia do mês que se indica.
- Conservar na geladeira (entre 2 °C e 8 °C).
- Conservar no embalagem original para protegê-lo da luz.
- Não congelar.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Synflorix
- Os princípios ativos são:
Uma dose de 0,5 ml contém:
Polissacarídeo do sorotipo pneumocócico 11,2 1 micrograma
Polissacarídeo do sorotipo pneumocócico 41,2 3 microgramas
Polissacarídeo do sorotipo pneumocócico 51,2 1 micrograma
Polissacarídeo do sorotipo pneumocócico 6B1,2 1 micrograma
Polissacarídeo do sorotipo pneumocócico 7F1,2 1 micrograma
Polissacarídeo do sorotipo pneumocócico 9V1,2 1 micrograma
Polissacarídeo do sorotipo pneumocócico 141,2 1 micrograma
Polissacarídeo do sorotipo pneumocócico 18C1,3 3 microgramas
Polissacarídeo do sorotipo pneumocócico 19F1,4 3 microgramas
Polissacarídeo do sorotipo pneumocócico 23F1,2 1 micrograma
1 adsorvido em fosfato de alumínio 0,5 miligramas de Al3+ no total
2 conjugado com proteína D (derivada de Haemophilus influenzaenão tipável) como proteína transportadora 9–16 microgramas
3 conjugado com toxoide tetânico como proteína transportadora 5–10 microgramas
4 conjugado com toxoide diftérico como proteína transportadora 3–6 microgramas
- Os demais componentes são: cloreto de sódio (para mais informações, ver seção 2) e água para preparações injetáveis
Aspecto do produto e conteúdo do envase
- Suspensão injetável em seringa pré-carregada
- Synflorix é uma suspensão turva de cor branca.
- Synflorix está disponível em seringa pré-carregada de 1 dose, com ou sem agulhas separadas; tamanhos de envase de 1, 10 e 50.
- Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Bélgica
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Bélgica/België/Belgien GlaxoSmithKline Pharmaceuticals s.a./n.v. Tel: + 32 10 85 52 00 | Lituânia GlaxoSmithKline Biologicals SA Tel: +370 80000334 |
?????? GlaxoSmithKline Biologicals SA ????: +359 80018205 | Luxemburgo/Luxemburgo GlaxoSmithKline Pharmaceuticals s.a./n.v. Tel: + 32 10 85 52 00 |
República Tcheca GlaxoSmithKline s.r.o. Tel: + 420 2 22 00 11 11 | Hungria GlaxoSmithKline Biologicals SA Tel.: +36 80088309 |
Dinamarca GlaxoSmithKline Pharma A/S Tlf: + 45 36 35 91 00 | Malta GlaxoSmithKline Biologicals SA Tel: +356 80065004 |
Alemanha GlaxoSmithKline GmbH & Co. KG Tel: + 49 (0)89 360448701 | Países Baixos GlaxoSmithKline BV Tel: + 31 (0)33 2081100 |
Estônia GlaxoSmithKline Biologicals SA Tel: +372 8002640 | Noruega GlaxoSmithKline AS Tlf: + 47 22 70 20 00 |
Grécia GlaxoSmithKline Μονοπρ?σωπη A.E.B.E Tηλ: + 30 210 68 82 100 | Áustria GlaxoSmithKline Pharma GmbH. Tel: + 43 (0)1 97075 0 |
Espanha GlaxoSmithKline, S.A. Tel: + 34 900 202 700 | Polônia GSK Services Sp. z o.o. Tel.: + 48 (22) 576 9000 |
França Laboratoire GlaxoSmithKline Tél: + 33 (0) 1 39 17 84 44 | Portugal GlaxoSmithKline - Produtos Farmacêuticos, Lda. Tel: + 351 21 412 95 00 |
Croácia GlaxoSmithKline Biologicals SA Tel.: +385 800787089 | Romênia GlaxoSmithKline Biologicals SA Tel: +40 800672524 |
Irlanda GlaxoSmithKline (Irlanda) Ltd Tel: + 353 (0)1 495 5000 | Eslovênia GlaxoSmithKline Biologicals SA Tel: +386 80688869 |
Islândia Vistor hf. Sími: +354 535 7000 | República Eslovaca GlaxoSmithKline Biologicals SA Tel: +421 800500589 |
Itália GlaxoSmithKline S.p.A. Tel:+ 39 (0)45 7741 111 | Finlândia GlaxoSmithKline Oy Puh/Tel: + 358 10 30 30 30 |
Chipre GlaxoSmithKline Biologicals SA Τηλ: +357 80070017 | Suécia GlaxoSmithKline AB Tel: + 46 (0)8 638 93 00 |
Letônia GlaxoSmithKline Biologicals SA Tel: +371 80205045 | Reino Unido (Irlanda do Norte) GlaxoSmithKline Biologicals SA Tel: +44 (0)800 221 441 |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada sobre este medicamento está disponível no site da Agência Europeia de Medicamentos http://www.ema.europa.eu.
Esta informação é destinada apenas a profissionais do setor sanitário:
Durante o armazenamento da seringa pré-carregada pode ser observado um depósito fino de cor branca com um sobrenadante claro transparente. Isso não constitui um sinal de deterioração.
Antes da administração, deve-se inspecionar visualmente o conteúdo da seringa pré-carregada tanto antes como após agitar para observar se existe alguma substância estranha e/ou variação do aspecto físico. Em caso de que se observe alguma dessas circunstâncias, descartar a vacina.
Deve-se deixar que a vacina atinja a temperatura ambiente antes de seu uso.
A vacina deve ser agitada bem antes de seu uso.
A vacina é destinada apenas para administração por via intramuscular. Não administrar por via intravascular.
Se Synflorix for administrado junto com outras vacinas, devem ser usados diferentes locais de injeção.
Synflorix não deve ser misturado com outras vacinas.
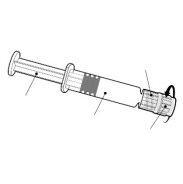
Instruções para a seringa pré-carregada
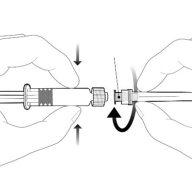
| Segure a seringa pelo corpo, não pelo émbolo. Desrosqueie a tampa da seringa girando-a no sentido contrário ao das agulhas do relógio. |
| Para inserir a agulha, conecte a base ao adaptador luer-locke gire-o um quarto de volta no sentido das agulhas do relógio até que sinta que se bloqueia. Não retire o émbolo da seringa do corpo. Se isso ocorrer, não administre a vacina. |
Eliminação de resíduos
A eliminação do produto não utilizado e de todos os materiais que tenham estado em contato com ele será realizada de acordo com a regulamentação local.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a SYNFLORIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDAFabricante: Glaxosmithkline BiologicalsRequer receita médicaForma farmacêutica: INJETÁVEL, 4 microgramas/doseSubstância ativa: pneumococcus, purified polysaccharides antigen conjugatedFabricante: Merck Sharp & Dohme B.V.Requer receita médicaForma farmacêutica: INJETÁVEL, 25 microgramas de cada serotipo/0,5mlSubstância ativa: pneumococcus, purified polysaccharides antigenFabricante: Merck Sharp & Dohme De Espana S.A.Requer receita médica
Alternativas a SYNFLORIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a SYNFLORIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA em Ukraina
Médicos online para SYNFLORIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de SYNFLORIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA – sujeita a avaliação médica e regras locais.