SUNLENCA 464 mg SOLUÇÃO INJETÁVEL

Pergunte a um médico sobre a prescrição de SUNLENCA 464 mg SOLUÇÃO INJETÁVEL

Como usar SUNLENCA 464 mg SOLUÇÃO INJETÁVEL
Introdução
Prospecto: informação para o paciente
Sunlenca 464 mg solução injetável
lenacapavir
Este medicamento está sujeito a monitorização adicional, o que agilizará a detecção de nova informação sobre a sua segurança. Pode contribuir comunicando os efeitos adversos que possa ter. A parte final da seção 4 inclui informação sobre como comunicar esses efeitos adversos.
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informação importante para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Sunlenca e para que é utilizado
- O que precisa saber antes de que lhe administrem Sunlenca
- Como é administrado Sunlenca
- Possíveis efeitos adversos
- Conservação de Sunlenca
- Conteúdo do envase e informação adicional
1. O que é Sunlenca e para que é utilizado
Sunlenca contém o princípio ativo lenacapavir. Trata-se de um medicamento antirretroviral conhecido como um inibidor da cápside.
Sunlenca é um medicamento de ação prolongada e é utilizado em combinação com outros medicamentos antirretroviraispara tratar o vírus da imunodeficiência humana tipo 1 (VIH), o vírus que causa a síndrome da imunodeficiência adquirida (sida).
É utilizado para tratar a infecção por VIH em adultos com opções de tratamento limitadas (por exemplo, quando outros medicamentos antirretrovirais não são suficientemente eficazes ou não são adequados).
O tratamento com Sunlenca em combinação com outros antirretrovirais reduz a quantidade de VIH presente no organismo. Isso melhorará a função do sistema imunitário (as defesas naturais do organismo) e diminuirá o risco de desenvolver doenças associadas à infecção por VIH.
2. O que precisa saber antes de que lhe administrem Sunlenca
Não receba Sunlenca
- Se é alérgico a lenacapavir ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
- Se está tomando algum dos seguintes medicamentos:
- rifampicina, utilizada para tratar algumas infecções bacterianas como a tuberculose
- carbamazepina, fenitoína, utilizadas para prevenir as crises convulsivas
- erva de São João (Hypericum perforatum), um medicamento à base de plantas utilizado para a depressão e a ansiedade
?Se acredita que isso se aplica a si, não receba Sunlenca e informe o seu médico imediatamente.
Advertências e precauções
Consulte o seu médico antes de usar Sunlenca
- Consulte o seu médico ou farmacêutico se tem ou teve doença hepática grave ou se os testes mostraram problemas de fígado. O seu médico avaliará detidamente se tratar ou não com Sunlenca.
Enquanto estiver usando Sunlenca
Uma vez que comece a usar Sunlenca, esteja atento a:
- Sinais de inflamação ou infecção.
?Se notar algum desses sintomas, informe o seu médico imediatamente.Para mais informação, ver seção 4, Possíveis efeitos adversos.
As consultas periódicas são importantes
É importante que assista às suas consultas agendadaspara receber a injeção de Sunlenca para controlar a infecção por VIH e evitar que a sua doença piore. Fale com o seu médico se está considerando interromper o tratamento. Se houver um atraso na administração da sua injeção ou se deixar de receber Sunlenca, terá que tomar outros medicamentos para tratar a infecção por VIH e reduzir o risco de desenvolver resistência viral.
Crianças e adolescentes
Não administre este medicamento a crianças menores de 18 anos de idade. Não se estudou ainda o uso de Sunlenca em pacientes menores de 18 anos de idade, por isso se desconhece como é seguro e eficaz o medicamento neste grupo de idade.
Outros medicamentos e Sunlenca
Informa o seu médico ou farmacêutico se está tomando, tomou recentemente ou possa ter que tomar qualquer outro medicamento. Sunlenca pode interagir com outros medicamentos. Isso pode impedir que Sunlenca ou outros medicamentos funcionem corretamente ou piorar os efeitos adversos. Em alguns casos, o seu médico pode ter que ajustar a dose ou verificar as concentrações sanguíneas.
Medicamentos que nunca se devem tomar com Sunlenca:
- rifampicina, utilizada para tratar algumas infecções bacterianas como a tuberculose
- carbamazepina, fenitoína, utilizadas para prevenir as crises convulsivas
- erva de São João (Hypericum perforatum), um medicamento à base de plantas utilizado para a depressão e a ansiedade
?Se está tomando algum desses medicamentos, não receba Sunlenca injetável e informe o seu médico imediatamente.
Consulte o seu médico especialmente se está tomando:
- antibióticos que contenham:
- rifabutina
- antiepilépticos, utilizados para tratar a epilepsia e prevenir as crises convulsivas (convulsões), que contenham:
- oxcarbazepina ou fenobarbital
- medicamentos utilizados para tratar o VIH, que contenham:
- atazanavir/cobicistat, efavirenz, nevirapina, tipranavir/ritonavir ou etravirina
- medicamentos utilizados para tratar a cefaleia migrañosa, que contenham:
- dihidroergotamina ou ergotamina
- medicamentos utilizados para tratar a impotência e a hipertensão pulmonar, que contenham:
- sildenafilo ou tadalafilo
- medicamentos utilizados para tratar a impotência, que contenham:
- vardenafilo
- corticoesteroides (também conhecidos como “esteroides”) administrados por via oral ou mediante injeção, utilizados para tratar alergias, doenças inflamatórias intestinais e outras doenças diversas que implicam inflamação no organismo, que contenham:
- dexametasona ou hidrocortisona/cortisona
- medicamentos utilizados para reduzir o colesterol, que contenham:
- lovastatina ou simvastatina
- antiarrítmicos utilizados para tratar problemas cardíacos, que contenham:
- digoxina
- medicamentos utilizados para ajudar a dormir, que contenham:
- midazolam ou triazolam
- anticoagulantes utilizados para prevenir e tratar os coágulos de sangue, que contenham:
- rivaroxabán, dabigatrán ou edoxabán
?Informe o seu médico se está tomando algum desses medicamentosou se começar a tomar algum desses medicamentos durante o tratamento com Sunlenca. Não interrompa o tratamento sem consultar o seu médico.
Sunlenca é um medicamento de ação prolongada. Deve saber que, se decidir interromper ou mudar o tratamento para outro após consultar o seu médico, concentrações baixas de lenacapavir (o princípio ativo de Sunlenca) podem permanecer no seu organismo durante vários meses após a última injeção. Não se prevê que a presença dessas concentrações baixas restantes afete outros medicamentos antirretrovirais que tome posteriormente para tratar a infecção por VIH. No entanto, a presença de concentrações baixas de lenacapavir no seu organismo pode afetar outros medicamentos que tome nos 9 meses seguintes à última injeção de Sunlenca. Pergunte ao seu médico se esses medicamentos são seguros para si após interromper o tratamento com Sunlenca.
Gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Como medida de precaução, deve evitar o uso de Sunlenca durante a gravidez a menos que o seu médico lhe indique o contrário.
Recomenda-se que as mulheres que apresentam infecção por VIH não deem o peito aos seus filhos, pois a infecção por VIH-1 pode ser transmitida ao bebê através do leite materno. Se está amamentando ou tem intenção de amamentar, fale com o seu médico o mais rápido possível.
Condução e uso de máquinas
Não se prevê que Sunlenca afete a sua capacidade para conduzir ou utilizar máquinas.
Sunlenca contém sódio
Este medicamento contém menos de 1 mmol de sódio (23 mg) por injeção; isto é, é essencialmente “isento de sódio”.
3. Como é administrado Sunlenca
Sunlenca é utilizado em combinação com outros medicamentos antirretroviraispara tratar a infecção por VIH. O seu médico lhe indicará quais outros medicamentos deve tomar para tratar a infecção por VIH e quando deve tomá-los.
O tratamento com Sunlenca começa com a tomada de comprimidos por via oral, seguido de injeções administradas pelo seu médico ou enfermeiro, tal como se descreve a seguir.
Consulte o seu médico antes de tomar os comprimidos.O médico lhe informará quando deve começar a tomar os comprimidos e para quando se programará a sua consulta para receber as primeiras injeções.
Dia 1 de tratamento:
- Dois comprimidos por via oral. Estes podem ser tomados com ou sem alimentos.
Dia 2 de tratamento:
- Dois comprimidos por via oral. Estes podem ser tomados com ou sem alimentos.
Dia 8 de tratamento:
- Um comprimido por via oral. Este pode ser tomado com ou sem alimentos.
Dia 15 de tratamento:
- Duas injeções no abdômen (a barriga) administradas ao mesmo tempo pelo seu médico ou enfermeiro.
A cada 6 meses:
- Duas injeções no abdômen administradas ao mesmo tempo pelo seu médico ou enfermeiro.
Se lhe administrarem mais Sunlenca injetável do que o devido
O seu médico ou um enfermeiro lhe administrará este medicamento, por isso é pouco provável que lhe administrem demasiado. Informe o médico ou o enfermeiro se lhe preocupar.
Se esquecer uma injeção de Sunlenca
- É importante que assista às suas consultas agendadas a cada 6 meses para receber as injeções de Sunlenca. Isso ajudará a controlar a infecção por VIH e a evitar que a sua doença piore.
- Se acredita que não poderá comparecer à sua consulta para receber as injeções, ligue para o seu médico o mais rápido possível para discutir as suas opções de tratamento.
Consulte o prospecto de Sunlenca comprimidos se esquecer de tomar ou vomitar os comprimidos.
Se interromper o tratamento com Sunlenca
Não interrompa o tratamento com Sunlenca sem falar com o seu médico. Continue o tratamento com as injeções de Sunlenca enquanto o seu médico o recomendar. Interromper Sunlenca pode afetar gravemente o funcionamento de tratamentos futuros para o VIH.
?Fale com o seu médico se desejar interromper o tratamento com as injeções de Sunlenca.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Possíveis efeitos adversos graves: informe um médico imediatamente
- Qualquer sinal de inflamação ou de infecção. Em alguns pacientes com infecção avançada por VIH (sida) e antecedentes de infecções oportunistas (infecções que ocorrem em pessoas com um sistema imunitário débil), podem produzir-se sinais e sintomas de inflamação por infecções previas pouco após iniciar o tratamento contra o VIH. Acredita-se que esses sintomas se devem a uma melhoria da resposta imunitária do organismo, que lhe permite combater infecções que poderiam ter estado presentes sem sintomas óbvios.
- Podem produzir-se também distúrbios autoimunitários, nos quais o sistema imunitário ataca os tecidos saudáveis do organismo, após começar a tomar medicamentos para a infecção por VIH. Os distúrbios autoimunitários podem produzir-se muitos meses após o início do tratamento. Esteja atento a qualquer sintoma de infecção ou outros sintomas, como:
- debilidade muscular
- debilidade do organismo que se inicia nas mãos e nos pés e se desloca para o tronco
- palpitações, tremor ou hiperatividade
?Se notar algum desses sintomas ou qualquer sintoma de inflamação ou infecção, informe o seu médico imediatamente.
Efeitos adversos muito frequentes
(podem afetar mais de 1 de cada 10 pessoas)
- Reações no local da injeção de Sunlenca.
Os sintomas podem incluir:
- dor e desconforto
- um caroço ou massa endurecida
- reação inflamatória como vermelhidão, picazão e inchação
Efeitos adversos frequentes
(podem afetar até 1 de cada 10 pessoas)
- Náuseas
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informação sobre a segurança deste medicamento.
5. Conservação de Sunlenca
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta do frasco e na caixa após {CAD}. A data de validade é o último dia do mês que se indica.
Este medicamento não requer qualquer temperatura especial de conservação. Conservar no embalagem original para protegê-lo da luz.
6. Conteúdo do envase e informação adicional
Composição de Sunlenca
O princípio ativo é lenacapavir. Cada frasco monodose contém 463,5 mg de lenacapavir.
Os outros componentes são
Macrogol (E1521), água para preparações injetáveis.
Aspecto de Sunlenca e conteúdo do envase
Sunlenca solução injetável (injetável) é uma solução transparente, de amarela a marrom, sem partículas visíveis. Sunlenca é apresentado em dois frascos de vidro que contêm 1,5 ml de solução injetável cada um. Estes frascos vêm incluídos em um kit de administração que também contém 2 dispositivos de acesso ao frasco (um dispositivo que permitirá ao seu médico ou enfermeiro extrair Sunlenca do frasco), 2 seringas descartáveis e 2 agulhas para injeção.
Título da autorização de comercialização
Gilead Sciences Ireland UC
Carrigtohill
County Cork, T45 DP77
Irlanda
Responsável pela fabricação
Gilead Sciences Ireland UC
IDA Business & Technology Park
Carrigtohill
County Cork
Irlanda
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização:
Bélgica Gilead Sciences Belgium SRL-BV Tel: + 32 (0) 24 01 35 50 | Lituânia Gilead Sciences Poland Sp. z o.o. Tel.: + 48 22 262 8702 |
Grécia Gilead Sciences Ireland UC Tel: + 353 (0) 1 686 1888 | Luxemburgo Gilead Sciences Belgium SRL-BV Tel: + 32 (0) 24 01 35 50 |
República Tcheca Gilead Sciences s.r.o. Tel: + 420 910 871 986 | Hungria Gilead Sciences Ireland UC Tel.: + 353 (0) 1 686 1888 |
Dinamarca Gilead Sciences Sweden AB Tlf: + 46 (0) 8 5057 1849 | Malta Gilead Sciences Ireland UC Tel: + 353 (0) 1 686 1888 |
Alemanha Gilead Sciences GmbH Tel: + 49 (0) 89 899890-0 | Países Baixos Gilead Sciences Netherlands B.V. Tel: + 31 (0) 20 718 36 98 |
Estônia Gilead Sciences Poland Sp. z o.o. Tel.: +48 22 262 8702 | Noruega Gilead Sciences Sweden AB Tlf: + 46 (0) 8 5057 1849 |
Chipre Gilead Sciences Ελλάς Μ.ΕΠΕ. Τηλ: + 30 210 8930 100 | Áustria Gilead Sciences GesmbH Tel: + 43 1 260 830 |
Espanha Gilead Sciences, S.L. Tel: + 34 91 378 98 30 | Polônia Gilead Sciences Poland Sp. z o.o. Tel.: + 48 22 262 8702 |
França Gilead Sciences Tél: + 33 (0) 1 46 09 41 00 | Portugal Gilead Sciences, Lda. Tel: + 351 21 7928790 |
Croácia Gilead Sciences Ireland UC Tel: + 353 (0) 1 686 1888 | Romênia Gilead Sciences (GSR) S.R.L. Tel: + 40 31 631 18 00 |
Irlanda Gilead Sciences Ireland UC Tel: + 353 (0) 214 825 999 | Eslovênia Gilead Sciences Ireland UC Tel: + 353 (0) 1 686 1888 |
Islândia Gilead Sciences Sweden AB Sími: + 46 (0) 8 5057 1849 | República Eslovaca Gilead Sciences Slovakia s.r.o. Tel: + 421 232 121 210 |
Itália Gilead Sciences S.r.l. Tel: + 39 02 439201 | Finlândia Gilead Sciences Sweden AB Puh/Tel: + 46 (0) 8 5057 1849 |
Chipre Gilead Sciences Ελλάς Μ.ΕΠΕ. Τηλ: + 30 210 8930 100 | Suécia Gilead Sciences Sweden AB Tel: + 46 (0) 8 5057 1849 |
Letônia Gilead Sciences Poland Sp. z o.o. Tel.: + 48 22 262 8702 | Reino Unido (Irlanda do Norte) Gilead Sciences Ireland UC Tel: + 44 (0) 8000 113 700 |
Data da última revisão deste prospecto:
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos: http://www.ema.europa.eu.
-----------------------------------------------------------------------------
Esta informação está destinada apenas a profissionais de saúde:
Instruções de uso-Sunlenca 464 mg solução injetável
O kit contém
2 frascos |
|
2 dispositivos de acesso ao frasco |
|
2 seringas |
|
2 agulhas para injeção |
|
Todos os componentes são para uso único.
São necessárias duas injeções de 1,5 mlpara uma dose completa. É necessário utilizar o dispositivo de acesso ao frasco.
Verifique que:
- O frasco contém uma solução de amarela a marrom, sem partículas
- O conteúdo não está danificado
- O medicamento não está vencido
| |
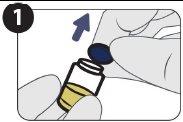
| Retire a tampa. |
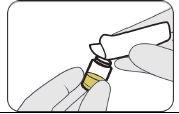
| Limpe o lacre do frasco com uma toalhita embebida em álcool. |
| |
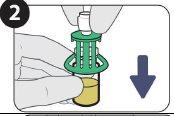
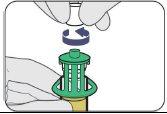
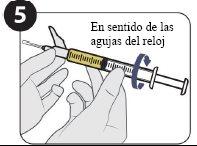
| Empurre para baixo. |
| Gire para retirar. |
| |
|
|
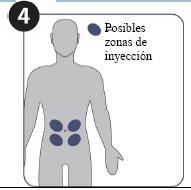
| |
| Possíveis zonas de injeção (a um mínimo de 5 cm do umbigo) |
| |
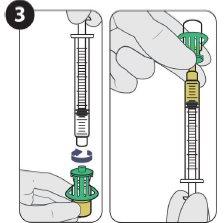
| Acople a agulha para injeção e encha 1,5 ml. |
| |
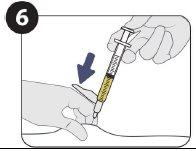
| Injete 1,5 ml de Sunlenca por via subcutânea |
| |
| Repita os passos para a 2ª injeção em uma nova zona de injeção. |
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a SUNLENCA 464 mg SOLUÇÃO INJETÁVELForma farmacêutica: COMPRIMIDO, 300 mgSubstância ativa: lenacapavirFabricante: Gilead Sciences Ireland Unlimited CompanyRequer receita médicaForma farmacêutica: COMPRIMIDO, 150 mgSubstância ativa: maravirocFabricante: Viiv Healthcare B.V.Requer receita médicaForma farmacêutica: COMPRIMIDO, 300 mgSubstância ativa: maravirocFabricante: Viiv Healthcare B.V.Requer receita médica
Alternativas a SUNLENCA 464 mg SOLUÇÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a SUNLENCA 464 mg SOLUÇÃO INJETÁVEL em Ukraine
Médicos online para SUNLENCA 464 mg SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de SUNLENCA 464 mg SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.