RELISTOR 12 mg/0,6 ml SOLUÇÃO INJETÁVEL

Pergunte a um médico sobre a prescrição de RELISTOR 12 mg/0,6 ml SOLUÇÃO INJETÁVEL

Como usar RELISTOR 12 mg/0,6 ml SOLUÇÃO INJETÁVEL
Introdução
Prospecto: informação para o utilizador
Relistor 12 mg/0,6 ml solução injectável
Bromuro de metilnaltrexona
Leia todo o prospecto atentamente antes de começar a usar este medicamento,porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que o ler novamente.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Relistor e para que é utilizado
- O que necessita de saber antes de começar a usar Relistor
- Como usar Relistor
- Possíveis efeitos adversos
- Conservação de Relistor
- Conteúdo do envase e informação adicional
1. O que é Relistor e para que é utilizado
Relistor contém um princípio ativo denominado bromuro de metilnaltrexona que actua bloqueando os efeitos adversos dos medicamentos opioides para a dor que afectam o intestino.
Está indicado para o tratamento da constipação produzida por medicamentos para a dor moderada a intensa chamados opioides (por exemplo, morfina ou codeína). É utilizado para doentes quando outros medicamentos para a constipação (laxantes) não deram resultado. O seu médico prescreveu-lhe opioides. O seu médico indicar-lhe-á se deve continuar com a sua terapia laxante habitual ou interrompê-la quando começar a tomar este medicamento.
O medicamento só deve ser utilizado em adultos (com 18 anos de idade ou mais).
2. O que necessita de saber antes de começar a usar Relistor
Não use Relistor
- se é alérgico a bromuro de metilnaltrexona ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6).
- se si ou o seu médico suspeitam que tem ou teve obstrução intestinal ou que o seu abdómen se encontra num estado que requer uma intervenção cirúrgica imediata (este estado deve ser diagnosticado pelo seu médico)
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar Relistor
- Se tem sintomas estomacais graves que persistem ou pioram, contacte o seu médico imediatamente, pois poderá tratar-se de perfuração da parede intestinal (perfuração intestinal). Ver a secção 4.
- Se tem a doença de Crohn ou uma úlcera gastrointestinal.
- Se sente mal-estar, vomita, treme, tem suores, tem dor abdominal e/ou sente o seu ritmo cardíaco rápido logo após tomar Relistor, fale com o seu médico.
- Se tem uma doença grave de fígado ou rim.
- Se começar a ter uma diarreia grave ou persistente (deposições aquosas repetidas), suspenda o tratamento e consulte o seu médico imediatamente.
- É importante que tenha um banho e, se necessário, disponha de ajuda, pois poderá ter uma deposição nos 30 minutos após a injeção do medicamento.
- Informa o seu médico se sente dor estomacal persistente, náuseas ou vómitos, tanto se aparecem pela primeira vez como se pioram os que já tinha.
- Informa o seu médico se lhe foi feita uma colostomia, se tem um catéter peritoneal ou sofre de doença diverticular ou impactação fecal, pois este medicamento deve ser utilizado com precaução nestes casos.
- Se recebe tratamento paliativo para a sua doença avançada, este medicamento só deve ser utilizado por tempo limitado, que por norma será inferior a 4 meses.
- Este medicamento não deve ser utilizado no tratamento de doentes com constipação não relacionada com o uso de opioides. Informa o seu médico se já padecia de constipação antes de tomar os medicamentos opioides (para a dor).
Crianças e adolescentes
Não administre este medicamento a crianças e adolescentes menores de 18 anos, pois se desconhecem os riscos e benefícios potenciais
Uso de Relistor com outros medicamentos
Informa o seu médico ou farmacêutico se está a utilizar, utilizou recentemente ou poderá ter que utilizar qualquer outro medicamento.
Poderá ser que o seu médico lhe permita tomar outros medicamentos, mesmo os que estivesse a utilizar antes para a constipação.
Gravidez e amamentação
Desconhecem-se os efeitos que o bromuro de metilnaltrexona pode produzir em mulheres grávidas.
O seu médico decidirá se pode utilizar Relistor em caso de estar grávida.
As mulheres que utilizem este medicamento não devem estar em período de amamentação, porque se desconhece se o bromuro de metilnaltrexona passa para o leite materno.
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Condução e uso de máquinas
O mareio é um efeito adverso frequente deste medicamento. Isto poderá afectar a sua capacidade para conduzir ou manejar máquinas.
Informação importante sobre alguns dos componentes de Relistor
Este medicamento contém menos de 23 mg (1 mmol) de sódio por dose, pelo que se considera essencialmente “isento de sódio”.
3. Como usar Relistor
Siga exactamente as instruções de administração deste medicamento indicadas pelo seu médico.
Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
A dose recomendada para doentes com dor crónica (excepto doentes que recebem tratamento paliativo para doença avançada) é de 12 mg de bromuro de metilnaltrexona (0,6 ml de solução) administrada mediante injeção subcutânea (debaixo da pele), a demanda, como mínimo 4 vezes por semana e como máximo uma vez por dia (7 vezes por semana).
A dose recomendada para doentes que recebem tratamento paliativo para doença avançada é de 8 mg de bromuro de metilnaltrexona (0,4 ml de solução) para doentes que pesem entre 38 -61 kg ou uma dose de 12 mg (0,6 ml de solução) para doentes que pesem entre 62-114 kg. A dose é administrada cada 48 horas (cada 2 dias) mediante injeção subcutânea (debaixo da pele).
O seu médico determinará a dose.
Este medicamento é administrado mediante injeção sob a pele (injeção subcutânea) em: (1) a parte superior das pernas (coxas), (2) o abdómen (barriga, debaixo do umbigo) e (3) a parte superior dos braços (se não se injetar si mesmo). (Ver INSTRUÇÕES PARA PREPARAR E ADMINISTRAR UMA INJEÇÃO DE RELISTOR).
Depois de lhe ser administrada a injeção, poderá ter uma deposição num prazo de tempo que varia de alguns minutos a várias horas. Por isso, é recomendável que tenha uns sanitários ou uma cama próxima de si.
Se usar mais Relistor do que deve
Se utilizou mais medicamento do que devia (ou bem porque se injetou demasiada quantidade de uma só vez, ou bem por utilizar mais de uma injeção em 24 horas), poderá marear-se ao levantar-se, de modo que informe um médico ou farmacêutico imediatamente. Leve o cartonagem do medicamento sempre consigo, mesmo que esteja vazio.
Se esqueceu de usar Relistor
Se esqueceu de administrar-se uma dose, informe o seu médico ou farmacêutico o mais rápido possível. Não tome uma dose dupla para compensar as doses esquecidas.
Se interromper o tratamento com Relistor
Consulte um médico ou farmacêutico se desejar interromper o tratamento com este medicamento.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Foram observados casos de perfuração da parede intestinal (perfuração gastroduodenal) em doentes que utilizam Relistor. Desconhece-se a frequência deste acontecimento de acordo com os dados disponíveis. Se sofre dor estomacal intensa ou persistente, deixe de tomar este medicamento e ligue imediatamente para o seu médico.
Os seguintes efeitos adversos são muito frequentes e podem afectar mais de 1 de cada 10 doentes. Se experimentar alguns destes efeitos adversos de forma intensa ou persistente, consulte o seu médico:
- Dor abdominal (dor estomacal)
- Náuseas
- Diarreia (deposições líquidas frequentes)
- Flatulência (arrotos, ventosidades)
Outros efeitos adversos frequentes que podem afectar até 1 de cada 10 doentes são:
- Mareio (tontura)
- Sintomas semelhantes aos do síndrome de abstinência de opioides (como sensação de frio, arrepios, rinorreia, suores, pele de galinha, sofocos, latidos rápidos)
- Reacções no local de injeção (por exemplo, comichão, queimadura, dor, vermelhidão, inflamação no local onde lhe foi administrada a injeção)
- Vómitos
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante a comunicação de efeitos adversos, pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Relistor
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no envase e no frasco após EXP. A data de validade é o último dia do mês que se indica.
Este medicamento não requer qualquer temperatura especial de conservação.
Mantenha o frasco no envase para protegê-lo da luz.
Só deve utilizar este medicamento se a solução for transparente, de incolora a cor amarela clara, e não contém partículas ou posos.
Os medicamentos não devem ser deitados fora por os despejos nem para o lixo. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Deste modo, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Relistor
- O princípio ativo é brometo de metilnaltrexona. Cada frasco de 0,6 ml contém 12 mg de brometo de metilnaltrexona. Um ml de solução contém 20 mg de brometo de metilnaltrexona.
- Os outros componentes são cloreto de sódio, edetato de sódio e cálcio, cloridrato de glicina, água para injeção, ácido clorídrico (para ajustar o pH) e hidróxido de sódio (para ajustar o pH).
Aspecto do produto e conteúdo do envase
Relistor é uma solução injetável. É transparente, de incolora a cor amarela clara e não contém partículas visíveis.
Cada frasco contém 0,6 ml de solução.
Os envases que contêm mais de um frasco apresentam envases de cartão interiores com: um frasco, uma seringa de 1 ml com agulha retrátil e duas torundas impregnadas em álcool.
Estão disponíveis as seguintes apresentações:
1 frasco
Envase com 2 frascos, 2 seringas para injeção com agulhas retráteis e 4 torundas impregnadas em álcool (contém 2 envases de cartão interiores)
Envase com 7 frascos, 7 seringas para injeção com agulhas retráteis e 14 torundas impregnadas em álcool (contém 7 envases de cartão interiores).
Pode ser que apenas alguns tamanhos de envases estejam comercializados.
Título da autorização de comercialização
Bausch Health Ireland Limited
3013 Lake Drive
Citywest Business Campus
Dublin 24, D24PPT3
Irlanda
Responsável pela fabricação
Bausch Health Ireland Limited
3013 Lake Drive
Citywest Business Campus
Dublin 24, D24PPT3
Irlanda
Bausch Health Poland Sp. z o. o.,
ul. Przemyslowa 2,
35-959 Rzeszów,
Polônia
Przedsiebiorstwo Farmaceutyczne Jelfa SA
ul. Wincentego Pola 21
58-500 Jelenia Góra,
Polônia
Data da última revisão deste prospecto: 11/2023
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos (EMA) http://www.ema.europa.eu/.
PERGUNTAS PARA O PACIENTE
Esta seção contém perguntas importantes que você precisará responder antes de usar e durante o tratamento com Relistor.
Se você responder “Não” a qualquer uma das seguintes perguntas durante o curso do seu tratamento com o medicamento, por favor, entre em contato com seu médico, enfermeiro ou farmacêutico.
- Você está recebendo terapia opioide (como morfina ou codeína) para sua doença?
- Passaram-se 48 horas ou mais desde sua última evacuação intestinal?
- Você está familiarizado com a técnica de autoinjeção ou seu médico (ou enfermeiro ou farmacêutico) a explicou?
- Você tem suficiente mobilidade para chegar ao banheiro, ou tem alguém que o cuide e possa ajudá-lo?
- Você tem o número de contato do seu centro de saúde?
INSTRUÇÕES PARA PREPARAR E ADMINISTRAR UMA INJEÇÃO DE RELISTOR
Esta seção é dividida nas subseções seguintes:
Introdução
Etapa 1: Instruções prévias à injeção
Etapa 2: Preparação da seringa
Etapa 3: Escolha e preparação do local de injeção
Etapa 4a: Injeção de Relistor utilizando o envase que dispõe de seringa e agulha retrátil
Etapa 4b: Injeção de Relistor utilizando uma seringa e agulha normais
Etapa 5: Eliminação de resíduos
Introdução
As seguintes instruções explicam como injetar Relistor. Por favor, leia-as cuidadosamente e siga-as passo a passo. Seu médico, enfermeiro ou farmacêutico o instruirá sobre as técnicas de autoadministração. Não tente administrar uma injeção até que esteja seguro de que sabe como fazer. Esta injeção não deve ser misturada na mesma seringa com nenhum outro medicamento.
Pode ser que você tenha um envase que contenha um envase de cartão interior com tudo o que é necessário para injetar ou, por outro lado, pode ser que você tenha apenas o frasco de medicamento. Se você receber apenas o frasco, precisará de vários algodões (torundas) com álcool e uma seringa de injeção.
Etapa 1: Instruções prévias à injeção
- Escolha uma superfície plana, limpa e bem iluminada onde possa colocar o conteúdo do seu envase de Relistor. Certifique-se de que tem tempo suficiente para completar a injeção.
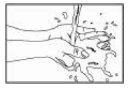
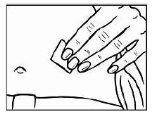
- Lave minuciosamente as mãos com sabão e água morna.
|
- Prepare os materiais necessários para a injeção, o frasco de Relistor, uma seringa de 1 ml para a injeção subcutânea (com ou sem agulha retrátil), 2 torundas impregnadas com álcool e uma gaze ou algodão.
- Certifique-se de que a solução que se encontra dentro do frasco é transparente, de incolora a cor amarela clara e não contém partículas visíveis. Se não for assim, não use a solução. Entre em contato com seu farmacêutico, enfermeira ou médico para que o aconselhem.
Etapa 2: Preparação da seringa
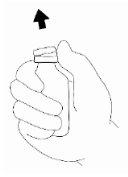
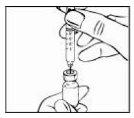
- Remova a tampa de plástico protetora do frasco.
|
- Limpe a tampa de borracha do frasco com uma torunda impregnada com álcool e coloque-a na superfície de trabalho plana. Certifique-se de não tocar novamente a tampa de borracha.
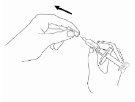
- Pegue a seringa da sua superfície de trabalho. Segure o cilindro (corpo) da seringa com uma mão e puxe o capuchão da agulha reta para fora. Deixe o capuchão da agulha na superfície de trabalho. NÃO TOQUE A AGULHA NEM PERMITA QUE ELA ROCE QUALQUER OUTRA SUPERFÍCIE.
|
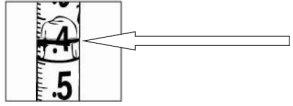
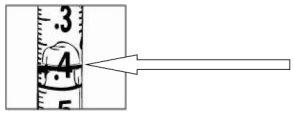
Com cuidado, puxe o êmbolo da seringa bem até a marca de 0,4 ml para 8 mg de Relistor ou até a marca de 0,6 ml para 12 mg de Relistor. Seu médico, enfermeiro ou farmacêutico o informará sobre a dosagem que foi prescrita e com que frequência deve injetá-la. Para pacientes que recebem tratamento paliativo para doença avançada, as dosagens mais comuns estão incluídas na tabela seguinte. Geralmente a dosagem é dada a cada 48 horas (cada dois dias) por meio de uma injeção subcutânea (debaixo da pele).
Peso do paciente em kg | Encha a seringa até o nível de ml (dosagem) |
Menos de 38 kg | 0,15 mg/kg |
38-61 kg | 0,4 ml (8 mg) |
62-114 kg | 0,6 ml (12 mg) |
Mais de 114 kg | 0,15 mg/kg |
Para pacientes com dor crônica (exceto pacientes que recebem tratamento paliativo para doença avançada), carregue a seringa até a marca de 0,6 ml para 12 mg de Relistor.
| Puxe com cuidado o êmbolo até a marca correta da seringa (por exemplo, 0,4 ml se foram prescritos 8 mg) |
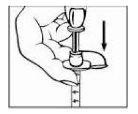
- Insira a agulha reta para baixo no centro da tampa do frasco. Não insira a agulha em ângulo, pois pode se curvar ou quebrar. Para que não escorregue, segure com a outra mão o frasco sobre a superfície de trabalho. Você notará uma leve resistência quando a agulha atravessar a tampa. Verifique se a ponta da agulha está dentro do frasco.
|
- Para expulsar o ar da seringa, empurre suavemente o êmbolo para baixo para injetar o ar no frasco de Relistor.
|
- Se estiver usando a seringa com agulha retrátil fornecida, NÃO EMPURRE OÊMBOLO ATÉ O FIM. Pare de empurrar o êmbolo quando notar resistência. Se empurrar o êmbolo até o fim, ouvirá um “clic”, o que significará que o mecanismo de segurança foi ativado, após o que a agulha desaparecerá na seringa. Se isso acontecer, descarte o produto e comece novamente com outro frasco e outra seringa.
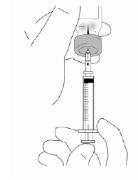
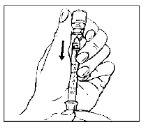
Com a agulha ainda no frasco, dê a volta ao frasco completamente (ver figura). Mantenha a seringa à altura dos olhos de tal forma que veja as marcas de dosagem e certifique-se de que a ponta da agulha está sempre dentro do líquido. Puxe o êmbolo lentamente até a marca de 0,4 ml ou de 0,6 ml da seringa ou como foi aconselhado, dependendo da dosagem prescrita pelo seu médico, enfermeiro ou farmacêutico. Pode ser que você observe que resta um pouco de líquido ou bolhas dentro do frasco uma vez que a seringa esteja cheia apropriadamente, é normal.
|
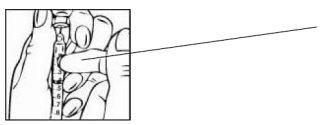
- Com a agulha ainda metida no frasco de Relistor dado a volta (invertido), verifique se há bolhas de ar na seringa. Se houver bolhas, golpeie suavemente a seringa com um dedo para fazer com que elas subam para a parte superior; continue segurando o frasco de Relistor e a seringa. Empurre suavemente o êmbolo para cima até que saiam todas as bolhas de ar. Se você derramar parte da solução no frasco, puxe lentamente o êmbolo para trás para extrair novamente a quantidade correta de solução para a seringa. Devido ao design de segurança da seringa, uma pequena bolha de ar pode resistir à extração. Não se preocupe com isso, pois não afetará a exatidão da dosagem nem representará um risco para a sua saúde.
| Golpeie a seringa colocada boca para baixo e elimine todas as bolhas de ar empurrando o êmbolo para cima |
- Certifique-se sempre de que tem a dosagem correta na seringa. Se não tiver certeza, entre em contato com seu médico, enfermeiro ou farmacêutico.
| Certifique-se de que tem a dosagem correta na seringa (por exemplo, 0,4 ml se foram prescritos 8 mg). |
- Retire a seringa e a agulha do frasco. Mantenha a agulha unida à seringa. Não toque a agulha nem permita que ela roce qualquer superfície. Uma vez que o medicamento esteja na seringa, ele deve ser usado nas 24 horas seguintes, pois Relistor é afetado pela luz e pode não funcionar corretamente se for deixado na seringa por mais de 24 horas.
|
Etapa 3: Escolha e preparação do local de injeção
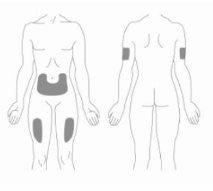
- As três zonas do corpo recomendadas para a injeção de Relistor são: (1) parte superior das pernas (coxas), (2) abdômen (barriga) e (3) parte superior dos braços (somente se outra pessoa aplicar a injeção).
|
- Recomenda-se mudar o local de injeção cada vez que se administrar uma injeção. Evite injeções repetidas exatamente no mesmo local usado anteriormente. Não injete em zonas em que a pele esteja sensível, tenha hematomas, esteja vermelha ou esteja dura. Evite zonas com cicatrizes ou estrias.
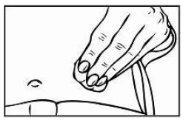
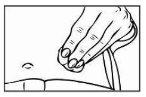
- Para preparar a zona da pele em que se vai injetar Relistor, limpe o local de injeção com uma torunda impregnada de álcool. NÃO TOQUE NOVAMENTE ESTA ZONA ANTES DE ADMINISTRAR A INJEÇÃO. Deixe o ponto de injeção secar ao ar antes da injeção.
|
Etapa 4a: Injeção de Relistor utilizando o envase que dispõe de seringa e agulha retrátil
- Segure a seringa cheia com a agulha apontando para cima, e examine novamente a seringa para ver se contém bolhas de ar. Se houver bolhas, golpeie suavemente a seringa com um dedo até que as bolhas de ar subam para a parte superior da seringa. Empurre lentamente o êmbolo para cima para expulsar as bolhas de ar fora da seringa.
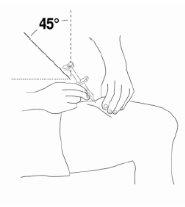
- Segure a seringa com uma mão como se fosse um lápis. Com a outra mão, pegue suavemente um pedaço da zona limpa da pele e segure-a firmemente.
- Insira toda a agulha na pele em um ângulo leve (45 graus) com um movimento rápido e curto.
|
- Uma vez inserida a agulha, solte o pedaço da pele e empurre lentamente o êmbolo totalmente para baixo até que a seringa esteja vazia e você ouça um clique.
- Quando ouvir um “clic”, isso significa que se injetou todo o conteúdo, após o que a agulha se retrai automaticamente da pele e fica coberta (dentro da seringa). Pode ocorrer um pequeno sangramento no local de injeção. Pressione com uma gaze ou algodão sobre o local de injeção. Não esfregue o local de injeção. Se necessário, pode cobrir o local de injeção com um adesivo.
|
Etapa 4b: Injeção da solução Relistor utilizando uma seringa e agulha normais
- Segure a seringa cheia com a agulha apontando para cima, e examine novamente a seringa para ver se contém bolhas de ar. Se houver bolhas, golpeie suavemente a seringa com um dedo até que as bolhas de ar subam para a parte superior da seringa. Empurre lentamente o êmbolo para cima para expulsar as bolhas de ar fora da seringa.
Empurre lentamente o êmbolo para cima para expulsar as bolhas de ar fora da seringa.
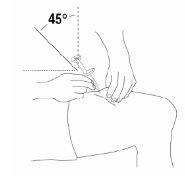
- Segure a seringa com uma mão como se fosse um lápis. Com a outra mão, pegue suavemente um pedaço da zona limpa da pele e segure-a firmemente.
- Insira toda a agulha na pele em um ângulo leve (45 graus) com um movimento rápido e curto.
|
- Uma vez inserida a agulha, solte o pedaço da pele e empurre lentamente o êmbolo totalmente para baixo para injetar Relistor.
- Uma vez que a seringa esteja vazia, retire com um movimento rápido a agulha da pele, no mesmo ângulo em que a inseriu. Pode ocorrer um pequeno sangramento no local de injeção. Pressione com uma gaze ou algodão sobre o local de injeção. Não esfregue o local de injeção. Se necessário, pode cobrir o local de injeção com um adesivo.
|
Etapa 5: Eliminação de resíduos
A seringa com a agulha retrátil ou a seringa e agulha NUNCA devem ser reutilizadas. Não coloque NUNCA o capuchão novamente na agulha. Elimine a seringa com a agulha retrátil ou a agulha e a seringa em um recipiente resistente a perfurações, como indicado pelo seu médico, enfermeira ou farmacêutico.

Quanto custa o RELISTOR 12 mg/0,6 ml SOLUÇÃO INJETÁVEL em Espanha em 2025?
O preço médio do RELISTOR 12 mg/0,6 ml SOLUÇÃO INJETÁVEL em dezembro de 2025 é de cerca de 37.12 EUR. Os valores podem variar consoante a região, a farmácia e a necessidade de receita. Confirme sempre com uma farmácia local ou fonte online para obter informações atualizadas.
- País de registo
- Preço médio em farmácia37.12 EUR
- Disponibilidade em farmáciasProblema de disponibilidade reportado
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a RELISTOR 12 mg/0,6 ml SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, 12 mgSubstância ativa: methylnaltrexone bromideFabricante: Bausch Health Ireland LimitedRequer receita médicaForma farmacêutica: COMPRIMIDO, 12,5 mgSubstância ativa: naloxegolFabricante: Grünenthal GmbhRequer receita médicaForma farmacêutica: COMPRIMIDO, 25 mgSubstância ativa: naloxegolFabricante: Grünenthal GmbhRequer receita médica
Médicos online para RELISTOR 12 mg/0,6 ml SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de RELISTOR 12 mg/0,6 ml SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.