PERGOVERIS (300 UI + 150 UI)/0,48 mL SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDA


Como usar PERGOVERIS (300 UI + 150 UI)/0,48 mL SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDA
Introdução
Prospecto: informação para o utilizador
Pergoveris (300 UI + 150 UI)/0,48 ml solução injetável em caneta pré-carregada
folitropina alfa/lutropina alfa
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Pergoveris e para que é utilizado
- O que precisa saber antes de começar a usar Pergoveris
- Como usar Pergoveris
- Efeitos adversos possíveis
- Conservação de Pergoveris
- Conteúdo do envase e informações adicionais
1. O que é Pergoveris e para que é utilizado
O que é Pergoveris
Pergoveris contém dois princípios ativos diferentes denominados “folitropina alfa” e “lutropina alfa”. Ambos pertencem à família de hormonas chamadas “gonadotropinas”, que estão implicadas na reprodução e na fertilidade.
Para que é utilizado Pergoveris
Este medicamento é utilizado para estimular o desenvolvimento dos folículos (cada um contendo um óvulo) nos ovários com o fim de ajudá-la a engravidar. Está destinado ao uso em mulheres adultas (18 anos de idade ou mais) com níveis baixos (déficit grave) de “hormona foliculoestimulante” (FSH) e “hormona luteinizante” (LH). Normalmente, estas mulheres são inférteis.
Como actua Pergoveris
Os princípios ativos de Pergoveris são cópias das hormonas naturais FSH e LH. No corpo:
- a FSH estimula a produção de óvulos
- a LH estimula a libertação dos óvulos.
Ao substituir as hormonas ausentes, Pergoveris permite às mulheres com níveis baixos de FSH e LH desenvolver um folículo, a partir do qual se libertará um óvulo, após uma injeção da hormona “gonadotropina coriónica humana (hCG)”. Isso ajuda as mulheres a engravidar.
2. O que precisa saber antes de começar a usar Pergoveris
Antes de iniciar o tratamento deve ser avaliada a sua fertilidade e a do seu parceiro por parte de um médico experiente no tratamento dos distúrbios da fertilidade.
Não use Pergoveris:
- se é alérgico à hormona foliculoestimulante (FSH), à hormona luteinizante (LH) ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- se tem um tumor cerebral (no hipotálamo ou na hipófise).
- se tem ovários grandes ou bolsas de líquido no interior dos ovários (quistes ováricos) de origem desconhecida.
- se tem hemorragia vaginal inexplicável.
- se tem cancro dos ovários, do útero ou da mama.
- se tem uma afecção que impossibilitaria um embarazo normal, como menopausa precoce, malformações dos órgãos sexuais ou tumores benignos no útero.
Não utilize este medicamento se alguma das condições acima se aplica a si. Se não tem certeza, consulte o seu médico, farmacêutico ou enfermeiro antes de começar a usar este medicamento.
Advertências e precauções
Consulte o seu médico, farmacêutico ou enfermeiro antes de começar a usar Pergoveris.
Porfiria
Consulte o seu médico antes de iniciar o tratamento, se si ou algum membro da sua família padece porfiria (uma incapacidade para degradar as porfirinas que pode transmitir-se de pais a filhos).
Informar imediatamente o seu médico se:
- a sua pele se torna frágil e lhe saem bolhas com facilidade, especialmente nas zonas expostas ao sol com frequência.
- tem dor de estômago, de braços ou pernas.
Nestes casos, o seu médico pode recomendar-lhe interromper o tratamento.
Síndroma de hiperestimulação ovárica (SHO)
Este medicamento estimula os seus ovários, o que aumenta o risco de experimentar síndroma de hiperestimulação ovárica (SHO). Isso ocorre quando os seus folículos se desenvolvem demasiado e se transformam em quistes de grande tamanho. Se tem dor na região pélvica, aumenta de peso rapidamente, tem náuseas ou vómitos ou dificuldade para respirar, consulte imediatamente o seu médico, que pode ordenar-lhe interromper o tratamento (ver na secção 4, em “Efeitos adversos mais graves”).
Em caso de que não ovule e se respeitam a dose e a pauta posológica recomendadas, o SHO grave é menos provável que ocorra. O tratamento com Pergoveris raramente causa SHO grave. Isso é mais provável se se administra o medicamento que se usa para a maturação folicular final (que contém gonadotropina coriónica humana, hCG) (ver detalhes na secção 3, em “Que quantidade se deve usar”). Em caso de desenvolver SHO, o seu médico pode não lhe prescrever hCG neste ciclo de tratamento e aconselhá-lo a que se abstenha de realizar o coito ou que utilize um método anticonceptivo de barreira durante pelo menos 4 dias.
O seu médico assegurará um controlo cuidadoso da resposta ovárica, mediante ecografias e análises de sangue (determinações do estradiol), antes e durante o tratamento.
Embarazo múltiplo
Se usa Pergoveris, tem um risco mais alto de engravidar de mais de um bebé de cada vez (“embarazo múltiplo”, geralmente gémeos) do que se engravidasse por concepção natural. O embarazo múltiplo pode causar complicações médicas para si e os seus bebés. Pode reduzir o risco de embarazo múltiplo usando a dose correcta de Pergoveris às horas correctas.
Para minimizar o risco de embarazo múltiplo, recomenda-se realizar ecografias e análises de sangue.
Aborto
Se se submete a estimulação dos seus ovários para produzir óvulos, a probabilidade de ter um aborto é maior do que na média das mulheres.
Embarazo ectópico
As mulheres que já sofreram alguma vez bloqueio ou danos das trompas de Falópio (enfermidade tubárica) apresentam risco de embarazo com implantação do embrião fora do útero (embarazo ectópico). Isso é assim tanto se o embarazo é por concepção espontânea como se é logrado mediante tratamentos de fertilidade.
Problemas de coagulação do sangue (episódios tromboembólicos)
Consulte o seu médico antes de começar a usar Pergoveris se si ou algum membro da sua família já sofreu alguma vez coágulos de sangue na perna ou no pulmão, infarto de miocárdio ou acidente vascular cerebral. Pode ter um risco mais alto de sofrer coágulos de sangue graves ou de agravar os coágulos existentes com o tratamento com Pergoveris.
Tumores dos órgãos sexuais
Foram comunicados tumores nos ovários e noutros órgãos sexuais, tanto benignos como malignos, em mulheres que foram submetidas a múltiplas pautas para o tratamento da infertilidade.
Reacções alérgicas
Foram comunicados casos isolados de reacções alérgicas não graves a Pergoveris. Se si já teve alguma vez este tipo de reacção com um medicamento semelhante, consulte o seu médico antes de começar a usar Pergoveris.
Crianças e adolescentes
Pergoveris não deve ser utilizado em crianças e adolescentes menores de 18 anos de idade.
Outros medicamentos e Pergoveris
Informar o seu médico ou farmacêutico se está a utilizar, utilizou recentemente ou possa ter que utilizar qualquer outro medicamento.
Não use Pergoveris com outros medicamentos na mesma injeção. Pode usar Pergoveris com um preparado de folitropina alfa autorizado em injeções diferentes se o seu médico o prescrever.
Embarazo e amamentação
Não use Pergoveris se está grávida ou em período de amamentação.
Condução e uso de máquinas
Não se espera que este medicamento afete a sua capacidade para conduzir ou utilizar máquinas.
Pergoveris contém sódio
Pergoveris contém menos de 1 mmol de sódio (23 mg) por dose; isto é, é essencialmente “isento de sódio”.
3. Como usar Pergoveris
Siga exactamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
Uso deste medicamento
- Pergoveris está desenhado para ser injetado justo debaixo da pele (por via subcutânea). Para minimizar a irritação cutânea, seleccione um local de injeção diferente cada dia.
- O seu médico ou enfermeiro ensinar-lhe-á a usar a caneta pré-carregada de Pergoveris para se injetar o medicamento.
- Se estão de acordo com que possa administrar Pergoveris com segurança, doravante poderá preparar e injetar o medicamento si mesma em casa.
- Se se administra Pergoveris si mesma, leia e siga atentamente as “Instruções de uso”.
Que quantidade se deve usar
Uma pauta de tratamento começa com a dose recomendada de Pergoveris que contém 150 unidades internacionais (UI) de folitropina alfa e 75 UI de lutropina alfa, cada dia.
- Em função da resposta, o seu médico pode decidir adicionar diariamente uma dose de um preparado de folitropina alfa autorizado à injeção de Pergoveris. Neste caso, normalmente a dose de folitropina alfa é incrementada cada 7 ou 14 dias em 37,5-75 UI.
- O tratamento continua até que se obtenha a resposta desejada. Isso acontece quando se desenvolveu um folículo adequado, avaliado mediante ecografias e análises de sangue.
- Podem ser necessárias até cinco semanas.
Quando se obtém a resposta desejada, será administrada uma injeção única de gonadotropina coriónica humana (hCG) de 24 a 48 horas após a sua última injeção de Pergoveris. O melhor momento para manter relações sexuais é o mesmo dia da injeção de hCG e no dia seguinte. Como alternativa, também pode ser realizada inseminação intrauterina ou outro procedimento de reprodução medicamente assistida, a critério do seu médico.
Se se obtém uma resposta excessiva, será interrompido o tratamento e não lhe será administrada hCG (ver na secção 2, em “Síndroma de hiperestimulação ovárica (SHO)”). Neste caso, o seu médico prescrever-lhe-á uma dose de folitropina alfa mais baixa no ciclo seguinte.
Se usa mais Pergoveris do que deve
Desconhecem-se os efeitos de uma sobredose de Pergoveris; no entanto, pode esperar-se que se produza um SHO. Não obstante, isso só ocorrerá se se administrar hCG (ver na secção 2, em “Síndroma de hiperestimulação ovárica (SHO)”).
Se esqueceu de usar Pergoveris
Não use uma dose dupla para compensar as doses esquecidas. Entre em contacto com o seu médico.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Efeitos adversos possíveis
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora não todas as pessoas os sofram.
Efeitos adversos mais graves
Consulte o seu médico imediatamente se detectar algum dos efeitos adversos que se listam a seguir. O médico poderá dizer-lhe que deixe de usar Pergoveris.
Reacções alérgicas
As reacções alérgicas, como erupção cutânea, rubor da pele, bolhas, inchaço da face com dificuldade para respirar, por vezes podem ser graves. Este efeito adverso é muito raro.
Síndroma de hiperestimulação ovárica (SHO)
- Dor pélvica, acompanhada de náuseas ou vómitos. Podem ser sintomas do síndroma de hiperestimulação ovárica (SHO). É possível que os seus ovários tenham reagido de forma excessiva ao tratamento e se tenham desenvolvido quistes ováricos ou bolsas de líquido de grande tamanho (ver na secção 2 em “Síndroma de hiperestimulação ovárica (SHO)”). Este efeito adverso é frequente. Se lhe acontecer isso, o seu médico terá que examiná-la o mais breve possível.
- O SHO pode agravar-se com ovários claramente aumentados de tamanho, diminuição da produção de urina, aumento de peso, dificuldade para respirar e/ou possível acumulação de líquido no abdómen ou no peito. Este efeito adverso é pouco frequente (pode afectar até 1 de cada 100 pessoas).
- As complicações do SHO como torção ovárica ou coagulação do sangue ocorrem em raras ocasiões (podem afectar até 1 de cada 1 000 pessoas).
- Os problemas de coagulação do sangue graves (episódios tromboembólicos), normalmente com SHO grave, ocorrem muito raramente. Isso poderá causar dor no peito, sensação de falta de ar, acidente vascular cerebral ou infarto de miocárdio. Em casos raros isso também poderá ocorrer independentemente do SHO (ver na secção 2 em “Problemas de coagulação do sangue (episódios tromboembólicos)”).
Outros efeitos adversos
Muito frequentes (podem afectar mais de 1 de cada 10 pessoas)
- bolsas de líquido no interior dos ovários (quistes ováricos)
- dor de cabeça
- reacções locais no local de injeção como dor, picazón, hematomas, inchaço ou irritação.
Frequentes (podem afectar até 1 de cada 10 pessoas)
- diarreia
- dor no peito
- náuseas ou vómitos
- dor abdominal ou pélvica
- cãibras ou distensão abdominal
Muito raros (podem afectar até 1 de cada 10 000 pessoas)
- o asma pode piorar.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Pergoveris
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e na caixa após CAD. A data de validade é o último dia do mês que se indica.
Conservar em frigorífico (entre 2 °C e 8 °C). Não congelar.
Conservar no embalagem original para protegê-lo da luz.
Uma vez aberta, a caneta pré-carregada pode ser conservada durante um máximo de 28 dias fora do frigorífico (a 25 °C). Não use nenhuma porção de medicamento restante na caneta pré-carregada após 28 dias.
Não utilize Pergoveris se observar sinais visíveis de deterioração, se o líquido contém partículas ou não é transparente.
Após a injeção, elimine a agulha usada de forma segura.
Os medicamentos não devem ser deitados pelo saneamento nem para o lixo. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do frasco e informações adicionais
Composição de Pergoveris
Os princípios ativos são folitropina alfa e lutropina alfa.
- Cada caneta pré-carregada de Pergoveris (300 UI + 150 UI)/0,48 ml contém 300 UI (unidades internacionais) de folitropina alfa e 150 UI de lutropina alfa em 0,48 ml e pode administrar duas doses de Pergoveris 150 UI/75 UI.
Os demais componentes são:
- Sacarose, monohidrocloruro de arginina, poloxámero 188, metionina, fenol, hidrogenofosfato de disódio dihidrato, dihidrogenofosfato de sódio monohidrato e água para preparações injetáveis. São adicionadas pequenas quantidades de ácido fosfórico concentrado e de hidróxido sódico para manter níveis de acidez (níveis de pH) normais.
Aspecto do produto e conteúdo do frasco
Pergoveris é apresentado como uma solução injetável transparente incolora a ligeiramente amarela em uma caneta pré-carregada multidose:
- Pergoveris (300 UI + 150 UI)/0,48 ml é apresentado em embalagens que contêm 1 caneta pré-carregada multidose e 5 agulhas para injeção descartáveis.
Título da autorização de comercialização
Merck Europe B.V., Gustav Mahlerplein 102, 1082 MA Amsterdam, Países Baixos
Responsável pela fabricação
Merck Serono S.p.A, Via delle Magnolie 15 (Zona industrial), 70026 Modugno (Bari), Itália
Data da última revisão deste prospecto: (MM/AAAA)
Outras fontes de informação
A informação detalhada deste medicamento está disponível na página web da Agência Europeia de Medicamentos: http://www.ema.europa.eu.
Instruções de uso
Pergoveris
(300UI + 150UI)/0,48ml (450UI + 225UI)/0,72ml (900UI + 450UI)/1,44ml
Solução injetável em caneta pré-carregada
Folitropina alfa/Lutropina alfa
Informação importante sobre a caneta pré-carregada de Pergoveris
- Leia as instruções de uso e o prospecto antes de usar a caneta pré-carregada Pergoveris.
- Siga sempre todas as indicações dessas instruções de uso e a formação que lhe foi proporcionada pelo profissional de saúde, pois podem ser distintas das recebidas anteriormente. Esta informação permitirá evitar erros no tratamento ou infecções por picada de agulha ou lesões por quebra do vidro.
- A caneta pré-carregada de Pergoveris é apenas para injeção por via subcutânea.
- Use apenas a caneta pré-carregada de Pergoveris se o profissional de saúde lhe ensinar como usá-la corretamente.
- O profissional de saúde lhe dirá quantas canetas pré-carregadas de Pergoveris precisa para completar o seu tratamento.
- Coloque a injeção à mesma hora todos os dias.
- A caneta está disponível em três apresentações multidose diferentes:
(300 UI + 150 UI)/0,48 ml |
|
(450 UI + 225 UI)/0,72 ml |
|
(900 UI + 450 UI)/1,44 ml |
|
Nota:
- A dose máxima que pode selecionar é 300 UI para a apresentação de (300 UI + 150 UI)/0,48 ml.
- A dose máxima que pode selecionar é 450 UI para as apresentações de (450 UI + 225 UI)/0,72 ml e de (900 UI + 450 UI)/1,44 ml.
- O botão de ajuste da dose gira em incrementos de 12,5 UI até alcançar a dose desejada.
Consulte o prospecto para obter mais informações sobre a posologia recomendada e siga sempre a dose que lhe foi recomendada pelo seu profissional de saúde.
- Os números da janela de informação da doserepresentam o número de unidades internacionais (UI) e mostram a dose de folitropina alfa. Seu profissional de saúde lhe dirá quantas UI de folitropina alfa devem ser injetadas todos os dias.
- Os números mostrados na janela de informação da doseajudam a:
|
|
(Figura 2). |
|
(Figura 3). |
|
- Retire a agulha da caneta imediatamente após cada injeção.
Nãoreutilize as agulhas.
Nãocompartilhe a caneta ou as agulhas com nenhuma outra pessoa.
Nãouse a caneta pré-carregada de Pergoveris se ela caiu, ou se a caneta está rachada ou danificada, pois isso pode causar lesões.
Como usar o diário de tratamento da caneta pré-carregada de Pergoveris
No final das instruções de uso, está incluído um diário de tratamento. Use o diário de tratamento para anotar a quantidade injetada.
Injetar uma quantidade incorreta de medicamento pode afetar o tratamento.
- Anotar o número do dia de tratamento (coluna 1), a data (coluna 2), a hora da injeção (coluna 3) e o volume da caneta (coluna 4).
- Anotar a dose que lhe foi prescrita (coluna 5).
- Verificar se selecionou a dose correta antes de efetuar a injeção (coluna 6).
- Depois da injeção, ler o número indicado na janela de informação da dose.
- Confirmar se recebeu uma injeção completa (coluna 7) ou anotar o número indicado na janela de informação da dosese for distinto de “0” (coluna 8).
- Quando necessário, realizar outra injeção com uma segunda caneta, selecionando a dose restante que aparece escrita na seção “Quantidade a ajustar para uma segunda injeção” (coluna 8).
- Anotar essa dose restante na seção “Quantidade ajustada para a injeção”na próxima linha (coluna 6).
O uso do diário de tratamento para anotar a(s) injeção(ões) diária(s) permite verificar se recebeu a dose prescrita completa todos os dias.
Exemplo de um diário de tratamento utilizando uma caneta de (450 UI + 225 UI)/0,72 ml:
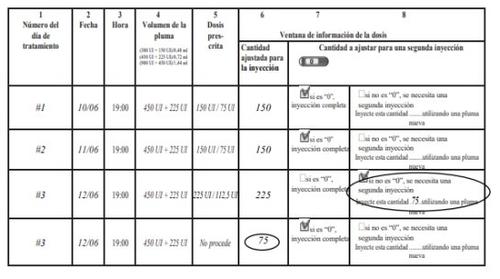
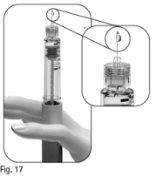
Familiarize-se com a caneta pré-carregada de Pergoveris
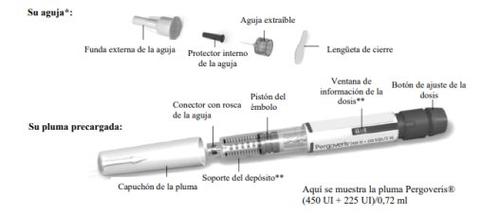
- Apenas para fins ilustrativos. As agulhas fornecidas podem ter um aspecto ligeiramente diferente.
** Os números da janela de informação da dosee do suporte do depósito representam o número de Unidades Internacionais (UI) do medicamento.
Passo1 Reúna os materiais
Nãouse um micro-ondas nem nenhum outro elemento calefactor para aquecer a caneta. | |
|
|
Nãouse nenhum utensílio, pois seu uso pode danificar a caneta. | |
| |
Nãouse a caneta pré-carregada de Pergoveris se já passou a data de validade ou se na caneta pré-carregada não está escrito Pergoveris. |
|
Paso2 Prepárese para a injeção
| |
Nãouse a caneta pré-carregada se o medicamento mudou de cor ou está turvo, pois isso pode causar uma infecção.
|
|
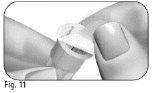
Escolha um local de injeção: | |
Nãotoque nem cubra a pele que acabou de limpar. |
|
Paso3 Acople a agulha
Importante:certifique-se sempre de usar uma agulha nova para cada injeção. Reutilizar as agulhas pode causar uma infecção. |
|
| |
| |
| |
|
|
| |
Nãouse a agulha se ela está danificada ou vencida ou se a capa externa da agulha ou a lingueta de fechamento está danificada ou solta. Usar agulhas vencidas ou agulhas com linguetas de fechamento ou capas externas da agulha danificadas pode causar uma infecção. Jogue-a em um contêiner para objetos cortantes e perfurantes e pegue uma agulha nova. | |
Nãoaperte muito a agulha ao acoplá-la, pois poderia ser difícil removê-la após a injeção. |
|
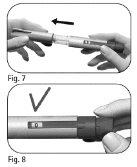
Nãodescarte a capa externa da agulha, pois isso evitará lesões por picada de agulha e infecções ao separar a agulha da caneta pré-carregada. |
|
Nãorecoloque o protetor interno da agulha, pois isso pode provocar lesões por picada de agulha e infecções. |
|
|
Se | Então |
|
Usa uma caneta nova | Verifique se há uma gotícula de líquido na ponta da agulha.
prossiga com o Paso 4 Selecione a dose.
ponta da agulha ou nas proximidades, deve realizar os passos que se indicam na próxima seçãopara eliminar o ar do sistema. | |
Reutiliza uma caneta | Nãoé necessário verificar se há uma gotícula de líquido. Prossiga diretamente com o Paso 4 Selecione a dose |
Se não observar nenhuma gotícula de líquido na ponta ou nas proximidades da primeira vez que usar uma caneta nova:

- Gire com cuidado o botão de ajuste da dose para a frente até que seja mostrado “25”na janela de informação da dose(Figura 18).
- Pode girar o botão de ajuste da dose para trás se o girou mais além de “25”.
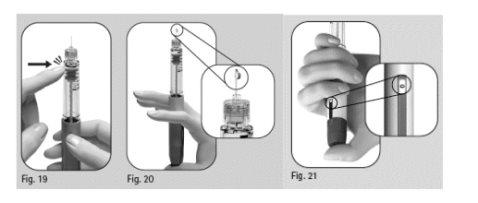
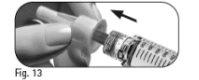
- Segure a caneta com a agulha apontando para cima.
- Golpeie suavemente o suporte do depósito (Figura 19).
- Pulse o botão de ajuste da dose por completo. Aparecerá uma gotícula de líquido na ponta da agulha (Figura 20).
- Verifique se a janela de informação da doseindica “0” (Figura 21).
- Prossiga com o Paso4 Selecione a dose.
Se não aparecer uma gotícula de líquido, entre em contato com o profissional de saúde.
Paso4 Selecione a dose
- Gire o botão de ajuste da dose até que a dose desejada apareça na janela de informação da dose.
- Exemplo: se a dose desejada é “150” UI, confirme que a janela de informação da dose mostra “150” (Figura 22). Injetar uma quantidade incorreta de medicamento pode afetar o tratamento.
|
|
|
|
- Verifique se a janela de informação da doseindica a dose prescrita completaantes de continuar com o próximo passo.
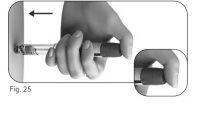
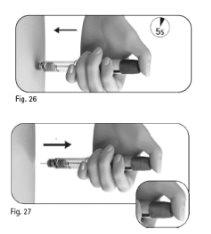
Paso5 Injete a dose
Importante:injete a dose como lhe foi ensinado pelo profissional de saúde. | |
|
|
|
|
Nota:quanto maior for a dose, mais tempo levará para injetá-la. | |
|
|
Nãosolte o botão de ajuste da dose até ter retirado a agulha da pele. |
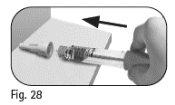
Paso6 Retire a agulha após cada injeção
|
|
| |
|
|
|
|
|
|
Nãoreutilize nem compartilhe nenhuma agulha usada. |
Paso7 Após a injeção
Se a janela de informações da dose mostrar “0”, completou a dose. Se a janela de informações da dose mostrar um número maior que “0”,a caneta pré-carregada de Pergoveris está vazia. Você não recebeu a dose prescrita completa e deve realizar o passo 7.2 descrito abaixo. |
|
|
|
Paso8 Conservação da caneta pré-carregada de Pergoveris
|
|
| |
| |
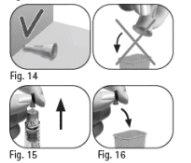
Nãoconserve a caneta com a agulha ainda acoplada, pois isso pode causar uma infecção. | |
Nãoreutilize a caneta pré-carregada de Pergoveris se ela caiu, ou se a caneta está trincada ou danificada, pois isso pode causar lesões. | |
Entre em contato com o profissional de saúde se tiver alguma dúvida. |
Diário de tratamento da caneta pré-carregada de Pergoveris
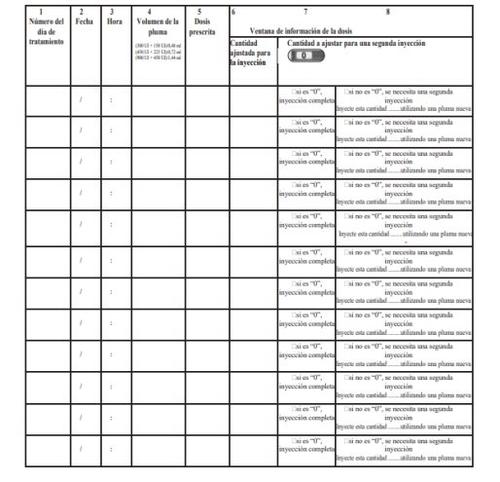
Data da última revisão destas instruções de uso:
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a PERGOVERIS (300 UI + 150 UI)/0,48 mL SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDAForma farmacêutica: INJETÁVEL, 450 UI/225 UISubstância ativa: combinationsFabricante: Merck Europe B.V.Requer receita médicaForma farmacêutica: INJETÁVEL, 900 UI/450 UISubstância ativa: combinationsFabricante: Merck Europe B.V.Requer receita médicaSubstância ativa: combinationsFabricante: Merck Europe B.V.Requer receita médica
Alternativas a PERGOVERIS (300 UI + 150 UI)/0,48 mL SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDA noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a PERGOVERIS (300 UI + 150 UI)/0,48 mL SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDA em Украина
Médicos online para PERGOVERIS (300 UI + 150 UI)/0,48 mL SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDA
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de PERGOVERIS (300 UI + 150 UI)/0,48 mL SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDA – sujeita a avaliação médica e regras locais.