FINTEPLA 2,2 mg/ml SOLUÇÃO ORAL

Pergunte a um médico sobre a prescrição de FINTEPLA 2,2 mg/ml SOLUÇÃO ORAL

Como usar FINTEPLA 2,2 mg/ml SOLUÇÃO ORAL
Introdução
Prospecto: informação para o paciente
Fintepla 2,2 mg/ml solução oral
fenfluramina
Este medicamento está sujeito a acompanhamento adicional, o que agilizará a detecção de nova informação sobre a sua segurança. Pode contribuir comunicando os efeitos adversos que possa ter. A parte final da seção 4 inclui informação sobre como comunicar esses efeitos adversos.
Leia todo o prospecto atentamente antes de que o senhor ou seu filho/a comece a tomar este medicamento, porque contém informação importante para o senhor.
- Conserva este prospecto, porque pode ter que relê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito apenas para o senhor ou para seu filho/a, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que o senhor ou que seu filho/a, porque pode prejudicá-las.
- Se o senhor ou seu filho/a experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Fintepla e para que é utilizado
- O que precisa saber antes de que o senhor ou seu filho comece a tomar Fintepla
- Como tomar Fintepla
- Posíveis efeitos adversos
- Conservação de Fintepla
- Conteúdo do envase e informação adicional
1. O que é Fintepla e para que é utilizado
Fintepla contém o princípio ativo fenfluramina.
Fintepla é utilizado como tratamento complementar para tratar as crises convulsivas de pacientes de 2 anos de idade ou mais que têm um tipo de epilepsia denominado síndrome de Dravet ou outro denominado síndrome de Lennox-Gastaut. Pode ajudar a reduzir o número e a gravidade das crises.
Não se conhece exatamente como age Fintepla. No entanto, acredita-se que age aumentando a atividade cerebral de uma substância denominada serotonina e o receptor sigma 1, o que pode reduzir as crises.
2. O que precisa saber antes de que o senhor ou seu filho/a comece a tomar Fintepla
Não tome Fintepla
- se é alérgico a fenfluramina ou a algum dos outros componentes deste medicamento (incluídos na seção 6);
- se padece um problema cardíaco como a «enfermidade valvular cardíaca» ou a «hipertensão arterial pulmonar» (tensão arterial elevada nas artérias dos pulmões);
- se tomou uns medicamentos que se denominam inibidores da monoamino-oxidase durante as últimas 2 semanas.
Não tome Fintepla se se cumprem em seu caso algumas das condições acima. Se não estiver seguro, consulte o médico, farmacêutico ou enfermeiro antes de tomar Fintepla.
Advertências e precauções
Consulte o seu médico, farmacêutico ou enfermeiro antes de começar a tomar Fintepla se:
- o senhor ou seu filho/a padece glaucoma;
- o senhor ou seu filho/a teve pensamentos relacionados com lesionar-se ou suicidar-se;
- o senhor ou seu filho/a está tomando um medicamento denominado ciproheptadina, que se utiliza para tratar alergias ou para melhorar o apetite.
Se alguma das situações acima for aplicável em seu caso (ou se tiver alguma dúvida), consulte o seu médico ou farmacêutico antes de tomar Fintepla.
Análises e controles
Antes de começar o tratamento com Fintepla, o médico deve rever o estado do coração do paciente com um ecocardiograma (ECO). O médico verificará que as válvulas cardíacas não apresentam nenhuma anomalia e que a tensão arterial entre o coração e os pulmões não é demasiado elevada. Uma vez que o paciente tenha começado a tomar Fintepla, terá que se submeter a uma ecocardiografia a cada 6 meses durante os 2 primeiros anos e luego uma vez ao ano. Se se interromper o tratamento com Fintepla, o paciente terá que realizar uma ecocardiografia quando tenham transcorrido 3-6 meses da última dose.
O seu médico também deverá verificar o seu peso antes do tratamento e durante o mesmo, pois Fintepla pode provocar perda de peso.
«Síndrome serotoninérgico»
Indique ao médico ou farmacêutico, antes de tomar Fintepla, se o senhor ou seu filho/a está tomando medicamentos que possam aumentar o nível cerebral de serotonina. Isso se deve ao fato de que tomar esses medicamentos junto com Fintepla pode provocar o síndrome serotoninérgico, um distúrbio que pode ter um desfecho mortal. Os medicamentos que podem aumentar o nível de serotonina são:
- «triptanos» (como o sumatriptano) que se utiliza para a enxaqueca;
- medicamentos IMAO, que se usam para a depressão;
- medicamentos ISRS ou IRSN, que se usam para a depressão e ansiedade.
Esteja atento aos possíveis sintomas do síndrome serotoninérgico, que incluem:
- agitação, ver coisas que não existem (alucinações) ou desmaios;
- problemas circulatórios e cardíacos como sentir o pulso acelerado, subidas e descidas da tensão sanguínea, alta temperatura corporal, suores;
- temblores musculares e descoordenação;
- sensação de doença ou doença real e diarreia.
Informar ao médico imediatamente se apresentar algum desses efeitos adversos que se mencionaram acima.
Outros medicamentos e Fintepla
Informar ao médico ou farmacêutico se o senhor ou seu filho/a está tomando, tomou recentemente ou pudesse ter que tomar qualquer outro medicamento. Isso se deve ao fato de que Fintepla pode afetar o mecanismo de ação de outros medicamentos. Além disso, alguns medicamentos podem afetar o mecanismo de ação de Fintepla.
Fintepla pode provocar sonolência. O paciente pode sentir ainda mais sonolência se tomar medicamentos como os antidepressivos ou bem álcool ao mesmo tempo que Fintepla.
Em particular, informar ao médico ou farmacêutico se o senhor ou seu filho/a está tomando, tomou recentemente ou pudesse ter que tomar:
- estiripentol, um medicamento para a epilepsia, pois a dose de Fintepla pode ter que ser reduzida;
- «triptanos», medicamentos IMAO, IRSN ou ISRS, véase mais acima o apartado «Síndrome serotoninérgico»;
- carbamazepina, primidona, rifampicina, fenobarbital e outros barbitúricos, fenitoína ou efavirenz, pois pode ser necessário aumentar a dose de Fintepla.
Também deve falar com um médico ou farmacêutico se o senhor ou seu filho/a fuma, pois pode ser necessário aumentar a dose de Fintepla.
Gravidez e lactação
Se a paciente ou sua filha está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico antes de utilizar este medicamento.
Condução e uso de máquinas
Fale com o seu médico sobre a condução e o uso de máquinas, ou bem se o senhor ou seu filho/a vai empreender atividades tais como o ciclismo ou outros esportes, porque pode sentir sonolência após tomar este medicamento.
Fintepla contém p-hidroxibenzoato sódico de etilo (E 215) e p-hidroxibenzoato sódico de metilo (E 219)
Pode provocar reações alérgicas (possivelmente retardadas).
Fintepla contém dióxido de enxofre (E 220)
Raramente pode provocar reações de hipersensibilidade e broncoespasmo.
Fintepla contém glicose
Pode prejudicar os dentes.
Se o seu médico lhe indicou que padece uma intolerância a certos açúcares, consulte com ele antes de tomar este medicamento.
Fintepla contém sódio
Este medicamento contém menos de 1 mmol de sódio (23 mg) por 12 ml; isto é, essencialmente “isento de sódio”.
3. Como tomar Fintepla
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
O seu médico, farmacêutico ou enfermeiro calculará o volume de dose até a dose máxima recomendada, utilizando a fórmula:
Peso (kg) x dose baseada no peso (mg/kg) ÷ 2,2 mg/ml = ml de dose duas vezes ao dia
A dose calculada deve ser arredondada para o incremento graduado mais próximo.
A tabela seguinte só deve ser usada como verificação do volume de dose calculado. A tabela 1 não substituia necessidade de calcular o volume de dose específico.
Tabela 1: Intervalo de volumes de dose em ml para comprovar o cálculo | |||||
Dose sem STP concomitante* | Dose com STP concomitante ** | ||||
Categoria do peso | Dose de início | Dia7‑13 | Dia14 e posteriores | Dose de início | Dia7 e posteriores |
0,1 mg/kg duas vezes ao dia | 0,2 mg/kg duas vezes ao dia | 0,35 mg/kg duas vezes ao dia | 0,1 mg/kg duas vezes ao dia | 0,2 mg/kg duas vezes ao dia | |
3‑5 kg | 0,2‑0,3 ml | 0,3‑0,5 ml | 0,5‑0,8 ml | 0,2‑0,3 ml | 0,3‑0,5 ml |
5‑7 kg | 0,3‑0,4 ml | 0,5‑0,7 ml | 0,8‑1,2 ml | 0,3‑0,4 ml | 0,5‑0,7 ml |
7‑10 kg | 0,4‑0,5 ml | 0,7‑1 ml | 1,2‑1,6 ml | 0,4‑0,5 ml | 0,7‑1 ml |
10‑15 kg | 0.5‑0.7 ml | 1‑1,4 ml | 1,6‑2,4 ml | 0,5‑0,7 ml | 1‑1,4 ml |
15‑20 kg | 0.7‑1 ml | 1,4‑1,9 ml | 2,4‑3,2 ml | 0,7‑1 ml | 1,4‑1,9 ml |
20‑30 kg | 1‑1,4 ml | 1,9‑2,8 ml | 3,2‑4,8 ml | 1‑1,4 ml | 1,9‑2,8 ml |
30‑38 kg | 1,4‑1,8 ml | 2,8‑3,5 ml | 4,8‑6 ml (dose máxima) | 1,4‑1,8 ml | 2,8‑3,5 ml |
38‑43 kg | 1,8‑2 ml | 3,5‑4 ml | 6 ml (dose máxima) | 1,8‑2 ml | 3,5‑4 ml (dose máxima) |
43‑55 kg | 2‑2,5 ml | 4‑5 ml | 6 ml (dose máxima) | 2‑2,5 ml | 4 ml (dose máxima) |
55‑65 kg | 2,5‑3 ml | 5‑6 ml (dose máxima) | 6 ml (dose máxima) | 2,5‑3 ml | 4 ml (dose máxima) |
65‑86 kg | 3‑4 ml | 6 ml (dose máxima) | 6 ml (dose máxima) | 3‑4 ml (dose máxima) | 4 ml (dose máxima) |
86‑130 kg | 4‑6 ml (dose máxima) | 6 ml (dose máxima) | 6 ml (dose máxima) | 4 ml (dose máxima) | 4 ml (dose máxima) |
*Sem STP concomitante: a dose máxima de 13 mg duas vezes ao dia corresponde a 6 ml duas vezes ao dia. **Com STP concomitante: a dose máxima de 8,6 mg duas vezes ao dia corresponde a 4 ml duas vezes ao dia. |
Que quantidade deve tomar
- O médico indicará quantos mililitros deve tomar em cada dose.
- Tome o medicamento duas vezes ao dia.
- O médico iniciará o tratamento com o paciente com uma dose baixa. Essa dose será gradualmente aumentada de acordo com o nível de eficácia do medicamento e de como afeta o paciente.
- A quantidade máxima que o paciente pode tomar é de 6 ml duas vezes ao dia.
- Se estiver tomando estiripentol, a quantidade máxima que pode tomar é de 4 ml duas vezes ao dia.
- Não tome mais do que a dose prescrita, pois pode ter efeitos adversos graves.
Como tomar este medicamento
- Tome este medicamento por via oral.
- Tome o medicamento com comida ou entre comidas.
- Fintepla solução oral é compatível com uma dieta cetogênica.
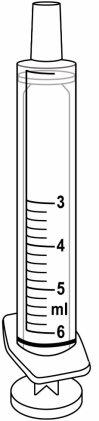
- O medicamento é um líquido. Utilize as seringas para tomada oral que se proporcionam para medir a dose, tal como se explica mais abaixo.
- Utilize a seringa verde de 3 ml para doses de até 3,0 ml.
- Utilize a seringa púrpura de 6 ml para doses compreendidas entre 3,2 e 6,0 ml.
- Fintepla solução oral é compatível com a maioria das sondas de alimentação enteral.
- Para lavar a sonda de alimentação, encha com água a seringa que se vai utilizar para aplicar a dose e lave o tubo. Repita a operação 3 vezes.
Jeringa de 3 ml – verde | Jeringa de 6 ml – púrpura |
|
|
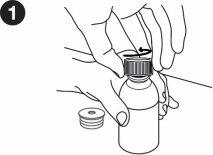
| Escriba na caixa a data em que abriu o frasco pela primeira vez. Deve colocar o adaptador do frasco na primeira vez que o abrir. As instruções seguintes indicam como colocar o adaptador. Inserção do adaptador de frasco: Quando o frasco for aberto pela primeira vez, é necessário pressionar o adaptador para que entre nele. Lave e seque as mãos. Retire o adaptador do frasco de sua embalagem. Coloque o frasco sobre uma superfície plana e dura. Abra o frasco. |
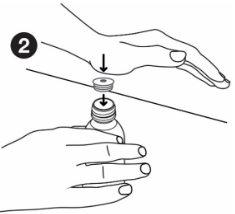
| Segure o frasco com firmeza. Alinee o adaptador com a parte superior do frasco. Insira a pressão o adaptador, com a palma da mão, até que fique alinhado com o nível superior do frasco. Deixe o adaptador colocado após utilizar o medicamento. Enrosque o tampão do frasco sem remover o adaptador. |
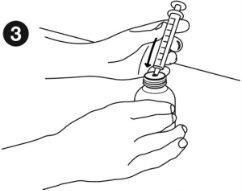
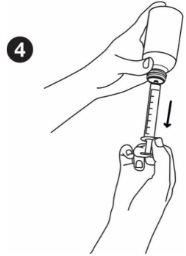
| Tomada do medicamento: Antes de medir a dose, certifique-se de que o êmbolo está introduzido ao máximo na seringa para tomada oral. Mantenha bem segurado o frasco do medicamento sobre uma superfície plana e dura. Insira o extremo da seringa para tomada oral no adaptador do frasco até que não possa empurrar mais. |
| Segure e mantenha unidas a seringa e o frasco e dê-lhes a volta, fazendo que fiquem boca abaixo. Extraia lentamente o êmbolo da seringa para sacar a dose correta. Segure e mantenha unidas a seringa e o frasco e dê-lhes a volta. Segurando o frasco com firmeza, retire suavemente a seringa do adaptador. |
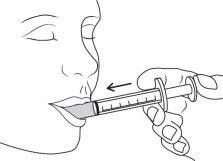
| Coloque o extremo da seringa no interior da boca do paciente. Empurre suavemente o êmbolo até que tenha chegado ao fundo. Permanecerá uma pequena quantidade na ponta da seringa. É normal. Não lance o medicamento para a parte traseira da garganta, pois isso poderia provocar engasgo. |
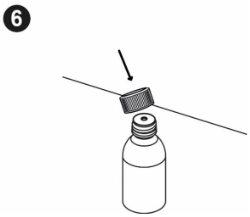
| Voltará a colocar o tampão no frasco e enrosque até que faça tope. Deixe sempre o adaptador colocado no frasco. |
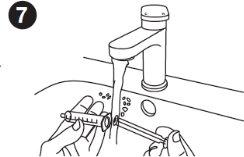
| Limpeza da seringa: Lave a seringa com água limpa e deixe que seque ao ar após cada uso. Lave o interior da seringa e o êmbolo. Lave a seringa utilizando o êmbolo para introduzir e expulsar água limpa. Repita este passo várias vezes. É correto separar o êmbolo da seringa e lavar cada parte. A seringa e o êmbolo podem ser lavados na máquina de lavar louça. A seringa e o êmbolo devem estar completamente secos antes do próximo uso. |
Se o senhor ou seu filho/a tomar mais Fintepla do que deve, a ação correta é:
Consultar o médico ou ir ao hospital diretamente. Leve consigo o frasco do medicamento. Podem produzir-se os efeitos seguintes: agitação, sonolência ou confusão, sofocos ou calor, tremores ou suor.
Se o senhor ou seu filho/a se esqueceu de tomar Fintepla
- Tome-o assim que se lembrar. No entanto, se for quase a hora de tomar a próxima dose, salte a dose que se esqueceu.
- Não tome uma dose dupla para compensar as doses esquecidas.
Se o senhor ou seu filho/a interromper o tratamento com Fintepla
Não deve interromper o tratamento com Fintepla sem falar antes com o seu médico. Se o seu médico decidir interromper o tratamento com este medicamento, pedirá que reduza lentamente a quantidade que toma cada dia. Reduzindo lentamente a dose, reduzir-se-á o risco de sofrer crises convulsivas e status epilepticus.
Entre três e seis meses após a última dose de Fintepla, o paciente deverá realizar um ecocardiograma.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Efeitos adversos possíveis
Tal como todos os medicamentos, este medicamento pode causar efeitos adversos, embora nem todas as pessoas os sofram.
Muito frequentes: podem afetar mais de 1 em cada 10 pessoas
- Diminuição do apetite
- Sonolência
- Diarréia
- Sentir cansaço, sonolência ou fraqueza
Frequentes: podem afetar até 1 em cada 10 pessoas
- Bronquite
- Comportamento anormal
- Mudanças de humor rápidas
- Agressividade
- Agitação
- Insônia
- Tremor de mãos, braços ou pés
- Problemas para coordenar os movimentos, caminhar e manter o equilíbrio
- Diminuição do tônus muscular
- Crisis convulsivas
- Crisis de longa duração (status epiléptico)
- Letargia
- Perda de peso
- Prisão de ventre
- Hipersecreção salivar
- Vômitos
- Erupção cutânea
Baixo nível de açúcar no sangue
- Elevação da prolactina no sangue
Frequência desconhecida(a frequência não pode ser estimada a partir dos dados disponíveis):
- Doença valvular cardíaca
- Irritabilidade
- Síndrome serotoninérgica
- Pressão arterial elevada nas artérias dos pulmões (hipertensão arterial pulmonar)
Informar ao seu médico ou enfermeiro se notar algum dos efeitos adversos da lista acima.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Fintepla
- Manter este medicamento fora da vista e do alcance das crianças.
- Não utilize este medicamento após a data de validade que aparece na caixa e no frasco após CAD. A data de validade é o último dia do mês que se indica.
- Não refrigerar ou congelar.
- Deve ser utilizado antes de transcorridos 3 meses da primeira abertura do frasco.
- Lavar a seringa após cada utilização.
- Se se deteriorar ou se perder uma seringa ou não puder ler as marcas da dose que apresenta, utilize outra seringa para tomada oral das que estão incluídas no pacote ou consulte o seu farmacêutico.
- Os medicamentos não devem ser jogados nos deságues ou na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
Composição de Fintepla
O princípio ativo é a fenfluramina. Cada mililitro contém 2,2 mg de fenfluramina (como cloreto de fenfluramina).
Os demais componentes são:
- P-hidroxibenzoato sódico de etilo (E 215)
- P-hidroxibenzoato sódico de metilo (E 219)
- Sucralosa (E 955)
- Hidroxietilcelulosa (E 1525)
- Fosfato monossódico (E 339)
- Fosfato dissódico (E 339)
- Pó com aroma de cerejas:
- Acácia (E 414)
- Glicose (de milho)
- Etibenzoato
- Preparações aromatizantes naturais
- Substâncias aromatizantes naturais
- Substâncias aromatizantes
- Maltodextrina (milho)
- Dióxido de enxofre (E 220)
- Citrato potássico (E 332)
- Ácido cítrico monohidratado (E 330)
- Água para preparações injetáveis
Aspecto do produto e conteúdo do envase
- Fintepla solução oral é fornecida como líquido claro, incolor, ligeiramente viscoso e com aroma de cerejas.
- A solução é apresentada em um frasco branco com um tampão de proteção para crianças e à prova de manipulações.
- Cada caixa contém:
- Frasco com 60 ml de solução oral, um adaptador de frasco, duas seringas para tomada oral de 3 ml com graduações de 0,1 ml e duas seringas de 6 ml com graduações de 0,2 ml.
- Frasco com 120 ml de solução oral, um adaptador de frasco, duas seringas para tomada oral de 3 ml com graduações de 0,1 ml e duas seringas de 6 ml com graduações de 0,2 ml.
- Frasco com 250 ml de solução oral, um adaptador de frasco, duas seringas para tomada oral de 3 ml com graduações de 0,1 ml e duas seringas de 6 ml com graduações de 0,2 ml.
- Frasco com 360 ml de solução oral, um adaptador de frasco, duas seringas para tomada oral de 3 ml com graduações de 0,1 ml e duas seringas de 6 ml com graduações de 0,2 ml.
- Pode ser que em seu país apenas alguns tamanhos de envases sejam comercializados.
Título da autorização de comercialização e responsável pela fabricação
Título da autorização de comercialização:
UCB Pharma S.A.,
Allée de la Recherche 60,
B-1070 Bruxelas,
Bélgica
Responsável pela fabricação:
Millmount Healthcare Ltd,
Millmount Site, Block 7,
City North Business Campus,
Stamullen,
Co. Meath,
K32 YD60,
Irlanda
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização:
Bélgica UCB Pharma S.A./NV Tel: + 32 / (0)2 559 92 00 | Lituânia UAB Medfiles Tel: +370 5 246 16 40 |
| Luxemburgo UCB Pharma SA/NV Tel: + 32 / (0)2 559 92 00 (Bélgica) |
República Tcheca UCB s.r.o. Tel: + 420 221 773 411 | Hungria UCB Hungria Kft. Tel.: + 36-(1) 391 0060 |
Dinamarca UCB Nordic A/S Tlf: + 45 / 32 46 24 00 | Malta Pharmasud Ltd. Tel: + 356 / 21 37 64 36 |
Alemanha UCB Pharma GmbH Tel: + 49 /(0) 2173 48 4848 | Países Baixos UCB Pharma B.V. Tel.: + 31 / (0)76-573 11 40 |
Estônia OÜ Medfiles Tel: +372 730 5415 | Noruega UCB Nordic A/S Tlf: + 47 / 67 16 5880 |
Grécia UCB Α.Ε. Τηλ: + 30 / 2109974000 | Áustria UCB Pharma GmbH Tel: + 43-(0)1 291 80 00 |
Espanha UCB Pharma, S.A. Tel: + 34 / 91 570 34 44 | Polônia UCB Pharma Sp. z o.o. / VEDIM Sp. z o.o. Tel: + 48 22 696 99 20 |
França UCB Pharma S.A. Tél: + 33 / (0)1 47 29 44 35 | Portugal UCB Pharma (Produtos Farmacêuticos), Lda Tel: + 351 21 302 5300 |
Croácia Medis Adria d.o.o. Tel: +385 (0) 1 230 34 46 | Irlanda UCB (Pharma) Ireland Ltd. Tel: + 353 / (0)1-46 37 395 |
Romênia UCB Pharma Romênia S.R.L. Tel: + 40 21 300 29 04 | Eslovênia Medis, d.o.o. Tel: + 386 1 589 69 00 |
Islândia Vistor hf. Simi: + 354 535 7000 | República Eslovaca UCB s.r.o., organizačná zložka Tel: + 421 (0) 2 5920 2020 |
Itália UCB Pharma S.p.A. Tel: + 39 / 02 300 791 | Finlândia UCB Pharma Oy Finlândia Puh/Tel: + 358 9 2514 4221 |
Chipre Lifepharma (Z.A.M.) Ltd Τηλ: + 357 22 056300 | Suécia UCB Nordic A/S Tel: + 46 / (0) 40 294 900 |
Letônia Medfiles SIA Tel: . +371 67 370 250 |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada sobre este medicamento está disponível no site da Agência Europeia de Medicamentos: https://www.ema.europa.eu. Também existem links para outros sites sobre doenças raras e medicamentos órfãos.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a FINTEPLA 2,2 mg/ml SOLUÇÃO ORALForma farmacêutica: COMPRIMIDO, 100 mgSubstância ativa: topiramateFabricante: Adamed Laboratorios S.L.U.Requer receita médicaForma farmacêutica: COMPRIMIDO, 200 mgSubstância ativa: topiramateFabricante: Adamed Laboratorios S.L.U.Requer receita médicaForma farmacêutica: COMPRIMIDO, 25 mgSubstância ativa: topiramateFabricante: Adamed Laboratorios S.L.U.Requer receita médica
Médicos online para FINTEPLA 2,2 mg/ml SOLUÇÃO ORAL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de FINTEPLA 2,2 mg/ml SOLUÇÃO ORAL – sujeita a avaliação médica e regras locais.