EVRA 203 microgramas/24 horas + 33,9 microgramas/24 horas Adesivo Transdérmico


Como usar EVRA 203 microgramas/24 horas + 33,9 microgramas/24 horas Adesivo Transdérmico
Introdução
Prospecto: informação para o utilizador
EVRA 203 microgramas/24 horas + 33,9 microgramas/24 horas patch transdérmiconorelgestromina/etinilestradiol
Coisas importantes que deve saber sobre os anticoncepcionais hormonais combinados (AHCs):
- São um dos métodos anticoncepcionais reversíveis mais fiáveis se utilizados corretamente.
- Aumentam ligeiramente o risco de sofrer um coágulo de sangue nas veias e nas artérias, especialmente no primeiro ano ou quando se reinicia o uso de um anticoncepcional hormonal combinado após uma pausa de 4 semanas ou mais.
- Esteja alerta e consulte o seu médico se acredita que pode ter sintomas de um coágulo de sangue (ver seção 2 “Coágulos de sangue”).
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito apenas para si e não deve dá-lo a outras pessoas, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é EVRA e para que se utiliza
- O que precisa saber antes de começar a usar EVRA
- Como usar EVRA
- Possíveis efeitos adversos
- Conservação de EVRA
- Conteúdo do envase e informação adicional
1. O que é EVRA e para que se utiliza
EVRA contém dois tipos de hormonas sexuais, um progestágeno chamado norelgestromina e um estrógeno chamado etinilestradiol.
Como contém duas hormonas, EVRA é considerado um “anticoncepcional hormonal combinado”.
É utilizado para prevenir a gravidez.
2. O que precisa saber antes de começar a usar EVRA
Considerações gerais
Antes de começar a usar EVRA, deve ler as informações sobre os coágulos de sangue na seção 2. É particularmente importante que leia os sintomas de um coágulo de sangue (ver seção 2 “Coágulos de sangue”).
Quando não deve usar EVRA
Não deve usar EVRA se tiver alguma das condições listadas abaixo. Se tiver alguma das condições listadas abaixo, deve informar seu médico. Seu médico discutirá com você qual outra forma de anticoncepção seria mais adequada.
- se tiver (ou já teve) um coágulo de sangue em um vaso sanguíneo das pernas (trombose venosa profunda, TVP), nos pulmões (embolia pulmonar, EP) ou em outros órgãos;
- se souber que padece um distúrbio que afeta a coagulação da sangue: por exemplo, deficiência de proteína C, deficiência de proteína S, deficiência de antitrombina III, fator V Leiden ou anticorpos antifosfolipídicos;
- se precisar de uma operação ou se passar muito tempo sem se levantar (ver seção “Coágulos de sangue”);
- se já sofreu um ataque cardíaco ou um acidente vascular cerebral;
- se tiver (ou já teve) uma angina de peito (uma condição que causa dor forte no peito e pode ser o primeiro sinal de um ataque cardíaco) ou um acidente isquêmico transitório (AIT, sintomas temporários de acidente vascular cerebral);
- se tiver alguma das seguintes doenças que podem aumentar seu risco de formação de um coágulo nas artérias:
- diabetes grave com lesão dos vasos sanguíneos
- pressão arterial muito alta
- níveis muito altos de gordura no sangue (colesterol ou triglicerídeos)
- uma condição chamada hiper-homocisteinemia
- se tiver (ou já teve) um tipo de enxaqueca chamada “enxaqueca com aura”;
- se for alérgico a norelgestromina, etinilestradiol ou a qualquer um dos outros componentes deste medicamento (incluídos na seção 6);
- se já lhe disseram que pode ter câncer de mama ou câncer de útero, colo do útero ou de vagina;
- se já teve um tumor no fígado ou uma doença do fígado pela qual seu fígado não funciona corretamente;
- se tiver hemorragia vaginal sem causa aparente.
- se tiver hepatite C e estiver em tratamento com medicamentos que contêm ombitasvir/paritaprevir/ritonavir e dasabuvir (ver também seção “Outros medicamentos e EVRA”).
Não deve usar este medicamento se tiver alguma das condições mencionadas anteriormente. Se não tiver certeza, consulte seu médico, farmacêutico ou enfermeiro antes de usar este medicamento.
Quando deve ter especial cuidado com EVRA
Quando deve consultar seu médico? Procure assistência médica urgente
“Coágulo de sangue [trombose]” a seguir). Para obter uma descrição dos sintomas desses efeitos adversos graves, consulte “Como reconhecer um coágulo de sangue” |
Advertências e precauções
Antes de usar este medicamento, é necessário que seu médico faça uma revisão médica.
Informar seu médico se sofrer qualquer uma das seguintes condições.
Se a condição se desenvolver ou piorar enquanto estiver usando EVRA, também deve informar seu médico.
- se padece doença de Crohn ou colite ulcerativa (doença inflamatória intestinal crônica);
- se padece lúpus eritematoso sistêmico (LES, uma doença que afeta seu sistema natural de defesa);
- se padece síndrome urêmico hemolítico (SUH, um distúrbio da coagulação da sangue que provoca insuficiência nos rins); se padece anemia falciforme (uma doença hereditária dos glóbulos vermelhos);
- se tiver níveis elevados de gordura no sangue (hipertrigliceridemia) ou antecedentes familiares positivos dessa condição. A hipertrigliceridemia está associada a um maior risco de sofrer pancreatite (inflamação do pâncreas);
- se precisar de uma operação ou passar muito tempo sem se levantar (ver seção 2 “Coágulos de sangue”);
- se acaba de dar à luz e corre maior risco de sofrer coágulos de sangue. Deve perguntar a seu médico quanto tempo depois do parto pode começar a tomar EVRA;
- se tiver inflamação das veias que há debaixo da pele (tromboflebite superficial)
- se tiver varizes;
COÁGULOS DE SANGUE
O uso de um anticonceptivo hormonal combinado como EVRA aumenta seu risco de sofrer um coágulo de sangue em comparação com não usá-lo. Em raros casos, um coágulo de sangue pode bloquear vasos sanguíneos e provocar problemas graves.
Podem se formar coágulos de sangue:
- nas veias (o que se chama “trombose venosa”, “tromboembolismo venoso” ou TEV)
- nas artérias (o que se chama “trombose arterial”, “tromboembolismo arterial” ou TEA)
A recuperação dos coágulos de sangue nem sempre é completa. Em raros casos, pode haver efeitos graves duradouros ou, muito raramente, podem ser mortais.
É importante lembrar que o risco global de um coágulo de sangue prejudicial devido a EVRA é pequeno.
CÓMO RECONHECER UM COÁGULO DE SANGUE
Procure assistência médica urgente se notar algum dos seguintes sinais ou sintomas.
Experimenta algum desses sinais? | O que é possível que esteja | |||
sofrendo? | ||||
? | inchaço de uma perna ou pé ou ao longo de uma veia da | Trombose venosa profunda | ||
perna ou pé, especialmente quando vai acompanhada de: | ||||
- | dor ou sensibilidade na perna, que talvez se | |||
note apenas ao se levantar ou ao caminhar; | ||||
- | aumento da temperatura na perna afetada; | |||
- | mudança de cor da pele da perna, p. ex. se | |||
transforma em pálida, vermelha ou azul. | ||||
? | falta de ar súbita sem causa conhecida ou respiração | Embolia pulmonar | ||
? | rápida; | |||
tos súbita sem uma causa clara, que pode arrastar sangue; | ||||
? | dor no peito aguda que pode aumentar ao respirar | |||
? | fundamente; | |||
aturdimento intenso ou tontura; | ||||
? | batimentos do coração acelerados ou irregulares; | |||
? | dor de estômago intenso. | |||
Se não tiver certeza, consulte um médico, pois alguns desses | ||||
sintomas como a tos ou a falta de ar podem ser confundidos com | ||||
uma condição mais leve como uma infecção respiratória (p. ex. um | ||||
“resfriado comum”) | ||||
Sintomas que ocorrem com mais frequência em um olho: | Trombose das veias | |||
? | perda imediata da visão, ou bem, | retinianas (coágulo de sangue | ||
? | visão borrosa indolora, que pode evoluir até | no olho) | ||
perda da visão. |
? | dor, desconforto, pressão, peso no peito; | Ataque cardíaco |
? | sensação de opressão ou plenitude no peito, braço ou debaixo | |
? | do esterno; | |
sensação de plenitude, indigestão ou sufocamento; | ||
? | malestar da parte superior do corpo que irradia para a | |
? | espalda, a mandíbula, a garganta, o braço e o estômago; | |
sudorese, náuseas, vômitos ou tontura; | ||
? | debilidade extrema, ansiedade ou falta de ar; | |
? | batimentos do coração acelerados ou irregulares. | |
? | debilidade ou entorpecimento súbito da face, braço ou | Acidente vascular cerebral |
? | perna, especialmente em um lado do corpo; | |
confusão súbita, dificuldade para falar ou para | ||
? | compreender; | |
dificuldade súbita de visão em um olho ou em ambos; | ||
? | dificuldade súbita para caminhar, tontura, perda do | |
? | equilíbrio ou da coordenação; | |
dor de cabeça súbita, intensa e prolongada sem causa | ||
? | conhecida; | |
perda da consciência ou desmaio, com ou sem | ||
convulsões. | ||
Às vezes os sintomas de acidente vascular cerebral podem ser breves, com uma | ||
recuperação quase imediata e completa, mas de todos os modos deve | ||
procurar assistência médica urgente, pois pode correr risco de | ||
sofrer outro acidente vascular cerebral. | ||
? | inchaço e ligeira coloração azul de uma extremidade; | Coágulos de sangue que |
? | dor de estômago intenso (abdomen agudo). | bloqueiam outros vasos |
sanguíneos | ||
COÁGULOS DE SANGUE EM UMA VEIA |
O que pode ocorrer se se forma um coágulo de sangue em uma veia?
- O uso de anticonceptivos hormonais combinados se relacionou com um aumento do risco de coágulos de sangue nas veias (trombose venosa). No entanto, esses efeitos adversos são raros. Ocorrem com mais frequência no primeiro ano de uso de um anticonceptivo hormonal combinado.
- Se se forma um coágulo de sangue em uma veia da perna ou do pé, pode provocar trombose venosa profunda (TVP).
- Se um coágulo de sangue se desloca desde a perna e se aloja nos pulmões, pode provocar uma embolia pulmonar.
- Em casos muito raros, pode se formar um coágulo em uma veia de outro órgão, como o olho (trombose das veias retinianas).
Quando é maior o risco de apresentar um coágulo de sangue em uma veia?
O risco de apresentar um coágulo de sangue em uma veia é maior durante o primeiro ano de tomar um anticonceptivo hormonal combinado pela primeira vez. O risco pode ser maior também se voltar a começar a tomar um anticonceptivo hormonal combinado (o mesmo medicamento ou um medicamento diferente) após uma interrupção de 4 semanas ou mais.
Depois do primeiro ano, o risco diminui, mas sempre é um pouco maior do que se não estivesse tomando um anticonceptivo hormonal combinado.
Quando deixa de tomar EVRA, seu risco de apresentar um coágulo de sangue retorna à normalidade em poucas semanas.
Qual é o risco de apresentar um coágulo de sangue?
O risco depende de seu risco natural de TEV e do tipo de anticonceptivo hormonal combinado que está tomando.
O risco global de apresentar um coágulo de sangue na perna ou nos pulmões (TVP ou EP) com EVRA é pequeno.
- De cada 10.000 mulheres que não usam nenhum anticonceptivo hormonal combinado e não estão grávidas, cerca de 2 podem apresentar um coágulo de sangue em um ano.
- De cada 10.000 mulheres que usam um anticonceptivo hormonal combinado que contém levonorgestrel, noretisterona ou norgestimato, cerca de 5-7 apresentarão um coágulo de sangue em um ano.
- De cada 10.000 mulheres que usam um anticonceptivo hormonal combinado que contém etonogestrel ou norelgestromina, como EVRA, entre 6 e 12 mulheres apresentarão um coágulo de sangue em um ano.
- O risco de ter um coágulo de sangue variará de acordo com seus antecedentes médicos pessoais (ver “Fatores que aumentam seu risco de um coágulo de sangue” a seguir).
Risco de apresentar um coágulo de | |
sangue em um ano | |
Mulheres que não utilizamum patch/comprimido/anel | Cerca de 2 de cada 10.000 mulheres |
vaginal hormonal combinado e que não estão grávidas | |
Mulheres que utilizam uma pílula anticonceptiva hormonal | Cerca de 5-7 de cada 10.000 mulheres |
combinada que contém levonorgestrel, noretisterona ou | |
norgestimato | |
Mulheres que utilizam EVRA | Cerca de 6-12 de cada 10.000 mulheres |
Fatores que aumentam seu risco de um coágulo de sangue em uma veia
O risco de ter um coágulo de sangue com EVRA é pequeno, mas algumas condições aumentam o risco. Seu risco é maior:
- se tiver excesso de peso (índice de massa corporal ou IMC superior a 30 kg/m2);
- se algum de seus parentes próximos teve um coágulo de sangue na perna, pulmão ou outro órgão em uma idade precoce (ou seja, antes dos 50 anos aproximadamente). Nesse caso, você também poderia ter um distúrbio hereditário da coagulação da sangue;
- se precisar de uma operação ou se passar muito tempo sem se levantar devido a uma lesão ou doença, ou se tiver a perna engessada. Talvez seja necessário interromper o uso de EVRA várias semanas antes da intervenção cirúrgica ou enquanto tiver menos mobilidade. Se precisar interromper o uso de EVRA, deve perguntar a seu médico quando pode começar a usá-lo novamente;
- ao aumentar a idade (em especial acima de 35 anos);
- se deu à luz há menos de algumas semanas.
O risco de apresentar um coágulo de sangue aumenta quanto mais condições tiver.
As viagens de avião (>4 horas) podem aumentar temporariamente o risco de um coágulo de sangue, especialmente se tiver algum dos outros fatores de risco listados.
É importante informar seu médico se sofrer qualquer uma das condições anteriores, mesmo que não tenha certeza. Seu médico pode decidir que é necessário interromper o uso de EVRA.
Se alguma das condições anteriores mudar enquanto estiver usando EVRA, por exemplo, um parente próximo experimenta uma trombose sem causa conhecida, ou você aumenta muito de peso, informe seu médico.
COÁGULOS DE SANGUE EM UMA ARTÉRIA
O que pode ocorrer se se forma um coágulo de sangue em uma artéria?
Assim como um coágulo de sangue em uma veia, um coágulo em uma artéria pode provocar problemas graves. Por exemplo, pode provocar um ataque cardíaco ou um acidente vascular cerebral.
Fatores que aumentam seu risco de um coágulo de sangue em uma artéria
É importante notar que o risco de um ataque cardíaco ou um acidente vascular cerebral devido ao uso de EVRA é muito pequeno, mas pode aumentar:
- com a idade (acima de 35 anos);
- se fumar. Quando usa um anticonceptivo hormonal combinado como EVRA, é aconselhável que pare de fumar. Se não for capaz de parar de fumar e tiver mais de 35 anos, seu médico pode aconselhar que use um tipo de anticonceptivo diferente;
- se tiver sobrepeso;
- se tiver pressão arterial alta;
- se algum parente próximo sofreu um ataque cardíaco ou um acidente vascular cerebral em uma idade precoce (menos de 50 anos). Nesse caso, você também poderia ter um maior risco de sofrer um ataque cardíaco ou uma apoplexia;
- se você ou algum parente próximo tiver um nível elevado de gordura no sangue (colesterol ou triglicerídeos);
- se padece enxaquecas, especialmente enxaquecas com aura;
- se tiver um problema cardíaco (distúrbio das válvulas, uma alteração do ritmo do coração chamada fibrilação auricular);
- se tiver diabetes.
Se tiver uma ou mais dessas condições ou se alguma delas for especialmente grave, o risco de apresentar um coágulo de sangue pode ser aumentado ainda mais.
Se alguma das condições anteriores mudar enquanto estiver usando EVRA, por exemplo, começa a fumar, um parente próximo experimenta uma trombose sem causa conhecida, ou você aumenta muito de peso, informe seu médico.
Distúrbios psiquiátricos:
Algumas mulheres que usam anticonceptivos hormonais como EVRA relataram depressão ou um estado de ânimo deprimido. A depressão pode ser grave e, às vezes, pode induzir pensamentos suicidas. Se experimentar alterações do estado de ânimo e sintomas depressivos, procure seu médico para obter aconselhamento médico adicional o mais rápido possível.
Além disso, consulte seu médico, farmacêutico ou enfermeiro antes de começar a usar EVRA se tiver ou já teve alguma das seguintes condições, ou se elas aparecerem ou piorarem durante o tratamento com EVRA:
- Acredita que pode estar grávida;
- Têm dores de cabeça que pioram ou aparecem com mais frequência;
- Pesa 90 kg ou mais; (equivalente a 14 st e 2 lb ou mais)
- Têm pressão arterial alta ou que tende a aumentar;
- Têm alguma doença da vesícula biliar, incluindo cálculos biliares ou inflamação da vesícula biliar;
- Têm uma alteração no sangue chamada porfiria;
- Têm um distúrbio nervoso em que se produzem movimentos repentinos do corpo chamado “coreia de Sydenham”;
- Teve erupções na pele com bolhas durante a gravidez (“herpes gestacional”);
- Têm perda de audição;
- Têm diabetes;
- Têm depressão;
- Têm epilepsia ou qualquer outro problema que cause convulsões;
- Têm alterações do fígado, incluindo cor amarela da pele e do branco do olho (icterícia);
- Têm ou já teve “manchas da gravidez”. Essas são pontos ou manchas marrons amareladas da pele, especialmente
- Manchas marrones na cara (chamadas “cloasma”). Pode ser que estas manchas não
desapareçam completamente, mesmo após deixar de utilizar EVRA. Proteja a sua pele do sol ou das radiações ultravioletas. Isso pode ajudar a prevenir que apareçam estas manchas ou a que não piorem.
- Tém problemas de rim.
Se não tiver certeza se padece alguma das afecções acima, consulte o seu médico ou farmacêutico antes de usar EVRA.
Doenças de transmissão sexual
Este medicamento não a protege contra a infecção por VIH (SIDA) ou contra qualquer outra doença de transmissão sexual. Isso inclui clamídia, herpes genital, verrugas genitais, gonorreia, hepatite B, sífilis. Utilize sempre preservativos para se proteger contra estas doenças.
Testes analíticos
- Se precisar que lhe façam um exame de sangue ou de urina, informe o seu médico ou o pessoal do laboratório de que está utilizando EVRA, pois os anticoncepcionais hormonais podem alterar alguns resultados analíticos.
Crianças e adolescentes
Não foi estudado EVRA em meninas e adolescentes menores de 18 anos. Não se deve utilizar EVRA em meninas e adolescentes que não tenham tido ainda a sua primeira menstruação.
Outros medicamentos e EVRA
Informa ao seu médico ou farmacêutico se está utilizando, utilizou recentemente ou poderia ter que utilizar qualquer outro medicamento.
Não utilize EVRA se tiver hepatite C e está tomando medicamentos que contenham ombitasvir/paritaprevir/ritonavir e dasabuvir, pois pode causar nos exames de sangue um aumento nos resultados da função hepática (aumento da enzima ALT hepática). O seu médico lhe receitará outro tipo de método anticonceptivo antes de iniciar o tratamento com estes medicamentos. EVRA pode ser reiniciado, aproximadamente, 2 semanas após o finalizar este tratamento. Ver seção “Quando não deve usar EVRA”.
Certos medicamentos e plantas medicinais podem impedir o funcionamento adequado de EVRA.
Se isso acontecer, você pode ficar grávida, ou pode experimentar sangramento inesperado.
Estes incluem medicamentos utilizados para o tratamento de:
- alguns antirretrovirais utilizados para tratar infecções por VIH/SIDA e vírus da hepatite C (denominados inibidores da protease e inibidores não nucleosídicos da transcriptase reversa como ritonavir, nevirapina, efavirenz)
- medicamentos para as infecções (como rifampicina e griseofulvina)
- medicamentos anticonvulsivantes (como barbitúricos, topiramato, fenitoína, carbamazepina, primidona, oxcarbazepina e felbamato)
- bosentán (um medicamento utilizado para tratar a tensão arterial alta nos vasos sanguíneos dos pulmões)
- erva-de-São-João ou hipérico, (uma planta medicinal utilizada para a depressão).
Se está utilizando alguns dos medicamentos mencionados acima, deve usar outro método anticonceptivo (como preservativo, diafragma ou espuma). O efeito de algum destes medicamentos pode durar até 28 dias após ter interrompido o seu uso. Consulte o seu médico ou farmacêutico sobre a utilização de outro método anticonceptivo se está utilizando EVRA juntamente com qualquer dos medicamentos acima mencionados.
EVRA pode reduzir o efeito de alguns medicamentos, como:
- medicamentos que contenham ciclosporina
- lamotrigina utilizado para a epilepsia [Isso pode aumentar o risco das crises (convulsões)].
Pode ser que o seu médico necessite ajustar a dosagem do outro medicamento. Consulte o seu médico ou farmacêutico antes de tomar qualquer medicamento.
Gravidez e amamentação
- Não utilize este medicamento se estiver grávida ou se acredita que possa estar.
- Deixe de utilizar este medicamento imediatamente se ficar grávida.
- Não utilize este medicamento se estiver a amamentar ou planeia amamentar.
Se acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Condução e uso de máquinas
Pode conduzir ou utilizar máquinas enquanto usa este medicamento.
Riscos do uso de anticoncepcionais hormonais combinados
A seguinte informação baseia-se em informações sobre os comprimidos anticoncepcionais combinados. Uma vez que o patch transdérmico EVRA contém hormonas semelhantes às utilizadas nos comprimidos anticoncepcionais combinados, é provável que tenha os mesmos riscos. O uso de qualquer comprimido anticoncepcional combinado implica riscos, os quais poderiam dar lugar a deficiência ou morte.
Não foi demonstrado que um patch transdérmico como EVRA seja mais seguro do que um comprimido anticoncepcional combinado administrado por via oral.
Anticoncepcionais hormonais combinados e o cancro
Cancro do colo do útero
O cancro do colo do útero também é detectado com mais frequência em mulheres que usam anticoncepcionais hormonais combinados. No entanto, pode ser devido a outras causas, incluindo as doenças de transmissão sexual.
Cancro da mama
Foram detectados casos de cancro da mama com mais frequência em mulheres que utilizam anticoncepcionais hormonais combinados. No entanto, é possível que os anticoncepcionais hormonais combinados não sejam a causa de que mais mulheres tenham cancro da mama. Isso pode ser devido ao facto de as mulheres que utilizam anticoncepcionais hormonais combinados serem examinadas mais frequentemente. Isso significaria que há mais possibilidades de que o cancro da mama seja detectado. O aumento do risco de ter cancro da mama diminui gradualmente após interromper o tratamento com os anticoncepcionais hormonais combinados. Após dez anos, o risco iguala-se ao das mulheres que nunca utilizaram anticoncepcionais hormonais combinados.
Cancro do fígado
Foram encontrados casos raros de tumores não cancerígenos no fígado em mulheres que tomam anticoncepcionais hormonais combinados. Ainda mais raramente, foram encontrados tumores cancerígenos no fígado. Isso pode produzir sangramentos dentro do corpo com um dolor muito forte na zona do estômago. Se sofrer este sintoma, deve contactar imediatamente o seu médico.
3. Como usar EVRA
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico.
Caso contrário, poderá aumentar o risco de engravidar.
- Consulte o seu médico ou farmacêutico se tiver dúvidas.
- Deve dispor de métodos anticonceptivos não hormonais (como preservativo, diafragma ou espuma) de reserva, caso cometa algum erro ao usar o patch.
Quantos patches devem ser usados
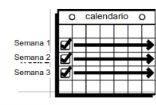
- Semanas 1, 2 e 3: Coloque um patch e deixe-o durante 7 dias exatamente.
- Semana 4: Não coloque um patch nesta semana.
Se não usou um método anticonceptivo hormonal durante o ciclo anterior
- Pode começar a usar este medicamento no primeiro dia do seu próximo período.
- Se passaram um ou mais dias desde o início do seu período, consulte o seu médico sobre a utilização temporária de um método anticonceptivo não hormonal.
Se mudar do comprimido anticonceptivo oral para EVRA
Se passar do comprimido anticonceptivo oral para este medicamento:
- Espere até que tenha a menstruação.
- Coloque o primeiro patch durante as primeiras 24 horas do período.
Se colocar o patch após o Dia 1 do período, deve:
- Usar simultaneamente um método anticonceptivo não hormonal até o Dia 8, momento de troca do patch.
Se não tiver a menstruação nos 5 dias posteriores à tomada do último comprimido anticonceptivo, consulte o seu médico antes de começar a usar este medicamento.
Se mudar do comprimido anticonceptivo baseado apenas em progestágeno, de um implante ou de um injetável para EVRA
- Pode começar o tratamento com este medicamento qualquer dia após deixar de tomar o comprimido anticonceptivo baseado apenas em progestágeno, ou no dia de extração do implante ou no dia que lhe tocar a próxima injeção.
- Coloque o patch no dia seguinte ao de deixar de tomar o comprimido anticonceptivo baseado apenas em progestágeno, no dia de extração do implante ou quando lhe tocar a próxima injeção.
- Deve usar simultaneamente um método anticonceptivo não hormonal até o Dia 8, momento de troca do patch.
Depois de um aborto espontâneo ou provocadoantesde 20 semanas de gestação
- Consulte o seu médico.
- Pode começar a usar este medicamento de forma imediata.
Se, quando começar a usar este medicamento, já passaram um ou mais dias desde o aborto espontâneo ou provocado, consulte o seu médico sobre a utilização temporária de um método anticonceptivo não hormonal.
Depois de um aborto espontâneo ou provocadodepoisde 20 semanas de gestação
- Consulte o seu médico.
Pode começar com este medicamento aos 21 dias após o aborto provocado ou espontâneo ou no primeiro dia do próximo período, o que ocorrer primeiro.
Depois do parto
- Consulte o seu médico.
- Se deu à luz e não está amamentando, não deve começar a usar este medicamento antes de 4 semanas após o parto.
- Se começar a usá-lo mais tarde de 4 semanas após o parto, use simultaneamente um método anticonceptivo não hormonal durante os primeiros 7 dias.
Se manteve relações sexuais desde o parto, espere até ter a sua primeira menstruação ou consulte o seu médico para se certificar de que não está grávida antes de começar a usar este medicamento.
Se está amamentando
- Consulte o seu médico.
- Não use este medicamento se estiver amamentando ou planejando amamentar (ver também seção 2, Gravidez e lactação).
Informação importante que deve seguir enquanto usa o patch
- Troque o patch EVRA no mesmo dia de cada semana, pois ele é projetado para funcionar durante 7 dias.
- Nunca deixe de usar o patch por mais de 7 dias seguidos.
- Os patches devem ser usados apenas um de cada vez.
- Não corte nem manipule o patch de nenhuma forma.
- Evite colocar o patch sobre uma área da pele que esteja vermelha, irritada ou cortada.
- O patch deve ser colado bem sobre a pele para funcionar corretamente.
- É necessário pressionar bem sobre o patch até que as bordas fiquem bem coladas.
- Não se devem aplicar cremes, óleos, loções, pós ou maquiagem na área da pele onde vai colocar o patch ou perto da área onde usa o patch. Isso poderia fazer com que o patch se descolasse.
- Não coloque um patch novo na mesma área da que acabou de remover o patch anterior. Se fizer isso, é mais provável que cause irritação.
- Verifique todos os dias se o patch não se descolou.
- Não deixe de usar os patches mesmo se não mantém relações sexuais com frequência.
Como usar o patch:
Se for a primeira vez que usa EVRA, espere até o dia em que tiver o período menstrual.
- Coloque o primeiro patch durante as primeiras 24 horas do período
- Se colocar o patch após o primeiro dia do período, deve usar um método anticonceptivo não hormonal até o Dia 8, quando trocar de patch
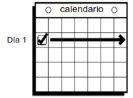
- O dia em que colocar o primeiro patch será o Dia 1. O “Dia de Troca do Patch” será este dia de cada semana.
Escolha um local no corpo para colocar o patch.
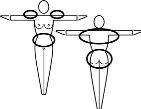
- Coloque sempre o patch sobre pele limpa, seca e sem pelos
- Coloque-o no glúteo, abdômen, exterior do braço ou parte superior das costas, em um local onde não roce com as roupas justas
- Nunca coloque o patch nas mamas.
| Usando os dedos, abra o envelope de alumínio.
Evite o contato com a superfície adesiva. |
| Coloque o patch na pele.
|
| Use o patch durante 7 dias (uma semana).
|
|
Coloque um novo patch. Isso faz um total de três semanas usando patches. A fim de evitar irritações, não coloque o patch novo exatamente no mesmo local que o anterior. |
| Não coloque nenhum patch na Semana 4 (Dia 22 a Dia 28).
|
| No seu próximo ciclo de quatro semanas.
|
Se quiser modificar o “Dia de Troca do Patch” para um dia diferente da semana, consulte o seu médico. Deve completar o ciclo atual e retirar o terceiro patch no dia correto. Durante a semana 4, pode escolher um Dia de Troca novo e colocar o primeiro patch nesse dia escolhido. Em nenhum caso devem transcorrer mais de 7 dias consecutivos sem patch.
Se quiser retardar a sua regra, coloque um patch no início da semana 4 (Dia 22) sem respeitar, portanto, a semana de descanso. Pode experimentar um sangramento leve ou intermenstrual. Não use mais de 6 patches consecutivos (portanto, não mais de 6 semanas). Quando tiver usado 6 patches consecutivos (durante 6 semanas consecutivas), não coloque outro patch na semana 7. Após 7 dias sem usar o patch, coloque um novo patch e comece o ciclo usando-o como Dia 1. Consulte o seu médico antes de decidir retardar a sua regra.
Atividades diárias enquanto usa os patches
- As atividades normais, como banhos, duchas, sauna e exercício, não devem afetar o desempenho do patch.
- O patch é projetado para permanecer no lugar durante este tipo de atividades.
- No entanto, é recomendado que verifique se o patch não se desprendeu após realizar essas atividades.
Se precisar colocar o patch em uma área nova do corpo em um dia diferente do seu “Dia de Troca do Patch”
Se o patch que usa for incômodo ou causar irritação:
- Pode removê-lo e colocar outro novo em uma área diferente do corpo até o próximo “Dia de Troca do Patch”
- Deve usar apenas um patch de cada vez.
Se tiver dificuldade em lembrar a troca do patch
- Consulte o seu médico, farmacêutico ou enfermeiro sobre como tornar a troca do patch mais fácil. Eles também podem aconselhá-lo sobre o uso de outro método anticonceptivo.
Se o patch começar a se descolar, as bordas se levantarem ou ele cair
Menos de um dia(até 24 horas):
- Tente colocar o patch novamente ou coloque um novo patch imediatamente.
- Não é necessário tomar outras medidas anticonceptivas.
- O “Dia de Troca do Patch” deve continuar sendo o mesmo.
- Não tente colocar o patch novamente se:
- o adesivo não adere
- colou em si mesmo ou em outra superfície
- tem alguma partícula colada
- se descolou ou caiu pela segunda vez.
- Não deve usar nenhum tipo de adesivo ou venda para prender o patch no lugar.
- Se não puder colocar o patch novamente, deve colocar outro patch novo imediatamente.
Mais de um dia(24 horas ou mais) ou se não souber por quanto tempo:
- Comece um novo ciclo de quatro semanas colocando um patch novo.
- A partir de agora, haverá um novo Dia 1 e um novo “Dia de Troca do Patch”.
- Deve usar anticonceptivos não hormonais adicionais durante a primeira semana do novo ciclo.
Pode engravidar se não seguir essas instruções.
Se esquecer de trocar o patch transdérmico
No início de qualquer ciclo de patch (Semana 1 - Dia 1):
Se esquecer de colocar o patch, pode correr um risco muito alto de engravidar.
- Deve usar anticonceptivos não hormonais adicionais durante uma semana.
- Coloque o primeiro patch do novo ciclo assim que se lembrar.
- Agora tem um novo “Dia de Troca do Patch” e um novo Dia 1.
Na metade do ciclo (Semana 2 ou 3):
Se esquecer de trocar o patch durante um ou dois dias (até 48 horas):
- Coloque um novo patch assim que se lembrar.
- O próximo patch será colocado no “Dia de Troca do Patch” habitual.
Não é necessário tomar outras medidas anticonceptivas.
Durante mais de 2 dias(48 horas ou mais):
- Se esquecer de trocar o patch durante mais de 2 dias, pode engravidar.
- Comece um novo ciclo de quatro semanas assim que se lembrar, colocando um novo patch.
- A partir de agora, haverá um novo “Dia de Troca do Patch” e um novo Dia 1.
- Deve usar anticonceptivos adicionais durante a primeira semana do novo ciclo.
No final do ciclo com patch (Semana 4):
Se esquecer de retirar o patch:
- Retire-o assim que se lembrar.
- Comece o novo ciclo no “Dia de Troca do Patch” habitual, o dia após o Dia 28.
Não é necessário o uso de anticonceptivos adicionais.
Se tiver ausência ou irregularidades no sangramento com EVRA
Este medicamento pode causar sangramento vaginal inesperado ou perdas (manchado) durante as semanas de uso do patch.
- Normalmente, isso deixa de ocorrer após os primeiros ciclos.
- Os erros no uso dos patches também podem causar manchado e hemorragia leve.
- Continue usando este medicamento e, se o sangramento persistir em ciclos posteriores aos três primeiros, consulte o seu médico ou farmacêutico.
Embora não tenha o período durante a semana sem o patch de EVRA (Semana 4), deve colocar um novo patch no “Dia de Troca do Patch” habitual.
- Se usou este medicamento corretamente e não teve o período, não significa necessariamente que esteja grávida.
- No entanto, se tiver duas faltas consecutivas, consulte o seu médico ou farmacêutico, pois poderia estar grávida.
Se usar mais EVRA do que o necessário (mais de um patch de EVRA ao mesmo tempo)
Retire os patches e consulte o seu médico imediatamente.
O uso de patches em excesso pode causar:
- Enjoo (náuseas) e vômitos
- Sangramento vaginal.
Se interromper o tratamento com EVRA
Pode ter uma menstruação irregular, leve ou ausência. Isso normalmente ocorre nos 3 primeiros meses, especialmente se os períodos não eram regulares antes de começar a usar este medicamento.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Efeitos adversos possíveis
Assim como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram. Se sofrer qualquer efeito adverso, especialmente se for grave e persistente, ou tiver algum cambio de saúde que acredite que possa dever-se a EVRA, consulte o seu médico.
Todas as mulheres que tomam anticoncepcionais hormonais combinados correm maior risco de apresentar coágulos de sangue nas veias [tromboembolismo venoso (TEV)] ou coágulos de sangue nas artérias (tromboembolismo arterial [TEA]). Para obter informações mais detalhadas sobre os diferentes riscos de tomar anticoncepcionais hormonais combinados, ver seção 2 “O que precisa saber antes de começar a usar EVRA”.
Efeitos adversos muito frequentes (podem afetar mais de 1 de cada 10 mulheres):
- Dor de cabeça
- Náuseas
- Sensibilidade nas mamas.
Efeitos adversos frequentes (podem afetar até 1 de cada 10 mulheres):
- Infecção vaginal por fungos, algumas vezes chamada candidíase
- Alterações do estado de ânimo, tais como depressão, mudanças de humor ou oscilações no estado de ânimo, ansiedade, choros
- Tonturas
- Enxaqueca
- Dor ou inchaço abdominal
- Vômitos ou diarreia
- Acne, erupção da pele, coceira da pele ou irritação da pele
- Espasmos musculares
- Problemas no peito, tais como dor, aumento do tamanho ou bultos no peito
- Mudanças no padrão do sangramento menstrual, cãibras uterinas, períodos dolorosos, secreção vaginal
- Problemas nas áreas da pele onde o patch foi aplicado, tais como vermelhidão, irritação, coceira ou erupção
- Sensação de cansaço ou de mal-estar
- Aumento de peso.
Efeitos adversos pouco frequentes (podem afetar até 1 de cada 100 mulheres):
- Reação alérgica, urticárias
- Inchaço devido à retenção de água no corpo
- Níveis altos de gorduras no sangue (como colesterol ou triglicerídeos)
- Problemas de sono (insônia)
- Diminuição do desejo sexual
- Eczema, vermelhidão da pele
- Produção anormal de leite na mama
- Síndrome pré-menstrual
- Secreção vaginal seca
- Outros problemas nas áreas da pele onde o patch foi aplicado
- Inchaço
- Pressão sanguínea alta ou aumento da pressão sanguínea.
- Aumento de apetite
- Perda de cabelo
- Sensibilidade à luz do sol.
Efeitos adversos raros (podem afetar até 1 de cada 1.000 mulheres):
Coágulos de sangue prejudiciais em uma veia ou artéria, por exemplo:
- em uma perna ou pé (ou seja, TVP)
- em um pulmão (ou seja, EP)
- ataque cardíaco
- acidente vascular cerebral
- mini-acidente vascular cerebral ou sintomas temporários semelhantes aos de um acidente vascular cerebral, o que se chama acidente isquêmico transitório (AIT)
- coágulos de sangue no fígado, estômago/intestino, rins ou olho.
As possibilidades de ter um coágulo de sangue podem ser maiores se tiver qualquer outra condição que aumente este risco (ver seção 2 para obter mais informações sobre as condições que aumentam o risco de sofrer coágulos de sangue e os sintomas de um coágulo de sangue).
- Câncer de mama, de colo do útero ou fígado
- Problemas nas áreas da pele onde o patch foi aplicado, como erupção com bolhas ou úlceras
- Tumores não cancerosos (benignos) nas mamas ou no fígado
- Mioma uterino
- Fúria ou sentir-se frustrada
- Aumento do desejo sexual
- Alteração do gosto
- Problemas com o uso de lentes de contato
- Aumento brusco repentino da pressão arterial (crise hipertensiva)
- Inflamação da vesícula biliar ou do cólon
- Células anormais no colo do útero
- Pontos ou manchas marrons no rosto
- Cálculos biliares ou bloqueio dos ductos biliares
- A pele e a parte branca dos olhos amarelam
- Níveis de açúcar ou insulina no sangue anormais
- Inchaço da face, boca, garganta ou língua
- Erupção cutânea com nódulos vermelhos dolorosos nas pernas e nos braços
- Coceira na pele
- Pele áspera, descamada, com coceira e vermelhidão
- Supressão da lactação
- Secreção vaginal
- Retenção de líquidos nas pernas
- Retenção de líquidos
- Inchaço nos braços, nas mãos, nas pernas ou nos pés.
Se tiver desconforto estomacal
- A quantidade de hormônios que obtém de EVRA não é afetada por estar doente (vômitos) ou diarreia.
- Não precisa utilizar medidas anticoncepcionais adicionais se tiver desconforto estomacal.
Pode ter manchado ou hemorragia leve ou sensibilidade nas mamas ou pode sentir mal-estar durante os primeiros 3 ciclos. Normalmente, esses sintomas desaparecem, mas se não for assim, consulte o seu médico ou farmacêutico.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de EVRA
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta após “CAD”. A data de validade é o último dia do mês que se indica.
Conservar no embalagem original para protegê-lo da luz e da umidade.
Não refrigerar ou congelar.
Os patches usados ainda contêm algumas hormonas ativas. Para proteger o meio ambiente, devem ser eliminados com cuidado. Para descartar o patch usado, deve:
- Despegar a etiqueta destinada a descartar o patch da parte exterior do envelope.
- Coloque o patch usado na etiqueta, de maneira que a parte adesiva cubra a zona sombreada.
- Feche a etiqueta, deixando dentro o patch, e jogue-a fora, mantendo-a fora do alcance das crianças.
Os medicamentos não devem ser jogados nos deságues ou na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
Composição de EVRA
Os princípios ativos são norelgestromina e etinilestradiol. Cada patch transdérmico de 20 cm2 contém 6 mg de norelgestromina e 600 microgramas de etinilestradiol.
Os princípios ativos são liberados durante 7 dias, liberando-se cada 24 horas uma média de 203 microgramas de norelgestromina e 34 microgramas de etinilestradiol.
Os demais componentes são: camada exterior: camada externa de polietileno pigmentado de baixa densidade,
camada interna de poliéster; camada intermediária: adesivo de poliisobutileno/polibuteno, crospovidona, material de poliéster sem tecer, lauril lactato; terceira camada: película de tereftalato de polietileno (PET), revestimento de polidimetilsiloxano.
Aspecto do produto e conteúdo do envase
EVRA é um patch transdérmico plástico, fino, de cor bege que leva gravado “EVRA”. A camada adesiva se pega sobre a pele após remover a camada protetora de plástico transparente.
EVRA é apresentado nos seguintes tamanhos de embalagem: Caixas de 3, 9 ou 18 patches em envelopes individuais forrados, envoltos de três em três, com uma lâmina transparente de plástico perfurada.
Pode ser que apenas alguns tamanhos de embalagens sejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização: Janssen-Cilag International NV Turnhoutseweg, 30, B-2340 Beerse, Bélgica.
Responsável pela fabricação: Janssen-Pharmaceutica NV, Turnhoutseweg 30, B-2340 Beerse, Bélgica.
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Bélgica Janssen-Cilag NV Antwerpseweg 15-17 B-2340 Beerse Tel/Tél: + 32 14 64 94 11 | Lituânia UAB "JOHNSON & JOHNSON" Konstitucijos pr. 21C LT-08130 Vilnius Tel: +370 5 278 68 88 |
Bulgária „??????? & ??????? ????????” ???? ?.?. ??????? 4 ?????? ???? ?????, ?????? 4 ????? 1766 ???.: +359 2 489 94 00 | Luxemburgo Janssen-Cilag NV Antwerpseweg 15-17 B-2340 Beerse Bélgica Tél/Tel: + 32 14 64 94 11 |
República TchecaJanssen-Cilag s.r.o. Walterovo námestí 329/1 CZ-158 00 Praha 5 – Jinonice Tel: +420 227 012 227 | Hungria Janssen-Cilag Kft. Nagyenyed u. 8-14 H-Budapeste, 1123 Tel: +36 1 884 2858 |
Dinamarca Janssen-Cilag A/S Bregnerødvej 133 DK-3460 Birkerød Tlf: +45 45 94 82 82 | Malta AM.MANGION LTD Mangion Building, Triq Gdida fi Triq Valletta MT-Hal-Luqa LQA 6000 Tel:+356 2397 6000 |
Alemanha Janssen-Cilag GmbH Johnson & Johnson Platz 1 D-41470 Neuss Tel: +49 2137 955 955 | Países Baixos Janssen-Cilag B.V. Graaf Engelbertlaan 75 NL-4837 DS Breda Tel: +31 76 711 1111 |
Estônia UAB "JOHNSON & JOHNSON" filial Estônia Lõõtsa 2 EE-11415 Tallinn Tel: +372 617 7410 | Noruega Janssen-Cilag AS Postboks 144 NO-1325-Lysaker Tlf: + 47 24 12 65 00 |
Grécia Janssen-Cilag Φαρμακευτικ? Α.Ε.Β.Ε. Λεωφ?ρος Ειρ?νης 56 GR-151 21 Πε?κη, Αθ?να Tηλ: +30 210 80 90 000 | Áustria Janssen-Cilag Pharma GmbH. Vorgartenstraße 206B A-1020 Viena Tel:+43 1 610 300 |
Espanha Janssen-Cilag, S.A. Paseo de las Doce Estrellas, 5-7 E-28042 Madrid Tel: +34 91 722 81 00 | Polônia Janssen-Cilag Polska Sp. z o.o. ul. Ilzecka 24 PL-02-135 Varsóvia Tel.: + 48 22 237 60 00 |
França Janssen-Cilag 1, rue Camille Desmoulins, TSA 91003 F-92787 Issy Les Moulineaux, Cedex 9 Tél: 0800 25 50 75 / + 33 1 55 00 40 03 | Portugal Janssen-Cilag Farmacêutica, Lda. Lagoas Park, Edifício 9 PT-2740-262 Porto Salvo Tel: +351 214 368 600 |
Croácia Johnson & Johnson S.E. d.o.o. Oreškoviceva 6h 10010 Zagreb Tel: +385 1 6610 700 | Romênia Johnson & Johnson România SRL Str. Tipografilor nr.11 – 15 Cladirea S-Park, Corp B3-B4, Etaj 3 013714 Bucareste, ROMÂNIA Tel: +40 21 207 18 00 |
Irlanda Janssen Sciences Ireland UC Barnahely Ringaskiddy IRL – Co. Cork P43 FA46 Tel: +353 1 800 709 122 | Eslovênia Johnson & Johnson d.o.o. Šmartinska cesta 53 SI-1000, Liubliana Tel. + 386 1 401 18 00 |
Islândia Janssen-Cilag AB c/o Vistor hf. Hörgatúni 2 IS-210 Garðabær Simi: (+354) 535 7000 | Eslováquia Janssen, Johnson & Johnson, s.r.o. CBC III, Karadžicova 12 SK-821 08 Bratislava Tel. +421 232 408 400 |
Itália Janssen-Cilag SpA Via M.Buonarroti, 23 I-20093 Cologno Monzese MI Tel: +39 02 2510 1 | Finlândia Janssen-Cilag Oy Vaisalantie/Vaisalavägen 2 FI-02130 Espoo/Esbo Puh/Tel: +358 207 531 300 |
Chipre Βαρν?βας Χατζηπαναγ?ς Λτδ Λεωφ?ρος Γι?ννου Κρανιδι?τη 226 Λατσι? CY-2234 Λευκωσ?α Τηλ: +357 22 207 700 | Suécia Janssen-Cilag AB Box 4042 SE-16904 Solna Tel: +46 8 626 50 00 |
Letônia UAB "JOHNSON & JOHNSON" filial Letônia Mukusalas iela 101 Riga, LV-1004 Tel: +371 678 93561 | Reino Unido Janssen-Cilag Ltd. 50-100 Holmers Farm Way High Wycombe Buckinghamshire HP12 4EG - UK Tel: +44 1 494 567 444 |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada deste medicamento está disponível na página web da Agência Europeia de Medicamentos: http://www.ema.europa.eu .
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a EVRA 203 microgramas/24 horas + 33,9 microgramas/24 horas Adesivo TransdérmicoForma farmacêutica: PENSAMENTO TRANSDÉRMICO, 203 microgramas/24 h + 33,9 microgramas/24 hSubstância ativa: norelgestromin and ethinylestradiolFabricante: Gedeon Richter Plc.Requer receita médicaForma farmacêutica: ADESIVO TRANSDÉRMICO, 203 microgramas/24 h + 33,9 microgramas/24 hSubstância ativa: norelgestromin and ethinylestradiolFabricante: Gedeon Richter Plc.Requer receita médicaForma farmacêutica: COMPRIMIDO, 2 mg/0,03 mgSubstância ativa: dienogest and ethinylestradiolFabricante: Laboratorios Cinfa S.A.Requer receita médica
Alternativas a EVRA 203 microgramas/24 horas + 33,9 microgramas/24 horas Adesivo Transdérmico noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a EVRA 203 microgramas/24 horas + 33,9 microgramas/24 horas Adesivo Transdérmico em Polónia
Médicos online para EVRA 203 microgramas/24 horas + 33,9 microgramas/24 horas Adesivo Transdérmico
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de EVRA 203 microgramas/24 horas + 33,9 microgramas/24 horas Adesivo Transdérmico – sujeita a avaliação médica e regras locais.