
CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃO

Pergunte a um médico sobre a prescrição de CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃO

Como usar CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃO
Introdução
Prospecto: informação para o paciente
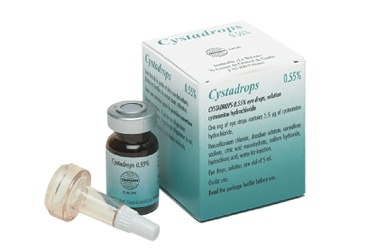
Cystadrops 3,8 mg/ml colírio em solução
cisteamina (mercaptamina)
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Cystadrops e para que é utilizado
- O que precisa saber antes de começar a usar Cystadrops
- Como usar Cystadrops
- Possíveis efeitos adversos
- Conservação de Cystadrops
- Conteúdo do envase e informações adicionais
1. O que é Cystadrops e para que é utilizado
O que é Cystadrops
Cystadrops é um colírio em solução que contém o princípio ativo cisteamina (também conhecido como mercaptamina).
Para que é utilizado
É utilizado para reduzir a quantidade de cristais de cistina na superfície do olho (córnea) em adultos e crianças maiores de 6 meses de idade com cistinose.
O que é a cistinose
A cistinose é uma doença hereditária rara em que o corpo é incapaz de eliminar o excesso de cistina (um aminoácido), provocando a acumulação de cristais de cistina em vários órgãos (como rins e olhos). A acumulação de cristais no olho pode conduzir a um aumento da sensibilidade à luz (fotofobia), deterioração da córnea (queratopatia) e perda da visão.
2. O que precisa saber antes de começar a usar Cystadrops
Não use Cystadrops
Se é alérgico à cisteamina ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar Cystadrops.
Outros medicamentos e Cystadrops
Informa o seu médico ou farmacêutico se está utilizando, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento.
Gravidez e lactação
Embora o nível de Cystadrops no sangue seja insignificante, devem ser tomadas precauções.
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Condução e uso de máquinas
Alguns minutos após o uso de Cystadrops pode notar que a sua visão se torna borrosa. Não conduza nem use máquinas até que a sua visão se aclare.
Cystadrops contém cloreto de benzalconio
Este medicamento contém 5 microgramas de cloreto de benzalconio em cada gota, equivalente a 0,1 mg/ml.
O cloreto de benzalconio pode ser absorvido pelas lentes de contato macias, alterando a sua cor. Retire as lentes de contato antes de usar este medicamento e espere 15 minutos antes de voltar a colocá-las.
O cloreto de benzalconio pode causar irritação ocular, especialmente se padece de olho seco ou outras doenças da córnea (camada transparente da zona frontal do olho). Consulte o seu médico se nota uma sensação estranha no olho, coceira ou dor no olho após usar este medicamento.
3. Como usar Cystadrops
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
Dose recomendada
- A dose recomendada é 1 gota em cada olho, 4 vezes ao dia durante as horas de vigília.
- O intervalo recomendado entre cada aplicação é de 4 horas (por exemplo, pode utilizar o colírio às 8 da manhã, às 12 do meio-dia, às 4 da tarde e às 8 da noite).
- Para evitar os olhos pegajosos pela manhã, deve aconselhar o paciente a aplicar a última gota pelo menos 30 minutos antes de ir para a cama.
- O seu médico pode reduzir a dose progressivamente (até uma dose diária total mínima de 1 gota em cada olho) dependendo dos resultados do exame oftálmico.
Utilize o colírio apenas nos seus olhos (via oftálmica).
Para usar o colírio, siga as seguintes instruções cuidadosamente.Essas instruções também estão disponíveis em um vídeo que pode encontrar em www.cystadrops.net ‘Deve incluir o código QR’
Paso 1: Antes de usar um frasco pela primeira vez
- O paciente deve levar consigo Cystadrops, a temperatura ambiente antes da primeira administração. Isso facilitará o uso das gotas.
- Imediatamente antes de usar um frasco pela primeira vez, anote a data de abertura no espaço fornecido na caixa.
- Lave as mãos cuidadosamente para evitar a contaminação bacteriana do conteúdo do frasco.
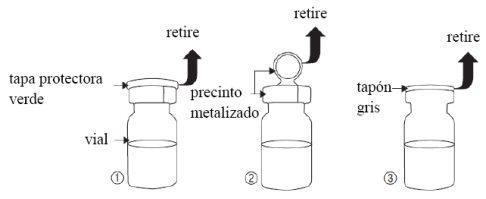
- Retire a tampa protetora verde (figura 1).
- Retire o lacre metalizado (figura 2).
- Retire a tampa cinza (figura 3) do frasco.
- Não toque na abertura do frasco após retirar a tampa cinza.
- Saia o conta-gotas da sua bolsa sem tocar a extremidade que irá colocada no frasco, insira-o (figura 4) no frasco. Não retire o conta-gotas do frasco.
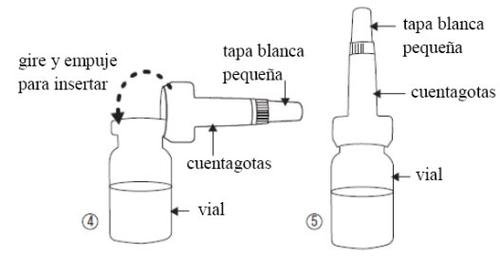
- Não perca a tampa branca pequena (figura 5) que vem na parte superior do conta-gotas.
Paso 2: Antes de usar o colírio
- Verifique a data de abertura que escreveu na caixa. Cystadrops pode ser usado durante um máximo de 7 dias desde o momento da sua abertura.
- Tome o frasco conta-gotas e coloque-se diante de um espelho.
- Lave as mãos.
Paso 3: Uso do colírio
- Segure o frasco conta-gotas para baixo, entre o polegar e os outros dedos. Mova o frasco conta-gotas firmemente para cima e para baixo para facilitar o preenchimento do conta-gotas.
- Desrosqueie a tampa branca pequena do conta-gotas.
- Incline a cabeça para trás. Puxe suavemente a pálpebra para baixo com um dedo limpo, até que se forme um espaço entre a pálpebra e o olho. Esse é o local de aplicação do colírio (figura 6).
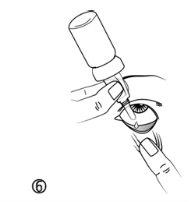
- Aproxime a ponta do frasco conta-gotas do olho. Pode usar um espelho se isso ajudar.
- Não toque no olho, na pálpebra, nas zonas adjacentes, nem em outras superfícies com o conta-gotas.Isso pode infectar o colírio.
- Pressione suavemente o conta-gotas para que caia uma gota de Cystadrops cada vez. Tenha especial cuidado para não tocar a ponta do conta-gotas com os dedos.
- Após usar Cystadrops, pressione com um dedo a borda do olho, junto à nariz (figura 7), em seguida, massageie suavemente a pálpebra superior para espalhar o colírio sobre o olho.
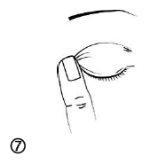
- Para evitar uma possível irritação, retire o excesso de medicamento ao redor do olho com um pano úmido (figura 8).
- Repita o passo 3 com o outro olho.
- Voltar a colocar a tampa branca pequena no conta-gotas imediatamente após o uso.
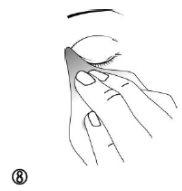
Paso 4: Conservação do colírio após o uso
- Guarde o frasco conta-gotas colocado na caixa.
- Mantenha Cystadrops a temperatura ambiente (para facilitar o uso do conta-gotas).
- Descarte 7 dias após a primeira abertura.
Se uma gota não cair no olho
Tente novamente.
Se usar Cystadrops com outro medicamento oftálmico
Deixe passar 10 minutos entre o uso de Cystadrops e o outro medicamento oftálmico. Administre as pomadas para os olhos no final.
Se usar lentes de contato macias
Não use o colírio com as lentes colocadas. Após usar o colírio, espere 15 minutos antes de voltar a colocar as lentes.
Se usar mais Cystadrops do que deve
Se aplicou demasiado colírio, lave os olhos preferencialmente com solução salina (se não for possível, com água morna). Não aplique mais gotas até que chegue o momento da sua próxima dose.
Se esquecer de usar Cystadrops
Espere até a próxima aplicação e, em seguida, continue com o esquema de tratamento habitual. Não utilize uma dose dupla para compensar as doses esquecidas.
Se interromper o tratamento com Cystadrops
Cystadrops deve ser usado diariamente para que o medicamento atue devidamente. Se deixar de utilizar Cystadrops, pode aumentar a acumulação de cristais de cistina no olho (córnea) e conduzir a uma maior sensibilidade à luz (fotofobia), deterioração da córnea (queratopatia) e perda da visão. Portanto, consulte com o seu médico antes de interromper este tratamento.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Normalmente pode continuar aplicando o colírio, a não ser que tenha efeitos graves. Se esses efeitos o preocupam, consulte o seu médico ou farmacêutico. Não interrompa o uso de Cystadrops sem consultar antes o seu médico.
Foram comunicados os seguintes efeitos adversos:
Efeitos adversos muito frequentes(podem afetar mais de 1 de cada 10 pessoas)
- dor ocular
- vermelhidão, coceira ou irritação dos olhos (ardor)
- lacrimejamento
- visão borrosa
- molestias no local onde se instilou o colírio (principalmente olhos e pestanas pegajosas), acumulação do medicamento nas pestanas ou ao redor dos olhos
Efeitos adversos frequentes(podem afetar até 1 de cada 10 pessoas)
- sensação anormal no olho, sensação de ter algo no olho
- olhos secos
- pálpebra inchada
- irritação da pálpebra
- alteração visual
- dor no local onde se instilou o colírio
- orzelo
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Cystadrops
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e na caixa após EXP.
Antes de abrir:
- Conservar em refrigerador (entre 2°C e 8°C).
- Conservar o frasco no embalagem exterior para protegê-lo da luz.
Após a primeira abertura:
- Anote a data de abertura do frasco no espaço fornecido na caixa.
- Cystadrops pode ser usado durante um máximo de 7 dias desde o momento da sua abertura.
- Conservar o frasco conta-gotas perfeitamente fechado no embalagem exterior para protegê-lo da luz.
- Conservar abaixo de 25°C.
- Não refrigerar.
- Deve descartar o frasco conta-gotas 7 dias após a primeira abertura, mesmo que não esteja vazio.Use um frasco novo.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
Composição de Cystadrops
- O princípio ativo é cisteamina (mercaptamina), em forma de cloreto de cisteamina. Um mililitro de colírio em solução contém 3,8 mg de cisteamina.
- Os outros componentes são cloreto de benzalconio (ver seção 2, em ‘Cystadrops contém cloreto de benzalconio’), EDTA dissódico, carmelosa sódica, ácido cítrico monohidratado, hidróxido sódico, ácido clorídrico e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Cystadrops é um colírio em solução transparente e viscosa.
Cada caixa contém:
- 1 frasco de vidro âmbar com 5 ml de colírio em solução,
- 1 conta-gotas.
Cystadrops está disponível em um envase que contém 1 caixa ou em um envase múltiplo que contém 4 caixas.
Pode ser que em seu país apenas alguns tamanhos de envases estejam comercializados.
Titular da autorização de comercialização
Recordati Rare Diseases
Tour Hekla52 Avenue du Général de Gaulle
92800 Puteaux
França
Fabricante
Recordati Rare Diseases
Tour Hekla52 Avenue du Général de Gaulle
92800 Puteaux
França
ou
Recordati Rare Diseases
Eco River Parc
30, rue des Peupliers
F-92000 Nanterre
França
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Bélgica Recordati Tel: +32 2 46101 36 | Lituânia Recordati AB. Tel: + 46 8 545 80 230 Suécia |
| Luxemburgo Recordati Tel: +32 2 46101 36 Bélgica |
República Tcheca Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 França | Hungria Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 França |
Dinamarca Recordati AB. Tel: +46 8 545 80 230 Suécia | Malta Recordati Rare Diseases Tel: +33 1 47 73 64 58 França |
Alemanha Recordati Rare Diseases Germany GmbH Tel: +49 731 140 554 0 | Países Baixos Recordati Tel: +32 2 46101 36 Bélgica |
Estônia Recordati AB. Tel: + 46 8 545 80 230 Estônia | Noruega Recordati AB. Tel: +46 8 545 80 230 Suécia |
Grécia Recordati Rare Diseases Tel: +33 1 47 73 64 58 França | Áustria Recordati Rare Diseases Germany GmbH Tel: +49 731 140 554 0 Alemanha |
Espanha Recordati Rare Diseases Spain S.L.U. Tel: + 34 91 659 28 90 | Polônia Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 França |
França Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 | Portugal Recordati Rare Diseases SARL Tel: +351 21 432 95 00 |
Croácia Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 França | Romênia Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 França |
Irlanda Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 França | Eslovênia Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 França |
Islândia Recordati AB. Simi: +46 8 545 80 230 Suécia | República Eslovaca Recordati Rare Diseases Tel: +33 (0)1 47 73 64 58 França |
Itália Recordati Rare Diseases Italy Srl Tel: +39 02 487 87 173 | Finlândia Recordati AB. Puh/Tel: +46 8 545 80 230 Suécia |
Chipre Recordati Rare Diseases Tel: +33 1 47 73 64 58 França | Suécia Recordati AB. Tel: +46 8 545 80 230 |
Letônia Recordati AB. Tel: + 46 8 545 80 230 Suécia |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada deste medicamento está disponível na página web da Agência Europeia de Medicamentos: https://www.ema.europa.eu. Também existem links para outras páginas web sobre doenças raras e medicamentos órfãos.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃOForma farmacêutica: COLÍRIO, 5,5 mg cloreto de sódio; 3 mg hipromelose/mlSubstância ativa: artificial tears and other indifferent preparationsFabricante: Alcon Healthcare S.A.Não requer receita médicaForma farmacêutica: COLÍRIO, 3,2 mg/mlSubstância ativa: artificial tears and other indifferent preparationsFabricante: Bausch & Lomb S.A.Não requer receita médicaForma farmacêutica: COLÍRIO, 3,2 mg/mlSubstância ativa: artificial tears and other indifferent preparationsFabricante: Bausch & Lomb S.A.Não requer receita médica
Alternativas a CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃO em Polónia
Alternativa a CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃO em Ukraine
Médicos online para CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de CYSTADROPS 3,8 mg/ml COLÍRIO EM SOLUÇÃO – sujeita a avaliação médica e regras locais.















