

ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada

Pergunte a um médico sobre a prescrição de ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada

Como usar ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada
Introdução
Prospecto: informação para o utilizador
Arixtra 5 mg/0,4 ml solução injetável
Arixtra 7,5 mg/0,6 ml solução injetável
Arixtra 10 mg/0,8 ml solução injetável
fondaparinux sódico
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto:
- O que é Arixtra e para que é utilizado
- O que precisa saber antes de começar a usar Arixtra
- Como usar Arixtra
- Posíveis efeitos adversos
- Conservação de Arixtra
- Conteúdo do envase e informação adicional
1. O que é Arixtra e para que é utilizado
Arixtra é um medicamento para tratar ou contribuir para evitar a formação de coágulos nos vasos sanguíneos (um agente antitrombótico). Arixtra contém uma substância sintética chamadafondaparinux sódico. Esta detém o efeito do factor de coagulação Xa “dez-A” no sangue e, por tanto, previne a formação de coágulos sanguíneos indesejados (trombos) nos vasos sanguíneos.
Arixtra é utilizado para tratar adultos que possuem algum coágulo sanguíneo nos vasos sanguíneos das suas pernas (trombose venosa profunda)e/ou nos pulmões (embolia pulmonar).
2. O que precisa saber antes de começar a usar Arixtra
Não use Arixtra:
- se é alérgicoa fondaparinux sódico ou a qualquer um dos outros componentes deste medicamento (incluídos na seção 6).
- se está sangrando de forma importante
- se padece uma infecção bacteriana do coração
- se padece uma doença renal grave.
- Informa ao seu médicose acredita que lhe afeta alguma destas situações. Se for assim, não deve utilizar
Arixtra.
Advertências e precauções:
Consulte o seu médico ou farmacêutico antes de começar a utilizar Arixtra:
- se teve complicações anteriormente durante o tratamento com heparina ou medicamentos semelhantes à heparina que causam uma diminuição na cifra de plaquetas sanguíneas (trombocitopenia induzida por heparina)
- se apresenta um risco de sangramento incontrolado(hemorragia), tal como
- úlcera gástrica
- distúrbios hemorrágicos
- sangramento no cérebrorecente (hemorragia intracraniana)
- cirurgia recentecerebral, de coluna vertebral ou oftalmológica;
- se apresenta uma doença hepática grave
- se apresenta uma doença renal
- se tem 75 anos ou mais.
- Informa ao seu médicose lhe afeta alguma destas situações.
Crianças e adolescentes
Arixtra não foi testado em crianças nem em adolescentes menores de 17 anos.
Uso de Arixtra com outros medicamentos
Informa ao seu médico ou farmacêutico se está utilizando, utilizou recentemente ou poderia ter que utilizar qualquer outro medicamento, mesmo os adquiridos sem receita.
O uso de outros medicamentos pode afetar a forma como Arixtra actua ou ser afectado por Arixtra.
Gravidez e amamentação
Arixtra não deve ser prescrito a mulheres grávidas a menos que se considere estritamente necessário. Não se recomenda a amamentação durante o tratamento com Arixtra. Se está grávida, ou em período de amamentação, acredita que possa estar grávida ou está planeando ficar grávida, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Arixtra contém sódio
Este medicamento contém menos de 23 mg de sódio por dose; por isso, é considerado essencialmente “isento de sódio”.
A seringa de Arixtra contém látex
O protector da agulha da seringa contém látex, que pode causar reacções alérgicas em pessoas sensíveis ao látex.
Informa ao seu médicose é alérgico ao látex antes de ser tratado com Arixtra.
3. Como utilizar Arixtra
Siga exactamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte o seu médico ou farmacêutico.
O seu peso | Dose normal |
Inferior a 50 kg | 5 mg uma vez ao dia |
Entre 50 e 100 kg | 7,5 mg uma vez ao dia |
Superior a 100 kg | 10 mg uma vez ao dia. Esta dose pode ser reduzida a |
7,5 mg uma vez ao dia se padece uma doença | |
renal moderada. |
Deve ser injetado aproximadamente à mesma hora todos os dias.
Como administrar Arixtra
- Arixtra é administrado por injeção sob a pele (subcutânea) num dobro cutâneo formado na área inferior do abdómen. As seringas estão pré-carregadas com a dose exacta que precisa. Há diferentes seringas para as doses de 5 mg, 7,5 mg e 10 mg.Para uma descrição detalhada do modo de emprego de Arixtra veja o final do prospecto.
- Nãoinjete Arixtra num músculo (intramuscularmente).
Durante quanto tempo deve utilizar Arixtra
Deve utilizar Arixtra durante o período de tempo que lhe tenha sido indicado pelo seu médico, porque Arixtra o previne de uma doença importante.
Se injetar mais Arixtra do que deve
Entre em contacto com o seu médico ou farmacêutico imediatamente porque há um aumento do risco de sangramento.
Se esquecer de usar Arixtra
- Administre a dose tão pronto quanto se lembrar. Não se injete uma dose dupla para compensar as doses esquecidas.
- Em caso de dúvida,entre em contacto com o seu médico ou farmacêutico.
Se interromper o tratamento com Arixtra
Se interromper o tratamento antes de que o seu médico o tenha indicado, o coágulo sanguíneo pode não ter sido tratado adequadamente e pode correr o risco de desenvolver um novo coágulo sanguíneo numa veia na sua perna ou no pulmão. Antes de interromper o tratamento, entre em contacto como seu médico ou farmacêutico.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Posíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Sintomas a que deve estar atento
Reacções alérgicas graves(anafilaxia): são muito raras (até 1 de cada 10.000) em pacientes que usam
Arixtra. Os sintomas incluem:
- inchaço, por vezes da face ou boca (angioedema), que causa dificuldades para engolir ou respirar
- colapso.
- Entre em contacto com um médico imediatamentese sofrer estes sintomas. Deixe de usar Arixtra.
Efeitos adversos frequentes
Estes podem afectar más de 1 de cada 100 pacientestratados com Arixtra.
- sangramento(por exemplo da zona onde se fez a operação, de uma úlcera de estômago existente ou da nariz, encias, sangue na urina, tos com sangue, sangramento ocular, sangramento nos espaços articulares, sangramento interno no útero)
- acumulação localizada de sangue(em qualquer órgão ou tecido corporal)
- anemia(diminuição do número de glóbulos vermelhos)
- equimoses
Efeitos adversos pouco frequentes
Estes podem afectar até 1 de cada 100 pacientestratados com Arixtra.
- inchaço (edema)
- dor de cabeça
- dor
- dor no peito
- dificuldade ao respirar
- erupção cutânea ou picazón na pele
- exsudado da ferida da operação
- febre
- estar ou sentir-se mareado (náuseas ou vómitos)
- redução ou aumento do número de plaquetas (células do sangue necessárias para a coagulação)aumento de algumas substâncias químicas (enzimas) produzidas pelo fígado
Efeitos adversos raros
Estes podem afectar até 1 de cada 1.000 pacientestratados com Arixtra.
- reacção alérgica
- sangramento interno no cérebro, fígado ou abdómen
- ansiedade ou confusão
- desmaio ou tontura, tensão baixa
- sonolência ou cansaço
- rubor
- tos
- dor e inflamação do local da injeção
- infecção de feridas
- aumento no sangue da quantidade de nitrógeno não proteico
- dor de pernas ou dor de estômago
- dispepsia
- diarreia ou obstipação
- incremento da bilirrubina (uma substância produzida pelo fígado) no sangue
- redução do potássio no sangue
- dor ao redor da parte superior do estômago ou ardor de estômago
Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Arixtra
- Mantenha este medicamento fora da vista e do alcance das crianças
- Conservar abaixo de 25ºC. Não congelar
- Não é necessário conservar Arixtra na geladeira
Não utilize este medicamento:
- depois da data de validade que aparece na etiqueta e no estojo
- se perceber a presença de partículas ou uma mudança de coloração na solução
- se observar que a seringa está danificada
- se a seringa foi aberta e não vai ser utilizada imediatamente.
Eliminação das seringas
Os medicamentos ou as seringas não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Arixtra
O princípio ativo:
- 5 mg de fondaparinux sódico em 0,4 ml de solução injetável
- 7,5 mg de fondaparinux sódico em 0,6 ml de solução injetável
- 10 mg de fondaparinux sódico em 0,8 ml de solução injetável
Os demais componentes são cloreto de sódio, água para preparações injetáveis e ácido clorídrico e/ou hidróxido de sódio para ajustar o pH (ver seção 2).
Arixtra não contém nenhum produto de animais.
Aspecto do produto e conteúdo do envase
Arixtra é uma solução injetável transparente e incolora ou ligeiramente amarelada. É apresentada em uma seringa pré-carregada para uso único, equipada com um sistema de segurança que contribui para evitar picadas acidentais após o seu uso.
É apresentada em embalagens de 2, 7, 10 e 20 seringas pré-carregadas. Pode ser que apenas alguns tamanhos de embalagens sejam comercializados.
Título da autorização de comercialização e responsável pela fabricação
Título da autorização de comercialização:
Viatris Healthcare Limited, Damastown Industrial Park, Mulhuddart, Dublin 15, DUBLIN, Irlanda
Responsável pela fabricação:
Aspen Notre Dame de Bondeville, 1 rue de l'Abbaye, F-76960 Notre Dame de Bondeville, França.
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada deste medicamento está disponível na página web da Agência Europeia de Medicamentos http://www.ema.europa.eu
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização.
Bélgica/Bélgica/Bélgica Viatris Tel: + 32 (0)2 658 61 00 ?????? ?????? ???? ???.: +359 2 44 55 400 República Checa Viatris CZ s.r.o. Tel: + 420 222 004 400 | Lituânia Viatris UAB Tel: +370 5 205 1288 Luxemburgo/Luxemburgo Viatris Tel: + 32 (0)2 658 61 00 (Bélgica/Bélgica) Hungria Viatris Healthcare Kft. Tel.: + 36 1 465 2100 |
Dinamarca Viatris ApS Tlf: +45 28 11 69 32 | Malta V.J. Salomone Pharma Ltd Tel: + 356 21 22 01 74 |
Alemanha Viatris Healthcare GmbH Tel: +49 800 0700 800 | Países Baixos Mylan Healthcare BV Tel: +31 (0)20 426 3300 |
Estônia Viatris OÜ Tel: + 372 6363 052 | Noruega Viatris AS Tlf: + 47 66 75 33 00 |
Grécia Viatris Hellas Ltd Τηλ: +30 2100 100 002 | Áustria Mylan Österreich GmbH Tel: +43 1 86390 |
Espanha Viatris Pharmaceuticals, S.L. Tel: +34 900 102 712 | Polônia Mylan Healthcare Sp. z o.o. Tel.: + 48 22 546 64 00 |
França Viatris Santé Tél: + 33 (0)4 37 25 75 00 | Portugal Viatris Healthcare, Lda. Tel: + 351 21 412 72 00 |
Croácia Viatris Hrvatska d.o.o. Tel: +385 1 23 50 599 | Romênia BGP Products SRL Tel: +40 372 579 000 |
Irlanda Mylan Ireland Limited Tel: +353 1 8711600 | Eslovênia Viatris d.o.o. Tel: + 386 1 23 63 180 |
Islândia Icepharma hf Sími: +354 540 8000 | República Eslovaca Viatris Slovakia s.r.o. Tel: +421 2 32 199 100 |
Itália Viatris Italia S.r.l. Tel: + 39 02 612 46921 | Finlândia Viatris Oy Puh/Tel: +358 20 720 9555 |
Chipre Varnavas Hadjipanayis Ltd Τηλ: +357 2220 7700 | Suécia Viatris AB Tel: + 46 (0)8 630 19 00 |
Letônia Viatris SIA Tel: +371 676 055 80 | Reino Unido (Irlanda do Norte) Mylan IRE Healthcare Limited +353 18711600 |
Desenho 3. Serinha com um sistema manualde proteção da agulha com o capuchão de segurança cobrindo a agulha DEPOIS DO
USO
Tipos de seringas de segurança:
Há dois tipos de seringas de segurança para Arixtra, projetadas para proteger contra picadas acidentais após o seu uso. Um tipo de seringas tem um sistema automáticode proteção da agulha e o outro tem um sistema manual.
Componentes das seringas:
- Protetor da agulha
? Émbolo
? Zona de sujeição (com os dedos)
- Capuchão de segurança da agulha
Desenho 1.Serinha com um sistema automáticode proteção da agulha

Seringa com um sistema manualde proteção da agulha
Desenho 2. Serinha com um sistema manualde proteção da agulha
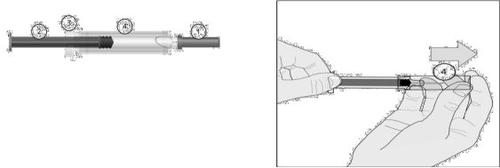
DESCRIÇÃO DO MODO DE EMPLEO DE ARIXTRAInstruções de uso
Estas instruções servem para os dois tipos de seringas (com sistema automático e com sistema manual de proteção da agulha).
Quando houver uma instrução diferente entre seringas, será especificado claramente.
- Lave cuidadosamente as mãoscom água e sabão e seque-as com uma toalha.
- Retire a serinha do envase e verifique que:
- não passou a data de validade
- a solução é transparente e incolora e não contém partículas
- a serinha não foi aberta ou danificada
- Sente-se ou deite-se em uma posição confortável.Selecione um ponto na zona inferior do abdômen (barriga), ao menos a 5 cm abaixo do umbigo (desenho A).
Para cada injeção alterne o lado esquerdo e direitoda zona inferior do abdômen. Isso ajudará a reduzir as molestias no local de injeção.
Se não for possível a injeção na zona inferior do abdômen, pergunte ao seu médico.
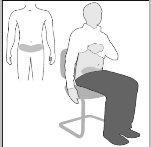
Desenho A
- Limpe a área de injeção com uma toalha ou algodão impregnado em álcool.
- Retire o protetor da agulha: primeiro girando (desenho
B1) e luego puxando para fora desde o corpo da serinha (desenho B2).
Descarte o protetor da agulha.
Nota importante
- Não toque a agulhae impida que ela entre em contato com qualquer superfície antes da injeção.
- É habitual encontrar uma pequena bolha de ar na serinha. Não tente eliminar essa bolha de arantes de aplicar a injeçãopois se poderia perder parte do medicamento.
- Pegue suavemente a pele que limpou previamente até formar um dobra. Segure o dobra entre o polegar e o índice durante toda a injeção (desenho C).
- Segure firmemente a serinha pela zona de sujeição. Insira a agulha em toda a sua longitude dentro do dobra cutâneo formando um ângulo reto (desenho D).
Desenho B1
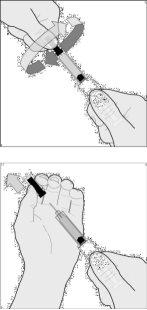
Desenho B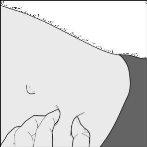
Desenho C
Desenho D
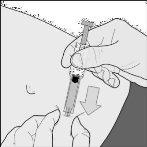
- Injete TODO o conteúdo da serinha pressionando para baixo o émbolo até o máximo(desenho E).
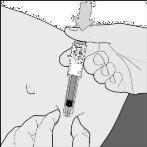
Desenho E
Seringa com sistema automático
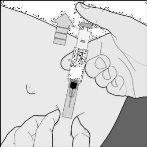
- Solte o émboloe a agulha se deslocará automaticamente desde a pele até um capuchão de segurança onde ficará bloqueada permanentemente (desenho F).
Desenho F
Seringa com sistema manual
- Depois da injeção, segure a serinha pelo capuchão de segurança da agulha com os dedos de uma mão, agarre com os dedos da outra mão a zona de sujeição e puxe para trás. Esta ação libera o capuchão. Deslize o capuchão pelo corpo da serinha até que fique bloqueado em uma posição que cubra a agulha tal como mostrado no desenho 3.
Não coloque a agulha usada no cubo de lixo.Descarte-a seguindo as instruções que o seu médico ou farmacêutico lhe deu.

Quanto custa o ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada em Espanha em 2025?
O preço médio do ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada em dezembro de 2025 é de cerca de 164.86 EUR. Os valores podem variar consoante a região, a farmácia e a necessidade de receita. Confirme sempre com uma farmácia local ou fonte online para obter informações atualizadas.
- País de registo
- Preço médio em farmácia164.86 EUR
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregadaForma farmacêutica: INJETÁVEL, 1,5 mgSubstância ativa: fondaparinuxFabricante: Viatris Healthcare LimitedRequer receita médicaForma farmacêutica: INJETÁVEL, 2,5 mgSubstância ativa: fondaparinuxFabricante: Viatris Healthcare LimitedRequer receita médicaForma farmacêutica: INJETÁVEL, 7,5 mgSubstância ativa: fondaparinuxFabricante: Viatris Healthcare LimitedRequer receita médica
Alternativas a ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada em Ukraine
Médicos online para ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ARIXTRA 5 mg/0,4 mL Solução injetável, seringa pré-carregada – sujeita a avaliação médica e regras locais.














