AMGEVITA 40 mg SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDA


Como usar AMGEVITA 40 mg SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDA
Introdução
Prospecto: informação para o paciente
AMGEVITA 40mg solução injetável em caneta pré-carregada
Adalimumab
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Seu médico lhe dará um cartão de informação para o paciente, que contém informações
de segurança importantes que precisa conhecer antes e durante o tratamento com
AMGEVITA. Conserva este cartão de informação para o paciente.
- Se tiver alguma dúvida, consulte seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si e não deve dá-lo a outras
pessoas, embora tenham os mesmos sintomas que você, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte seu médico ou farmacêutico, mesmo que se trate
de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é AMGEVITA e para que é utilizado
- O que precisa saber antes de começar a usar AMGEVITA
- Como usar AMGEVITA
- Posíveis efeitos adversos
- Conservação de AMGEVITA
- Conteúdo do envase e informações adicionais
1. O que é AMGEVITA e para que é utilizado
AMGEVITA contém como substância ativa adalimumab, um medicamento que atua sobre o sistema imunológico (defesa) do corpo.
AMGEVITA está indicado no tratamento de doenças inflamatórias que se descrevem a seguir:
- Artrite reumatoide
- Artrite idiopática juvenil poliarticular
- Artrite associada a entesite
- Espondilite anquilosante
- Espondiloartrite axial sem evidência radiográfica de espondilite anquilosante
- Artrite psoriásica
- Psoríase em placas
- Hidradenite supurativa
- Doença de Crohn
- Colite ulcerativa
- Uveíte não infecciosa
A substância ativa de AMGEVITA, adalimumab, é um anticorpo monoclonal humano. Os anticorpos monoclonais são proteínas que atacam uma diana específica.
A diana de adalimumab é uma proteína chamada fator de necrose tumoral (TNFα), que intervém no sistema imune (defesa) e se encontra em níveis elevados nas doenças inflamatórias descritas acima. Mediante o ataque ao TNFα, AMGEVITA diminui o processo de inflamação nessas doenças.
Artrite reumatoide
A artrite reumatoide é uma doença inflamatória das articulações.
AMGEVITA é utilizado para tratar a artrite reumatoide em adultos. Se você padece artrite reumatoide ativa moderada a grave, pode ser que seja administrado antes outros medicamentos modificadores da doença, tais como metotrexato. Em caso de que a resposta a esses medicamentos não seja suficiente, será administrado AMGEVITA para tratar sua artrite reumatoide.
AMGEVITA também pode ser utilizado no tratamento da artrite reumatoide grave, ativa e progressiva sem tratamento prévio com metotrexato.
AMGEVITA reduz o dano dos cartílagos e ossos das articulações produzido pela doença e melhora o desempenho físico.
Normalmente, AMGEVITA é utilizado junto com metotrexato. Se seu médico determinar que o metotrexato não é apropriado, AMGEVITA pode ser administrado sozinho.
Artrite idiopática juvenil poliarticular e artrite associada a entesite
A artrite idiopática juvenil poliarticular e a artrite associada a entesite são doenças inflamatórias das articulações que normalmente aparecem pela primeira vez na infância.
AMGEVITA é utilizado para tratar a artrite idiopática juvenil poliarticular em pacientes a partir dos 2 anos de idade e a artrite associada a entesite em pacientes a partir dos 6 anos de idade. Pode ter recebido primeiro outros fármacos modificadores da doença, como metotrexato. Se não responder suficientemente bem a esses medicamentos, receberá AMGEVITA para tratar sua artrite idiopática juvenil poliarticular ou artrite associada a entesite.
Espondilite anquilosante e espondiloartrite axial sem evidência radiográfica de espondilite anquilosante
A espondilite anquilosante e a espondiloartrite axial sem evidência radiográfica de espondilite anquilosante são doenças inflamatórias que afetam a coluna vertebral.
AMGEVITA é utilizado para tratar a espondilite anquilosante e a espondiloartrite axial sem evidência radiográfica de espondilite anquilosante em adultos. Se você tiver espondilite anquilosante ou espondiloartrite axial sem evidência radiográfica de espondilite anquilosante, será tratado primeiro com outros medicamentos e se não responder suficientemente a esses medicamentos, receberá AMGEVITA para reduzir os sinais e sintomas de sua doença.
Artrite psoriásica
A artrite psoriásica é uma inflamação das articulações associada à psoríase.
AMGEVITA é utilizado para tratar a artrite psoriásica em adultos. AMGEVITA reduz o dano articular que produz a doença no cartílago e no osso e melhora o desempenho físico.
Psoríase em placas em adultos e crianças
A psoríase em placas é uma doença da pele que causa áreas avermelhadas, escamosas, com crostas e cobertas por escamas prateadas. A psoríase em placas também pode afetar as unhas, provocando que se deteriorem, se engrossem e se levantem do leito da unha, o que pode ser doloroso. Acredita-se que a psoríase está causada por um defeito no sistema imunológico do corpo que leva a um aumento na produção de células da pele.
AMGEVITA é utilizado para tratar a psoríase em placas de moderada a grave em adultos. AMGEVITA também é utilizado para tratar a psoríase em placas grave em crianças e adolescentes entre 4 e 17 anos de idade que não tenham respondido ou não sejam bons candidatos para tratamento tópico e fototerapias.
Hidradenite supurativa em adultos e adolescentes
A hidradenite supurativa (às vezes denominada acne inverso) é uma doença inflamatória da pele crônica e frequentemente dolorosa. Os sintomas podem incluir nódulos sensíveis (bolhas) e abscessos (furúnculos) que podem secretar pus. Normalmente afeta áreas específicas da pele, como debaixo do peito, das axilas, zona interior dos músculos, virilha e nádegas. Também pode haver cicatrizes nas áreas afetadas.
AMGEVITA é utilizado para tratar a hidradenite supurativa em adultos e adolescentes a partir de 12 anos. AMGEVITA pode reduzir o número de nódulos e abscessos, e a dor que normalmente vai associada a esta doença. Pode ter recebido outros medicamentos previamente. Se não responder suficientemente bem a esses medicamentos, receberá AMGEVITA.
Doença de Crohn em adultos e crianças
A doença de Crohn é uma doença inflamatória do trato digestivo.
AMGEVITA é utilizado para tratar a doença de Crohn em adultos e crianças de idades compreendidas entre os 6 e os 17 anos. Se você padece doença de Crohn, será tratado primeiro com outros medicamentos. Se não responder suficientemente a esses medicamentos, receberá AMGEVITA para reduzir os sinais e sintomas da doença de Crohn.
Colite ulcerativa em adultos e crianças
A colite ulcerativa é uma doença inflamatória do intestino grosso.
AMGEVITA é utilizado para tratar a colite ulcerativa de moderada a grave em adultos e crianças de idades compreendidas entre os 6 e os 17 anos. Se você sofre colite ulcerativa, pode ser que primeiro lhe sejam prescritos outros medicamentos. Se você não responder bem a esses medicamentos, lhe serão prescritos AMGEVITA para reduzir os sinais e os sintomas de sua doença.
Uveíte não infecciosa em adultos e crianças
A uveíte não infecciosa é uma doença inflamatória que afeta certas partes do olho.
AMGEVITA é utilizado para tratar
- Adultos com uveíte não infecciosa com inflamação que afeta a zona posterior do olho.
- Crianças desde os 2 anos de idade com uveíte crônica não infecciosa com inflamação que afeta a parte frontal do olho.
Esta inflamação pode conduzir a uma diminuição da visão e/ou a presença de motas no olho (pontos negros ou linhas finas que se movem ao longo do campo de visão). AMGEVITA atua reduzindo esta inflamação.
2. O que precisa saber antes de começar a usar AMGEVITA
Não use AMGEVITA
- se for alérgico a adalimumab ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- se padece uma infecção grave, incluindo tuberculose ativa, sepsis (infecção sanguínea) ou outras infecções oportunistas (infecções incomuns associadas a um sistema imunológico debilitado (ver “Advertências e precauções”). Em caso de ter sintomas de qualquer infecção, por exemplo: febre, feridas, cansaço, problemas dentários, é importante que informe ao seu médico.
- se padece insuficiência cardíaca moderada ou grave. É importante que diga ao seu médico se teve ou tem algum problema cardíaco sério (ver “Advertências e precauções”).
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar AMGEVITA:
Reacções alérgicas
- Se notar uma reacção alérgica com sintomas como opressão no peito, dificuldade para respirar, tontura, inchaço ou erupção cutânea, interrompa a administração de AMGEVITA e entre em contacto com o seu médico imediatamente, pois, em casos raros, estas reacções podem por em perigo a vida.
Infecções
- Se padece qualquer infecção, incluindo as crónicas ou as localizadas (por exemplo: uma úlcera na perna), consulte o seu médico antes de começar o tratamento com AMGEVITA. Se não tiver certeza, entre em contacto com o seu médico.
- Com o tratamento com AMGEVITA poderá contrair infecções com mais facilidade. Este risco pode ser maior se tiver danos nos pulmões. Estas infecções podem ser graves e incluem tuberculose, infecções causadas por vírus, fungos, parasitas ou bactérias ou outras infecções oportunistas e sepsis que poderiam, em casos raros, por em perigo a sua vida. Por esta razão, é importante que, em caso de ter sintomas como febre, feridas, cansaço ou problemas dentários, diga ao seu médico. O seu médico poderá recomendar que interrompa temporariamente o tratamento com AMGEVITA.
Tuberculose
- Como se têm descrito casos de tuberculose em pacientes em tratamento com adalimumab, o seu médico o examinará em busca de sinais ou sintomas de tuberculose antes de começar o seu tratamento com AMGEVITA. Isso incluirá a realização de uma avaliação médica minuciosa, incluindo a sua história médica e as provas adequadas de diagnóstico (por exemplo, radiografia de tórax e a prova da tuberculina). A realização e resultados destas provas devem ser anotados na sua cartão de informação para o paciente. É muito importante que informe ao seu médico em caso de ter padecido tuberculose ou ter estado em contacto com um paciente de tuberculose.
- Pode desenvolver-se tuberculose durante o tratamento, mesmo que tenha recebido tratamento preventivo para a tuberculose.
- Se aparecerem sintomas de tuberculose (tos persistente, perda de peso, mal-estar geral, febrícula) ou de qualquer outra infecção durante ou uma vez finalizado o tratamento, entre em contacto imediatamente com o seu médico.
Infecções recorrentes/por viagens
- Avise o seu médico se reside ou viaja por regiões em que infecções fúngicas como histoplasmose, coccidioidomicose ou blastomicose são endémicas.
- Informa ao seu médico se tem antecedentes de infecções recorrentes ou outras patologias ou factores que aumentem o risco de infecções.
Vírus da hepatite B
- Informa ao seu médico se é portador do vírus da hepatite B (VHB), se teve infecções activas com VHB activo ou se pensa que possa correr risco de contrair o VHB. O seu médico deve realizar uma análise para o VHB. AMGEVITA pode causar a reativação do VHB em pessoas portadoras deste vírus. Em casos raros, especialmente se está a tomar outros medicamentos que suprimem o sistema imunológico, a reativação do VHB pode por em perigo a sua vida.
Ter mais de 65 anos
- Se tiver mais de 65 anos, pode ser mais susceptível de padecer infecções enquanto está em tratamento com AMGEVITA. Tanto o senhor como o seu médico devem prestar atenção especial à aparência de sinais de infecção enquanto estiver sendo tratado com AMGEVITA. É importante informar ao seu médico se tiver sintomas de infecções, como febre, feridas, sensação de cansaço ou problemas dentários.
Intervenções cirúrgicas ou dentárias
- Se lhe vão realizar uma intervenção cirúrgica ou dentária, informe ao seu médico de que está a tomar AMGEVITA. O seu médico poderá recomendar que interrompa temporariamente o tratamento com AMGEVITA.
Doença desmielinizante
- Se padece ou desenvolve uma doença desmielinizante como a esclerose múltipla, o seu médico decidirá se deve ser tratado ou continuar em tratamento com AMGEVITA. Informe imediatamente ao seu médico se experimenta sintomas tais como alterações na visão, fraqueza nos braços ou pernas ou entorpecimento ou formigamento em qualquer parte do corpo.
Vacinas
- Certas vacinas contêm bactérias ou vírus vivos, mas debilitados, que provocam doenças que podem causar infecções e não devem ser administradas se estiver em tratamento com AMGEVITA. Consulte com o seu médico antes da administração de qualquer tipo de vacina. Se for possível, recomenda-se que as crianças actualizem o seu calendário de vacinações de acordo com as orientações actuais de vacinação antes de iniciar o tratamento com AMGEVITA.
- Se receber AMGEVITA enquanto está grávida, o seu filho pode ter um risco maior de sofrer infecções durante aproximadamente os 5 meses seguintes à última dose que tenha recebido de AMGEVITA durante a gravidez. É importante que informe ao médico do seu filho e a outros profissionais de saúde sobre o uso de AMGEVITA durante a gravidez, para que eles possam decidir se o seu filho deve receber alguma vacina.
Insuficiência cardíaca
- Se padece insuficiência cardíaca ligeira e está em tratamento com AMGEVITA, o seu médico deve fazer-lhe um seguimento contínuo da sua insuficiência cardíaca. É importante que informe ao seu médico se teve ou tem algum problema cardíaco sério. Em caso de que apareçam novos sintomas de insuficiência cardíaca ou piorem os actuais (por exemplo: dificuldade em respirar, ou inchaço dos pés), deve entrar em contacto com o seu médico imediatamente. O seu médico decidirá se deve continuar a tomar AMGEVITA.
Febre, cardenales, sangramento ou palidez
- Em alguns pacientes, o organismo pode ser incapaz de produzir um número suficiente do tipo de células sanguíneas que ajudam o corpo a lutar contra as infecções (glóbulos brancos) ou das que contribuem para parar as hemorragias (plaquetas). Se tiver febre persistente, cardenales ou sangra muito facilmente ou está muito pálido, consulte imediatamente o seu médico. O seu médico pode decidir a interrupção do tratamento.
Cancro
- Em muito raras ocasiões, têm-se dado casos de certos tipos de cancro em crianças e adultos tratados com adalimumab ou outros agentes que bloqueiam o TNF. As pessoas com artrite reumatoide de graus mais graves e que padecem a doença desde há muito tempo podem ter um risco maior que a média de desenvolver um linfoma (um cancro que afeta o sistema linfático), e leucemia (um cancro que afeta a sangue e à medula óssea).
- Se estiver em tratamento com AMGEVITA, o risco de padecer linfoma, leucemia e outros tipos de cancro pode aumentar. Tem-se observado, em raras ocasiões, um tipo de linfoma específico e grave em pacientes em tratamento com adalimumab. Alguns destes pacientes recebiam tratamento também com azatioprina ou 6-mercaptopurina. Informe ao seu médico se está a tomar azatioprina ou 6-mercaptopurina com AMGEVITA.
- Além disso, têm-se observado casos de cancro de pele (tipo não melanoma) em pacientes que usam adalimumab. Avise ao seu médico se, durante ou após o tratamento, aparecerem novas lesões na pele ou se as lesões existentes mudam de aparência.
- Têm-se registado cancros, diferentes do linfoma, em pacientes com uma determinada doença pulmonar, denominada Doença Pulmonar Obstrutiva Crónica (DPOC), tratados com outro agente bloqueante do TNF. Se tiver DPOC, ou fuma muito, deve consultar o seu médico se o tratamento com um bloqueante do TNF é adequado no seu caso.
Doenças autoimunes
- Em raras ocasiões, o tratamento com AMGEVITA poderá dar origem a um síndroma semelhante ao lúpus. Entre em contacto com o seu médico se tiver sintomas como erupção persistente sem explicação, febre, dor nas articulações ou cansaço.
Com o fim de melhorar a rastreabilidade deste medicamento, o seu médico ou farmacêutico deve registar o nome e o número de lote do medicamento administrado na sua história clínica. No caso de que lhe seja solicitada esta informação num futuro, o senhor também pode tomar nota destes detalhes.
Crianças e adolescentes
- Vacinas: se for possível, o seu filho deve estar atualizado com todas as vacinas antes de usar AMGEVITA.
- Não administre AMGEVITA a crianças com artrite idiopática juvenil poliarticular menores de 2 anos.
- Não administre AMGEVITA a crianças com psoríase em placas menores de 4 anos.
- Não administre AMGEVITA a crianças com doença de Crohn ou colite ulcerosa menores de 6 anos.
Uso de AMGEVITA com outros medicamentos
Informa ao seu médico ou farmacêutico se está a tomar ou tomou recentemente ou poderá ter que tomar qualquer outro medicamento.
AMGEVITA pode ser tomado com metotrexato ou com certos medicamentos antirreumáticos modificadores da doença (sulfassalazina, hidroxicloroquina, leflunomida e preparações injetáveis a base de sais de ouro), esteroides ou medicamentos para a dor, incluídos os anti-inflamatórios não esteroides (AINEs).
Não deve utilizar AMGEVITA com medicamentos cujos princípios activos sejam anakinra ou abatacept devido a um aumento do risco de infecções graves. Se tiver alguma dúvida, consulte o seu médico.
Gravidez e amamentação
- Deve considerar o uso de métodos anticonceptivos adequados para evitar engravidar e continuar com o seu uso durante pelo menos 5 meses após o último tratamento com AMGEVITA.
- Se está grávida, acha que pode estar grávida ou tem intenção de ter um bebé, peça conselho ao seu médico sobre o uso deste medicamento.
- AMGEVITA deve ser usado durante a gravidez apenas se for necessário.
- De acordo com um estudo em gravidez, não houve um maior risco de defeitos congénitos quando a mãe tinha recebido tratamento com AMGEVITA durante a gravidez, comparado com as mães com a mesma doença que não receberam tratamento com AMGEVITA.
- AMGEVITA pode ser usado durante a amamentação.
- Se utilizar AMGEVITA enquanto está grávida, o seu filho pode ter um risco mais alto de contrair uma infecção.
- É importante que informe ao pediatra e a outros profissionais de saúde sobre o uso de AMGEVITA durante a gravidez antes de que o bebé receba qualquer vacina. Para mais informações sobre vacinas, ver a secção “Advertências e precauções”.
Condução e uso de máquinas
A influência de AMGEVITA sobre a capacidade para conduzir, andar de bicicleta ou utilizar máquinas é pequena. Podem produzir-se sensação de que a sala dá voltas (vertigem) e alterações da visão após tomar AMGEVITA.
AMGEVITA contém sódio
Este medicamento contém menos de 1 mmol de sódio (23 mg) por dose de 0,8 ml; isto é, essencialmente “isento de sódio”.
3. Como usar AMGEVITA
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico.
Adultos com artrite reumatoide, artrite psoriásica, espondilite anquilosante ou espondiloartrite axial sem evidência radiográfica de espondilite anquilosante
AMGEVITA é injetado sob a pele (via subcutânea). A dose normal em adultos com artrite reumatoide, espondilite anquilosante, espondiloartrite axial sem evidência radiográfica de espondilite anquilosante e para pacientes com artrite psoriásica é de 40 mg administrados em semanas alternadas como dose única.
No caso da artrite reumatoide, o tratamento com metotrexato é mantido durante o uso de AMGEVITA. Se o seu médico determinar que o metotrexato é inadequado, AMGEVITA pode ser administrado sozinho.
Se você sofre de artrite reumatoide e não recebe metotrexato durante o tratamento com AMGEVITA, o seu médico pode decidir dar-lhe 40 mg cada semana ou 80 mg cada duas semanas.
Crianças, adolescentes e adultos com artrite idiopática juvenil poliarticular
Crianças, adolescentes e adultos desde 2 anos de idade com peso de 30 kg ou mais
A dose recomendada de AMGEVITA é 40 mg administrados em semanas alternadas.
Crianças, adolescentes e adultos com artrite associada a entesite
Crianças, adolescentes e adultos desde 6 anos de idade com peso de 30 kg ou mais
A dose recomendada de AMGEVITA é 40 mg em semanas alternadas.
Adultos com psoríase em placas
A posologia normal em adultos com psoríase em placas consiste em uma dose inicial de 80 mg (como duas injeções de 40 mg em um dia), seguida de 40 mg em semanas alternadas começando em uma semana após a dose inicial. Deve continuar injetando AMGEVITA durante tanto tempo quanto o seu médico indicar. Dependendo da sua resposta, o seu médico pode aumentar a dose para 40 mg semanais ou 80 mg cada duas semanas.
Crianças e adolescentes com psoríase em placas
Crianças e adolescentes desde 4 a 17 anos de idade com 30 kg de peso ou mais
A dose recomendada de AMGEVITA é uma dose inicial de 40 mg, seguida de 40 mg uma semana depois. A partir daí, a dose habitual é de 40 mg em semanas alternadas.
Adultos com hidradenite supurativa
A pauta de dosificação habitual para a hidradenite supurativa é de uma dose inicial de 160 mg (como quatro injeções de 40 mg em um dia ou duas injeções de 40 mg por dia durante dois dias consecutivos), seguida de uma dose de 80 mg (como duas injeções de 40 mg em um dia) duas semanas depois. Depois de mais duas semanas, continue com uma dose de 40 mg semanais ou 80 mg cada duas semanas, conforme prescrito pelo seu médico. Recomenda-se que use diariamente um líquido antiséptico nas zonas afetadas.
Adolescentes com hidradenite supurativa a partir de 12 a 17 anos de idade, com um peso de 30 kg ou mais
A dose recomendada de AMGEVITA é uma dose inicial de 80 mg (como duas injeções de 40 mg em um dia), seguida de 40 mg em semanas alternadas começando uma semana depois. Se tiver uma resposta inadequada a AMGEVITA 40 mg em semanas alternadas, o seu médico pode aumentar a dose para 40 mg semanais ou 80 mg cada duas semanas.
Recomenda-se que use diariamente um líquido antiséptico nas zonas afetadas.
Adultos com doença de Crohn
A pauta de dosificação habitual para a doença de Crohn é de 80 mg (como duas injeções de 40 mg em um dia), inicialmente, seguido de 40 mg em semanas alternadas começando duas semanas depois. Se for necessária uma resposta mais rápida, o seu médico pode prescrever uma dose inicial de 160 mg (como quatro injeções de 40 mg em um dia ou duas injeções de 40 mg por dia durante dois dias consecutivos), seguido de 80 mg (como duas injeções de 40 mg em um dia) duas semanas depois, e a partir daí 40 mg em semanas alternadas. Dependendo da sua resposta, o seu médico pode aumentar a dose para 40 mg semanais ou 80 mg cada duas semanas.
Crianças e adolescentes com doença de Crohn
Crianças e adolescentes desde 6 a 17 anos de idade com peso inferior a 40 kg
A pauta de dosificação habitual é de 40 mg inicialmente seguido de 20 mg duas semanas depois. Se for necessária uma resposta mais rápida, o seu médico pode prescrever uma dose inicial de 80 mg (como duas injeções de 40 mg em um dia) seguido de 40 mg duas semanas depois.
A partir daí, a dose habitual é de 20 mg em semanas alternadas. Dependendo da sua resposta, o seu médico pode aumentar a frequência da dose para 20 mg semanais.
A caneta pré-carregada de 40 mg não pode ser usada para a dose de 20 mg. Está disponível uma seringa pré-carregada de 20 mg para a dose de 20 mg.
Crianças e adolescentes desde 6 a 17 anos com peso de 40 kg ou mais
A pauta de dosificação habitual é de 80 mg (como duas injeções de 40 mg em um dia) inicialmente seguido de 40 mg duas semanas depois. Se for necessária uma resposta mais rápida, o seu médico pode prescrever uma dose inicial de 160 mg (como quatro injeções de 40 mg em um dia ou duas injeções de 40 mg por dia durante dois dias consecutivos) seguido de 80 mg (como duas injeções de 40 mg em um dia) duas semanas depois.
A partir daí, a dose habitual é de 40 mg em semanas alternadas. Dependendo da sua resposta, o seu médico pode aumentar a dose para 40 mg semanais ou 80 mg cada duas semanas.
Adultos com colite ulcerativa
A posologia normal de AMGEVITA em adultos com colite ulcerativa é de 160 mg inicialmente (como quatro injeções de 40 mg em um dia ou duas injeções de 40 mg por dia durante dois dias seguidos) seguidas de 80 mg (como duas injeções de 40 mg em um dia) duas semanas depois, e a partir daí 40 mg em semanas alternadas. Dependendo da sua resposta, o seu médico pode aumentar a dose para 40 mg semanais ou 80 mg cada duas semanas.
Crianças e adolescentes com colite ulcerativa
Crianças e adolescentes desde 6 anos com um peso inferior a 40 kg
A dose habitual de AMGEVITA é de 80 mg (como duas injeções de 40 mg em um dia) inicialmente, seguida de uma dose de 40 mg (como uma injeção de 40 mg) duas semanas depois. A partir daí, a dose habitual é de 40 mg em semanas alternadas.
Os pacientes que atingem 18 anos enquanto recebem tratamento com 40 mg em semanas alternadas devem continuar com a dose prescrita.
Crianças e adolescentes desde 6 anos com um peso de 40 kg ou superior
A dose habitual de AMGEVITA é de 160 mg (como quatro injeções de 40 mg em um dia ou duas injeções de 40 mg ao dia em dois dias consecutivos) inicialmente, seguida de uma dose de 80 mg (como duas injeções de 40 mg em um dia) duas semanas depois. A partir daí, a dose habitual é de 80 mg em semanas alternadas.
Os pacientes que atingem 18 anos enquanto recebem tratamento com 80 mg em semanas alternadas devem continuar com a dose prescrita.
Adultos com uveíte não infecciosa
A dose habitual em adultos com uveíte não infecciosa é uma dose inicial de 80 mg, (como duas injeções de 40 mg em um dia), seguida de 40 mg em semanas alternadas começando uma semana após a dose inicial. Deve continuar injetando AMGEVITA durante o tempo que o seu médico indicar.
Em uveíte não infecciosa, pode-se continuar o tratamento com corticosteroides ou outros medicamentos que afetam o sistema imunológico durante o uso de AMGEVITA. AMGEVITA também pode ser administrado sozinho.
Crianças e adolescentes desde os 2 anos de idade com uveíte crônica não infecciosa
Crianças e adolescentes desde 2 anos de idade com peso menor que 30 kg
A dose habitual de AMGEVITA é de 20 mg em semanas alternadas junto com metotrexato.
O seu médico pode prescrever uma dose inicial de 40 mg que pode ser administrada uma semana antes de começar com a pauta habitual.
A caneta pré-carregada de 40 mg não pode ser usada para a dose de 20 mg. Está disponível uma seringa pré-carregada de 20 mg para a dose de 20 mg.
Crianças e adolescentes desde 2 anos de idade com um peso de 30 kg ou mais
A dose habitual de AMGEVITA é de 40 mg em semanas alternadas junto com metotrexato.
O seu médico pode prescrever uma dose inicial de 80 mg que pode ser administrada uma semana antes de começar com a pauta habitual.
Forma e via de administração
AMGEVITA é injetado sob a pele (via subcutânea).
São fornecidas instruções detalhadas sobre como injetar AMGEVITA na seção “Instruções de uso”.
Se usar mais AMGEVITA do que deve
Se acidentalmente se injetar AMGEVITA com mais frequência do que a pautada pelo seu médico, informe disso ao seu médico. Sempre leve a caixa do medicamento consigo, mesmo se estiver vazia.
Se esquecer de usar AMGEVITA
Se esquecer de administrar uma injeção, deve injetar a próxima dose de AMGEVITA assim que se lembrar. Depois, a próxima dose será administrada como habitualmente, como se não se tivesse esquecido de uma dose.
Se interromper o tratamento com AMGEVITA
A decisão de deixar de usar AMGEVITA deve ser discutida com o seu médico. Os seus sintomas podem voltar após a interrupção do tratamento.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram. A maioria dos efeitos adversos é leve a moderada. No entanto, alguns podem ser graves e requerer tratamento. Os efeitos adversos podem aparecer até 4 meses após a última injeção de AMGEVITA.
Entre em contato com o seu médico imediatamente se notar algum dos seguintes sinais de reação alérgica ou insuficiência cardíaca:
- erupção grave, urticária ou outros sinais de reação alérgica;
- inchaço do rosto, mãos, pés;
- dificuldade para respirar, engolir;
- falta de ar ao fazer exercícios ou ao estar deitado, inchaço dos pés.
Entre em contato com o seu médico assim que possível se notar algum dos seguintes efeitos
- sinais de infecção, tais como febre, ganas de vomitar, feridas, problemas dentários, sensação de queimadura ao urinar;
- sensação de fraqueza ou cansaço;
- tosse;
- formigamento;
- entorpecimento;
- visão dupla;
- fraqueza nos braços ou pernas;
- sinais de câncer de pele, tais como uma protuberância ou uma ferida aberta que não se cura;
- sinais e sintomas de alterações no sangue, como febre persistente, cardenais, hemorragias e palidez.
Os sintomas descritos anteriormente podem ser sinais dos efeitos adversos listados a seguir, que foram observados com adalimumabe.
Muito frequentes (podem afetar mais de 1 em cada 10 pessoas)
- reações no local de injeção (incluindo dor, inchaço, vermelhidão ou coceira);
- infecções do trato respiratório (incluindo resfriado, corrimento, sinusite, pneumonia);
- dor de cabeça;
- dor abdominal;
- náuseas e vômitos;
- erupção cutânea;
- dor muscular.
Frequentes (podem afetar até 1 em cada 10 pessoas)
- infecções graves (incluindo septicemia e gripe);
- infecções intestinais (incluindo gastroenterite);
- infecções da pele (incluindo celulite e herpes);
- infecção de ouvido;
- infecções orais (incluindo infecção dentária e úlceras bucais);
- infecções no sistema reprodutor;
- infecção do trato urinário;
- infecções por fungos;
- infecção nas articulações;
- tumores benignos;
- câncer de pele;
- reações alérgicas (incluindo alergia sazonal);
- desidratação;
- mudanças de humor (incluindo depressão);
- ansiedade;
- dificuldade para dormir;
- alterações sensoriais, como formigamento, coceira ou entorpecimento;
- enxaqueca;
- compressão da raiz nervosa (incluindo dor na parte baixa das costas e na perna);
- alterações visuais;
- inflamação do olho;
- inflamação da pálpebra e inchaço do olho;
- tontura (sensação de vertigem ou como se o quarto desse voltas);
- sensação de pulso acelerado;
- pressão arterial alta;
- rubor;
- hematomas;
- tosse;
- asma;
- dificuldade para respirar;
- sangramento gastrointestinal;
- dispepsia (indigestão, inchaço e azia);
- refluxo ácido;
- síndrome do olho seco (incluindo secura nos olhos e boca);
- coceira;
- erupção cutânea com coceira;
- hematomas;
- inflamação da pele (como eczema);
- quebra de unhas das mãos e dos pés;
- aumento da transpiração;
- perda de cabelo;
- psoríase de nova aparição ou piora da psoríase existente;
- espasmos musculares;
- sangue na urina;
- problemas renais;
- dor no peito;
- edema;
- febre;
- diminuição de plaquetas no sangue, o que aumenta o risco de sangramento ou hematomas;
- problemas de cicatrização.
Pouco frequentes (podem afetar até 1 em cada 100 pessoas)
- infecções oportunistas (que incluem tuberculose e outras infecções que ocorrem quando a resistência à doença diminui);
- infecções neurológicas (incluindo meningite viral);
- infecções do olho;
- infecções bacterianas;
- diverticulite (inflamação e infecção do intestino grosso);
- câncer, incluindo o câncer que afeta o sistema linfático (linfoma) e melanoma (câncer de pele);
- alterações imunológicas que podem afetar os pulmões, pele e gânglios linfáticos (a apresentação mais frequente é sarcoidose);
- vasculite (inflamação dos vasos sanguíneos);
- tremer;
- neuropatia;
- acidente vascular cerebral;
- perda de audição, zumbido;
- sensação de pulso irregular como saltos;
- problemas cardíacos que podem causar dificuldade para respirar ou inchaço dos tornozelos;
- ataque cardíaco;
- saco na parede de uma artéria maior, inflamação e coagulação em uma veia, bloqueio de um vaso sanguíneo;
- doenças pulmonares que podem causar dificuldade para respirar (incluindo inflamação);
- embolia pulmonar (bloqueio de uma artéria do pulmão);
- derrame pleural (armazenamento anormal de fluido no espaço pleural);
- inflamação do pâncreas que causa uma dor grave no abdômen e nas costas;
- dificuldade para engolir;
- inchaço facial;
- inflamação da vesícula; pedras na vesícula;
- gordura no fígado;
- sudores noturnos;
- cicatrizes;
- crise muscular anormal;
- lúpus eritematoso sistêmico (incluindo inflamação da pele, coração, pulmões, articulações e outros órgãos);
- interrupções do sono;
- impotência;
- inflamações.
Raros (podem afetar até 1 em cada 1.000 pessoas)
- leucemia (câncer que afeta o sangue e a medula óssea);
- reação alérgica grave com choque;
- esclerose múltipla;
- alterações nervosas (como inflamação do nervo óptico e síndrome de Guillain-Barré que pode provocar fraqueza muscular, sensações anormais, formigamento nos braços e na parte superior do corpo);
- parada cardíaca;
- fibrose pulmonar (cicatriz no pulmão);
- perfuração intestinal (buraco na parede intestinal);
- hepatite (inflamação do fígado);
- reativação do vírus da hepatite B;
- hepatite autoimune (inflamação do fígado causada pelo próprio sistema imunológico do corpo);
- vasculite cutânea (inflamação dos vasos sanguíneos na pele);
- síndrome de Stevens-Johnson (reação potencialmente mortal com sintomas semelhantes à gripe e erupções cutâneas com bolhas);
- inchaço facial associado a reações alérgicas;
- eritema multiforme (erupção inflamatória na pele);
- síndrome semelhante ao lúpus;
- angioedema (inflamação da pele localizada);
- reação liquenoide na pele (erupção cutânea vermelha-púrpura com coceira).
Frequência não conhecida (não pode ser estimada a partir dos dados disponíveis)
- linfoma hepatoesplênico de células T (câncer sanguíneo raro que é frequentemente mortal);
- carcinoma de células de Merkel (um tipo de câncer de pele);
- sarcoma de Kaposi, um câncer pouco comum relacionado à infecção pelo vírus do herpes humano 8. O sarcoma de Kaposi geralmente se manifesta com mais frequência como lesões cutâneas de cor púrpura;
- insuficiência hepática;
- piora de uma doença chamada dermatomiosite (vista como erupção cutânea acompanhada de fraqueza muscular);
- aumento de peso (para a maioria dos pacientes, o aumento de peso foi reduzido).
Alguns efeitos adversos observados com adalimumabe não têm sintomas e só podem ser identificados por meio de um exame de sangue. Estes incluem:
Muito frequentes (podem afetar mais de 1 em cada 10 pessoas)
- baixo recuento sanguíneo de células brancas;
- baixo recuento sanguíneo de células vermelhas;
- aumento de lípidos no sangue;
- aumento de enzimas hepáticas.
Frequentes (podem afetar até 1 em cada 10 pessoas)
- alto recuento sanguíneo de células brancas;
- baixo recuento sanguíneo de plaquetas;
- aumento de ácido úrico no sangue;
- valores anormais de sódio no sangue;
- baixo nível de cálcio no sangue;
- baixo nível de fosfato no sangue;
- glicose alta no sangue;
- valores altos de lactato desidrogenase no sangue;
- presença de autoanticorpos no sangue;
- baixo nível de potássio no sangue.
Pouco frequentes (podem afetar até 1 em cada 100 pessoas)
- valores de bilirrubina elevados (exame de função hepática).
Raros (podem afetar até 1 em cada 1.000 pessoas)
- recuentos baixos no sangue para células brancas, células vermelhas e plaquetas.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente por meio do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de AMGEVITA
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e no envase após EXP ou CAD. A data de validade é o último dia do mês que se indica.
Conservar em frigorífico (entre 2 °C e 8 °C). Não congelar.
Conservar no embalagem original para protegê-lo da luz.
Pode armazenar uma pluma precargada individual de AMGEVITA a temperaturas até um máximo de 25 °C durante um período máximo de 14 dias. A pluma precargada deve estar protegida da luz e deve ser descartada se não for usada durante um período de 14 dias.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de AMGEVITA
- O princípio ativo é adalimumabe. Cada pluma contém 40 mg de adalimumabe em 0,8 ml de solução.
- Os demais componentes são ácido acético glacial, sacarose, polissorbato 80, hidróxido de sódio e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
AMGEVITA é uma solução transparente de incolora a ligeiramente amarelada.
Cada envase contém 1, 2, 4 ou 6 plumas precargadas SureClick de um só uso.
Título da autorização de comercialização e responsável pela fabricação
Amgen Europe B.V.
Minervum 7061
4817 ZK Breda
Países Baixos
Título da autorização de comercialização
Amgen Europe B.V.
Minervum 7061
4817 ZK Breda
Países Baixos
Fabricante
Amgen Technology Ireland UC
Pottery Road
Dun Laoghaire
CoDublin
Irlanda
Fabricante
Amgen NV
Telecomlaan 5-7
1831 Diegem
Bélgica
Pode solicitar mais informações sobre este medicamento, dirigindo-se ao representante local do titular da autorização de comercialização.
Bélgica/Bélgica/Bélgica s.a. Amgen n.v. Tel: +32 (0)2 7752711
República Checa Amgen s.r.o. Tel: +420 221 773 500 Dinamarca Amgen, filial af Amgen AB, Sverige Tlf: +45 39617500 Alemanha Amgen GmbH Tel: +49 89 1490960 Estônia Amgen Switzerland AG Vilniaus filialas Tel: +372 586 09553 Grécia Amgen Ελλάς Φαρμακευτική Ε.Π.Ε. Τηλ: +30 210 3447000 Espanha Amgen S.A. Tel: +34 93 600 18 60 França Amgen S.A.S. Tél: +33 (0)9 69 363 363 Croácia Amgen d.o.o. Tel: +385 (0)1 562 57 20 Irlanda Amgen Ireland Limited Tel: +353 1 8527400 Islândia Vistor hf. Sími: +354 535 7000 Itália Amgen S.r.l. Tel: +39 02 6241121 Chipre C.A. Papaellinas Ltd Τηλ: +357 22741 741 Letônia Amgen Switzerland AG Rigas filiale Tel: +371 257 25888 | Lituânia Amgen Switzerland AG Vilniaus filialas Tel: +370 5 219 7474 Luxemburgo/Luxemburgo s.a. Amgen Bélgica/Bélgica Tél/Tel: +32 (0)2 7752711 Hungria Amgen Kft. Tel.: +36 1 35 44 700 Malta Amgen S.r.l. Itália Tel: +39 02 6241121 Países Baixos Amgen B.V. Tel: +31 (0)76 5732500 Noruega Amgen AB Tlf: +47 23308000 Áustria Amgen GmbH Tel: +43 (0)1 50 217 Polônia Amgen Biotechnologia Sp. z o.o. Tel.: +48 22 581 3000 Portugal Amgen Biofarmacêutica, Lda. Tel: +351 21 4220606 Romênia Amgen România SRL Tel: +4021 527 3000 Eslovênia AMGEN zdravila d.o.o. Tel: +386 (0)1 585 1767 República Eslovaca Amgen Slovakia s.r.o. Tel: +421 2 321 114 49 Finlândia Orion Pharma Puh/Tel: +358 10 4261 Suécia Amgen AB Tel: +46 (0)8 6951100 Reino Unido (Irlanda do Norte)Amgen Limited Tel: +44 (0)1223 420305 |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos: http://www.ema.europa.eu.
Instruções de uso: AMGEVITA pluma precargada SureClick de um só uso Via subcutânea | |||||||||||
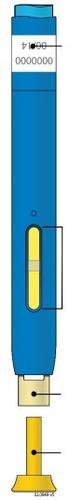
Guia dos componentes | |||||||||||
Antes de usar | Depois de usar | ||||||||||
Botão azul de início | |||||||||||
|
|
|
| ||||||||
Importante:A agulha está no interior |
Importante Antes de utilizar a pluma precargada de AMGEVITA, leia esta informação importante: Usar sua pluma precargada de AMGEVITA
|
Paso 1: Preparação |
A. | Saia uma pluma precargada de AMGEVITA do envase. | |||
Levante com cuidado e em linha reta a pluma precargada para sair da caixa. Volta a meter no frigorífico o envase original com as plumas precargadas sem usar. Para uma injeção mais confortável, deixe a pluma precargada a temperatura ambiente entre 15 a 30minutos antes de aplicar a injeção.
| ||||
B. | Inspeccione a pluma precargada de AMGEVITA. | |||
| ||||
Certeza de que o medicamento da janela seja transparente e entre incolora e ligeiramente amarelada.
| ||||
Em qualquer um desses casos, use uma pluma precargada nova. |
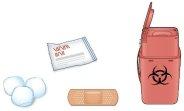
C. | Reúna todos os materiais que precisa para a injeção. | |
Lave bem as mãos com água e sabão. Sobre uma superfície de trabalho limpa e bem iluminada, coloque uma pluma precargada nova. Além disso, precisará desses materiais adicionais, já que não estão incluídos no envase:
| ||
|
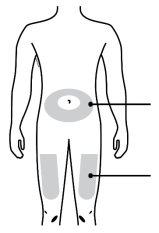
D. | Prepare e limpe a zona de injeção. | ||
| |||
Pode utilizar:
Limpe a zona de injeção com um toalhete com álcool. Deixe que a pele seque.
|
Paso 2: Prepare-se |
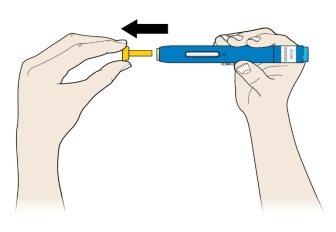
E. | Saia o capuchão amarelo, puxando-o em linha reta, apenas quando estiver pronto para a injeção. |
| |
É normal que na ponta da agulha ou do protetor de segurança amarelo haja uma gota de líquido.
|
F. | Estire ou puxe a zona de injeção para criar uma superfície firme. |
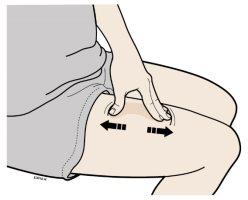
Método do estiramento | |
| |
Estire firmemente a pele deslocando o polegar e os dedos em direções opostas para criar uma zona de uns 5centímetros de largura. | |
Ou | |
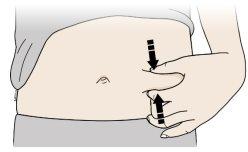
Método do puxão | |
| |
Puxe firmemente a pele entre o polegar e os dedos abrangendo uma zona de uns 5centímetros de largura. | |
Importante:Manter a pele estirada ou puxada durante a injeção. |
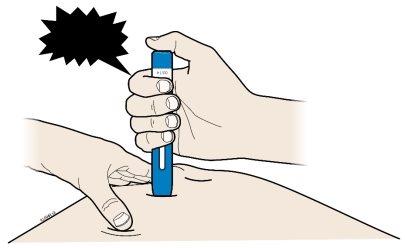
Paso 3: Injete |
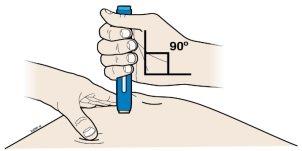
G. | Mantenha a pele estirada ou puxada. Uma vez retirado o capuchão amarelo, coloquea pluma precargada sobre a pele com um ângulo de 90 graus. |
| |
Importante:Não toque no botão azul de início ainda. |
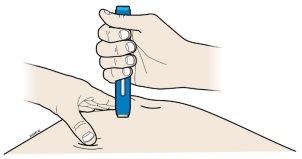
H. | Empurrecom firmeza a pluma precargada sobre a pele até que pare de se mover. | ||
| |||
Importante:Deve empurrar a pluma todo o que puder, mas não toque no botão de início azul até que esteja pronto para a injeção. |
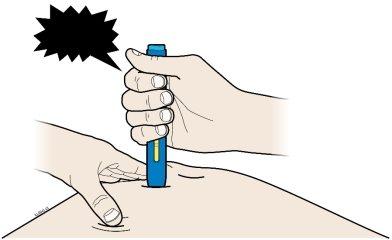
I. | Quando estiver pronto para a injeção, pressioneo botão de início azul. Ouvirá um clique. |
|
J. | Continue empurrandosobre a pele. A injeção pode levar uns 10 segundos para ser concluída. | ||||||||
|
Paso 4: Terminar |
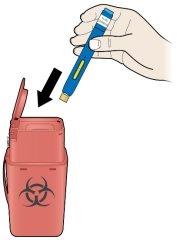
K. | Elimine a pluma precargada usada e o capuchão amarelo da agulha. |
| |
Importante:Mantenha o contenedor para descartar objetos pontiagudos fora da vista e do alcance das crianças. |
L. | Examine o local da injeção. |
Se observar sangue, pressione o local da injeção com um algodão ou uma gaze. Nãoesfregue o local da injeção. Aplique uma tirita se necessário. |
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ComposiçãoSACAROSA (72 mg mg), POLISORBATO 80 (0,8 mg mg), HIDROXIDO DE SODIO (E 524) (C. S. mg mg)
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a AMGEVITA 40 mg SOLUÇÃO INJETÁVEL EM CANETA PREENCHIDAForma farmacêutica: INJETÁVEL, 20 mgSubstância ativa: adalimumabFabricante: Amgen Europe B.V.Requer receita médicaForma farmacêutica: INJETÁVEL, 20 mgSubstância ativa: adalimumabFabricante: Amgen Europe B.V.Requer receita médicaForma farmacêutica: INJETÁVEL, 40 mgSubstância ativa: adalimumabFabricante: Amgen Europe B.V.Requer receita médica





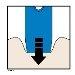 Empurrar
Empurrar