ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL

Pergunte a um médico sobre a prescrição de ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL

Como usar ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Introdução
Prospecto: informação para o utilizador
ADYNOVI250UI/2ml pó e solvente para solução injectável
ADYNOVI500UI/2ml pó e solvente para solução injectável
ADYNOVI1000UI/2ml pó e solvente para solução injectável
rurioctocog alfa pegol (factor VIII humano de coagulação recombinante pegilado)
Este medicamento está sujeito a vigilância adicional, o que facilitará a detecção de nova informação sobre a sua segurança. Pode contribuir comunicando os efeitos adversos que possa ter. A parte final da secção 4 inclui informação sobre como comunicar efeitos adversos.
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informação importante para si.
- Conservar este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é ADYNOVI e para que é utilizado
- O que precisa saber antes de começar a usar ADYNOVI
- Como usar ADYNOVI
- Possíveis efeitos adversos
- Conservação de ADYNOVI
- Conteúdo do envase e informação adicional
1. O que é ADYNOVI e para que é utilizado
ADYNOVI contém o princípio ativo rurioctocog alfa pegol, factor VIII humano de coagulação pegilado. O factor VIII humano de coagulação foi modificado para prolongar a duração da sua ação. O factor VIII é necessário para que o sangue forme coágulos e para deter as hemorragias. Nos doentes com hemofilia A (falta congénita de factor VIII) não está presente ou não actua de forma correcta.
ADYNOVI é utilizado para o tratamento e a prevenção da hemorragia em doentes a partir de 12 anos com hemofilia A (um distúrbio hemorrágico hereditário provocado pela ausência de factor VIII).
2. O que precisa saber antes de começar a usar ADYNOVI
Não use ADYNOVI:
- se é alérgico ao rurioctocog alfa pegol, octocog alfa ou a algum dos outros componentes deste medicamento (incluídos na secção 6)
- se é alérgico às proteínas de rato ou hamster
Se tiver alguma dúvida, consulte o seu médico.
Advertências e precauções
Consulte o seu médico antes de começar a usar ADYNOVI.
Existe um risco muito pequeno de que sofra uma reacção anafiláctica (uma reacção alérgica grave repentina) a ADYNOVI. Deve conhecer os sinais iniciais das reacções alérgicas, tais como erupção, habão urticarial, ronchas, picor generalizado, inchação de lábios e língua, dificuldade para respirar, ruídos ao respirar (sibilância), opressão no peito, sensação de malestar geral e tontura. Estes podem ser sintomas iniciais de choque anafiláctico. Outros sintomas podem incluir tontura intensa, perda de consciência e muita dificuldade para respirar.
Se aparecer algum destes sintomas, interrompa de forma imediata a injeção e consulte o seu médico. Os sintomas graves, como a dificuldade para respirar e o (pré)desmaio, necessitam de tratamento urgente.
Se sofrer de alguma doença cardíaca, informe o seu médico, porque existe um risco maior de complicações por formação de coágulos no sangue.
Doentes que desenvolvem inibidores do factorVIII
A formação de inibidores (anticorpos) é uma complicação conhecida que pode ocorrer durante o tratamento com todos os medicamentos compostos por factor VIII. Estes inibidores, em especial em grandes quantidades, impedem que o tratamento funcione de forma correcta, por isso si e o seu filho serão controlados cuidadosamente por si desenvolverem ditos inibidores. Se a sua hemorragia ou a do seu filho não estiver a ser controlada com ADYNOVI, consulte o seu médico de forma imediata.
Complicações relacionadas com o catéter
Se precisar utilizar um catéter venoso central (CVC), deve ter em conta o risco de complicações relacionadas com dito dispositivo, tais como infecções locais, presença de bactérias no sangue e trombose na zona do catéter.
Crianças e adolescentes
ADYNOVI só pode ser utilizado em adolescentes e adultos (maiores de 12 anos). As advertências e precauções que se indicam também se aplicam aos adolescentes.
Outros medicamentos e ADYNOVI
Informe o seu médico se está a utilizar, utilizou recentemente ou possa ter que utilizar qualquer outro medicamento.
Gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico antes de utilizar este medicamento. A hemofilia A afecta apenas raramente as mulheres. Por isso, não se dispõe de experiência em relação ao uso de ADYNOVI durante a gravidez e a amamentação.
Condução e uso de máquinas
ADYNOVI não tem influência sobre a capacidade para conduzir ou utilizar máquinas.
ADYNOVI contém sódio
Este medicamento contém 0,45 mmol de sódio (10 mg) por frasco. Isto deve ser tido em conta em doentes com dietas pobres em sódio.
3. Como usar ADYNOVI
O tratamento com ADYNOVI será iniciado e supervisionado por um médico com experiência no tratamento de doentes com hemofilia A.
O seu médico calculará a sua dose de ADYNOVI com base no seu estado e peso corporal e se é utilizado para a prevenção ou para o tratamento da hemorragia. A frequência da administração dependerá de como ADYNOVI actua no seu caso. O tratamento de substituição com ADYNOVI é normalmente um tratamento de por vida.
Siga exactamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico.
Prevenção da hemorragia
A dose habitual de ADYNOVI é de 40 a 50 UI por kg de peso corporal, administrada 2 vezes por semana.
Tratamento da hemorragia
A dose de ADYNOVI é calculada com base no seu peso corporal e nos níveis de factor VIII que se pretendem alcançar. Os níveis de factor VIII a alcançar dependerão da gravidade e da localização da hemorragia.
Consulte o seu médico se acredita que o efeito de ADYNOVI é insuficiente.
O seu médico realizará os análises de laboratório adequados para se certificar de que tem os níveis adequados de factor VIII. Isto é especialmente importante se se vai submeter a cirurgia maior.
Uso em crianças e adolescentes
ADYNOVI só pode ser utilizado em adolescentes e adultos (maiores de 12 anos). A dose para os adolescentes é calculada também com base no peso corporal e é a mesma que para os adultos.
Como se administra ADYNOVI
Normalmente o médico ou o enfermeiro injectam ADYNOVI numa veia (via intravenosa). Si ou qualquer outra pessoa podem também administrar a injeção de ADYNOVI, mas apenas após receberem a formação adequada. As instruções detalhadas para a autoadministração são descritas no final deste prospecto.
Se usar mais ADYNOVI do que deve
Siga exactamente as instruções de administração de ADYNOVI indicadas pelo seu médico. Consulte o seu médico se tiver dúvidas. Se injectar uma dose maior de ADYNOVI do que a recomendada, consulte o seu médico o mais breve possível.
Se esquecer de usar ADYNOVI
Não se injecte uma dose dupla para compensar as doses esquecidas. Administre a próxima injeção como está estabelecido e continue como o seu médico indicou.
Se interromper o tratamento com ADYNOVI
Não deixe de usar ADYNOVI sem consultar o seu médico.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode provocar efeitos adversos, embora nem todas as pessoas os sofram.
Se ocorrerem reações alérgicas (anafilácticas) graves e repentinas, deve parar de forma imediata a injeção. Contacte o seu médico de forma imediatase tiver algum dos seguintes sintomas iniciais de reações alérgicas:
- erupção, habão urticarial, ronchas, picor generalizado,
- inchação de lábios e língua,
- dificuldade para respirar, ruídos ao respirar, opressão no peito,
- sensação de malestar geral,
- tontura e perda de consciência.
Os sintomas graves, como a dificuldade para respirar e o (quase)desmaio, necessitam de tratamento urgente imediato.
Nos doentes que receberam tratamento prévio com factor VIII (mais de 150 dias de tratamento), podem formar-se anticorpos inibidores (ver secção 2) com pouca frequência (menos de 1 de cada 100 doentes). Se isto acontecer, o medicamento que toma pode deixar de funcionar correctamente e si pode sofrer uma hemorragia persistente. Nesse caso, contacte o seu médico de forma imediata.
Efeitos secundários frequentes(podem afectar até 1 de cada 10 pessoas)
Cefaleia, náuseas, diarreia, erupção
Efeitos adversos pouco frequentes(podem afectar até 1 de cada 100 pessoas)
Rubefacção, reacção alérgica (hipersensibilidade)
Inibidores do factor VIII (para doentes que tenham recebido tratamento anterior com factor VIII (mais de 150 dias de tratamento))
Outros efeitos adversos em crianças
Espera-se que a frequência, o tipo e a gravidade das reacções adversas em crianças sejam os mesmos que nos adultos.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, si pode contribuir para proporcionar mais informação sobre a segurança deste medicamento.
5. Conservação de ADYNOVI
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e na caixa após CAD. A data de validade é o último dia do mês que se indica.
Conservar em frigorífico (entre 2 ºC e 8 ºC).
Não congelar.
Conservar blister no embalagem exterior para protegê-lo da luz.
Durante o seu período de validade, o frasco de pó pode ser conservado a temperatura ambiente (até 30 ºC) durante um período único que não exceda 3 meses. Nesse caso, este medicamento caduca no final deste período de 3 meses ou na data de validade impressa no frasco de produto, o que ocorrer primeiro. Por favor, anote no embalagem do medicamento a data de finalização do período de conservação a temperatura ambiente de 3 meses. O medicamento não pode ser refrigerado novamente após ser conservado a temperatura ambiente. Não refrigerar o medicamento após a preparação.
Utilizar o medicamento num prazo de 3 horas após a dissolução completa do pó.
Este medicamento é para um só uso. Eliminar a solução não utilizada de forma adequada.
Os medicamentos não devem ser deitados fora pela sanita nem para o lixo. Pergunte ao seu farmacêutico como se livrar dos embalagens e dos medicamentos que já não precisa. Deste modo, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de ADYNOVI
- O princípio ativo é rurioctocog alfa pegol (fator VIII humano de coagulação produzido mediante tecnologia de DNA recombinante). Cada frasco de pó contém nominalmente 250, 500 ou 1000 UI de rurioctocog alfa pegol.
- O dissolvente contém 2 ml de água esterilizada para preparações injetáveis.
- Os demais ingredientes são manitol, trealose diidratado, histidina, glutationa, cloreto de sódio, cloreto de cálcio diidratado, tris(hidroximetil)aminometano, polissorbato 80 e água esterilizada para preparações injetáveis. ADYNOVI contém sódio, ver seção 2.
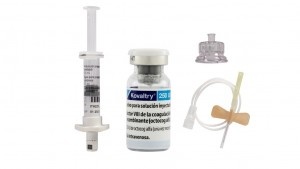
Aspecto do produto e conteúdo do envase
ADYNOVI é fornecido sob a forma de pó e dissolvente para solução injetável. O pó é um pó de cor branca a esbranquiçada que se desmenuza. O dissolvente é uma solução incolor e transparente. Após a reconstituição, a solução é transparente, incolor e livre de partículas estranhas.
Título da autorização de comercialização
Baxalta Innovations GmbH
Industriestrasse 67
A-1221 Viena
Tel: +44(0)1256 894 959
correio eletrônico: [email protected]
Fabricante
Baxalta Belgium Manufacturing SA
Boulevard René Branquart 80
B-7860 Lessines
Bélgica
Data da última revisão deste prospecto:
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos: http://www.ema.europa.eu/
Instruções para a preparação e administração
ADYNOVI não deve ser misturado com outros medicamentos ou dissolventes.
Recomenda-se fortemente registrar o nome e o número do lote do produto cada vez que se administra ADYNOVI. O blister tem etiquetas que podem ser removidas.
Instruções para a reconstituição
- Não utilizar após a data de validade que aparece nas etiquetas e no envase.
- Não utilizar se a tampa do blister não estiver perfeitamente selada.
- Não refrigerar o medicamento após a preparação.
- Se o medicamento ainda estiver na geladeira, pegue o blister selado (contém os frascos de pó e dissolvente pré-montados no sistema para reconstituição) e espere até que atinja a temperatura ambiente (entre 15 °C e 25 °C).
- Lave as mãos com sabão e água morna.
- Abrir o blister de ADYNOVI removendo a tampa. Retire o sistema BAXJECT III do blister.
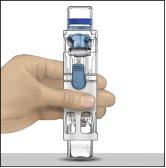
- Coloque o frasco de pó em uma superfície plana com o frasco de dissolvente em cima (Figura 1). O frasco de dissolvente tem uma linha azul. Não remova o protetor azul até que seja indicado mais adiante.
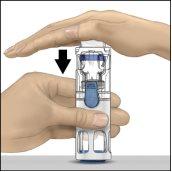
- Enquanto segura o frasco de pó com uma mão no sistema BAXJECT III, pressione com força o frasco de dissolvente com a outra mão até que o sistema fique totalmente contraído e o dissolvente entre no frasco de pó (Figura 2). Não incline o sistema até que a transferência esteja concluída.
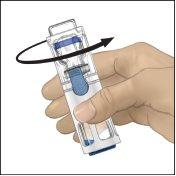
- Verifique se a transferência do dissolvente foi concluída. Agite suavemente até que todo o material se dissolva (Figura 3). Verifique se o pó está completamente dissolvido; se não estiver, toda a solução reconstituída não passará pelo filtro do dispositivo. O medicamento se dissolve rapidamente (normalmente em menos de 1 minuto). Após a reconstituição, a solução deve ser transparente, incolor e livre de partículas estranhas.
Figura1 | Figura2 | Figura3 |
|
|
|
Instruções para a injeção
Durante a administração, é necessária uma técnica antiséptica (em condições de limpeza e poucos germes).
Nota importante:
- Examine a solução preparada para detectar partículas ou mudanças de cor antes da administração (a solução deve ser transparente, incolor e livre de partículas).
Não utilize se a solução não for totalmente transparente ou o produto não estiver dissolvido completamente.
- Remova o protetor azul do dispositivo BAXJECT III. Não introduza ar na seringa. Conecte a seringa ao BAXJECT III. Recomenda-se utilizar uma seringa Luer-lock.
- Coloque o sistema com a boca para baixo (com o frasco de pó para cima). Retire a solução reconstituída para a seringa puxando o êmbolo para fora lentamente.
- Desconecte a seringa, conecte uma agulha de borboleta à seringa e injete a solução reconstituída em uma veia. A solução deve ser administrada lentamente, a uma velocidade determinada de acordo com o nível de confort do paciente, que não supere 10 ml por minuto. (Ver seção 4 "Efeitos adversos possíveis").
- Elimine a solução não utilizada de forma apropriada.
‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑
Esta informação é destinada apenas a profissionais do setor de saúde:
Tratamento a demanda
No caso de episódios de sangramento seguintes, a atividade de fator VIII não deve ser inferior ao nível de atividade plasmática dado (em % da normalidade ou UI/dl) no período correspondente. A seguinte tabela pode ser utilizada como guia posológica em cirurgia e nos episódios de sangramento:
Tabela1Guia posológica de dosagem em episódios de sangramento e cirurgia | ||
Grau de sangramento/tipo de procedimento cirúrgico | Nível de fatorVIII requerido (% ou UI/dl) | Frequência das doses (horas)/duração do tratamento (dias) |
Sangramento | ||
Hemartrose incipiente ou sangramento muscular ou oral. | 20 – 40 | Repetir as injeções a cada 12 a 24 horas. Pelo menos 1 dia, até que o episódio de sangramento se resolva, com base na dor, ou até que ocorra a cicatrização. |
Hemartrose mais extensa, sangramento muscular ou hematoma | 30 – 60 | Repetir as injeções a cada 12 a 24 horas durante 3-4 dias ou mais até que a dor e a discapacidade aguda se resolvam. |
Sangramentos potencialmente mortais. | 60 – 100 | Repetir as injeções a cada 8 a 24 horas até que o risco desapareça. |
Cirurgia | ||
MenorIncluindo extração dental | 30 – 60 | A cada 24 horas, pelo menos 1 dia, até que ocorra a cicatrização. |
Maior | 80 – 100 (pré e pós-operatório) | Repetir as injeções a cada 8 a 24 horas até que a ferida cicatrize adequadamente e, em seguida, continue o tratamento por pelo menos mais 7 dias para manter uma atividade de fator VIII de 30% a 60% (UI/dl). |
Profilaxia
Para a profilaxia a longo prazo, a dose recomendada é de 40 a 50 UI de ADYNOVI por kg de peso corporal duas vezes por semana, a intervalos de 3 a 4 dias. Os ajustes de dose e intervalos de administração podem ser considerados com base nos níveis de fator VIII obtidos e na tendência hemorrágica individual (ver seção 5.2).
População pediátrica
A posologia do tratamento a demanda em pacientes pediátricos (12 a 18 anos de idade) é a mesma que para pacientes adultos. O tratamento profilático para pacientes de 12 a <18 anos é o mesmo que para pacientes adultos. a segurança longo prazo de adynovi em crianças menores 12 ainda não foi estabelecida. os ajustes dose e intervalos administração podem ser considerados com base nos níveis fator viii obtidos na tendência hemorrágica individual (ver seção 5.2).< p>
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, 1.000 UISubstância ativa: coagulation factor VIIIFabricante: Takeda Manufacturing Austria AgRequer receita médicaForma farmacêutica: INJETÁVEL, 1500 UISubstância ativa: coagulation factor VIIIFabricante: Takeda Manufacturing Austria AgRequer receita médicaForma farmacêutica: INJETÁVEL, 1000 UI - após reconstituição em 2 ml de água para injetáveis, a dose é de 500 UI/mlSubstância ativa: coagulation factor VIIIFabricante: Takeda Manufacturing Austria AgRequer receita médica
Alternativas a ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Polónia
Alternativa a ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Ukraine
Médicos online para ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ADYNOVI 250 UI / 2 mL PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.