
Ondansetron Kalceks
Zapytaj lekarza o receptę na Ondansetron Kalceks

Jak stosować Ondansetron Kalceks
Ulotka dołączona do opakowania: informacja dla użytkownika
ONDANSETRON KALCEKS, 2 mg/ml, roztwór do wstrzykiwań/do infuzji
Ondansetronum
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, pielęgniarki lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, pielęgniarce lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest ONDANSETRON KALCEKS i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku ONDANSETRON KALCEKS
- 3. Jak stosować ONDANSETRON KALCEKS
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać ONDANSETRON KALCEKS
- 6. Zawartość opakowania i inne informacje
1. Co to jest ONDANSETRON KALCEKS i w jakim celu się go stosuje
ONDANSETRON KALCEKS zawiera substancję czynną o nazwie ondansetron. Należy ona do grupy
leków przeciwwymiotnych, które łagodzą nudności i wymioty.
Dorośli
Ondansetron jest stosowany w zapobieganiu i hamowaniu nudności i wymiotów wywołanych
chemioterapią i radioterapią oraz w zapobieganiu i leczeniu nudności i wymiotów po operacji
chirurgicznej.
Dzieci i młodzież
Ondansetron jest stosowany w zapobieganiu i hamowaniu nudności i wymiotów wywołanych
chemioterapią u dzieci w wieku powyżej 6 miesięcy i u młodzieży.
Ondansetron jest stosowany w zapobieganiu i leczeniu nudności i wymiotów w okresie
pooperacyjnym u dzieci w wieku powyżej 1 miesiąca i u młodzieży.
2. Informacje ważne przed zastosowaniem leku ONDANSETRON KALCEKS
Kiedy nie stosować leku ONDANSETRON KALCEKS:
- jeśli pacjent ma uczulenie na ondansetron lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6);
- jeśli pacjent przyjmuje apomorfinę (stosowaną w leczeniu choroby Parkinsona).
Pacjent nie otrzyma leku ONDANSETRON KALCEKS, jeśli którekolwiek z powyższych go dotyczy.
Jeśli pacjent nie jest pewien, czy którekolwiek z powyższych go dotyczy, należy porozmawiać z
lekarzem lub pielęgniarką przed zastosowaniem tego leku.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku ONDANSETRON KALCEKS należy omówić to z lekarzem lub
pielęgniarką, jeśli:
- pacjent ma objawy reakcji alergicznej, takie jak swędzenie, trudności w oddychaniu lub obrzęk twarzy, warg, gardła lub języka;
- pacjent miał kiedykolwiek uczulenie na inne leki przeciw nudnościom i wymiotom (np. granisetron lub palonosetron);
- pacjent ma problemy z sercem; może wystąpić tymczasowa zmiana w elektrokardiogramie (EKG);
- pacjent przyjmuje leki stosowane w zaburzeniach rytmu serca (leki przeciwarytmiczne) lub leki obniżające ciśnienie krwi i tętno podczas spoczynku (beta-blokery);
- pacjent ma zaparcia lub chorobę jelit, która może prowadzić do zaparć;
- pacjent ma problemy z wątrobą lub przyjmuje jakiekolwiek leki, które mogą być szkodliwe dla wątroby (hepatotoksyczne leki stosowane w chemioterapii). W takich przypadkach czynność wątroby będzie ściśle monitorowana, szczególnie u dzieci i młodzieży;
- wykonano badanie krwi w celu sprawdzenia czynności wątroby (ondansetron może wpływać na wyniki);
- pacjent ma problemy z poziomem soli mineralnych we krwi, takich jak potas i magnez;
- pacjent planuje mieć operację migdałków. W takim przypadku pacjent musi być dokładnie monitorowany.
Jeśli pacjent nie jest pewien, czy którekolwiek z powyższych go dotyczy, należy porozmawiać
z lekarzem lub pielęgniarką przed zastosowaniem tego leku.
ONDANSETRON KALCEKS a inne leki
Należy powiedzieć lekarzowi lub pielęgniarce o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować.
W szczególności, należy powiedzieć lekarzowi lub pielęgniarce, jeśli pacjent przyjmuje którykolwiek
z poniższych leków:
- apomorfinę (patrz „Kiedy nie stosować leku ONDANSETRON KALCEKS”);
- karbamazepinę lub fenytoinę (stosowane w leczeniu padaczki);
- ryfampicynę (stosowaną w leczeniu zakażeń, takich jak gruźlica);
- tramadol (lek przeciwbólowy);
- leki stosowane w leczeniu depresji i (lub) zaburzeń lękowych:
- leki z grupy selektywnych inhibitorów wychwytu zwrotnego serotoniny (ang. SSRIs) w tym fluoksetyna, paroksetyna, sertralina, fluwoksamina, citalopram, escitalopram;
- leki z grupy inhibitorów wychwytu zwrotnego serotoniny i noradrenaliny (ang. SNRIs) w tym wenlafaksyna i duloksetyna.
W przypadku jednoczesnego podawania z lekami na określone choroby serca, mogą wystąpić zmiany
w obrazie EKG. Jednoczesne stosowanie leków uszkadzających serce (np. antracyklin (takich jak
doksorubicyna, daunorubicyna) lub trastuzumab), antybiotyków (takich jak erytromycyna), leków
przeciwgrzybiczych (takich jak ketokonazol), leków przeciwarytmicznych (takich jak amiodaron)
i beta-blokerów (takich jak atenolol lub tymolol) może zwiększać ryzyko zaburzeń rytmu serca.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza przed zastosowaniem tego leku.
Ciąża
Nie należy stosować leku ONDANSETRON KALCEKS podczas pierwszego trymestru ciąży. Wynika
to z tego, że lek ONDANSETRON KALCEKS może nieznacznie zwiększyć ryzyko urodzenia dziecka
z rozszczepem wargi i (lub) podniebienia (otworu lub szczeliny w górnej wardze i (lub) podniebieniu).
Jeśli pacjentka jest w ciąży, przypuszcza że może być w ciąży lub gdy planuje mieć dziecko, powinna
poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Kobiety w wieku rozrodczym
Kobietom w wieku rozrodczym może być zalecone stosowanie skutecznej antykoncepcji.
Karmienie piersią
Przed rozpoczęciem leczenia ondansetronem należy przerwać karmienie piersią.
Płodność
Ondansetron nie ma wpływu na płodność.
Prowadzenie pojazdów i obsługiwanie maszyn
Ondansetron nie ma wpływu lub wywiera nieistotny wpływ na zdolność prowadzenia pojazdów
i obsługiwania maszyn.
ONDANSETRON KALCEKS zawiera sód
Ten lek zawiera 3,52 mg sodu (głównego składnika soli kuchennej) na ml roztworu. Odpowiada to
0,18% maksymalnej zalecanej dobowej dawki sodu w diecie u osób dorosłych.
3. Jak stosować ONDANSETRON KALCEKS
Ondansetron jest podawany przez lekarza lub pielęgniarkę w powolnym wstrzyknięciu lub infuzji
dożylnej lub jako wstrzyknięcie domięśniowe.
Ondansetron jest również dostępny w innych postaciach farmaceutycznych odpowiednich do
podawania doodbytniczego i (lub) doustnego, co pozwala na indywidualne dostosowanie dawki.
Jednak ONDANSETRON KALCEKS jest przeznaczony do podawania wyłącznie dożylnie lub
domięśniowo.
Dorośli
Zapobieganie nudnościom i wymiotom wywołanym chemioterapią lub radioterapią
- W dniu stosowania chemioterapii lub radioterapiiOndansetron zostanie podany bezpośrednio przed chemioterapią lub radioterapią. Zazwyczaj stosowana dawka u dorosłych to 8 mg, podane w postaci powolnego wstrzyknięcia dożylnego lub domięśniowego, lub powolnej infuzji dożylnej.
- W kolejnych dniachPo początkowym leczeniu, lekarz może zalecić, by ondansetron był przyjmowany doustnie lub doodbytniczo. W razie potrzeby należy postępować zgodnie z instrukcjami na odpowiedniej ulotce dołączonej do opakowania. Zawsze należy przyjmować ondansetron zgodnie z zaleceniami lekarza.
W razie potrzeby dawkę można zwiększyć do 32 mg na dobę.
Zapobieganie i leczenie nudności oraz wymiotów po operacji chirurgicznej
Zazwyczaj stosowana dawka u dorosłych to 4 mg podawane poprzez powolne wstrzyknięcie dożylne
lub domięśniowe.
Dzieci i młodzież
Zapobieganie nudnościom oraz wymiotom wywołanych chemioterapią u dzieci w wieku powyżej 6
miesiąca oraz u młodzieży
U dzieci, lek ten podaje się powoli do żyły (dożylnie) bezpośrednio przed chemioterapią (zalecana
dawka: 5 mg/m lub 0,15 mg/kg). Dawka dożylna nie może przekraczać 8 mg. Podawanie doustne
można rozpocząć 12 godzin później. To leczenie można kontynuować do 5 dni po chemioterapii.
Dawkę doustną oblicza się na podstawie masy lub powierzchni ciała. Całkowita dawka dobowa nie
może przekraczać dawki 32 mg dla dorosłych.
Zapobieganie i leczenie nudności i wymiotów po operacji chirurgicznej u dzieci w wieku powyżej
1 miesiąca i młodzieży
U dzieci, dawka jest obliczana na podstawie masy lub powierzchni ciała. Całkowita dawka dobowa nie
może przekraczać dawki 32 mg dla osób dorosłych. Dawka jest podawana w powolnym wstrzyknięciu
dożylnym przed, w trakcie lub po indukcji znieczulenia.
Pacjenci w podeszłym wieku (powyżej 65. roku życia)
Ondansetron jest dobrze tolerowany u pacjentów powyżej 65. roku życia.
Nudności i wymioty wywołane chemioterapią i radioterapią
U pacjentów w wieku 65 lat lub starszych, wszystkie dawki dożylne należy rozcieńczyć i podać
w postaci infuzji trwającej nie krócej niż 15 minut. Jeśli konieczne jest wielokrotne dawkowanie,
należy je podawać w odstępie co najmniej 4 godzin.
U pacjentów w wieku od 65 do 74 lat, dawka początkowa wynosi 8 mg lub 16 mg. U pacjentów
w wieku powyżej 75 lat, dawka początkowa nie powinna przekraczać 8 mg.
Zapobieganie i leczenie nudności oraz wymiotów po operacji chirurgicznej
Dane dotyczące stosowania u osób w podeszłym wieku są ograniczone.
Pacjenci z zaburzeniami czynności wątroby
U pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby, całkowita dawka
dobowa nie powinna przekraczać 8 mg.
Pacjenci z zaburzeniami czynności nerek
Nie jest wymagana modyfikacja dawki, częstości ani drogi podawania.
Zastosowanie większej niż zalecana dawki leku ONDANSETRON KALCEKS
Lekarz lub pielęgniarka poda pacjentowi dorosłemu lub dziecku zastrzyk leku ONDANSETRON
KALCEKS, więc jest mało prawdopodobne, aby pacjent dorosły lub dziecko otrzymali zbyt dużą
dawkę leku. Jeśli uważa się, że pacjent dorosły lub dziecko otrzymali zbyt dużą dawkę lub pominięto
dawkę, należy powiedzieć o tym lekarzowi lub pielęgniarce.
Mogą wystąpić następujące objawy: zaburzenia widzenia, ciężkie zaparcia, niskie ciśnienie krwi
i zwolnione bicie serca.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się
do lekarza, farmaceuty lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Działania niepożądane u dzieci i młodzieży są podobne do tych u dorosłych.
Ciężkie reakcje alergiczne.Występują one rzadko u osób stosujących ondansetron. Objawy
obejmują:
- Wypukła i swędząca wysypka skórna (pokrzywka)
- Obrzęk, czasami twarzy lub ust (obrzęk naczynioruchowy) z trudnościami w oddychaniu
- Krótkotrwała utrata przytomności
Jeśli u pacjenta wystąpi którykolwiek z powyższych objawów, należy natychmiast skontaktować się
z lekarzem. Należy przerwać stosowanie leku.
Bardzo częste działania niepożądane(mogą wystąpić u więcej niż 1 na 10 pacjentów)
- Ból głowy
Częste działania niepożądane(mogą wystąpić u mniej niż 1 na 10 pacjentów)
- Uczucie gorąca lub zaczerwienienie skóry
- Zaparcia
- Zaczerwienienie
- Podrażnienie w miejscu wstrzyknięcia (po wstrzyknięciu dożylnym)
Niezbyt częstedziałania niepożądane(mogą wystąpić u mniej niż 1 na 100 pacjentów)
- Drgawki
- Mimowolne ruchy lub drgania mięśni
- Nieregularne lub wolne bicie serca
- Ból w klatce piersiowej
- Niskie ciśnienie krwi
- Czkawka
- Zwiększenie aktywności enzymów wątrobowych
Rzadkie działanianiepożądane(mogą wystąpić u mniej niż 1 na 1 000 pacjentów)
- Zaburzenia rytmu serca (które czasami powodują nagłą utratę przytomności)
- Zawroty głowy
- Przejściowe niewyraźne widzenie lub zaburzenia widzenia
Bardzo rzadkie działania niepożądane(mogą wystąpić u mniej niż 1 na 10 000 pacjentów)
- Rozległa wysypka z pęcherzami i złuszczaniem naskórka, obejmująca znaczną część ciała (toksyczne martwicze oddzielanie się naskórka)
- Przemijający zanik widzenia
Częstość nieznana (nie może być określona na podstawie dostępnych danych)
- Suchość w jamie ustnej
- Niedokrwienie mięśnia sercowego (do objawów należą: nagły ból w klatce piersiowej lub ucisk w klatce piersiowej)
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce.
Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych będzie można zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać ONDANSETRON KALCEKS
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Brak specjalnych zaleceń dotyczących temperatury przechowywania leku.
Przechowywać ampułki w opakowaniu zewnętrznym w celu ochrony przed światłem.
Po otwarciu ampułki
Po otwarciu lek powinien być zużyty natychmiast.
Okres ważności po rozcieńczeniu
Stabilność chemiczna i fizyczna podczas użycia została wykazana w okresie 7 dni w temperaturze
25 °C i 2-8 °C.
Z mikrobiologicznego punktu widzenia, rozcieńczony roztwór należy zużyć natychmiast. Jeśli roztwór
nie zostanie zużyty natychmiast, za czas i warunki przechowywania przed użyciem odpowiada
użytkownik i zwykle nie powinien być on dłuższy niż 24 godziny w temperaturze 2-8°C, jeśli
rozcieńczenie miało miejsce w kontrolowanych i zwalidowanych warunkach aseptycznych.
Nie stosować tego leku po upływie terminu ważności zamieszczonym na etykiecie ampułki po: „EXP”
i na pudełku tekturowym po: „Termin ważności (EXP)”. Termin ważności oznacza ostatni dzień
podanego miesiąca.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera ONDANSETRON KALCEKS
- Substancją czynną jest ondansetron. Każdy ml roztworu zawiera ondansetronu chlorowodorek dwuwodny w ilości odpowiadającej 2 mg ondansetronu. Każda ampułka z 2 ml roztworu zawiera ondansetronu chlorowodorek dwuwodny w ilości odpowiadającej 4 mg ondansetronu. Każda ampułka z 4 ml roztworu zawiera ondansetronu chlorowodorek dwuwodny w ilości odpowiadającej 8 mg ondansetronu.
- Pozostałe składniki to: sodu chlorek, kwas cytrynowy jednowodny, sodu cytrynian dwuwodny, woda do wstrzykiwań.
Jak wygląda ONDANSETRON KALCEKS i co zawiera opakowanie
Przezroczysty, bezbarwny roztwór, wolny od widocznych cząstek.
2 ml lub 4 ml roztworu w ampułkach z bezbarwnego szkła typu I z punktem OPC i kolorową
obwódką.
Ampułki zapakowane są w osłonkę. Osłonka zapakowana jest w tekturowe pudełko.
Wielkości opakowań:
5, 10 lub 25 ampułek
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
AS KALCEKS
Krustpils iela 71E
LV-1057 Rīga
Łotwa
Tel.: +371 67083320
E-mail: [email protected]
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego i w Zjednoczonym Królestwie (Irlandii Północnej) pod następującymi nazwami:
Łotwa
Ondansetron Kalceks 2 mg/ml šķīdums injekcijām/infūzijām
Austria, Bułgaria, Chorwacja, Czechy, Dania, Estonia, Finlandia, Niemcy, Węgry, Islandia, Litwa,
Norwegia, Słowacja, Szwecja:
Ondansetron Kalceks
Belgia
Ondansetron Kalceks 2 mg/ml, solution injectable/pour perfusion
Ondansetron Kalceks 2 mg/ml, oplossing voor injectie/infusie
Ondansetron Kalceks 2 mg/ml, Injektions-/Infusionslösung
Grecja
ONDANSETRON/KALCEKS
Irlandia, Wielka Brytania (Irlandia Północna): Ondansetron 2 mg/ml solution for injection/infusion
Włochy
Ondansetrone Kalceks
Holandia
Ondansetron Kalceks 2 mg/ml, oplossing voor injectie/infusie
Polska
ONDANSETRON KALCEKS
Rumunia
Ondansetron Kalceks 2 mg/ml soluţie injectabilă/perfuzabilă
Słowenia
Ondansetron Kalceks 2 mg/ml raztopina za injiciranje/infundiranje
Hiszpania
Ondansetron Kalceks 2 mg/ml soluciόn inyectable y para perfusiόn
Data ostatniej aktualizacji ulotki: 02/2022
------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Więcej informacji na temat tego leku znajduje się w Charakterystyce Produktu Leczniczego (ChPL).
Przedawkowanie
Objawy i oznaki
Doświadczenie dotyczące przedawkowania ondansetronu jest ograniczone, ale w razie
przypadkowego przedawkowania można spodziewać się następujących objawów zatrucia: zaburzenia
widzenia, ciężkie zaparcia, niedociśnienie tętnicze i epizod wazowagalny z przemijającym blokiem
przedsionkowo-komorowym drugiego stopnia. We wszystkich przypadkach objawy ustąpiły
całkowicie. Ondansetron wydłuża odstęp QT w sposób zależny od dawki.
Dzieci i młodzież
Po nieumyślnym doustnym przedawkowaniu ondansetronu (przekroczenie szacowanego spożycia
4 mg/kg) u niemowląt i dzieci w wieku od 12 miesięcy do 2 lat zgłaszano przypadki pediatryczne
wskazujące na zespół serotoninowy.
Postępowanie
Nie ma specyficznego antidotum dla ondansetronu. W przypadku podejrzenia przedawkowania należy
zastosować odpowiednie leczenie objawowe i podtrzymujące. Zaleca się monitorowanie EKG. Dalsze
leczenie powinno być zgodne ze wskazaniami klinicznymi lub zaleceniami krajowego ośrodka
ds. zatruć, jeśli jest to możliwe.
Nie jest zalecane używanie ipekakuany do leczenia przedawkowania, ponieważ jest mało
prawdopodobne, aby pacjenci zareagowali ze względu na przeciwwymiotne działanie samego
ondansetronu.
Niezgodności
ONDANSETRON KALCEKS roztwór do wstrzykiwań/do infuzji nie powinien być podawany w tej
samej strzykawce lub zestawie infuzyjnym co jakikolwiek inny lek.
Nie mieszać tego produktu leczniczego z innymi produktami leczniczymi, oprócz wymienionych
poniżej.
Specjalne środki ostrożności dotyczące usuwania i przygotowania produktu leczniczego do stosowania
Wyłącznie do jednorazowego użytku.
Produkt leczniczy powinien być sprawdzony wzrokowo przed użyciem. Produktu leczniczego nie
należy stosować, jeśli widoczne są jakiekolwiek oznaki rozkładu (np. cząstki lub zmiana barwy).
Produktu leczniczego ONDANSETRON KALCEKS nie należy sterylizować w autoklawie.
Produkt może być rozcieńczany z następującymi dożylnymi roztworami do infuzji:
- 9 mg/ml (0,9%) roztwór chlorku sodu;
- 50 mg/ml (5%) roztwór glukozy;
- 100 mg/ml (10%) roztwór mannitolu;
- płyn Ringera;
- 3 mg/ml (0,3%) roztwór chlorku potasu i 9 mg/ml (0,9%) roztwór chlorku sodu;
- 3 mg/ml (0,3%) roztwór chlorku potasu i 50 mg/ml (5%) roztwór glukozy;
- płyn Ringera z mleczanami.
Wykazano, że ONDANSETRON KALCEKS jest zgodny ze strzykawkami polipropylenowymi (PP),
butelkami z szkła typu I, workami infuzyjnymi z polietylenu (PE), polichlorku winylu (PVC) i octanu
etylowinylu (EVA) oraz drenami z PVC i PE po rozcieńczeniu wyżej wymienionymi roztworami do
infuzji. Wykazano, że nierozcieńczony roztwór ONDANSETRON KALCEKS do wstrzykiwań/do
infuzji jest zgodny ze strzykawkami PP.
Zgodność z innymi lekami
Ondansetron można podawać we wlewie dożylnym (1 mg na godzinę). Następujące produkty
lecznicze mogą być podawane przez miejsce Y zestawu podającego ondansetron dla stężeń
ondansetronu od 16 do 160 µg/ml (np. odpowiednio, 8 mg/500 ml i 8 mg/50 ml):
- Cisplatyna
- 5-Fluorouracyl
- Karboplatyna
- Etopozyd
- Ceftazydym
- Cyklofosfamid
- Doksorubicyna
- Deksametazon
Instrukcja otwierania ampułki
- 1) Obrócić ampułkę kolorowym punktem w górę. Jeśli w górnej części ampułki znajduje się roztwór, należy delikatnie stuknąć palcem, aby przenieść cały roztwór do dolnej części ampułki.
- 2) Użyć obu rąk, aby otworzyć ampułkę; trzymając dolną część ampułki w jednej ręce, drugą ręką odłamać górną część ampułki w kierunku od kolorowego punktu (patrz obrazek poniżej).
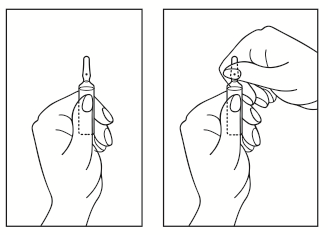
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie
z lokalnymi przepisami.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterAS Kalceks
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Ondansetron KalceksPostać farmaceutyczna: Tabletki, 8 mgSubstancja czynna: ondansetronProducent: Egis Pharmaceuticals PLCWymaga receptyPostać farmaceutyczna: Roztwór, 2 mg/mlSubstancja czynna: ondansetronWymaga receptyPostać farmaceutyczna: Roztwór, 4 mgSubstancja czynna: ondansetronWymaga recepty
Odpowiedniki Ondansetron Kalceks w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Ondansetron Kalceks – Hiszpania
Odpowiednik Ondansetron Kalceks – Ukraina
Lekarze online w sprawie Ondansetron Kalceks
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Ondansetron Kalceks – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














